- Spontandissektion der Kranzarterien: Epidemiologie und Behandlung
Nicht nur Patienten mit erhöhtem kardiovaskulären Risikoprofil können ein akutes Koronarsyndrom erleiden. Vor allem bei Frauen finden sich in der invasiven Abklärung eines Herzinfarktes oft keine sklerotischen Veränderungen der epikardialen Gefässe. Eine wichtige Differentialdiagnose für die Troponinerhöhung im Blut, die eben nicht auf eine Plaqueruptur oder eine Plaqueerosion mit intravasaler Thrombusbildung zurückzuführen ist, stellt die spontane Koronardissektion dar. Diese beruht auf einer spontanen Trennung einzelner Schichten der Koronararterienwand, die weder atherosklerotisch, noch traumatisch oder iatrogen bedingt ist (1).
Les patients présentant un profil de risque cardiovasculaire accru ne sont pas les seuls à pouvoir souffrir d’un syndrome coronarien aigu. En particulier chez les femmes, le bilan invasif de l’ infarctus du myocarde ne révèle souvent pas de changements sclérotiques des vaisseaux épicardiques. Un diagnostic différentiel important pour l’ élévation de la troponine dans le sang, qui n’ est pas due à une rupture de plaque ou à une érosion de plaque avec formation de thrombus intravasculaire, est la dissection coronaire spontanée. Elle est basée sur une séparation spontanée des différentes couches de la paroi de l’ artère coronaire, qui n’ est ni athérosclérotique, ni traumatique, ni iatrogène (1).
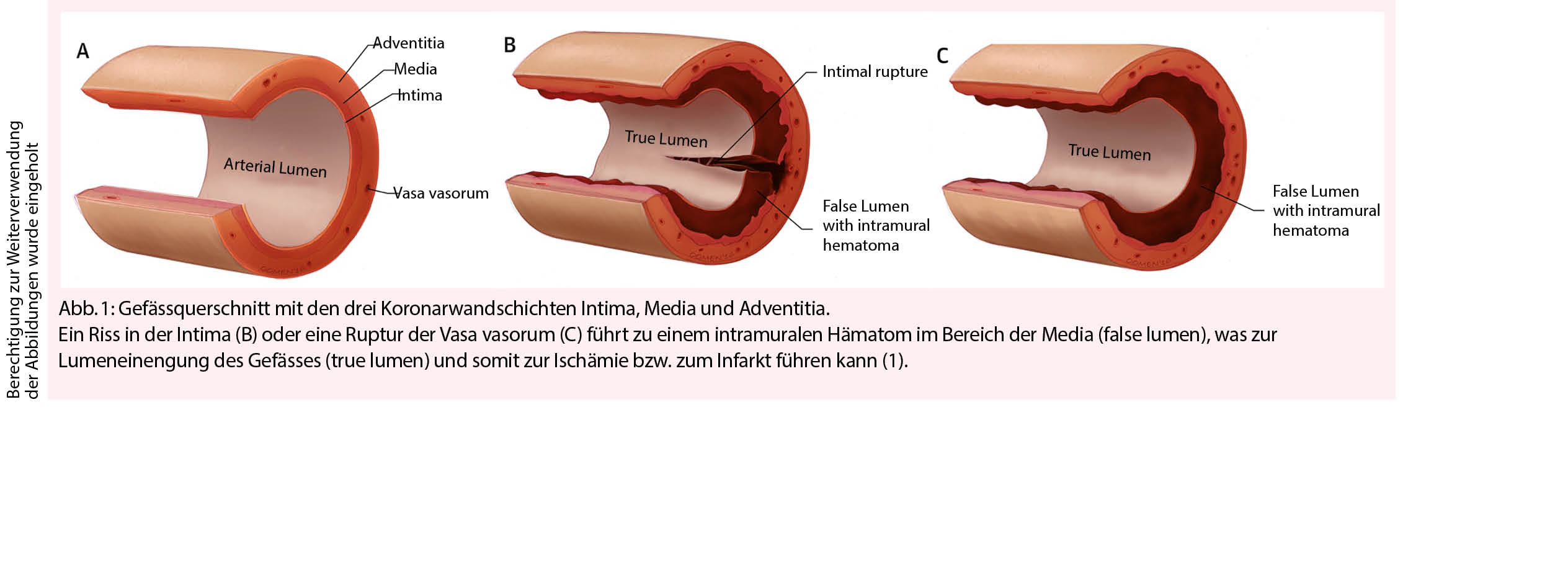
Durch einen Riss in der Intima oder eine spontane Ruptur der Vasa vasorum bildet sich ein intramurales Hämatom innerhalb oder zwischen einer dieser drei Schichten (2). Das wahre Gefässlumen wird komprimiert, was den koronaren Blutfluss behindern und so zum Infarkt führen kann (Abbildung 1) (3).
Epidemiologie
Spontane Koronardissektionen verursachen 1-4% aller akuten Koronarsyndrome (3). In 0.5% aller plötzlichen Herztode lässt sich autoptisch eine Koronardissektion als Ursache nachweisen (4). Bei mehr als 90% aller Patienten mit Koronardissektionen handelt es sich um Frauen ohne konventionelle Risikofaktoren (5). Allerdings wurde bei diesen Patienten eine höhere Prävalenz von Migräne, Depressionen und Angstzuständen festgestellt (6). Bis zu 35% aller Herzinfarkte bei Frauen < 50 Jahren und 43% aller schwangerschaftsassoziierten Herzinfarkte (vorwiegend drittes Trimester oder post-partum; 1.8 Dissektionen pro 100 000 Schwangerschaften) sind auf spontane Koronardissektionen zurückzuführen (7, 8). Obwohl grundsätzlich jede Altersgruppe betroffen sein kann, liegt das Durchschnittsalter von Patienten mit spontanen Koronardissektionen mit 45-53 Jahren deutlich unter dem von Patienten mit atherosklerotisch bedingten Herzinfarkten (5, 7). Weil spontane Koronardissektionen in der Realität aufgrund des geringen Verdachts auf ein akutes Koronarsyndrom bei jungen Frauen vermutlich deutlich unterdiagnostiziert sind, ist die tatsächliche Inzidenz und Prävalenz in der Allgemeinbevölkerung nicht bekannt.
Aufgrund mangelnden Bewusstseins für dieses Krankheitsbild unter medizinischen Erstversorgern ist diese häufig fehldiagnostizierte Gruppe von Patienten am stärksten gefährdet, was sich in einer im Vergleich zu Männern gleichen Alters um das Doppelte erhöhten Sterblichkeit nach Herzinfarkt widerspiegelt (9, 10).
Behandlung
Jeder Thoraxschmerz ist ernst zu nehmen
Leitsymptome von Patienten mit spontaner Koronardissektion sind wie bei atherosklerotisch bedingten Koronarsyndromen Thoraxschmerzen unterschiedlichen Charakters bis hin zu epigastrischen Beschwerden oder Dyspnoe (5, 7, 11). Auch wenn die betroffene Person nicht dem typischen Bild eines kardialen Patienten mit entsprechendem kardiovaskulärem Risikoprofil entspricht, sollte bei Beschwerden dieser Art stets an den Herzinfarkt als erste Differentialdiagnose gedacht werden. Nach Diagnosestellung eines Herzinfarktes, welche neben dem klinischen Korrelat auf über die Norm erhöhte kardiale Biomarker (Troponin T/I) und je nach Restperfusion im betroffenen Herzmuskelareal Veränderungen im EKG basiert, sollte nicht auf die verschiedenen Ätiologien geachtet, sondern die möglichst rasche Revaskularisation angestrebt werden.
Herzkatheteruntersuchung als erstes und wichtigstes diagnostisches Mittel
Bis zum definitiven Nachweis einer spontanen Koronardissektion unterscheidet sich das Management dieser Patienten nicht von Patienten mit «herkömmlichem» Herzinfarkt. Eine Differenzierung zwischen einem atherosklerotisch und einem Dissektions-bedingten Koronarsyndrom ist erst mittels Koronarangiographie möglich, weshalb bei jedem STEMI oder NSTEMI nach der Notfallversorgung, welche die Gabe von Acetylsalicylsäure und einem Blutgerinnungshemmer (Heparin oder Fondaparinux) beinhaltet, eine zeitnahe invasive Abklärung oberste Priorität hat.
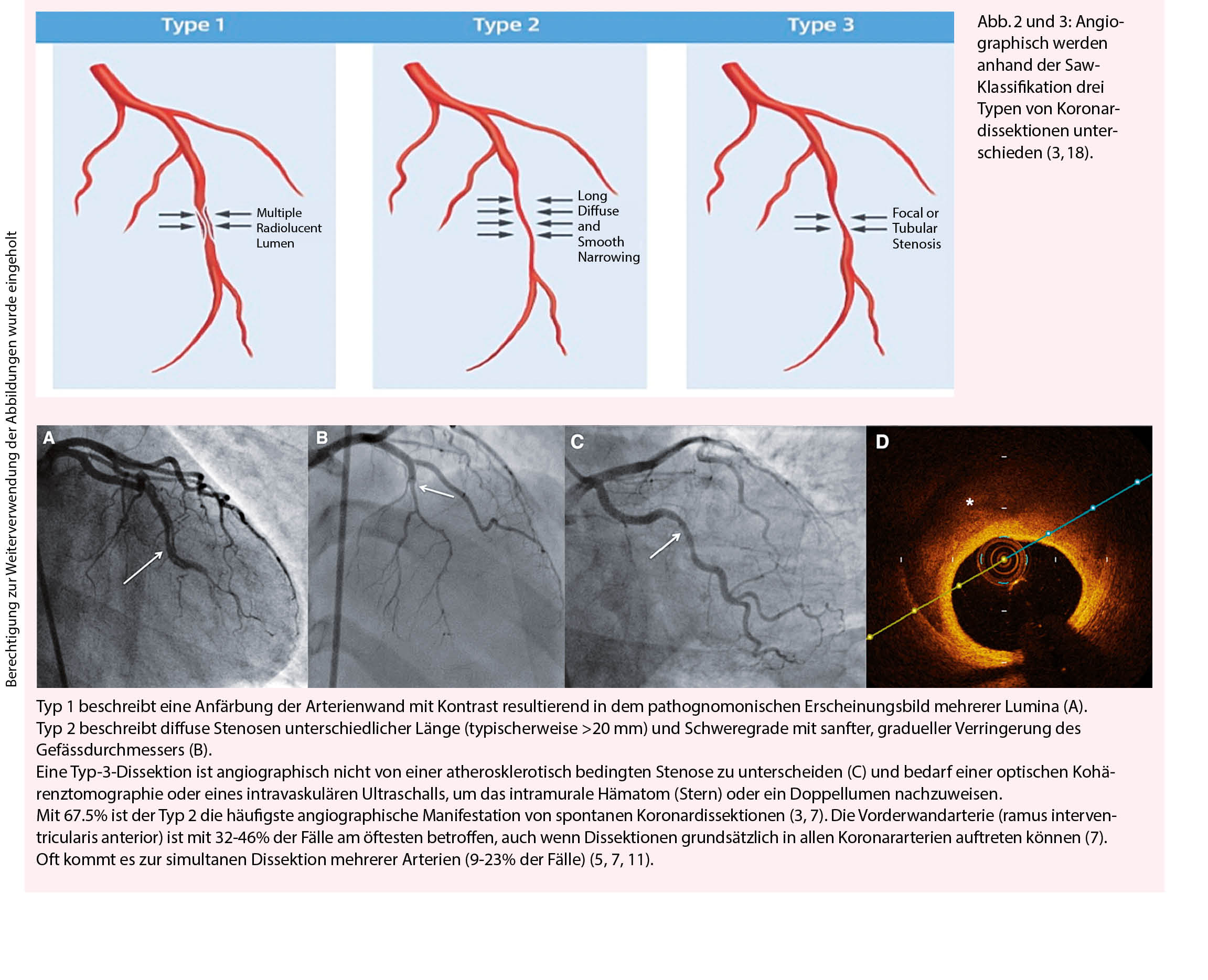
Bei der Interpretation der Koronarangiographie sollten vor allem junges Alter, weibliches Geschlecht und das Fehlen herkömmlicher kardiovaskulärer Risikofaktoren den Verdacht auf eine spontane Koronardissektion aufkommen lassen (10). Obwohl diese meist multifaktoriell bedingt ist, können das Vorhandensein prädisponierender Faktoren wie einer fibromuskulären Dysplasie (72-86% Prävalenz bei Patienten mit spontaner Koronardissektion (1, 7, 12)) oder anderen Vaskulopathien (Ehlers-Danlos, Marfan, o.ä.) oder dem akuten Schmerzereignis vorgängiger physischer oder psychischer Stress Hinweise für die Ätiologie des Herzinfarktes liefern (7, 13, 14).
Auf eine sorgfältige Durchführung der Koronarangiographie muss geachtet werden, da das Risiko einer iatrogenen, Katheter-induzierten Koronararterien-Dissektion bei diesen Patienten (3.4% Prävalenz) im Vergleich zur Gesamtpopulation aller Koronarangiographien (< 0.2% Prävalenz) erhöht ist (15). Auch die Verwendung intravaskulärer Bildgebung wie optischer Kohärenztomographie oder von intravaskulärem Ultraschall ist wegen des potenziellen Risikos der Erweiterung der Koronardissektion durch Führungsdraht oder Bildgebungskatheter bzw. der hydraulischen Verlängerung einer Dissektion durch die notwendige Hochdruck-Kontrastmittel-Injektion nur in Ausnahmefällen indiziert, wenn die Diagnose nach der Angiographie unklar bleibt und sich eine therapeutische Konsequenz ergibt (3, 12).
Konservatives Management und Indikation für Revaskularisation
Weil es bei 70-97% der nicht mittels perkutaner oder operativer Revaskularisation behan-
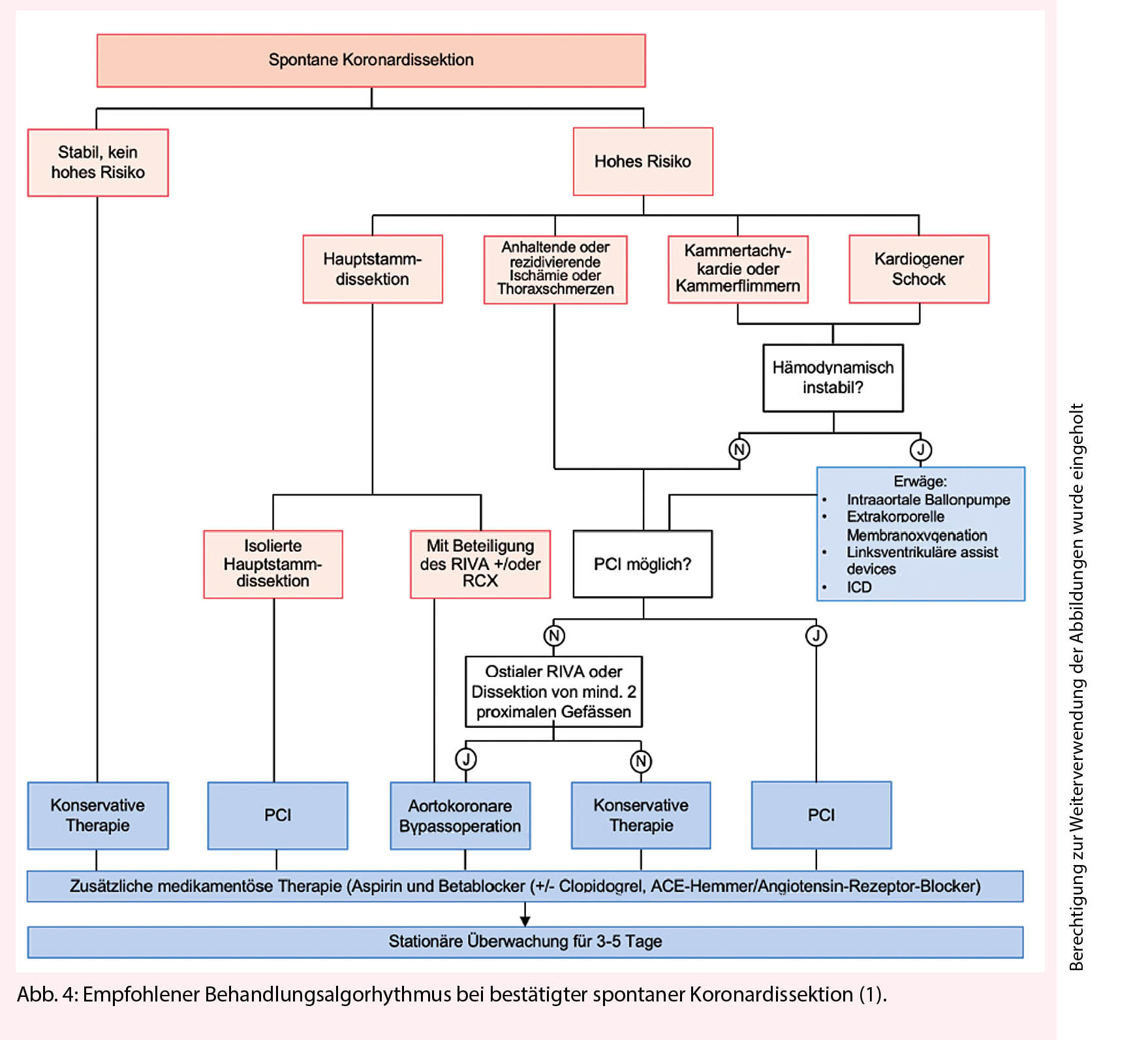
delten Patienten im Verlauf zu einer spontanen «Heilung» der Koronardissektion kommt (5, 11), ist bei klinisch stabilen Patienten ohne Hinweis auf anhaltende Ischämie ein konservativer Therapieansatz zu bevorzugen (3, 7, 11). Durch Ausbreitung des intramuralen Hämatoms kommt es allerdings bei 5-10% der Patienten innerhalb der ersten 7 Tage nach dem initialen Ereignis zu Komplikationen (7, 11), weshalb von Experten eine längere stationäre Überwachung von 3-5 Tagen empfohlen wird (Abb. 4) (1, 3).
Die perkutane Koronarintervention zur Behandlung spontaner Koronardissektionen geht im Vergleich zur Revaskularisation atherosklerotisch bedingter Ursachen mit relativ niedrigen Erfolgsraten (~50-70%; ~10% Bedarf einer notfallmässigen aortokoronaren Bypass-Operation) sowie einem erhöhten Risiko von In-Stent-Restenosen und Stentthrombosen nach Resorption des intramuralen Hämatoms sekundär malapponierter Stents einher (10). Aus diesem Grund sollte die interventionelle oder chirurgische Revaskularisation abhängig von der Koronaranatomie lediglich Hochrisiko-Patienten mit entweder Hauptstamm-Dissektion, anhaltender Ischämie, wiederkehrenden Thoraxschmerzen, ventrikulären Arrhythmien oder hämodynamischer Instabilität vorbehalten bleiben (Abb. 4) (1).
Medikamentöse Therapie
Während nach perkutaner Koronarintervention mit Stent-Implantation im Rahmen eines akuten Koronarsyndroms, egal welcher Ätiologie, eine duale Plättchenhemmung für ein Jahr Sinn macht, so gibt es keine einheitlichen Empfehlungen zur medikamentösen Therapie nach konservativ behandelter spontaner Koronardissektion. Basierend auf Beobachtungsstudien und Registerdaten empfehlen Experten jedoch auch bei spontanen Koronardissektionen als Ursache für einen Herzinfarkt eine langfristige Einnahme von Aspirin. Dies vor allem wenn zusätzlich eine fibromuskuläre Dysplasie vorhanden ist und kein erhöhtes Blutungsrisiko besteht (z.B. Menorrhagien). Die zusätzliche Gabe eines P2Y12-Inhibitors (Clopidogrel bevorzugt gegenüber Ticagrelor oder Prasugrel) ist wegen potentieller Ausbreitung des intramuralen Hämatoms umstritten (12), wird jedoch in Anbetracht des Blutungsrisikos der einzelnen Patienten vielerorts für 1-12 Monate nach einer spontanen Koronardissektion verabreicht (1). Antikoagulation, Thrombolyse und Glycoprotein IIb / IIIa-Inhibitoren sollten vermieden werden. Möglicherweise aufgrund einer verminderten Katecholaminwirkung scheinen Betablocker das Risiko für rezidivierende Koronardissektionen zu senken (1). ACE-Hemmer werden in Hinblick auf ein positives Remodeling der Infarktnarbe eingesetzt. Statine beeinflussen das Rezidivrisiko nicht und sind ausschliesslich Patienten mit begleitender Atherosklerose vorbehalten (6, 12).
Langfristiges Management
Aufgrund häufiger wiederkehrender kardiovaskulärer Ereignisse (50% in 10 Jahren; 35% durch rezidivierende Koronardissektionen) ist eine engmaschige Überwachung unerlässlich (1, 7, 11). Auf extreme körperliche Anstrengungen (insbesondere isometrische Kraftübungen) sollte verzichtet werden. Bei vorangegangener schwangerschaftsassoziierter spontaner Koronardissektion wird von weiteren Schwangerschaften abgeraten (16). Auch exogene Hormontherapien (inklusive Kontrazeption) sollten wegen möglicher Schwächung der arteriellen Media vermieden werden (1). Der Nutzen eines Cardioverter-Defibrillators (ICD) zur Verhinderung eines plötzlichen Herztodes sollte ähnlich wie bei Patienten mit atherosklerotisch bedingter koronarer Herzerkrankung bei rezidivierenden Herzrhythmusstörungen, schwerer Einschränkung der linksventrikulären Pumpfunktion ohne Besserung unter medikamentöser Therapie oder bei nachgewiesenen Myokardnarben in Abwägung der potenziellen Risiken und Komplikationen einer langjährigen ICD-Therapie evaluiert werden. Wegen häufig koexistierender extrakoronarer Dissektionen oder intrakranieller Aneurysmen wird bei Patienten mit spontaner Koronardissektion eine Abklärung anderer Gefässsysteme im Verlauf empfohlen (3, 7, 17). Die Teilnahme an speziellen kardialen Rehabilitationsprogrammen, welche auch psychosoziale Beratung beinhaltet, ist sinnvoll (6).
Copyright bei Aerzteverlag medinfo AG
Klinik für Kardiologie Stadtspital Triemli Zürich
Birmendorferstrasse 497
8063 Zürich
Thomas.gilhofer@triemli.ch
Stadtspital Zürich Triemli
Klinik für Kardiologie
Birmensdorferstrasse 497
8063 Zürich
franz.eberli@triemli.zuerich.ch
Die Autoren haben keine Interessenskonflikte in Zusammenhang mit diesem Artikel.
◆ Im Vergleich zu atherosklerotisch bedingter koronarer Herzerkrankung sind spontane Koronardissektionen mit spezifischen demographischen (>90% Frauen, 35% aller Herzinfarkte bei Frauen <50 Jahren) und prädisponierenden Merkmalen (Vaskulopathien, körperliche und emotionale Trigger) sowie unterschiedlichen diagnostischen, therapeutischen und prognostischen (relativ hohe Rezidivrate) Bedeutungen assoziiert.
◆ Das initiale Management beim Herzinfarkt durch spontane Koronardissektion unterscheidet sich NICHT von dem eines «herkömmlichen» Herzinfarktes. Die rasche Koronarangiographie ist anzustreben.
◆ Die konservative Therapie mit Aspirin und gegebenenfalls Betablockern ist die bevorzugte Behandlungsstrategie. Perkutane oder chirurgische Revaskularisationen sind für Hochrisikopatienten mit hämodynamischer Instabilität oder anhaltender Ischämie reserviert.
Messages à retenir
◆ Par rapport à la coronaropathie athérosclérotique, les dissections coronaires spontanées sont associées à des caractéristiques démographiques (>90% de femmes, 35% de tous les infarctus du myocarde chez les femmes de moins de 50 ans) et prédisposantes (vasculopathies, déclencheurs physiques et émotionnels) spécifiques, ainsi qu’ à des significations diagnostiques, thérapeutiques et pronostiques différentes (taux de récidive relativement élevé).
◆ La prise en charge initiale de l’ infarctus du myocarde dû à une dissection coronaire spontanée n’ est PAS différente de celle de l’ infarctus du myocarde «classique». Une coronarographie promte s’ impose.
◆ Un traitement conservateur avec de l’ aspirine et des bêta-bloquants, si nécessaire, est la stratégie thérapeutique privilégiée. La revascularisation percutanée ou chirurgicale est réservée aux patients à haut risque présentant une instabilité hémodynamique ou une ischémie persistante.
Coronary Artery Dissection. J Am Coll Cardiol. 2016;68(3):297-312.
2. Saw J, Mancini GB, Humphries K, Fung A, Boone R, Starovoytov A, et al. Angiographic appearance of spontaneous coronary artery dissection with intramural hematoma proven on intracoronary imaging. Catheter Cardiovasc Interv. 2016;87(2):E54-61.
3. Hayes SN, Kim ESH, Saw J, Adlam D, Arslanian-Engoren C, Economy KE, et al. Spontaneous Coronary Artery Dissection: Current State of the Science: A Scientific Statement From the American Heart Association. Circulation. 2018;137(19):e523-e57.
4. Hill SF, Sheppard MN. Non-atherosclerotic coronary artery disease associated with sudden cardiac death. Heart. 2010;96(14):1119-25.
5. Rogowski S, Maeder MT, Weilenmann D, Haager PK, Ammann P, Rohner F, et al. Spontaneous Coronary Artery Dissection: Angiographic Follow-Up and Long-Term Clinical Outcome in a Predominantly Medically Treated Population. Catheter Cardiovasc Interv. 2017;89(1):59-68.
6. Saw J, Humphries K, Aymong E, Sedlak T, Prakash R, Starovoytov A, et al. Spontaneous Coronary Artery Dissection: Clinical Outcomes and Risk of Recurrence.
J Am Coll Cardiol. 2017;70(9):1148-58.
7. Saw J, Aymong E, Sedlak T, Buller CE, Starovoytov A, Ricci D, et al. Spontaneous coronary artery dissection: association with predisposing arteriopathies and precipitating stressors and cardiovascular outcomes. Circ Cardiovasc Interv. 2014;7(5):645-55.
8. Faden MS, Bottega N, Benjamin A, Brown RN. A nationwide evaluation of spontaneous coronary artery dissection in pregnancy and the puerperium. Heart. 2016;102(24):1974-9.
9. Vaccarino V, Parsons L, Every NR, Barron HV, Krumholz HM. Sex-based differences in early mortality after myocardial infarction. National Registry of Myocardial Infarction 2 Participants. N Engl J Med. 1999;341(4):217-25.
10. Gilhofer TS, Saw J. Spontaneous coronary artery dissection: update 2019. Curr Opin Cardiol. 2019;34(6):594-602.
11. Lettieri C, Zavalloni D, Rossini R, Morici N, Ettori F, Leonzi O, et al. Management and Long-Term Prognosis of Spontaneous Coronary Artery Dissection. Am J Cardiol. 2015;116(1):66-73.
12. Gilhofer TS, Saw J. Spontaneous coronary artery dissection: a review of complications and management strategies. Expert Rev Cardiovasc Ther. 2019;17(4):
275-91.
13. Henkin S, Negrotto SM, Tweet MS, Kirmani S, Deyle DR, Gulati R, et al. Spontaneous coronary artery dissection and its association with heritable connective
tissue disorders. Heart. 2016;102(11):876-81.
14. Grover P, Fitzgibbons TP. Spontaneous coronary artery dissection in a patient with autosomal dominant polycystic kidney disease: a case report. J Med Case Rep. 2016;10:62.
15. Prakash R, Starovoytov A, Heydari M, Mancini GB, Saw J. Catheter-Induced
Iatrogenic Coronary Artery Dissection in Patients With Spontaneous Coronary Artery Dissection. JACC Cardiovasc Interv. 2016;9(17):1851-3.
16. Tweet MS, Hayes SN, Gulati R, Rose CH, Best PJ. Pregnancy after spontaneous coronary artery dissection: a case series. Ann Intern Med. 2015;162(8):598-600.
17. Olin JW, Gornik HL, Bacharach JM, Biller J, Fine LJ, Gray BH, et al. Fibromuscular dysplasia: state of the science and critical unanswered questions: a scientific statement from the American Heart Association. Circulation. 2014;129(9):1048-78.
18. Saw J. Coronary angiogram classification of spontaneous coronary artery dissection. Catheter Cardiovasc Interv. 2014;84(7):1115-22.
info@herz+gefäss
- Vol. 11
- Ausgabe 5
- September 2021