- Update Herzinsuffizienz – Guidelines 2021
Die im August 2021 von der Europäischen Gesellschaft für Kardiologie (ESC) publizierten neuen Guidelines zur Behandlung der akuten und chronischen Herzinsuffizienz haben einen klaren Kurswechsel in der Behandlungsstrategie der Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) eingeleitet (1). Noch selten hat eine neue Behandlungsrichtlinie in der Herzinsuffizienz die Art und Weise, wie wir Patienten mit HFrEF optimal behandeln, so verändert, wie es die Neuauflage der Guidelines 2021 tut. Im Folgenden werden die wichtigsten Neuerungen in der Behandlung der HFrEF kurz zusammengefasst und in einen klinischen Kontext gestellt.
Vom «Trio» zu den «Fantastischen 4»
Nachdem in den letzten 20 Jahren die klassische RAAS-Inhibition (Renin-Angiotensin-Aldosteron-System Inhibition) die Therapie der HFrEF dominierte, wird nun durch die neuen Guidelines offiziell das Therapie-Armamentarium durch die Hemmung eines weiteren Systems, nämlich des Sodium-Glucose-Transporter Systems, ergänzt. In diesem Sinne wird das traditionelle Trio ARNI (Sacubitril/Valsartan) oder ACE-Hemmer, Betablocker und Mineralocorticoid-Rezeptor Blocker (MRA) durch die Hinzugabe eines SGLT-2 Hemmers ergänzt. Die Landmark Studien DAPA-HF (Dapagliflozin) und EMPEROR-Reduced (Empagliflozin) waren die Wegbereiter für diesen Paradigmenwechsel in der Herzinsuffizienztherapie bei reduzierter systolischer Pumpfunktion (LVEF <= 40%) (2,3). Beide Studien wiesen praktisch deckungsgleich eine hervorragende Reduktion des primären Endpunktes (kardiovaskulärer Tod oder Herzinsuffizienzhospitalisation) um 25% auf, was in einer «number needed to treat» (NNT) von 21 resultierte. Die in den Studien beobachtete prognostische Verbesserung durch die SGLT-2 Hemmer Therapie zeigte sich dabei unabhängig von der Begleittherapie, welche dem bisherigen Therapiestandard entsprach. Der Ritterschlag für die beiden SGLT-2 Hemmer Dapagliflozin und Empagliflozin zur Erstlinientherapie mit höchster Evidenz (Klasse IA Indikation) ist die klinisch wichtigste therapeutische Neuerung der 2021 Guidelines. Da die oben genannten vier Substanzklassen die Mortalität bei HFrEF effektiv senken, werden sie als die «Fantastischen 4» der modernen Herzinsuffizienztherapie bezeichnet (Abb. 1).
In den neuen Guidelines wird die Bedeutung von Sacubitril/Valsartan (ARNI) weiter gestärkt. Der prognostischen Überlegenheit einer Sacubitril/Valsartan Therapie gegenüber einer ACE-Hemmertherapie wurde bereits in den letzten Guidelines (2016) durch die Vergabe einer Klasse I Indikation für den Therapiewechsel bei stabilen ambulanten Patienten Rechnung getragen. Positive Studienergebnisse bei ACE-Hemmer-naiven Patienten und stationären Patienten nach Dekompensation (PIONEER Studie) konnten in der Zwischenzeit die Sicherheit und den prognostischen Nutzen eines frühen Therapiebeginns mit Sacubitril/Valsartan untermauern (4). In diesem Sinne kann neu bei ausgewählten Patienten der Einsatz von Sacubitril/Valsartan als Erstlinientherapie ohne vorherigen Einsatz von ACE-Hemmer erwogen werden (Klasse IIb Indikation). Wird zuerst eine ACE-Hemmer Therapie begonnen ist der Wechsel auf Sacubitril/Valsartan spätestens nach Auftitration des ACE-Hemmers empfohlen (Klasse 1 A Indikation). Dabei muss eine 36-stündige Therapiepause zwischen der letzten Gabe des ACE-Hemmers und der ersten Gabe von Sacubitril/Valsartan eingehalten werden. Die Therapiepause erübrigt sich, wenn von einem Sartan auf Sacubitril/Valsartan gewechselt wird.
Ziel: Zeitnahe Etablierung der «Fantastischen 4»
Das Mantra der langsamen, sequentiellen Auftitration der einzelnen Substanzklassen gemäss dem alten Therapiealgorithmus 1) ACE-Hemmer 2) Betablocker 3) MRA 4) Wechsel von ACE-Hemmer auf ARNI (Sacubitril/Valsartan) hat ausgedient. Neu wird empfohlen die «Fantastischen 4» so schnell wie möglich zu etablieren und in einem zweiten Schritt in der Dosis zu optimieren. Dabei ist die Wahl der Initiierungssequenz der einzelnen Substanzklassen dem Kliniker überlassen und soll sich nach dem hämodynamischen Profil, dem Phänotyp der Herzinsuffizienz und den entsprechenden Komorbiditäten orientieren. Auch die gleichzeitige Initiierung von mehreren Substanzklassen ist möglich, sofern dies die Hämodynamik und die Nierenfunktion, respektive der Elektrolytstatus zulässt. Die Erkenntnis, dass der Einsatz eines SGLT2-Hemmers oder Sacubitril/Valsartan unabhängig von der Dosierung der Begleittherapie bereits innerhalb von 30 Tagen einen entscheidenden prognostischen Vorteil bringt, favorisiert eine möglichst frühe Etablierung aller 4 prognostisch wirksamen Substanzklassen gegenüber einer zeitintensiven, schrittweisen Hinzugabe einer neuen Substanzklasse nach Auftitration der bereits etablierten Substanzklassen. In diesem Sinne heisst das Motto des neuen Therapiealgorithmus: Vollständig Etablieren, dann Auftitrieren.
Grundsätzlich können SGLT-2 Hemmer sehr früh nach Dekompensation oder Erstdiagnose einer Herzinsuffizienz, meist gleichzeitig mit ACE-Hemmern und Betablockern eingesetzt werden, da sie nur gering blutdrucksenkend wirken. Die Sorge um eine Nierenschädigung aufgrund des erwartungsgemäss ansteigenden Kreatinins nach SGLT-2 Hemmergabe (ev. noch ausgeprägter falls kombiniert mit ACE-Hemmer) ist unberechtigt, da der Kreatininanstieg Ausdruck der glomerulären Druckentlastung ist und langfristig nephroprotektiv wirkt. Bei sehr schnell und stark ansteigenden Kreatininwerten sollte allerdings an eine Hypovolämie gedacht und diese korrigiert werden. Patienten mit tendenziell hypertensiven Blutdruckwerten, insbesondere Patienten mit einer hypertensiven Herzkrankheit als führende Aetiologie einer Herzinsuffizienz, können früh, auch de novo mit Sacubitril/Valsartan behandelt werden. Sacubitril/Valsartan kann dabei gleichzeitig mit oder kurz gefolgt von SGLT-2 Hemmer, Betablocker und MRA eingesetzt werden.
Stellenwert von Vericiguat und Eisencarboxymaltose in der Therapie der HFrEF
Während die «Fantastischen 4» wenn immer möglich bei allen Patienten mit HFrEF eingesetzt werden, wird der Einsatz von Vericiguat und/oder Ferocarboxymaltose nur bei bestimmten Patientenprofilen empfohlen.
Vericiguat: Neue Indikation bei HFrEF
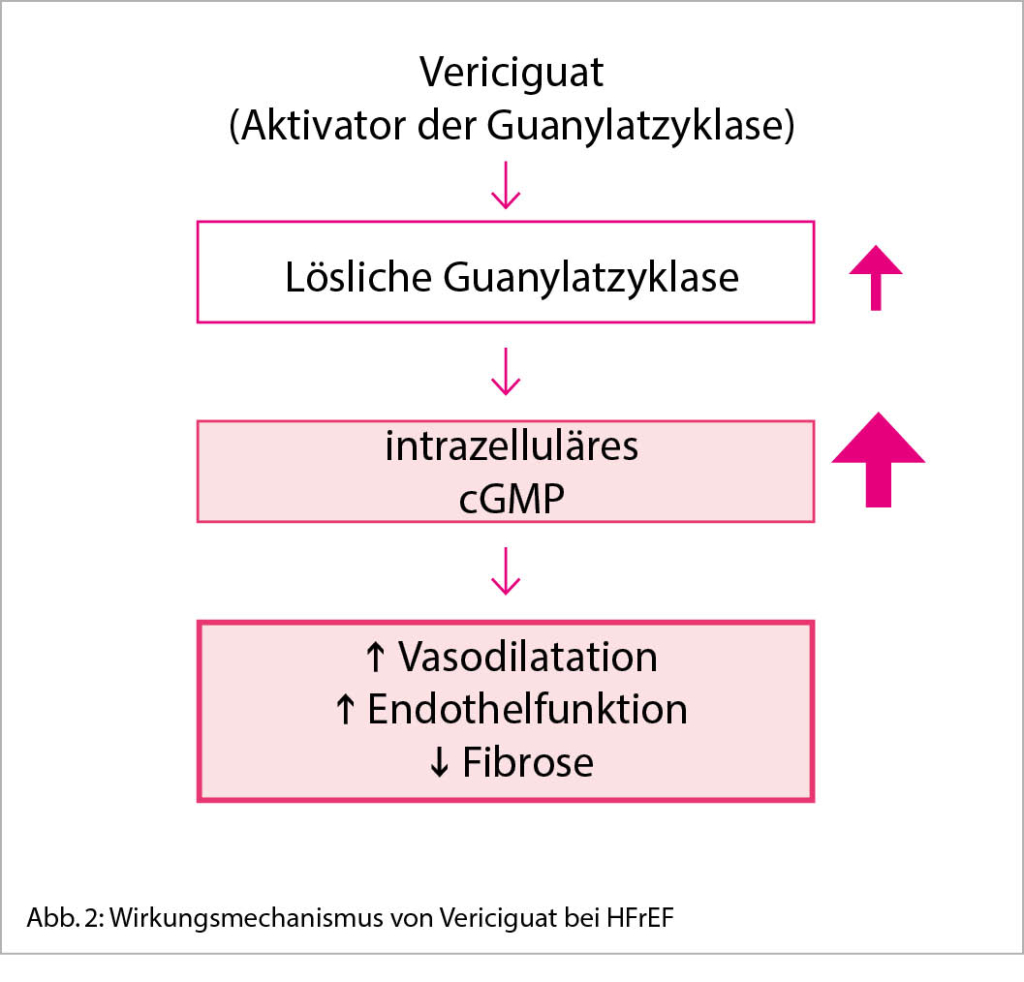
Vericiguat ist ein Aktivator der löslichen Guanylatzyklase und erhöht dadurch die Verfügbarkeit von zyklischem Guanosin-Monophosphat (cGMP), welches eine zentrale Bedeutung für die Endothelfunktion, Vasodilatation und damit für die Herzfunktion hat (Abb. 2). Herzinsuffizienz ist mit einer verminderten NO-Synthese und NO-vermittelten endogenen Aktivierung der Guanylatzyklase verbunden. Dadurch sinken die cGMP-Spiegel, was zu einer Beeinträchtigung der Herz- und Gefässfunktion führen kann. Vericiguat wirkt diesem Pathomechanismus entgegen, indem es die intrazellulären cGMP Spiegel unabhängig von NO hochhält. In der VICTORIA Studie wurde Vericiguat bei symptomatischen Patienten (NYHA II-IV) mit einer LVEF < 45% nach einer kardialen Dekompensation untersucht (5). Dabei führte die Behandlung mit Vericiguat im Vergleich zu Plazebo zu einer signifikanten Reduktion des primären Endpunktes bestehend aus erstmalige Herzinsuffizienzhospitalisation oder kardiovaskulärem Tod. Vericiguat bietet sich deshalb als zusätzliche Therapiemöglichkeit bei Patienten an, welche trotz optimal ausgebauter Herzinsuffizienztherapie ein i.v. Therapie-bedürftiges Dekompensationsereignis erlitten und erfolgreich stabilisiert wurden. Patienten, welche trotz Optimierung des Volumenstatus und der Diuretikatherapie weiterhin sehr hohe NT-proBNP Werte (> 5000 ng/L) aufweisen, sollten nicht mit Vericiguat behandelt werden, da in dieser Situation das Risiko einer Hospitalisation unter Vericiguat möglicherweise erhöht ist. Vor Beginn einer Therapie mit Vericiguat muss deshalb die ausreichende Stabilisierung des Patienten sichergestellt werden. Auch sollte der systolische Blutdruck vor Therapiebeginn > 100 mmHg betragen. Post-hoc Analysen bei Patienten mit Prädisposition für symptomatische Hypotonien attestierten Vericiguat eine gute Verträglichkeit in dieser vulnerablen Patientenpopulation. Sowohl ältere Patienten (> 75 Jahre), als auch Patienten mit bekannt tiefen Blutdruckwerten (100-110 mmHg systolisch), oder Patienten unter gleichzeitiger Therapie mit Sacubitril/Valsartan tolerierten die Therapie gut und profitierten unabhängig von der Höhe des Blutdrucks in Bezug auf eine Reduktion der Herzinsuffizienzhospitalisationen. (6). Da Vericiguat die Nierenfunktion und die Elektrolyte kaum beeinflusst, kann es auch bei fortgeschrittener Niereninsuffizienz bis zu einer glomerulären Filtrationsrate (GFR) von 15 ml/min bedenkenlos eingesetzt werden.
Eisencarboxymaltose: Erweiterte Indikation bei HFrEF
Eisenmangel, definiert als Ferritin < 100ng/ml oder Ferritin 100-300ng/ml bei gleichzeitiger Transferrinsättigung < 20%, ist eine prognostisch bedeutsame Komorbidität bei Patienten mit HFrEF. Jeder zweite Patient mit Herzinsuffizienz leidet an einem Eisenmangel. Neu empfehlen die Guidelines ein systematisches Screening für Eisenmangel bei allen Patienten mit Herzinsuffizienz. Bei symptomatischen Patienten mit einer LVEF < 45% und Eisenmangel wird die intravenöse Gabe von Eisencarboxymaltose zur Verbesserung der Leistungsfähigkeit und Lebensqualität bereits seit 2016 empfohlen. In den neuen Guidelines 2021 wird diese Empfehlung auf Patienten ausgeweitet, die kürzlich wegen Dekompensation stationär behandelt werden mussten. Grundlage für diese Indikationserweiterung ist die AFFIRM-AHF Studie, bei der die intravenöse Therapie mit Eisencarboxymaltose zu einer Reduktion der Re-Hospitalisationsraten nach Herzinsuffizienzdekompensation führte (7).
Einsatz von Life Vest, Defibrillator (ICD) und kardialer Resynchronisationstherapie (CRT)
Die Empfehlungen zum Einsatz einer Life Vest oder eines definitiven implantierten Defibrillators (ICD) haben in den neuen Guidelines nur geringe Adaptationen erfahren. Der Einsatz einer Life Vest kann bei Patienten mit Herzinsuffizienz und hohem Risiko für einen plötzlichen Herztod für eine begrenzte Zeit oder zur Überbrückung bis zu einer Implantation eines definitiven ICD’s erwogen werden. Nach einem Myokardinfarkt empfehlen die Guidelines weiterhin frühestens nach 40 Tagen die Implantation eines definitiven ICD’s, sollte sich die linksventrikuläre Ejektionsfraktion unter optimaler Herzinsuffizienztherapie bis zu diesem Zeitpunkt nicht über 35% erholt haben. Bei Patienten ohne kürzlich stattgehabten Myokardinfarkt soll der Entscheid zur Device Implantation im Rahmen der Primärprävention erst nach 3 Monaten optimaler Herzinsuffizienztherapie gemäss den gängigen LVEF-Kriterien (LVEF ≤ 35%) getroffen werden. Dabei ist zu unterscheiden, ob es sich bei der Kardiopathie um eine ischämische oder eine nicht-ischämische Kardiopathie handelt. Bei Letzterer ist das Risiko eines plötzlichen Herztodes gemäss neueren Daten geringer, weshalb hier ein Downgrading der Indikation von vormals Klasse I (ist empfohlen) auf neu Klasse IIa (sollte erwogen werden) erfolgte. Die kardiale Magnetresonanztomografie kann bei der Risikostratifizierung bezüglich eines plötzlichen Herztodes entscheidend weiterhelfen, indem es Hochrisikopatienten anhand des Ausmasses und Patterns der myokardialen Fibrosierung identifiziert. Auch bei der Indikation einer kardialen Resynchronisationtherapie wird nur noch bei einer LVEF ≤ 35% mit Linksschenkelblock und QRS-Dauer > 150 ms die höchste Empfehlung (Klasse I) ausgesprochen. Hingegen wurde die Empfehlung bei Linksschenkelblock mit schlankerem QRS-Komplex (QRS 130 – 149 ms) auf eine IIa Empfehlung herabgestuft.
Copyright bei Aerzteverlag medinfo AG
Klinik für Kardiologie
Universitätsspital Basel
Petersgraben 4
4031 Basel
otmar.pfister@usb.ch
Der Autor deklariert keine Interessenskonflikte im Zusammnehang mit diesem Artikel zu haben.
◆ Die «Fantastischen 4» (ARNI oder ACE-Hemmer, Betablocker, Mineralocorticoid Antagonist, SGLT-2 Hemmer) sind der neue Therapiestandard bei Herzinsuffizienz mit reduzierter Pumpfunktion (LVEF ≤40%)
◆ Die «Fantastischen 4» sollten früh (wenn möglich noch stationär) begonnen werden und ambulant auftitriert werden (Grundsatz: vollständig etablieren, dann auftitrieren)
◆ Die Korrektur eines Eisenmangels früh nach kardialer Dekompensation reduziert Herzinsuffizienz-Hospitalisationen
◆ Vericiguat ist eine neue Therapieoption für Patienten nach Dekompensation trotz optimaler Therapie. Kann auch bei schwerer Niereninsuffizienz eingesetzt werden.
1. McDonagh TA et al. Eur Heart J 2021
2. McMurray JJV et al. N Engl J Med 2019 (DAPA)
3. Packer M et al. N Engl J Med 2020
4. Morrow DA et al. Circulation 2019
5. Armstrong PW et al. New Engl J Med 2020
6. Lam CSP et al. J Am Heart Association 2021
7. Ponikowski P et al. Lancet 2020
info@herz+gefäss
- Vol. 12
- Ausgabe 2
- März 2022