- Eskalation und Deeskalation der Therapie bei Hochrisikomelanomen
Das fortgeschrittene Melanom war lange Zeit eine schwer behandelbare Erkrankung ohne wirksame Überlebensstrategien. Mit der Entwicklung von Checkpoint-Inhibitoren und Kinaseinhibitoren im 21. Jahrhundert haben sich die Therapieoptionen erheblich verbessert. Neueste Studien zeigen, dass die adjuvante Therapie mit Anti-PD1-Antikörpern das rezidivfreie Überleben bei Patienten im Stadium IIB/C ohne Lymphknotenbefall signifikant verbessert. Allerdings besteht die Herausforderung, die richtigen Patienten für eine Langzeitbehandlung zu identifizieren, da viele durch chirurgische Massnahmen allein geheilt werden könnten. Die neoadjuvante Therapie, bei der die systemische Therapie vor der operativen Entfernung der makroskopischen Lymphknotenmetastasen erfolgt, hat sich als vielversprechend erwiesen. Neoadjuvante Ansätze, insbesondere mit Anti-PD1-Antikörpern, können die Rezidivrate signifikant senken. Die histologische Analyse des Tumorgewebes nach neoadjuvanter Therapie könnte zudem helfen, Patienten zu identifizieren, die keine zusätzliche adjuvante Behandlung benötigen, was die Nebenwirkungen und Kosten reduziert. Die Implementierung der neoadjuvanten Therapie in die klinische Praxis ist jedoch mit Herausforderungen wie der fehlenden Zulassung in der Schweiz und der Notwendigkeit spezialisierter histopathologischer Beurteilungen verbunden. Zukünftige Forschungsanstrengungen sollten sich darauf konzentrieren, Kriterien zur Patientenselektion zu entwickeln und die Rolle histopathologischer Untersuchungen in der Prognose zu validieren. Eine Deeskalation der Therapieansätze könnte zu einer patientenorientierteren, ressourcenschonenden Medizin führen.
For a long time, advanced melanoma was a difficult-to-treat disease with no effective survival strategies. With the development of checkpoint inhibitors and kinase inhibitors in the 21st century, treatment options have improved considerably. Recent studies indicate that adjuvant therapy with anti-PD1-antibodies significantly improves the recurrence-free survival in stage IIB/C patients without lymph node involvement. However, the challenge is to identify the right patients for long-term treatment, as many could be cured by surgery alone. Neoadjuvant therapy, in which systemic treatment is administered before the surgical removal of the macroscopic lymph node metastases, has proven to be promising. Neoadjuvant approaches, particularly with anti-PD1-antibodies, can significantly reduce the recurrence rate. Additionally, histological analysis of tumor tissue after neoadjuvant therapy could help identify patients who do not require further adjuvant treatment, thereby reducing side effects and costs. However, the implementation of neoadjuvant therapy in clinical practice faces challenges, such as the lack of approval in Switzerland and the need for specialized histopathological assessments. Future research efforts should focus on developing criteria for patient selection and validating the role of histopathological examinations in prognosis. A de-escalation of therapeutic approaches could lead to more patient-centered, resource-efficient medicine.
Keywords: Melanoma, high-risk, neoadjuvant, adjuvant, therapy
Einleitung
Das fortgeschrittene Melanom gehörte jahrzehntelang zu den Erkrankungen ohne Therapieansätze mit nachgewiesenem Einfluss auf das Überleben, bis im ersten und zweiten Jahrzehnt unseres Jahrtausends neue therapeutische Ansätze wie die Therapie mit Checkpoint-Inhibitoren oder mit Kinaseinhibitoren für diesen Tumor entwickelt wurden.
Die neuen therapeutischen Ansätze wurden inzwischen auch im adjuvanten Bereich erfolgreich etabliert. Zuletzt zeigten klinische Studien, dass die adjuvante Therapie mit Anti-PD1-Antikörpern auch im Stadium IIB/C (ohne Lymphknotenbefall) die Prognose deutlich verbessert. Es muss allerdings darauf hingewiesen werden, dass in dieser Situation zahlreiche Patienten behandelt werden, die durch die chirurgischen Massnahmen allein geheilt wären. Deshalb stellt sich hier die Frage, wie wir die richtigen Patienten für eine Langzeitbehandlung identifizieren können. Die neoadjuvante Therapie ist in diesem Zusammenhang eine interessante Option (1).
Aktuelle Studienergebnisse zur adjuvanten und neoadjuvanten Therapie beim Melanom
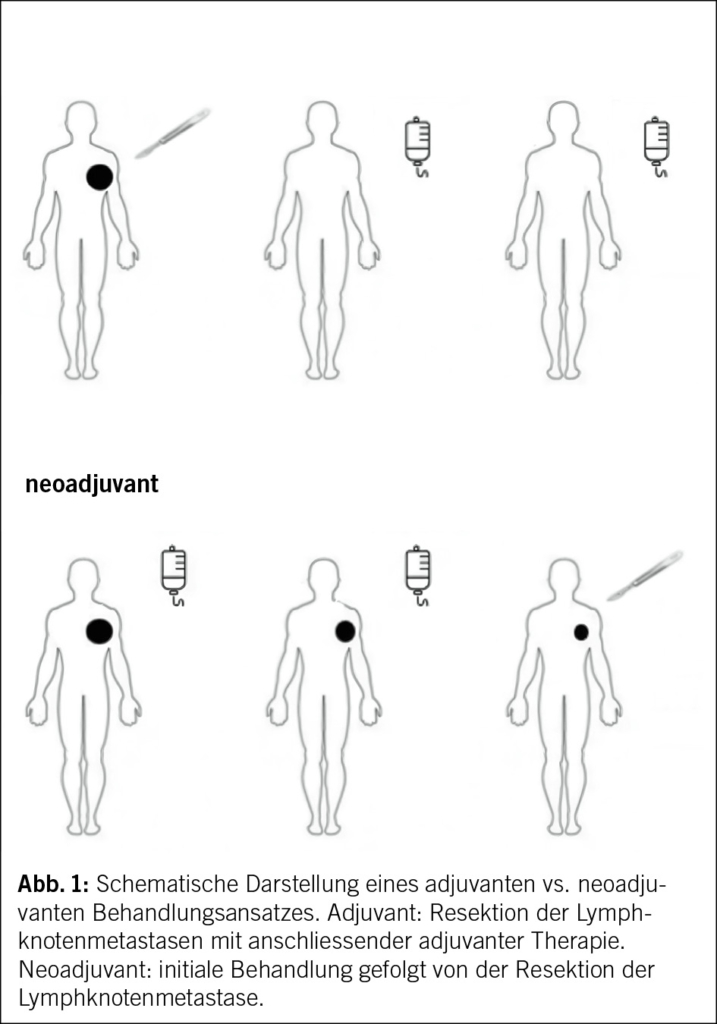
In der adjuvanten/neoadjuvanten Therapie des Melanoms haben vor allem Anti-PD1-Antikörper die Behandlungsergebnisse revolutioniert. Aufgrund prospektiv randomisierter Studien sind inzwischen die Anti-PD1-Antikörper Nivolumab und Pembrolizumab sowie die Kinaseinhibitor-Kombination Dabrafenib und Trametinib zur adjuvanten Therapie des Melanoms seit mehreren Jahren zugelassen. Während bei der adjuvanten Therapie zunächst sämtliche Tumormanifestationen chirurgisch entfernt werden und dann vorbeugend eine Therapie typischerweise für die Dauer von einem Jahr erfolgt, wird der Operationszeitpunkt bei der neoadjuvanten Therapie verschoben (Abb. 1). Das bedeutet, dass zunächst eine Systemtherapie eingeleitet wird, für etwa 8–12 Wochen. Danach wird die Tumormanifestation operativ entfernt.
Die Durchführbarkeit und der Langzeitnutzen dieser neuen, neoadjuvanten Strategie wurden für mehrere Medikamente bereits gezeigt. In grösseren Phase-II-Studien mit der Kombination von Ipilimumab und Nivolumab zeigte sich eine unerwartet hohe Rate von Rezidivfreiheit (2).
Inzwischen liegen auch prospektiv randomisierte Studien vor. So wurde zum Beispiel die intraläsionale Therapie mit dem gentechnologisch modifizierten Herpes-simplex-Virus TVEC prospektiv randomisiert untersucht (3). Dabei erhielt ein Teil der Patienten 6 Injektionen mit diesem Virus, bevor die Operation durchgeführt wurde. Die anderen Patienten wurden konventionell behandelt. Adjuvante Therapien konnten nach Ermessen der Studienzentren nach Wahl durchgeführt werden. Bei der Auswertung zeigte sich, dass die Patienten im Kontrollarm mehr adjuvante Therapien erhalten hatten. Für diese Studie liegen nun Langzeitergebnisse vor. Es findet sich ein deutlicher Vorteil bezüglich rezidivfreiem Intervall, aber auch eine verbesserte Überlebensrate nach 5 Jahren für die neoadjuvant behandelten Patienten.
Eine weitere grössere prospektiv randomisierte Studie hat die adjuvante Therapie mit Pembrolizumab direkt verglichen mit der neoadjuvanten Therapie (4). Im Rahmen dieser Studie waren die Zahl und die Dosis der Immuntherapie in beiden Therapiearmen gleich. Einzig wurde der Operationszeitpunkt im neoadjuvanten Arm um ca. 12 Wochen verzögert. Die Auswertung dieser Studie zeigte einen erstaunlichen Vorteil für die Patienten, die neoadjuvant behandelt wurden. Die Rezidivrate konnte um etwa 40 % gesenkt werden.
In der neuesten Phase-III-Studie wurden Patienten mit resektablem, makroskopischem Stadium-III-Melanom randomisiert in zwei Gruppen eingeteilt: Eine erhielt 2 Zyklen neoadjuvanter Therapie mit Ipilimumab und Nivolumab, gefolgt von einer Operation, während die andere Gruppe zuerst operiert wurde und anschliessend 12 Zyklen adjuvanter Nivolumab-Therapie erhielt (5). Mit der neoadjuvanten Therapie konnte eine signifikant überlegene Ereignisfreiheit im Vergleich zur adjuvanten Therapie erzielt werden. Die neoadjuvante Therapie führte bei der Mehrheit der Patienten zu einem erstaunlichen pathologischen Ansprechen (komplettes bzw. fast komplettes Ansprechen bei 59 %). Im Vergleich dazu lag die rezidivfreie Überlebensrate bei den neoadjuvant behandelten Patienten mit partiellem oder fehlendem pathologischen Ansprechen trotz anschliessender adjuvanter Therapie über 12 Monate deutlich niedriger (76.1 % bzw. 57 %).
Aufgrund dieser randomisierten Studien wird die neoadjuvante Therapie bereits heute standardmässig in verschiedenen Behandlungsguidelines empfohlen und wurde u. a. mit Anti-PD-Inhibitor bereits in Australien für diese neue Indikation zugelassen.
Während die neoadjuvante Behandlung mit den Tyrosinkinaseinhibitoren Dabrafenib plus Trametinib im Vergleich zur neoadjuvanten Anti-PD1-Therapie zu hohen pathologischen Ansprechraten führte, hatten Patienten mit komplettem pathologischem Ansprechen jedoch immer noch ein hohes Rezidivrisiko. Im Gegensatz dazu sind die Unterschiede zwischen BRAF-/MEK-Inhibitor-Therapie und Anti-PD1-Therapie im adjuvanten Ansatz nicht so markant, da sowohl die Kinaseinhibitor-Kombination als auch Anti-PD-1(Programmed cell death protein-1)-Antikörper das Rezidivrisiko in ähnlicher Weise verringern.
Wie in der Einführung erwähnt, liegt ein Problem in der adjuvanten/neoadjuvanten Therapie darin, dass viele Patienten unnötigerweise einer toxischen Therapie exponiert werden.
Hier bietet insbesondere der neoadjuvante Therapieeinsatz eine überzeugende Option zur präzisen Abschätzung der Therapiebedürftigkeit. Bei der operativen Entfernung nach der neoadjuvanten Therapiephase wird das entfernte Gewebe histologisch aufgearbeitet und der Anteil an Tumorgewebe bestimmt. Ein erheblicher Teil der Patienten zeigt bei dieser Untersuchung keine Tumorreste mehr, sondern nur noch entzündliche Veränderungen. Diese als histologisch komplette oder fast komplette Remission bezeichneten Phänomene erlauben es möglicherweise, die Notwendigkeit einer weiteren adjuvanten Therapie abzuschätzen. So weisen die Ergebnisse einer grossen internationalen Studie darauf hin, dass Patienten mit kompletter oder fast kompletter pathologischer Remission keiner zusätzlichen Behandlung mehr bedürfen. Damit könnte die adjuvante Therapie für diese Patienten verkürzt werden sowie potenzielle Nebenwirkungen und Kosten reduziert werden (2). Es ist jedoch eine längere Nachbeobachtungszeit erforderlich, bevor dieses Behandlungskonzept in der klinischen Praxis eingesetzt werden kann.
Die Einführung der neoadjuvanten Therapie in die klinische Routine ist jedoch mit einigen Schwierigkeiten verbunden.
So ist zum Beispiel in der Schweiz die neoadjuvante Therapie nicht zugelassen. Da die Studien zu diesem Therapieansatz in der Regel nicht durch pharmazeutische Unternehmen gesponsert wurden, sind sie auch kaum in der Lage, die Zulassung dieser Therapieform zu beantragen. Ein weiteres Problem ist die korrekte Ausführung der Operation mit der Entfernung der wichtigen Referenzmetastase und die kompetente histopathologische Aufarbeitung. Dies erfordert sehr viel Erfahrung. Spezialisierte pathologische Zentren für diese wichtige Aufgabe gibt es kaum.
Trotz der beeindruckenden klinischen Daten zu neoadjuvanten Therapien beim Hochrisikomelanom bleiben zum aktuellen Zeitpunkt noch Fragen offen, wie zum Beispiel: Was für Daten sind erforderlich, um die klinische Praxis in der Chirurgie des Melanoms zu ändern?
Fazit und Ausblick
Die erfolgreiche Einführung der Immun- und zielgerichteten Behandlungen im Frühstadium des Melanoms führt zu einer grossen Patientenpopulation, die für diese Behandlungen qualifiziert. Je mehr frühere Krankheitsstadien diesen Behandlungen zugeführt werden, desto höher ist der Anteil an Patienten, die unnötig behandelt werden. Hier stellt sich definitiv die Frage der richtigen Patientenselektion. Die Aufgabe der akademischen Zentren heute besteht nun darin, Kriterien zu erarbeiten, wie Patienten selektioniert werden können. Neben zahlreichen molekularbiologischen Ansätzen (5) erscheint hier der neoadjuvante Ansatz vielversprechend, weil er die Reaktion des Tumorgewebes auf eine Behandlung histologisch analysieren kann. Aus den Ergebnissen kann abgeleitet werden, ob und welche therapeutischen Massnahmen später noch nötig sein werden. Wird die Verlässlichkeit der histopathologischen Untersuchungen für die Prognose weiter bestätigt, können vielleicht sogar bildgebende Verfahren in der Nachsorge dieser Patienten reduziert werden.
Deeskalation von therapeutischen Strategien ist eine wichtige Aufgabe der modernen personalisierten, ressourcenbewussten Medizin.
Prof. Dr. med. Reinhard Dummer 1,2
Dr. med. Lara Valeska Maul 1
Dr. med. Egle Ramelyte 1
PD Dr. med. Joanna Mangana 1
1 Klinik für Dermatologie, Universitätsspital Zürich, Rämistrasse 100, 8091 Zürich
2 Kantonsspital Aarau, Hautkrebszentrum, Bahnhofplatz 3C, 5001 Aarau
Copyright
Aerzteverlag medinfo AG
Zweitabdruck aus Therapeutische Umschau 05/25
– Senior Consultant
Klinik für Dermatologie
Universitätsspital Zürich
Rämistrasse 100, 8091 Zürich
reinhard.dummer@usz.ch
– Leiter Hautkrebszentrum
Kantonsspital Aarau, Hautkrebszentrum
Bahnhofplatz 3C
5001 Aarau
reinhard.dummer@ksa.ch
Klinik für Dermatologie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
Klinik für Dermatologie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
Prof. Dr. med. Reinhard Dummer erklärt potenzielle Interessenkonflikte mit: Novartis, Merck Sharp & Dhome (MSD), Bristol Myers Squibb (BMS), Roche, Amgen, Takeda, Pierre Fabre, Sun Pharma, Sanofi, Catalym, Second Genome, Regeneron, T3 Pharma, MaxiVAX SA, Pfizer und Simcere. Er ist Senior Medical Advisor bei Oncobit.
Dr. med. Lara Valeska Maul erklärt potenzielle Interessenkonflikte mit: Almirall, Amgen, Bristol Myers Squibb (BMS), Canfield, Eli Lilly, Incyte, Merck Sharp & Dohme (MSD), Novartis, Pierre Fabre, Roche und Sanofi.
Dr. med. Egle Ramelyte erklärt potenzielle Interessenkonflikte mit: Bristol Myers Squibb, Merck Sharp & Dohme, Pierre Fabre, Amgen, Sanofi, Kyowa Kirin, Takeda, Elli Lilly, Leo Pharma.
Kongress/Reiseunterstützung: Sanofi, Pierre Fabre, Kyowa Kirin, Galderma.
PD Dr. med. Joanna Mangana erklärt potenzielle Interessenkonflikte mit: Merck/Pfizer, Merck Sharp & Dohme, Novartis, Roche, Pierre Fabre, Amgen, Bristol Myers Squibb.
Kongress/Reiseunterstützung: Ultrasun, L’Oreal, Merck Sharp & Dohme, Bristol Myers Squibb und Pierre Fabre.
- Die Einführung neuer Medikamente hat die Heilungsaussichten beim Hochrisikomelanom deutlich verbessert. Der frühzeitige Einsatz vor allem im neoadjuvanten Ansatz führt zur Reduktion chirurgischer Massnahmen und Verbesserung der Lebensqualität.
1. Garbe C, Dummer R, Amaral T, et al. Neoadjuvant immunotherapy for melanoma is now ready for clinical practice. Nat Med 2023;29:1310–2. https://doi.org/10.1038/s41591-023-02336-1.
2. Reijers ILM, Menzies AM, van Akkooi ACJ, Versluis JM, van den Heuvel NMJ, Saw RPM, et al. Personalized response-directed surgery and adjuvant therapy after neoadjuvant ipilimumab and nivolumab in high-risk stage III melanoma: the PRADO trial. Nat Med 2022;28:1178–88. https://doi.org/10.1038/s41591-022-01851-x.
3. Dummer R, Gyorki DE, Hyngstrom J, et al. Neoadjuvant talimogene laherparepvec plus surgery versus surgery alone for resectable stage IIIB-IVM1a melanoma: a randomized, open-label, phase 2 trial. Nat Med 2021;27:1789–96. https://doi.org/10.1038/s41591-021-01510-7.
4. Patel SP, Othus M, Chen Y, et al. Neoadjuvant-Adjuvant or Adjuvant-Only Pembrolizumab in Advanced Melanoma. N Engl J Med 2023;388:813–23. https://doi.org/10.1056/NEJMoa2211437.
5. Blank CU, Lucas MW, Scolyer RA, et al. Neoadjuvant Nivolumab and Ipilimumab in Resectable Stage III Melanoma. N Engl J Med. 2024 Jun 2. doi: 10.1056/NEJMoa2402604.
6. Irmisch A, Bonilla X, Chevrier S, et al. The Tumor Profiler Study: integrated, multi-omic, functional tumor profiling for clinical decision support. Cancer Cell 2021;39:288–93. https://doi.org/10.1016/j.ccell.2021.01.004.
der informierte @rzt
- Vol. 15
- Ausgabe 12
- Dezember 2025