- Highlights vom ELCC Congress 2026
Vom 25. bis 28. März fand in Kopenhagen, Dänemark, der European Lung Cancer Congress (ELCC) 2026 statt. Rund 4000 Teilnehmer aus über 80 Ländern nahmen dieses Jahr am Kongress teil. Von den über 480 präsentierten Abstracts werden im Folgenden einige Highlights vorgestellt.
Pharma-Info: Unser erstes Video vom ELCC in Kopenhagen, organisiert von PharmaMar
Wie lassen sich aktuelle Fortschritte in der SCLC-Behandlung in die Praxis der schweizerischen Versorgungslandschaft übertragen?
Vielversprechende Wirksamkeit insbesondere bei höheren Dosen von Obrixtamig und bei Patienten mit SCLC
Julien Mazieres, et al. 409O A phase I dose escalation trial of obrixtamig + ezabenlimab in patients (pts) with small cell lung cancer (SCLC) or other neuroendocrine carcinomas (NECs) expressing DLL3
Vorbemerkungen
DLL3 ist häufig auf NECs, darunter SCLC, zu finden. Obrixtamig, ein DLL3/CD3-T-Zell-Engager, erhöht in SCLC-Modellen PD-1 und PD-L1. Die Kombination mit dem Immun-Checkpoint-Inhibitor Ezabenlimab könnte die Antitumorwirkung steigern. In einer Phase-I-Studie (NCT05879978) wird Obrixtamig plus Ezabenlimab bei fortgeschrittenen oder rezidivierten DLL3-positiven NECs getestet.
Studiendesign
• Die Studie schloss Patienten ein, bei denen mindestens eine Linie einer platinbasierten Chemotherapie versagt hatte oder die für die Standardtherapie (SoC) nicht in Frage kamen.
• Obrixtamig wurde wöchentlich in 3-Wochen-Zyklen verabreicht (1 Zyklus mit Dosissteigerung x3; anschliessend Zieldosis 30–1080 µg/kg); Ezabenlimab 240 mg wurde alle 3 Wochen verabreicht.
• Die Dosiseskalation erfolgte nach einem Bayes’schen Modell mit Überdosiskontrolle.
• Primärer Endpunkt: DLTs während des MTD-Bewertungszeitraums (Zyklus 1 + 1 Woche Zieldosis); weitere Endpunkte waren ORR, DCR und PFS.
Baseline
• Es erhielten 45 Patienten ≥ 1 Behandlungszyklus; Median der Zyklen: 5 (Bereich 1–31);
• Medianalter: 57 Jahre (Bereich 33–78); ECOG-PS 0/1: 33 %/67 %; vorherige Anti-PD-1/PD-L1-Therapie: 49 %.
Verträglichkeit
• Während der Dosiseskalationsphase traten drei DLTs auf, bei den Zieldosen keine; die MTD wurde nicht erreicht.
• Die häufigsten TRAEs sind unten aufgeführt.
• TRAEs des Grades (G)=3 traten bei 51 % der Patienten auf.
• 13 % der Patienten brachen die Behandlung aufgrund von TRAEs ab.
• Obrixtamig-bedingte neurologische unerwünschte Ereignisse (UE) des Grades 3 traten bei 3 (7 %) Patienten auf (ICANS [n = 2], Enzephalopathie).
• Es wurde kein CRS des Grades 3 beobachtet.
Behandlungsresultate
• 40 Patienten erhielten die klinisch wirksame Dosis von ≥ 90 µg/kg Obrixtamig.
• Bei diesen Patienten betrugen die ORR 30 %, die DCR 58 %, das mPFS 4,4 Monate und das mDoR 8,8 Monate.
• Bei der höchsten Dosis (1080 µg/kg; n = 12) betrugen die ORR 58 %, die DCR 83 %, das mPFS 10 Monate und das mDoR 8,8 Monate.
• Bei 18 Patienten mit SCLC in den Kohorten mit =90 µg/kg betrugen die ORR 33 %, die DCR 67 %, das mPFS 5,7 Monate und das mDoR NC.
Fazit
Obrixtamig + Ezabenlimab zeigte bei Patienten mit vorbehandelten DLL3+-NECs ein überschaubares Sicherheits- und Verträglichkeitsprofil. Eine laut den Studienautoren vielversprechende Wirksamkeit wurde insbesondere bei höheren Dosen von Obrixtamig und bei Patienten mit SCLC beobachtet.
Osimertinib plus CTx verlängert das PFS im Vergleich zur osi-Monotherapie bei fortgeschrittenem EGFRm-NSCLC mit TP53-Komutationen signifikant
Yunpeng Yang, et al. 2O Osimertinib (osi) with or without chemotherapy (CTx) as first-line treatment in EGFR-mutant (EGFRm) advanced NSCLC with concurrent TP53 mutations (TOP study)
Vorbemerkungen
TP53-Mutationen kommen bei EGFRm-NSCLC häufig vor und verschlechtern das Ergebnis einer EGFR-TKI-Monotherapie. Die FLAURA2-Studie zeigte, dass Osimertinib plus Chemotherapie wirksamer ist, aber ob TP53-Komutierte besonders profitieren, ist offen. Diese Phase-III-Studie untersucht genau diesen Aspekt bei Hochrisikopatienten.
Studiendesign
• Teilnahmeberechtigt waren erwachsene Patienten mit zuvor unbehandeltem fortgeschrittenem nicht-squamösem NSCLC, die EGFR-Ex-19-del/L858R-Mutationen und begleitende TP53-Mutationen aufwiesen.
• Die Patienten wurden im Verhältnis 1:1 randomisiert und erhielten entweder osi + CTx (osi 80 mg einmal täglich + Pemetrexed 500 mg/m² + Carboplatin AUC5, alle 3 Wochen über 4 Zyklen, gefolgt von osi 80 mg einmal täglich + Pemetrexed 500 mg/m² alle 3 Wochen)
• oder eine osi-Monotherapie (80 mg einmal täglich) bis zum Fortschreiten der Erkrankung oder bis zum Auftreten nicht tolerierbarer Toxizitäten.
• Die Patienten wurden nach WHO-PS (0/1), Vorliegen von Hirnmetastasen (ja/nein) und Mutationstypen (Ex19del/L858R) stratifiziert.
Baseline
• 294 Patienten wurden randomisiert der Gruppe „Osi + CTx“
(n = 146) oder der Gruppe „Osi“ (n = 148) zugewiesen.
• Ausgangsmerkmale: medianes Alter 57/57 Jahre; 51/56 % weiblich; 54/55 % Ex19del; 46/45 % L858R; 49/48 % ZNS-Metastasen.
Behandlungsresultate
• Osi + CTx verbesserte das PFS signifikant gegenüber Osi (HR 0,44; 95 % KI 0,32–0,61; p < 0,001; 59 % Reifegrad).
• Das mediane PFS betrug 34,0 gegenüber 15,6 Monaten. Dieser Vorteil war in allen vorab definierten Subgruppen konsistent, einschliesslich derjenigen mit ZNS-Metastasen oder L858R-Mutationen.
• Die ORR betrug 82,9 % in der Osi + CTx-Gruppe und 72,0 % in der Osi-Gruppe, und die mediane DoR betrug 32,7 Monate bzw. 15,3 Monate.
• Die OS war noch nicht ausgereift (30,6 %), es wurde ein Trend zu einem OS-Nutzen beobachtet, HR 0,57 (95 % KI 0,37, 0,87).
Verträglichkeit
• TRAE aller Grade ≥ 3 (osi + CTx/osi): 62,4 %/14,9 %; es wurden keine neuen Sicherheitssignale festgestellt.
Fazit
Dies ist die erste prospektive Phase-III-Studie, die laut den Studienautoren zeigt, dass osi plus CTx das PFS im Vergleich zur osi-Monotherapie bei fortgeschrittenem EGFRm-NSCLC mit TP53-Komutationen signifikant verlängert. Diese Ergebnisse deuten darauf hin, dass diese Hochrisikopopulation möglicherweise stärker von einer Kombinationstherapie profitiert.
Zeitpunkt der ersten ICI-Gabe könnte in der ersten Tageshälfte eine umsetzbare Intervention sein
Solange Peters, et al. LBA2 ETOP-Roche i-TIMES: Immunotherapy timing investigation on lung cancer survival
Vorbemerkungen
Die i-TIMES-Studie untersuchte, ob der Zeitpunkt der Immun-Checkpoint-Inhibitor-Gabe (früh oder spät am Tag) das Überleben von Lungenkrebspatienten beeinflusst. Zudem wird geprüft, ob dies auch für andere solide Tumoren gilt.
Studiendesign
• Für die Analyse kamen von Roche gesponserte Phase-II- oder Phase-III-RCTs in Frage, die mindestens einen ICI-Arm (allein oder in Kombination mit einer anderen Behandlung) und das OS als einen der primären Endpunkte aufwiesen.
• Die primäre Kohorte umfasst Lungenkrebspatienten mit ≥ 2 Zyklen ICI-Gaben und verfügbaren Zeitangaben.
• Die Einteilung des Zeitpunkts der ICI-Gabe basiert auf dem Beginn der ersten beiden Zyklen: Früh: bis 12:00 Uhr; Spät: nach 12:00 Uhr.
Behandlungsresultate
• Die primäre Zielkohorte umfasst 3165 Patienten mit einer medianen Gesamtnachbeobachtungszeit von 42,6 Monaten (m).
• 1272 (40 %) wurden der Early-Gruppe zugeordnet, 1014 (32 %) der Late-Gruppe, während 879 (28 %) Patienten einen gemischten Zeitpunkt aufwiesen.
• Das Matching-Verfahren führte zu einer endgültigen Analysekohorte von 1610 Patienten (805 in jeder Gruppe; 580 Todesfälle in der Early-Gruppe; 601 in der Late-Gruppe).
• Die mediane Gesamtüberlebenszeit (OS) betrug 18,4 Monate (95 %-KI 16,5–19,8) in der Early-Gruppe und 15,9 Monate (14,3–17,5) in der Late-Gruppe.
• Die entsprechende OS-HR für „Spät“ gegenüber „Früh“, stratifiziert nach Studie, betrug 1,104 (95 % KI 0,984–1,238), wobei die Obergrenze des 95 % KI den vorab festgelegten Grenzwert überschritt.
• In einer Sekundäranalyse der jeweiligen Lungenkrebspatienten, die nur mit Chemotherapie behandelt wurden und ähnlich gematcht waren (n = 516), betrug das OS-HR 0,817 (95 % KI 0,673–0,992) zugunsten der späten Verabreichung.
Fazit
i-TIMES konnte keine Nichtunterlegenheit der späten gegenüber der frühen Verabreichung der ersten beiden ICI-Zyklen (allein oder in Kombination mit Chemotherapie) hinsichtlich des OS bei Lungenkrebspatienten nachweisen, was die Diskussion eröffnet, dass der Zeitpunkt der ersten ICI-Gabe in der ersten Tageshälfte eine umsetzbare Intervention sein könnte.
Für die Studie verantwortliche juristische Person: ETOP IBCSG Partners Foundation.
MK-1084 + Pembrolizumab zeigte in der KANDLELIT-001-Studie eine klinisch bedeutsame Wirksamkeit
Adrian Sacher, et al. 4MO Updated results for MK-1084 + pembrolizumab in KRAS G12C-mutated (mut) metastatic non-small cell lung cancer (mNSCLC) enrolled in KANDLELIT-001
Vorbemerkung
Die Phase-I-Studie KANDLELIT-001 (NCT05067283) bestätigt laut Forschern, dass der orale, selektive KRAS-G12C-GDP-Kovalenzinhibitor der nächsten Generation MK-1084 ein gutes Sicherheitsprofil aufweist und vielversprechende Antitumoraktivität zeigt. Er wurde entweder allein oder in Kombinationstherapie bei Patienten mit soliden Tumoren, die eine KRAS-G12C-Mutation besitzen, eingesetzt.
Die Autoren berichten über aktualisierte Daten für Patienten mit KRAS-G12C-mutiertem mNSCLC.
Studiendesign
• Patienten in den Armen 1 und 3 wiesen einen beliebigen KRAS-G12C-mutierten soliden Tumor mit mindestens einer vorangegangenen systemischen Therapie auf und erhielten eine MK-1084-Monotherapie mit 25–800 mg/Tag.
• Patienten in Arm 2 hatten unbehandeltes mNSCLC mit einem PD-L1-TPS von ≥ 1 % und erhielten MK-1084 25–400 mg/Tag + Pembrolizumab 200 mg alle 3 Wochen.
• Patienten in Arm 4 hatten unbehandeltes nicht-squamöses mNSCLC und erhielten MK-1084 50–200 mg/Tag + Pembrolizumab 200 mg, Carboplatin und Pemetrexed alle 3 Wochen.
• Dosislimitierende Toxizitäten (DLTs) und Sicherheit waren primäre Endpunkte; ORR, DCR und PFS gemäss RECIST v1.1 nach Beurteilung durch den Prüfer waren sekundäre Endpunkte.
Behandlungsresultate
• Zum Datencutoff am 23. Juli 2025 befanden sich 146 Patienten in den Armen 1 und 3, darunter 32 (22 %) mit mNSCLC, 87 Patienten in Arm 2 und 46 Patienten in Arm 4.
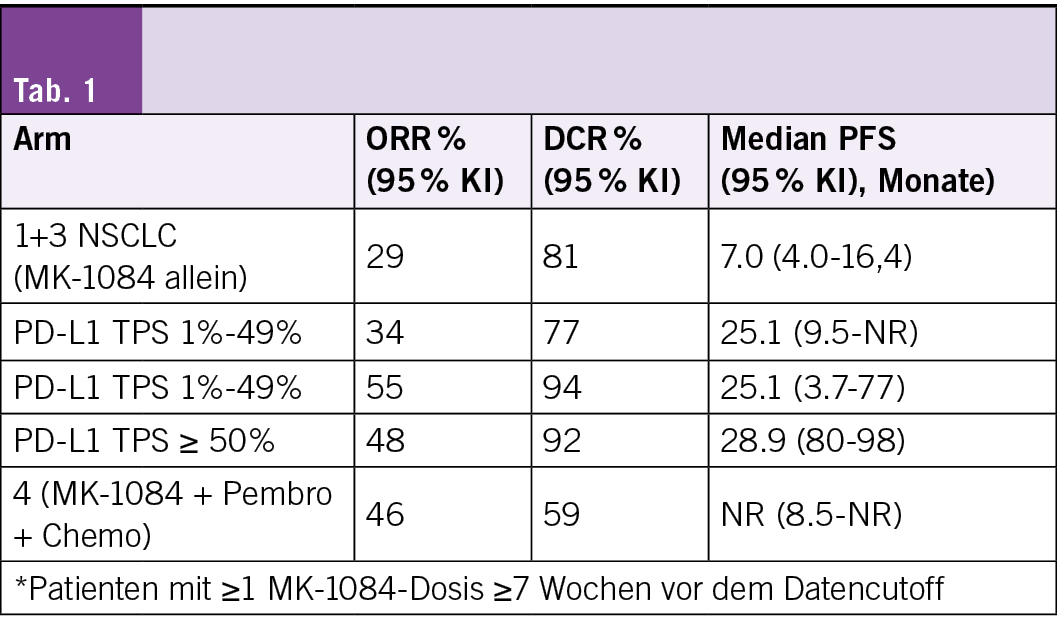
• Die mediane Nachbeobachtungszeit betrug 27,9 Monate, 14,1 Monate, 14,6 Monate bzw. 12,1 Monate. Die ORR in Arm 2 (MK-1084 + Pembro) betrug 92 % (TPS = 50 %), bei einem entsprechenden medianen PFS von 29 Monaten (Vergleiche Tabelle im Originalabstract).
• 15 (10 %) Patienten in den Armen 1 und 3, 26 (30 %) Patienten in Arm 2 und 28 (61 %) Patienten in Arm 4 wiesen arzneimittelbedingte unerwünschte Ereignisse (UE) des Grades 3–4 auf, darunter jeweils 3 %, 8 % und 11 % mit erhöhten ALT-Werten des Grades 3–4 sowie 3 %, 9 % und 9 % mit erhöhten AST-Werten des Grades 3–4.
• 1 Patient verstarb an einer arzneimittelbedingten Myelosuppression und einer verminderten Thrombozytenzahl (Arm 2) und 1 an einer arzneimittelbedingten immunvermittelten Myositis (Arm 4).
Fazit
MK-1084 zusammen mit Pembrolizumab erzielte in der KANDLELIT-001-Studie laut Studienautoren eine klinisch bedeutende Wirksamkeit – insbesondere zeigte sich bei Patienten mit PD-L1-TPS = 50 % eine Ansprechrate von über 90 %. Die Nebenwirkungen waren kontrollierbar; die Rate schwerwiegender ALT/AST-Erhöhungen blieb unter 10 %. Das insgesamt positive Verhältnis zwischen Nutzen und Risiko unterstützt die weitere Untersuchung in der laufenden Phase-III-Studie KANDLELIT-004. Dort wird MK-1084 + Pembrolizumab als Erstlinientherapie gegen Placebo + Pembrolizumab bei KRAS-G12C-mutiertem mNSCLC mit PD-L1-TPS = 50 % verglichen.
Adagrasib zeigte einen bedeutenden klinischen Nutzen
Jarushka Naidoo, et al. 5MO Phase II ETOP ADEPPT trial: Adagrasib in patients with KRASG12C-mutant NSCLC who are elderly or have poor performance status – Final results
Vorbemerkungen
KRAS-G12C-Mutationen treten laut den Studienautoren bei 10–15 % der Fälle von nicht-kleinzelligem Lungenkrebs (NSCLC) auf.
Adagrasib ist ein KRAS-G12C-Inhibitor der zweiten Generation, der bei vorbehandelten NSCLC-Patienten mit einem ECOG-Leistungsstatus (PS) von 0–1 Wirksamkeit gezeigt hat. Ein grosser Teil der KRAS-positiven NSCLC-Patienten ist jedoch älter oder weist einen ECOG-PS von 2 auf.
Diese Studie bewertet die Wirksamkeit, Toxizität und Lebensqualität (QoL) von Adagrasib in diesen unterrepräsentierten Populationen.
Studiendesign
• ADEPPT (NCT05673187) ist eine prospektive, internationale Phase-II-Studie zu Adagrasib (600 mg zweimal täglich bis zur Progression oder inakzeptabler Toxizität) bei vorbehandelten Patienten mit KRASG12C-mutiertem NSCLC, mit zwei parallelen einarmigen Kohorten.
• Teilnahmeberechtigt waren Patienten ≥ 70 Jahre mit einem ECOG-PS von 0–1 (Kohorte A [A]) oder ≥ 18 Jahre mit einem ECOG-PS von 2 (Kohorte B [B]).
Behandlungsresultate
• Es wurden 32 von 34 Patienten in die Kohorten A/B aufgenommen.
• In A/B: 66 %/62 % waren männlich, 97 %/97 % ehemalige bzw. aktuelle Raucher, 100 %/91 % Adenokarzinome, 16 %/32 % wiesen zu Studienbeginn Hirnläsionen auf.
• Die mediane (m) Nachbeobachtungszeit betrug 16,8/18,5 Monate (Mo). Die mittlere relative Dosisintensität lag bei 72 %/79 %.
• In Kohorte A wurde der primäre Endpunkt erreicht. Die cORR betrug 31 % (10 bestätigte Ansprechraten).
• Die Gesamt-ORR betrug 34 %, mPFS 7,6 Mo, mOS 9,5 Mo, mDoR NR.
• In Kohorte B wurde der primäre Endpunkt nicht erreicht. Die cORR betrug 18 % (6 bestätigte Ansprechraten).
• Die Gesamt-ORR betrug 38 %, mPFS 2,7 Mo, mOS 4,3 Mo, mDoR 2,4 Mo.
Verträglichkeit
• Behandlungsbedingte unerwünschte Ereignisse (TRAEs) des Grades ≥ 3 traten bei 41 %/62 % der Patienten in A/B auf, mit 1 tödlichem TRAE (plötzlicher Tod, Ursache unbekannt, Kohorte B).
• Nach 12 Wochen betrug der mittlere Anstieg des QoL-Index gegenüber dem Ausgangswert 2,3/6,6 in den Gruppen A/B, basierend auf 18/11 Patienten, die noch in Behandlung waren.
Fazit
Adagrasib zeigte laut den Studienautoren einen bedeutenden klinischen Nutzen mit einem überschaubaren Sicherheitsprofil bei älteren Patienten mit ECOG-PS 0–1, während die Wirksamkeit bei Patienten mit ECOG-PS 2 begrenzt war, jedoch eine verbesserte Lebensqualität (QoL) mit sich brachte.
Zugabe von Durvalumab nach SBRT scheint das Tumorwachstum mit fraglichem klinischen Nutzen zu verlangsamen
Andreas Hallqvist, et al. 221 MOStereotactic body radiotherapy (SBRT) followed by durvalumab in early-stage non-small cell lung cancer (NSCLC) patients: Results from a randomized phase II trial (ASTEROID)
Vorbemerkungen
SBRT gilt als Standardtherapie bei inoperablem Frühstadium-NSCLC und sorgt für gute lokale Kontrolle. Dennoch bekommen viele Patienten Fernmetastasen. Wegen fehlender Daten und hoher Gebrechlichkeit ist eine Chemotherapie selten, während Immuntherapie als vielversprechend betrachtet wird, da sie meist gut verträglich ist und mit Strahlentherapie Synergie zeigen könnte. Die ASTEROID-Studie prüft daher, ob Durvalumab nach SBRT die Tumorkontrolle bei peripheren T1-2N0M0-Tumoren verbessert.
Studiendesign
• Randomisierte, multizentrische, offene Phase-II-Studie zum Vergleich von SBRT allein in 3–4 Fraktionen (Arm A) mit SBRT gefolgt von Durvalumab 1500 mg i.v. alle 4 Wochen über 12 Monate (Arm B).
• Primärer Endpunkt war die Zeit bis zur Progression (TTP), mit dem krankheitsfreien Überleben (DFS) und dem Gesamtüberleben (OS) als sekundären Endpunkten.
Baseline
• Zwischen 2018 und 2024 wurden 104 Patienten an 12 nordischen Krankenhäusern eingeschlossen.
• 57 % waren Frauen, 71 % hatten Adenokarzinome, 83 % hatten T1A-Tumoren, 33 % hatten einen Leistungsstatus (PS) von 0, 67 % einen PS von 1–2.
• Das Medianalter betrug 78 (56–89) Jahre und der mittlere FEV1-Wert lag bei 1,8 (Bereich 0,7–4,5) L.
• Die mediane Anzahl der Durvalumab-Infusionen betrug 11 (1–12).
Verträglichkeit
• Nebenwirkungen (CTCAE v4.0) im Zusammenhang mit der SBRT wurden bei 22 von 54 Patienten (41 %) in Arm A und bei 15 von 49 (31 %) in Arm B berichtet, wobei die häufigsten Ereignisse Müdigkeit, Husten, Schmerzen und Dyspnoe des Grades 1–2 waren, mit einer Pneumonitis des Grades 3 in Arm A.
• In Arm B berichteten 36 von 49 Patienten (73 %) über unerwünschte Ereignisse im Zusammenhang mit Durvalumab, hauptsächlich Grad 1 und 2, wobei die häufigsten Ereignisse Hautreaktionen (39 %), Pruritus (24 %) und Müdigkeit (22 %) waren und zwei Patienten symptomatische Ereignisse des Grades 3 (Hautreaktion und Pneumonitis) erlitten.
Behandlungsresultate
• Zum Zeitpunkt der Datenerhebung mit einer medianen Nachbeobachtungszeit von 33 Monaten (13–64) hatten zehn Patienten in Arm A und drei Patienten in Arm B eine Progression, wobei sich die TTP durch die Zugabe von Durvalumab signifikant verbesserte (p = 0,054), jedoch kein Unterschied hinsichtlich DFS oder OS festzustellen war.
Fazit
Die Zugabe von Durvalumab nach SBRT scheint laut den Studienautoren das Tumorwachstum zu verlangsamen, doch der klinische Nutzen bei dieser gebrechlichen Population mit hoher konkurrierender Mortalität bleibt ungewiss.
Becotarug plus Osimertinib zeigte ein vielversprechendes und klinisch bedeutsames Überleben
Jinhui Xue, et al. 7MO Becotarug (JMT101) and osimertinib (Osi) in patients (pts) with platinum-pretreated EGFR exon 20 insertion-mutated (ex20ins) non-small cell lung cancer (NSCLC): Final overall survival (OS) and subgroup analyses from the BECOME phase II study
Vorbemerkungen
In der Phase-II-Studie BECOME zeigte Becotarug (Beco) in Kombination mit Osi laut den Studienautoren vielversprechende Wirksamkeit und ein vertretbares Sicherheitsprofil bei platinvorbehandeltem EGFR-ex20ins-positivem nicht-kleinzelligem Lungenkrebs (vgl. ELCC 2024, 137MO). Hier berichten die Autoren über die endgültigen Analysen zum Gesamtüberleben (OS) und die Wirksamkeitsergebnisse in den Subgruppen.
Studiendesign
• Die Patienten erhielten Beco 6 mg/kg alle zwei Wochen und Osi 160 mg einmal täglich.
• Die OS sowie Subgruppenanalysen nach EGFR-ex20ins-Lokalisationen und ctDNA-Status zu Studienbeginn wurden als sekundäre Endpunkte vorab festgelegt.
Behandlungsresultate
• Zum 18. August 2025 betrug die mediane (m) Nachbeobachtungszeit 26,7 Monate (Mo).
• Die mOS in der ITT-Gruppe (N = 112) betrug 18,0 Monate (95 % KI, 13,4–22,5).
• Bei den Insertionen (INS) handelte es sich um helikale Insertionen (HI, n = 9), Near-Loop-Insertionen (NL, n = 64) und Far-Loop-Insertionen (FL, n = 39);
• Patienten mit FL-INS zeigten ein numerisch längeres PFS und ein statistisch signifikant längeres OS im Vergleich zu NL-INS (HR = 0,58; P = 0,03), wie in der Tabelle im Originalabstract dargestellt.
• Unter den 43 Patienten mit gepaarten Gewebe- und Blutproben zum Studienbeginn waren 16 ctDNA-positiv (+) und 27 ctDNA-negativ (-).
• Ein unabhängiges Begutachtungskomitee bestätigte, dass ORR und DCR bei ctDNA-positiven (ctDNA+) Patienten 43,8 % (95 % KI, 19,8–70,2) bzw. 75,0 % (95 % KI, 47,6–92,7) betrugen, gegenüber 59,3 % (95 % KI, 38,8–77,6) bzw. 96,3 % (95 % KI, 81,0–99,9) bei ctDNA-negativen Patienten.
• Nach dem ctDNA-Status zu Studienbeginn wurden keine signifikanten Unterschiede bei der ORR (P = 0,361) oder der DCR (P = 0,056) beobachtet;
• die mPFS betrug 6,9 Monate (95 % KI, 2,7–NE) gegenüber 14,5 Monaten (95 % KI, 8,2–NE), p = 0,008; die mOS betrug 19,2 Monate (95 % KI, 13,4–NE) gegenüber 36,6 Monaten (95 % KI, 36,6–NE), p = 0,048, mit statistischen Unterschieden.
Fazit
Becotarug plus Osimertinib zeigte laut den Studienautoren ein vielversprechendes und klinisch bedeutsames Überleben bei platinvorbehandeltem EGFR-ex20ins-positivem NSCLC. Im Vergleich zu Patienten mit NL-INS zeigten Patienten mit FL-INS ein statistisch signifikant längeres OS. Bei Patienten mit ctDNA (-) zu Studienbeginn wurden deutlich grössere Überlebensvorteile beobachtet.
Daten sprechen für den Einsatz der perioperativen Pembro-Therapie plus neoadjuvanter Chemotherapie bei resektablem NSCLC im Frühstadium
Martin Reck, et a. 222MO Exploratory analysis of participants without pathological complete response (pCR) in the KEYNOTE-671 study of perioperative pembrolizumab (pembro) in early-stage NSCLC after 5 years of follow-up
Vorbemerkungen
In der Phase-3-Studie KEYNOTE-671 bei nicht-kleinzelligem Lungenkrebs (NSCLC) im Frühstadium verbesserte laut den Studienautoren die perioperative Gabe von Pembrolizumab in Kombination mit einer neoadjuvanten Chemotherapie (Chemo) das ereignisfreie Überleben (EFS), das Gesamtüberleben (OS), das signifikante pathologische Ansprechen und die pCR im Vergleich zur neoadjuvanten Chemotherapie signifikant. Das EFS war in explorativen Analysen bei Teilnehmern, die keine pCR erreichten, verlängert (HR, 0,69; 95 % KI, 0,55–0,85).
Die Autoren berichten über die Ergebnisse bei Pt. ohne pCR aus der KEYNOTE-671-Studie nach 5 Jahren Nachbeobachtung.
Studiendesign
• Teilnahmeberechtigte Patienten im Alter von ≥ 18 Jahren mit zuvor unbehandeltem, resezierbarem NSCLC im Stadium II–IIIB (N2) gemäss AJCC v8 wurden im Verhältnis 1:1 randomisiert und erhielten
• entweder 200 mg Pembrolizumab oder Placebo alle 3 Wochen plus Chemotherapie über 4 Zyklen, gefolgt von einer Operation und adjuvanter Behandlung mit Pembrolizumab oder Placebo alle 3 Wochen über bis zu 13 Zyklen (≥ 9 Monate).
• Zu den primären Endpunkten gehörten die EFS gemäss RECIST v1.1 durch den Prüfer und das OS; zu den sekundären Endpunkten gehörte die pCR durch einen verblindeten Pathologen eines zentralen Labors.
Behandlungsergebnisse
• Von den 397 Patienten, die der Pembro-Gruppe zugewiesen wurden, und den 400 Patienten in der Placebo-Gruppe erreichten 72 (18,1 %) bzw. 16 (4,0 %) eine pCR; davon erhielten 67 Patienten (93,1 %) in der Pembrolizumab-Gruppe und 15 Patienten (93,8 %) in der Placebo-Gruppe mindestens eine adjuvante Dosis und 47 (65,3 %) bzw. 12 (75,0 %) schlossen die adjuvante Therapie ab.
• Die mediane Zeit von der Randomisierung bis zum Datencutoff (3. Juli 2025) betrug bei Patienten ohne pCR 60,2 (Bereich: 42,6–85,8) Monate.
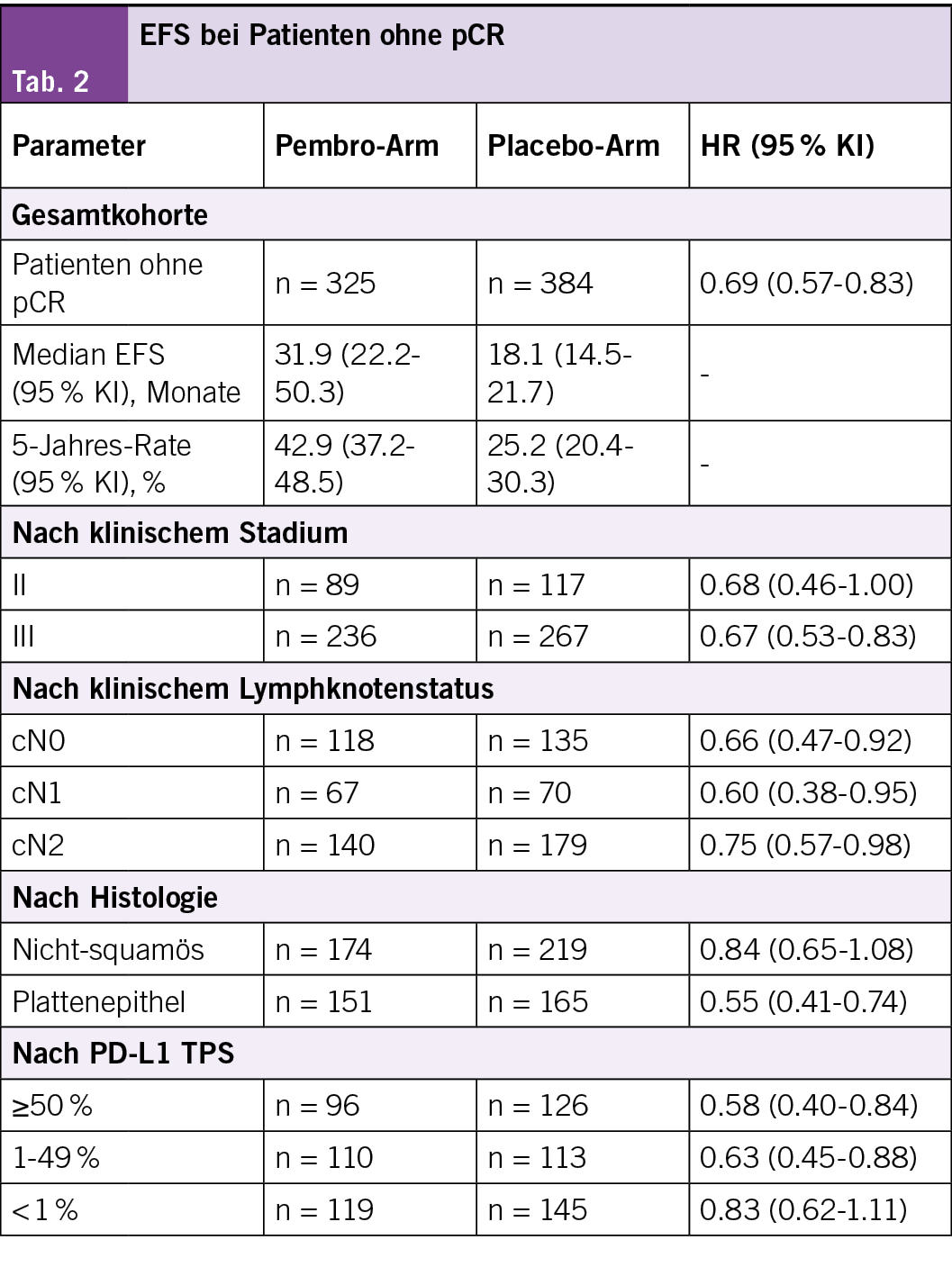
• Die HR für das EFS betrug 0,69 (95 % KI: 0,57–0,83) zugunsten der Pembro- gegenüber der Placebo-Gruppe (Tabelle).
• Die OS-Daten für diese Untergruppe sind noch nicht ausgereift.
Verträglichkeit
• Behandlungsbedingte unerwünschte Ereignisse (UE) des Grades 3 traten bei 143 von 324 (44,1 %) mit Pembro behandelten Patienten und bei 146 von 383 (38,1 %) mit Placebo behandelten Patienten auf.
• Immunvermittelte unerwünschte Ereignisse (UE) des Grades 3 und Infusionsreaktionen traten bei 21 (6,5 %) bzw. 7 Patienten (1,8 %) auf. (Tab. 2)
Fazit
Bei Patienten ohne pCR in der KEYNOTE-671 verlängerte laut den Studienautoren die perioperative Pembro-Therapie plus neoadjuvante Chemotherapie auch nach 5 Jahren Nachbeobachtungszeit weiterhin das EFS, unabhängig von den klinischen Ausgangsmerkmalen. Diese Daten sprechen für den Einsatz der perioperativen Pembro-Therapie plus neoadjuvanter Chemotherapie bei resektablem NSCLC im Frühstadium.
Perioperative Pembro plus neoadjuvante Chemotherapie verbesserte die pCR in allen Untergruppen
Margarita Majem, et al. 223 MOFive-year outcomes of participants with pathological complete response (pCR) enrolled in the KEYNOTE-671 trial of perioperative pembrolizumab (pembro) in early-stage NSCLC
Vorbemerkungen
Die Phase-3-Studie KEYNOTE-671 zeigt, dass perioperativ Pembrolizumab plus neoadjuvante Chemotherapie bei frühem NSCLC das ereignisfreie und Gesamtüberleben sowie das pathologische Ansprechen und die pCR im Vergleich zur neoadjuvanten Chemotherapie allein signifikant verbessert. Teilnehmer mit vollständiger pathologischer Remission hatten ein verlängertes EFS (HR 0,33; 95 % KI 0,09–1,22). Die Wirksamkeit nach fünf Jahren wird berichtet.
Studiendesign
• Teilnahmeberechtigte Patienten im Alter von ≥ 18 Jahren mit zuvor unbehandeltem, resektablem NSCLC im Stadium II, IIIA oder IIIB (N2) gemäss AJCC v8 wurden im Verhältnis 1:1 randomisiert und erhielten
• entweder 200 mg Pembrolizumab oder Placebo alle 3 Wochen plus Chemotherapie über 4 Zyklen, gefolgt von einer Operation und anschliessend adjuvanter Therapie mit 200 mg Pembrolizumab oder Placebo alle 3 Wochen über bis zu 13 Zyklen (≥ 9 Monate).
Behandlungsergebnisse
• Von 397 Patienten, die Pembro zugewiesen wurden, und 400, die Placebo erhielten, erreichten 72 (18,1 %) bzw. 16 (4,0 %) eine pCR, von denen 67 Patienten (93,1 %) in der Pembro-Gruppe und 15 Patienten (93,8 %) in der Placebo-Gruppe mindestens eine adjuvante Dosis erhielten und 47 (65,3 %) bzw. 12 (75,0 %) die adjuvante Therapie abschlossen.
• Die mediane Zeit von der Randomisierung bis zum Datencutoff (3. Juli 2025) betrug bei Patienten mit pCR 62,3 (Bereich: 43,3–84,7) Monate.
• In allen Subgruppen nach Krankheitsmerkmalen bei Studienbeginn erreichten mehr Patienten im Pembro-Arm als im Placebo-Arm eine pCR (Tabelle).
• Bei den Patienten mit pCR betrugen die 5-Jahres-EFS-Raten 80,8 % (95 % KI, 68,3 %–88,8 %) bzw. 55,7 % (95 % KI, 26,0 %–77,6 %); die EFS-HR betrug 0,37 (95 % KI, 0,14–1,00).
Fazit
Die perioperative Behandlung mit Pembrolizumab in Kombination mit einer neoadjuvanten Chemotherapie führte laut den Studienautoren zu einer Verbesserung der pathologischen Komplettremission (pCR) über alle Untergruppen hinsichtlich der Ausgangsmerkmale der Erkrankung. Darüber hinaus wurde im Vergleich zur alleinigen neoadjuvanten Chemotherapie selbst nach fünfjähriger Nachbeobachtung bei Patienten mit pCR eine verlängerte ereignisfreie Überlebenszeit (EFS) festgestellt. Diese Ergebnisse unterstreichen weiterhin die Empfehlung für den Einsatz von perioperativem Pembrolizumab plus neoadjuvanter Chemotherapie bei resektablem NSCLC im Frühstadium, auch bei Patienten mit pCR.
Subkutan verabreichtes Toripalimab weist ähnliche pharmakokinetische Profile und eine vergleichbare klinische Wirksamkeit wie intravenös verabreichtes Toripalimab auf
Lin Wu, et al. 8MO Subcutaneous versus intravenous toripalimab, in combination with chemotherapy, as a first-line treatment for recurrent or metastatic non-squamous (nsq) non-small cell lung cancer (NSCLC): A randomized phase III trial
Vorbemerkungen
Toripalimab in Kombination mit Chemotherapie ist in China sowie der EU (Anm. der Redaktion) für die Erstbehandlung von fortgeschrittenem nicht-kleinzelligem Lungenkrebs zugelassen. Um die Immuntherapie zu vereinfachen, wurde eine subkutane Version entwickelt. In einer randomisierten Phase-III-Studie (NCT06505837) wurden Pharmakokinetik, Wirksamkeit und Sicherheit von subkutanem und intravenösem Toripalimab plus Chemotherapie verglichen.
Studiendesign
• Patienten mit histologisch oder zytologisch bestätigtem rezidiviertem oder metastasiertem nsqNSCLC ohne EGFR-sensitive Mutationen oder ALK-Fusionen wurden im Verhältnis 1:1 randomisiert und erhielten entweder subkutanes Toripalimab (360 mg) oder intravenöses Toripalimab (240 mg) alle 3 Wochen plus Pemetrexed (500 mg/m²) und Carboplatin (Fläche unter der Kurve [AUC] = 5) oder Cisplatin (75 mg/m²) über bis zu 4 Zyklen.
• Patienten ohne Krankheitsprogression erhielten eine Erhaltungstherapie mit entweder subkutanem oder intravenösem Toripalimab plus Pemetrexed.
• Die koprimären Endpunkte waren die beobachtete Talspiegelkonzentration im Serum (Ctrough) am Ende von Zyklus 1 und die durch ein populationspharmakokinetisches Modell simulierte AUC von 0 bis 21 Tagen (AUC0-21day) während Zyklus 1.
Baseline
• Es wurden 396 Patienten aus 72 teilnehmenden Zentren in China randomisiert (198 in jedem Arm).
• Das geometrische Mittelverhältnis [90 %-Konfidenzintervall (KI)] für die beobachtete Ctrough und die modellsimulierte AUC0-21day betrug 1,31 (1,00–1,72) bzw. 0,90 (0,86–0,95), was die Nichtunterlegenheit der Exposition bei subkutaner (SC) gegenüber intravenöser (IV) Toripalimab-Gabe belegt.
Behandlungsergebnisse
• Die objektiven Ansprechraten betrugen 57,6 % in der subkutanen Gruppe und 49,5 % in der intravenösen Gruppe.
• Bei einer medianen Nachbeobachtungszeit von 7,1 Monaten betrug das mediane progressionsfreie Überleben in beiden Gruppen 8,1 Monate.
• Es traten keine neuen Sicherheitssignale auf.
Fazit
Subkutanes Toripalimab zeigt ähnliche Wirksamkeit und Sicherheit wie intravenöses Toripalimab. Es eignet sich als Erstlinien-Therapie für fortgeschrittenes nsqNSCLC in Kombination mit Chemotherapie.
Bedeutung von Sac-TMT als vielversprechende neue Behandlungsoption
Yunpeng Yang, et al. LBA4 Sacituzumab tirumotecan (sac-TMT) in patients (pts) with previously treated advanced EGFR-mutated (EGFRm) non-small cell lung cancer (NSCLC): Final overall survival (OS) analysis from the randomized OptiTROP-Lung03 study
Vorbemerkungen
Sac-TMT ist ein ADC, das spezifisch für TROP2 wirkt und einen speziellen bifunktionellen Linker besitzt. In der OptiTROP-Lung03-Studie (NCT05631262) zeigte Sac-TMT gegenüber Docetaxel bei vorbehandeltem EGFRm-NSCLC signifikante Vorteile beim progressionsfreien und Gesamtüberleben (PFS-HR: 0,30; OS-HR: 0,49; Fang et al., BMJ 2025). Die Autoren präsentieren hier die finale OS-Analyse sowie aktualisierte PFS- und Sicherheitsdaten.
Studiendesign
• Patienten mit fortgeschrittenem EGFRm-NSCLC, bei denen nach einer Behandlung mit EGFR-Tyrosinkinase-Inhibitoren (TKI) und einer platinbasierten Chemotherapie eine Progression eingetreten war, wurden im Verhältnis 2:1 randomisiert und erhielten
• entweder alle zwei Wochen 5 mg/kg Sac-TMT oder alle drei Wochen 75 mg/m² Docetaxel.
• Patienten mit nachgewiesener Progression unter Docetaxel konnten bei Eignung auf Sac-TMT umgestellt werden.
Behandlungsergebnisse
• Insgesamt wurden 137 Patienten randomisiert, um entweder Sac-TMT (n = 91) oder Docetaxel (n = 46) zu erhalten.
• Zum 11. Dezember 2025, bei einer medianen Nachbeobachtungszeit von 23,8 Monaten (Mo), betrug das vom Prüfer bewertete mediane PFS 7,9 Mo gegenüber 2,8 Mo (Sac-TMT gegenüber Docetaxel; HR 0,23, 95 % KI 0,15–0,35) und das mediane OS betrug 20,0 Monate gegenüber 13,5 Monaten (HR 0,63, 95 % KI 0,40–0,98).
• In der Docetaxel-Gruppe erhielten 41,3 % der Patienten Sac-TMT als nachfolgende Krebsbehandlung.
• Die adjustierte mediane OS nach dem RPSFT-Modell betrug 20,0 Monate gegenüber 11,2 Monaten (HR 0,45, 95 % KI 0,28, 0,73; 18-Monats-OS-Rate: 54,7 % gegenüber 9,1 %).
Verträglichkeit
• Behandlungsbedingte unerwünschte Ereignisse des Grades 3 traten bei 60,4 % gegenüber 73,9 % auf, und behandlungsbedingte schwerwiegende unerwünschte Ereignisse bei 20,9 % gegenüber 41,3 % der Patienten (Sac-TMT gegenüber Docetaxel).
• In der Sac-TMT-Gruppe wurden keine Fälle einer interstitiellen Lungenerkrankung berichtet.
Fazit
Sac-TMT bietet laut Studienautoren signifikante Verbesserungen beim PFS und OS gegenüber Docetaxel und weist ein gutes Sicherheitsprofil für Patienten mit fortgeschrittenem EGFRm-NSCLC auf. Die Daten sprechen für Sac-TMT als neue, vielversprechende Therapieoption.
Anhaltende Antitumoraktivität mit klinisch bedeutsamem Überlebensvorteil
Kai He, et a. 3O Anti-tumor activity of gotistobart compared to docetaxel in patients with metastatic squamous non-small cell lung cancer (sqNSCLC) progressing on PD-(L)1 inhibitors: Stage 1 PRESERVE-003 phase III trial
Vorbemerkungen
Gotistobart, ein neuartiger Antikörper, der Treg-Zellen in der Tumormikroumgebung gezielt durch CTLA-4-Hemmung angreift, hat in einer Phase-III-Studie bei Patienten mit fortgeschrittenem sqNSCLC unter PD-(L)1-Inhibitoren einen klinisch relevanten Überlebensvorteil gezeigt (HR: 0,46 [95 % KI: 0,25–0,84]; #OA01.01, NACLC 2025). Die Autoren präsentieren weitere Wirksamkeitsergebnisse aus Phase 1 dieser Studie.
Studiendesign
• Patienten mit metastasiertem NSCLC, deren Erkrankung unter PD-(L)1-Inhibitoren und platinbasierter Chemotherapie fortgeschritten war, wurden im Verhältnis 1:1 randomisiert und erhielten entweder Gotistobart (6 mg/kg mit zwei Initialdosen von 10 mg/kg alle drei Wochen) oder Docetaxel (75 mg/m² alle drei Wochen).
Behandlungsresultate
• Es wurden 217 Patienten in Phase 1 aufgenommen, darunter 87 Patienten mit sqNSCLC, die randomisiert Gotistobart (N = 45) oder Docetaxel (N = 42) erhielten, bei einer medianen Nachbeobachtungszeit von 14,5 Monaten.
• Das mediane PFS war ähnlich (2,4 Monate vs. 2,6 Monate), aber die 12-Monats-PFS-Rate betrug 25 % für Gotistobart und 0 % für Docetaxel, mit einer HR von 0,69 (95 % KI, 0,42, 1,13) zugunsten von Gotistobart.
• Die bestätigte ORR betrug 20 % (95 % KI: 9,6, 34,6) für Gotistobart und 4,8 % (95 % KI: 0,6, 16,2) für Docetaxel.
• Die mediane DoR betrug 11 Monate für Gotistobart gegenüber 3,8 Monaten für Docetaxel.
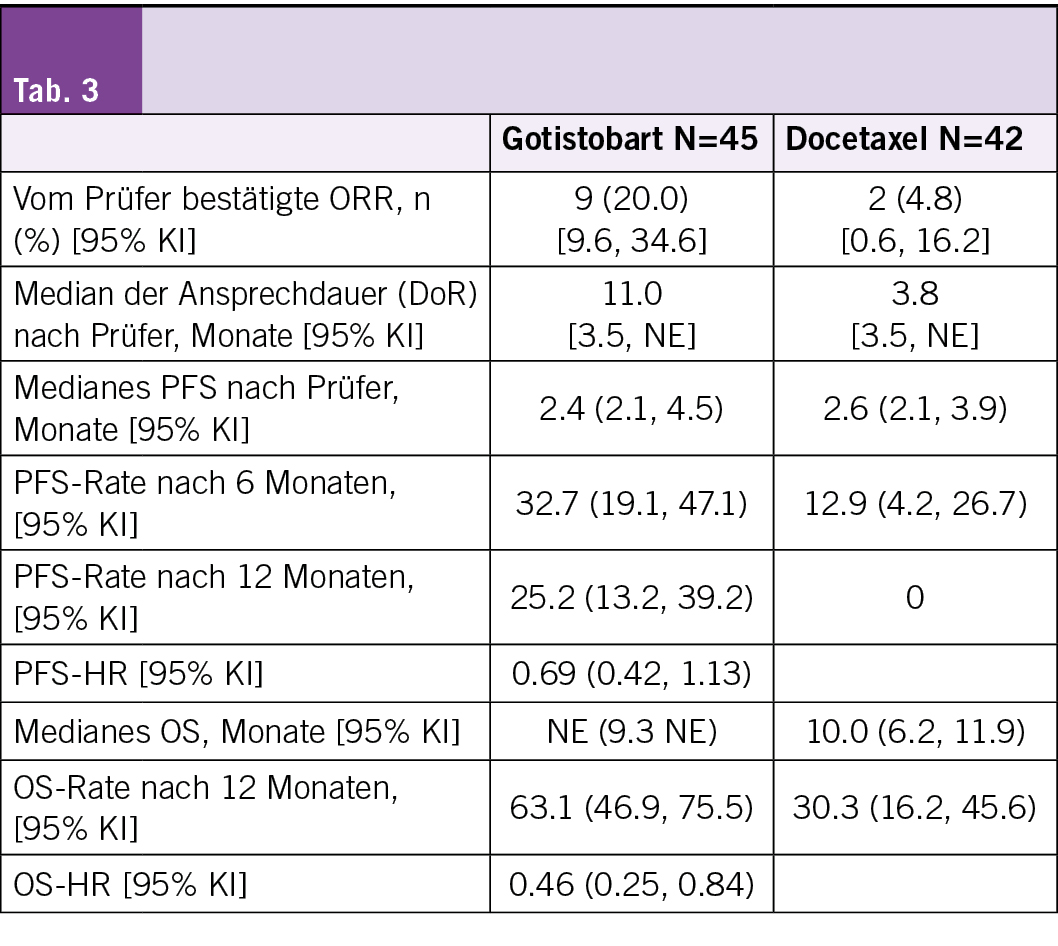
• Weitere Wirksamkeitsdaten sind in der Tab. 3 aufgeführt.
Fazit
Die Gotistobart-Monotherapie bietet eine chemotherapiefreie Behandlung für Patienten mit sqNSCLC, bei denen eine Anti-PD-(L)1-Therapie nicht mehr wirkt. Laut den Studienautoren zeigt sie einen deutlichen Überlebensvorteil gegenüber Docetaxel und erfüllt einen wichtigen Bedarf an wirksamen Therapieoptionen. Die zulassungsrelevante Phase-2-Studie rekrutiert derzeit weltweit Patienten.
Zongertinib zeigte eine anhaltende systemische und intrakranielle Wirksamkeit
John Heymach, et al. 6MO Zongertinib in treatment-naïve patients with HER2-mutant NSCLC, including those with active brain metastases: Beamion LUNG-1
Vorbemerkungen
Zongertinib ist laut den Studienautoren ein oral verabreichter, irreversibler TKI, der selektiv HER2 hemmt, während der Wildtyp-EGFR verschont bleibt, wodurch die damit verbundenen Toxizitäten minimiert werden.
Die Autoren berichten über die Wirksamkeit und Sicherheit von Zongertinib aus der Phase Ib der Beamion LUNG-1-Studie bei therapienaiven Patienten (Pts) mit HER2-mutiertem NSCLC (Kohorte 2) sowie bei Patienten mit aktiven Hirnmetastasen (Mets; Kohorte 4), einschließlich solcher ohne vorherige Hirnstrahlentherapie (RTx).
Studiendesign
• Patienten mit fortgeschrittenem/metastasiertem nicht-squamösem NSCLC mit einer HER2-Mutation innerhalb der Tyrosinkinasedomäne erhielten einmal täglich 120 mg Zongertinib.
• Die Patienten der Kohorte 2 waren therapienaiv; der primäre Endpunkt war das objektive Ansprechen (bestes Gesamtansprechen als vollständiges oder partielles Ansprechen; RECIST v1.1), und sekundäre Endpunkte umfassten die Ansprechdauer (DoR) und das progressionsfreie Überleben (PFS).
• Die Patienten der Kohorte 4 waren therapienaiv oder zuvor behandelt und wiesen aktive (d. h. symptomatische) Hirnmetastasen auf; der primäre Endpunkt war das objektive Ansprechen bei Läsionen des Zentralnervensystems (ZNS) nach RANO-BM.
Behandlungsresultate
• Es erhielten 74 Patienten in Kohorte 2 120 mg Zongertinib.
• Die bestätigte objektive Ansprechrate (ORR) betrug 76 % (95 % KI: 65–84).
• Die mediane Ansprechdauer (DoR) betrug 15,2 Monate (95 % KI: 9,8–nicht auswertbar [NE]) und das progressionsfreie Überleben (PFS) 14,4 Monate (95 % KI: 11,1–NE).
• Die durch RANO-BM bestätigte intrakranielle ORR betrug 47 % (95 % KI: 30–64); die mediane intrakranielle DoR betrug 6,9 Monate (95 % KI: 2,9–NE) und das intrakranielle PFS betrug 8,2 Monate (95 % KI: 4,1–11,3).
• Bei 8 therapienaiven Patienten betrug die durch RANO-BM bestätigte intrakranielle ORR 50 % (4 Patienten; 95 % KI: 22–79).
• Bei 17 Patienten mit zentral bestätigter messbarer ZNS-Erkrankung und ohne vorherige Hirnbestrahlung betrug die durch RANO-BM bestätigte intrakranielle ORR 59 % (95 % KI: 36–78);
• die mediane intrakranielle DoR betrug 6,2 Monate (95 % KI: 2,7–NE).
Verträglichkeit
• TRAEs traten bei 91 % auf (Grad ≥ 3: 19 %); hauptsächlich leichtgradige Diarrhoe. In Kohorte 4 erhielten 30 Patienten 120 mg Zongertinib.
Fazit
Nach Angaben der Studienautoren zeigte Zongertinib sowohl im gesamten Körper als auch im Gehirn eine anhaltende Wirksamkeit bei unbehandelten Patienten mit fortgeschrittenem oder metastasiertem HER2-mutiertem NSCLC. Besonders beeindruckend ist die Wirkung bei Patienten mit aktiven Hirnmetastasen – einer Gruppe, die üblicherweise von Studien ausgeschlossen wird –, selbst wenn diese zuvor keine Bestrahlung des Gehirns erhalten hatten. Die meisten Nebenwirkungen durch die Behandlung waren mild.