- Mammographie-Screening in der Schweiz
Das Mammographie-Screening ist ein zentraler Bestandteil der Brustkrebsfrüherkennung. In der Schweiz existieren kantonal organisierte Programme, ergänzt durch opportunistisches Screening. Ziel ist die Senkung der brustkrebsspezifischen Mortalität durch frühere Diagnose und weniger invasive Therapien. Randomisierte Studien und Beobachtungsstudien zeigen eine relative Mortalitätsreduktion von etwa 20–30 %, mit der höchsten Evidenz für Frauen zwischen 50 und 69 Jahren. Gleichzeitig treten potenzielle Nachteile wie falsch-positive Befunde und Überdiagnosen auf. Der Beitrag fasst die aktuelle Evidenzlage, Screening-Kennzahlen und Bias-Diskussionen zusammen und ordnet sie für die gynäkologische Praxis ein. Zudem werden rechtliche Rahmenbedingungen in der Schweiz sowie zukünftige Entwicklungen wie KI-basierte Auswertung und risikoangepasste Screeningstrategien diskutiert.
Mammography screening is a key component of early breast cancer detection. In Switzerland, screening is organized at the cantonal level and supplemented by opportunistic screening. The aim is to reduce breast cancer–specific mortality through earlier diagnosis and less invasive treatment. Randomized studies and observational studies show a relative reduction in mortality of about 20–30 %, with the strongest evidence for women between 50 and 69 years of age. At the same time, potential harms such as false-positive findings and overdiagnosis occur. This article summarizes the current evidence base, key screening performance indicators and ongoing debates regarding bias, and contextualizes these aspects for gynecological practice. In addition, the legal framework in Switzerland as well as future developments – such as AI-based evaluation and risk-adapted screening strategies – are discussed.
Keywords: Mammographie-Screening, Brustkrebsfrüherkennung, Schweiz, Mortalität, Überdiagnosen
Bedeutung des Mammographie-Screenings in der Schweiz
Brustkrebs ist die häufigste maligne Erkrankung der Frau in der Schweiz mit einem Lebenszeitrisiko von etwa 1 : 8. Zwischen 2018 und 2022 wurden jährlich etwa 6758 Neuerkrankungen bei Frauen und 59 bei Männern registriert (1). Im gleichen Zeitraum verstarben durchschnittlich 1370 Frauen und 7 Männer pro Jahr an einem Mammakarzinom (2). Während die Inzidenz steigt, ist die Mortalität seit den 1990er-Jahren rückläufig, was neben verbesserten Therapien vor allem auch auf Früherkennung zurückgeführt werden kann (3). Gynäkologinnen und Gynäkologen spielen eine zentrale Rolle als erste Anlaufstelle für Screeningberatung, Risikoeinschätzung und Einordnung von Screeningresultaten.
Organisation des Screenings in der Schweiz
Das Mammographie-Screening richtet sich primär an Frauen zwischen 50 und 69 Jahren, teilweise bis 74 Jahre, mit einem zweijährlichen Untersuchungsintervall. Für Frauen mit durchschnittlichem Risiko zeigt die Evidenz für dieses Intervall ein günstiges Nutzen-Schaden-Verhältnis (4). In der Schweiz bestehen heute in den meisten Kantonen organisierte Screeningprogramme, darunter Basel-Stadt, Basel-Landschaft, Bern, Genf, Waadt, Freiburg, Solothurn, Wallis, St. Gallen, Thurgau, Graubünden und Tessin. In anderen Kantonen erfolgt weiterhin ein opportunistisches Screening (5). Technischer Standard ist die digitale Vollfeldmammographie mit zwei Ebenen (CC, MLO). In vielen Programmen erfolgt eine Doppelbefundung, wodurch falsch-positive Rückrufe reduziert und Detektionsraten gesteigert werden können (6).
Evidenz für die Mortalitätsreduktion
Randomisierte kontrollierte Studien zeigen für das Mammographie-Screening eine relative Reduktion der brustkrebsspezifischen Mortalität von etwa 20 % (7). Europäische Beobachtungsstudien berichten eine Mortalitätsreduktion von 25–31 % bei eingeladenen Frauen und von 38–48 % bei tatsächlich teilnehmenden Frauen (8). Modelle bestätigen diesen populationsbezogenen Nutzen: Bei Frauen im Alter von 50 bis 69 Jahren können – abhängig vom Screeningintervall – etwa 400–740 Brustkrebstodesfälle pro 100 000 Frauen verhindert werden (9). Massnahmen der Sensibilisierung für Brustveränderungen und klinische Früherkennung ergänzen diese bildgebende Früherkennung.
Die Brustselbstuntersuchung kann die Wahrnehmung für Veränderungen der eigenen Brust fördern und zur frühzeitigen ärztlichen Abklärung beitragen, ohne dass bislang eine eigenständige Mortalitätsreduktion eindeutig belegt werden konnte (10). Die klinische Brustuntersuchung im Rahmen der gynäkologischen Vorsorge zeigt hingegen in randomisierten Studiendaten eine signifikante Verschiebung zu früheren Tumorstadien bei Diagnosestellung und in der Altersgruppe ≥ 50 Jahre eine Mortalitätsreduktion (11). Im Vergleich zur klinischen Brustuntersuchung zeigt die Mammographie im populationsbasierten Screening höhere Detektionsraten und ist mit einer deutlich stärkeren Reduktion der brustkrebsspezifischen Mortalität (RR 0.59) sowie fortgeschrittener Tumorstadien (RR 0.70) assoziiert (12).
Für die Schweiz wird geschätzt, dass unter 1000 Frauen, die über 20 Jahre am Screening teilnehmen, etwa vier brustkrebsbedingte Todesfälle verhindert werden (13).
Screening-Performance und diagnostische Kennzahlen
Typische Leistungskennzahlen moderner Mammographieprogramme umfassen (14):
• Detektionsrate: etwa 5–8 Karzinome pro 1000 Untersuchungen
• Sensitivität: ca. 87 %
• Spezifität: ca. 89 %
• positive prädiktive Werte: PPV1 etwa 4–5 %, PPV2 etwa 25 %
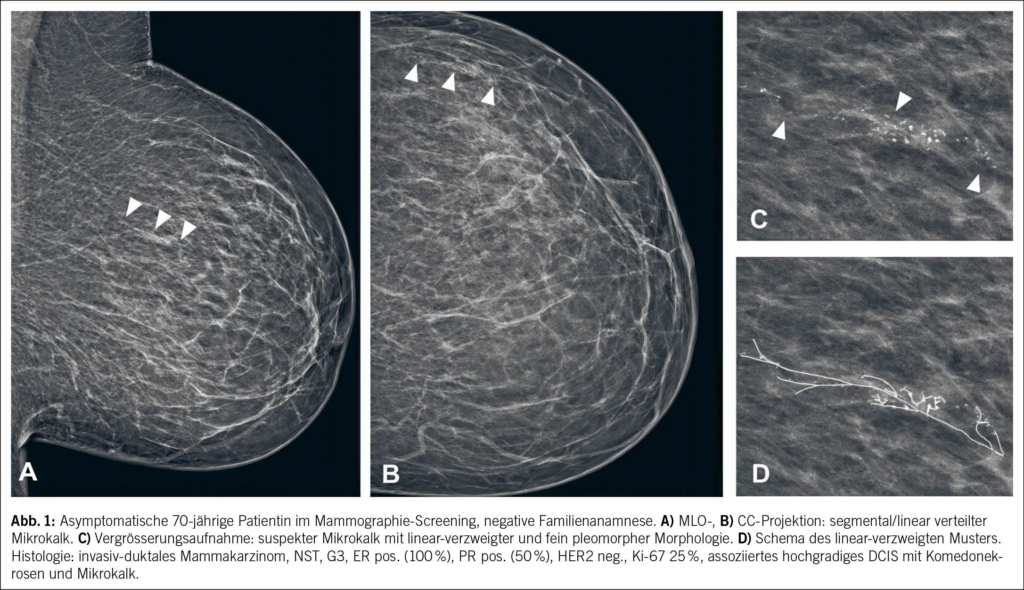
In Schweizer Screeningprogrammen lag zwischen 2019 und 2021 die Detektionsrate zwischen 5.3 und 9.7 pro 1000 Untersuchungen, mit positiven prädiktiven Werten von 4.3–11.1 % (15) (Abb. 1).
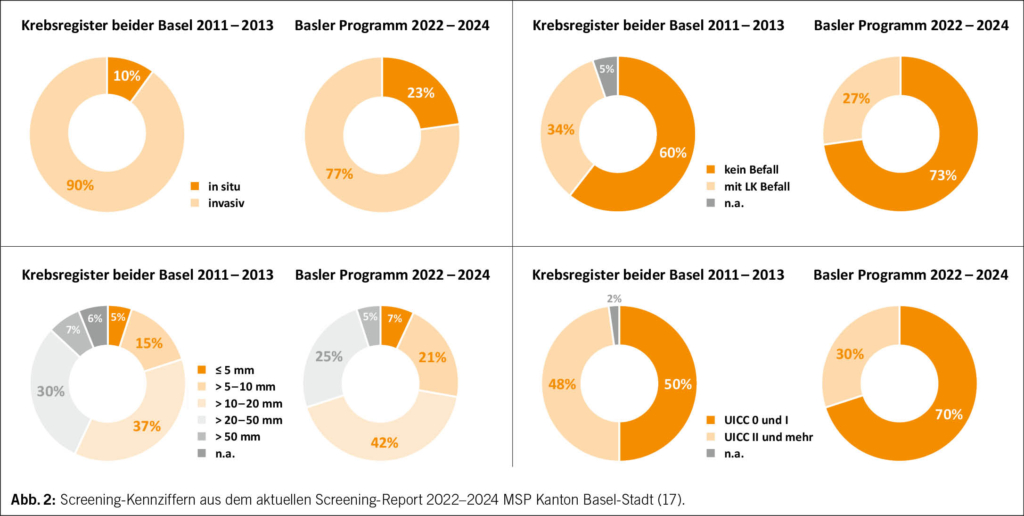
Die Mehrheit der diagnostizierten Tumoren befindet sich im frühen Stadium (15): 70.6 % UICC 0–I, 84 % nodal-negative invasive Tumoren und ca. 19.5 % DCIS. Die Recall-Rate («Rückrufrate») liegt typischerweise zwischen 3 und 7 %. Studien zeigen, dass höhere Recall-Raten nur geringe zusätzliche Detektionsgewinne bringen, während die Zahl falsch-positiver Befunde steigt (16) (Abb. 2).
Falsch-positive Befunde und psychologische Auswirkungen
Rückrufe zur weiteren Abklärung sind ein unvermeidbarer Bestandteil jedes Screening-Programms. Die 10-Jahres-Wahrscheinlichkeit für eine falsch-positive Biopsie liegt bei etwa 4.8 % bei zweijährlichem Screening (7).
Falsch-positive Screeningbefunde führen häufig zu kurzfristiger psychischer Belastung, zeigen jedoch keine nachweisbaren langfristigen psychologischen Folgen und beeinträchtigen die Teilnahmebereitschaft langfristig meist nur gering (18).
Biases und Überdiagnose im Screening
Die Interpretation von Screeningstudien wird durch verschiedene Biases beeinflusst. Der Lead-Time-Bias beschreibt eine scheinbare Überlebensverlängerung durch frühere Diagnosestellung. Für Mammakarzinome wird eine mittlere Lead-Time von etwa 2.3 Jahren geschätzt (19). Der Length-Time-Bias entsteht durch bevorzugte Detektion langsam wachsender Tumoren mit günstiger Biologie (20, 21). Aggressivere Tumoren treten häufiger als Intervallkarzinome auf (22). Die Überdiagnose wird in europäischen Analysen auf etwa 1–10 % der Screeningdiagnosen geschätzt (23).
Besondere Risikogruppen
Für Frauen mit erhöhtem Risiko gelten in der Schweiz spezielle Überwachungsprotokolle (BAG), exemplarisch (24):
• Lebenszeitrisiko 17–29 %: jährliche Mammographie 40–59 Jahre
• Lebenszeitrisiko ≥ 30 %: jährliche MRI- und Mammographie
• BRCA1/2, STK 11: jährliche MRI ab 25 Jahren
• PTEN, CDH1 und PALB2: jährlich MRI und Mammographie ab 30 Jahren
Die Risikobewertung kann beispielsweise mit IBIS-Risikomodellen erfolgen (z. B. https://ems-trials.org/riskevaluator/).
Dichtes Brustgewebe und ergänzende Bildgebung
Frauen mit extrem dichtem Brustgewebe (ACR D) haben mit einer Odds-Ratio von ca. 4.7 ein deutlich erhöhtes Brustkrebsrisiko (25, 26). Die EUSOBI-Empfehlungen sehen hierbei ein MRI-Screening bei sehr dichtem Brustgewebe vor (27), was allerdings auf nationaler Ebene in der Schweiz noch nicht gestützt wird. In der prospektiven multizentrischen Studie EA1141 Trial zeigte ein verkürztes Brust-MRT-Protokoll bei Frauen mit dichtem Brustgewebe eine signifikant höhere invasive Krebsdetektionsrate als die digitale Brusttomosynthese (11.8 vs. 4.8 pro 1000 untersuchte Frauen) sowie eine deutlich höhere Sensitivität (95.7 % vs. 39.1 %) bei geringerer Spezifität (86.7 % vs. 97.4 %) (28), während die Intervallkarzinom-Rate um ca. 50 % gesenkt werden konnte (29).
Perspektiven: KI und personalisiertes Screening
Neue Entwicklungen könnten das Screening künftig verändern. Beispielsweise zeigte die randomisierte MASAI-Studie (n ~ 80000 Frauen) mit KI-gestütztem Screening eine höhere Krebsdetektionsrate (6.4 vs. 5.0 pro 1000) bei gleichbleibender Recall-Rate und einem um 44 % reduzierten Befundungsaufwand (30). Langfristig könnten risikobasierte Screeningstrategien entstehen, die individuelle Risikofaktoren, Bilddaten und genetische Marker kombinieren.
Copyright
Aerzteverlag medinfo AG
MIBB akkreditiert (Minimalinvasive Brustbiopsien),
Leitender Arzt für Radiologie, Schwerpunkt Mammadiagnostik
und Onkologie
Kantonsspital Baselland
Rheinstrasse 26
4410 Liestal
Fachärztin für Gynäkologie und Geburtshilfe, Schwerpunkt gyn. Senologie
Stv. Chefärztin Frauenklinik Baselland
Leiterin Brustzentrum Baselland
Kantonsspital Baselland
Rheinstrasse 26
4410 Liestal
Die Autorenschaft hat keine Interessenskonflikte in Zusammenhang mit diesem Artikel deklariert.
- Das Mammographie-Screening reduziert die Brustkrebsmortalität um etwa 20–30 %.
- In der Schweiz bestehen überwiegend organisierte kantonale Screeningprogramme für Frauen zwischen 50–69 Jahre.
- Falsch-positive Befunde und Überdiagnosen treten auf, liegen jedoch in einem vertretbaren Verhältnis zum Nutzen.
- Gynäkologinnen und Gynäkologen spielen eine zentrale Rolle bei der Risikoberatung und dem Shared Decision Making.
- Zukünftige Screeningstrategien werden wahrscheinlich risikoadaptiert und KI-gestützt sein.
1. Neuerkrankungen (Inzidenz) | Krebsarten im Vergleich | Krebsmonitoring Schweiz [Internet]. [zitiert 5. März 2026]. Verfügbar unter:
https://krebs-monitoring.bfs.admin.ch/de/vergleich/neuerkrankungen/
2. Sterblichkeit (Mortalität) | Krebsarten im Vergleich | Krebsmonitoring Schweiz [Internet]. [zitiert 5. März 2026]. Verfügbar unter:
https://krebs-monitoring.bfs.admin.ch/de/vergleich/sterblichkeit/
3. Cardoso R, Ola I, Jansen L, Hackl M, Ihle P, Francart J, u. a. Breast cancer incidence, by stage at diagnosis, and mortality in 21 European countries in the era of mammography screening: an international population-based study. The Lancet Regional Health – Europe. 1. März 2026;62. doi:10.1016/j.lanepe.2025.101574 PubMed PMID: 41552365.
4. Canelo-Aybar C, Posso M, Montero N, Solà I, Saz-Parkinson Z, Duffy SW, u. a. Benefits and harms of annual, biennial, or triennial breast cancer mammography screening for women at average risk of breast cancer: a systematic review for the European Commission Initiative on Breast Cancer (ECIBC). Br J Cancer. März 2022;126(4):673–88. doi:10.1038/s41416-021-01521-8
5. Swiss Cancer Screening [Internet]. 2026 [zitiert 6. März 2026]. Angebote in Ihrem Kanton. Verfügbar unter: https://www.swisscancerscreening.ch/de/angebote-in-ihrem-kanton
6. Taylor-Phillips S, Stinton C. Double reading in breast cancer screening: considerations for policy-making. Br J Radiol. 1. Februar 2020;93(1106):20190610. doi:10.1259/bjr.20190610 PubMed PMID: 31617741; PubMed Central PMCID: PMC7055445.
7. Myers ER, Moorman P, Gierisch JM, Havrilesky LJ, Grimm LJ, Ghate S, u. a. Benefits and Harms of Breast Cancer Screening: A Systematic Review. JAMA. 20. Oktober 2015;314(15):1615–34. doi:10.1001/jama.2015.13183
8. Broeders M, Moss S, Nyström L, Njor S, Jonsson H, Paap E, u. a. The Impact of Mammographic Screening on Breast Cancer Mortality in Europe: A Review of Observational Studies. J Med Screen. 1. September 2012;19(1_suppl):14–25. doi:10.1258/jms.2012.012078
9. Yaffe MJ, Mittmann N, Lee P, Tosteson ANA, Trentham-Dietz A, Alagoz O, u. a. Clinical outcomes of modelling mammography screening strategies. Health Rep. Dezember 2015;26(12):9–15. PubMed PMID: 26676234; PubMed Central PMCID: PMC4869692.
10. Hackshaw AK, Paul EA. Breast self-examination and death from breast cancer: a meta-analysis. Br J Cancer. April 2003;88(7):1047–53. doi:10.1038/sj.bjc.6600847
11. Mittra I, Mishra GA, Dikshit RP, Gupta S, Kulkarni VY, Shaikh HKA, u. a. Effect of screening by clinical breast examination on breast cancer incidence and mortality after 20 years: prospective, cluster randomised controlled trial in Mumbai. BMJ. 24. Februar 2021;372:n256. doi:10.1136/bmj.n256 PubMed PMID: 33627312.
12. Yen AMF, Tsau HS, Fann JCY, Chen SLS, Chiu SYH, Lee YC, u. a. Population-Based Breast Cancer Screening With Risk-Based and Universal Mammography Screening Compared With Clinical Breast Examination: A Propensity Score Analysis of 1 429 890 Taiwanese Women. JAMA Oncol. 1. Juli 2016;2(7):915–21. doi:10.1001/jamaoncol.2016.0447
13. Swiss Cancer Screening [Internet]. [zitiert 6. März 2026]. Brustkrebsfrüherkennung in Zahlen. Verfügbar unter: https://www.swisscancerscreening.ch/de/krebs-frueherkennung/brust/brustkrebsfrueherkennung-in-zahlen
14. Lehman CD, Arao RF, Sprague BL, Lee JM, Buist DSM, Kerlikowske K, u. a. National Performance Benchmarks for Modern Screening Digital Mammography: Update from the Breast Cancer Surveillance Consortium. Radiology. April 2017;283(1):49–58. doi:10.1148/radiol.2016161174
15. Brändle K, Zwahlen M, Bulliard JL. Breast cancer screening programmes in Switzerland, 2019-2021 [Internet]. Centre universitaire de médecine générale et santé publique, Lausanne; 2024 [zitiert 5. März 2026]. Bericht Nr. Verfügbar unter: https://www.unisante.ch/fr/formation-recherche/recherche/publications/raisons-sante/raisons-sante-356 doi:10.16908/ISSN.1660-7104/356
16. van der Waal D, Abbey CK, Tetteroo E, Geertse TD, Smid-Geirnaerdt MJA, Sechopoulos I, u. a. Finding the optimal recall rate in breast cancer screening: results from the ROCS study. Eur Radiol. 5. März 2026;1–9. doi:10.1007/s00330-026-12370-5
17. Bettina Bringolf-Isler, Anna Altermatt, Viviane Hess. Mammografie-Screening-Prgramm Kanton Basel-Stadt Report 2020-2022 [Internet]. 2024 [zitiert 6. März 2026]. Verfügbar unter: https://irp.cdn-website.com/d99b2a19/files/uploaded/Mammografie_Report_2022-d2a39437.pdf
18. Miglioretti DL, Zhu W, Kerlikowske K, Sprague BL, Onega T, Buist DSM, u. a. Breast Tumor Prognostic Characteristics and Biennial vs Annual Mammography, Age, and Menopausal Status. JAMA Oncol. November 2015;1(8):1069–77. doi:10.1001/jamaoncol.2015.3084 PubMed PMID: 26501844; PubMed Central PMCID: PMC4644100.
19. Andersson TML, Rutherford MJ, Humphreys K. Assessment of lead-time bias in estimates of relative survival for breast cancer. Cancer Epidemiology. 1. Februar 2017;46:50–6. doi:10.1016/j.canep.2016.12.004
20. Cox B, Sneyd MJ. Bias in breast cancer research in the screening era. The Breast. 1. Dezember 2013;22(6):1041–5. doi:10.1016/j.breast.2013.07.046
21. Pálka I, Kelemen G, Ormándi K, Lázár G, Nyári T, Thurzó L, u. a. Tumor Characteristics in Screen-Detected and Symptomatic Breast Cancers. Pathol Oncol Res. 1. Juni 2008;14(2):161–7. doi:10.1007/s12253-008-9010-7
22. Lin C, Buxton MB, Moore D, Krontiras H, Carey L, DeMichele A, u. a. Locally advanced breast cancers are more likely to present as Interval Cancers: results from the I-SPY 1 TRIAL (CALGB 150007/150012, ACRIN 6657, InterSPORE Trial). Breast Cancer Res Treat. April 2012;132(3):871–9. doi:10.1007/s10549-011-1670-4 PubMed PMID: 21796368; PubMed Central PMCID: PMC3975048.
23. Puliti D, Duffy SW, Miccinesi G, De Koning H, Lynge E, Zappa M, u. a. Overdiagnosis in Mammographic Screening for Breast Cancer in Europe: A Literature Review. J Med Screen. 1. September 2012;19(1_suppl):42–56. doi:10.1258/jms.2012.012082
24. Eidgenössisches Departement des Innteren EDI- Bundesamt für Gesundheit BAG- Direktionsbereich Kranken- und Unfallersicherung. Überwachungsprotokoll zu Artikel 12d Absatz 1d der KLV [Internet]. Bern; 2021 [zitiert 13. März 2026]. Verfügbar unter: https://www.bag.admin.ch/dam/de/sd-web/tsAAOJplyMus/Art_12d_d_%C3%9Cberwachungsprotokoll_01_2021_D_fin.pdf
25. Boyd NF, Guo H, Martin LJ, Sun L, Stone J, Fishell E, u. a. Mammographic Density and the Risk and Detection of Breast Cancer. New England Journal of Medicine. 18. Januar 2007;356(3):227–36. doi:10.1056/NEJMoa062790
26. McCormack VA, dos Santos Silva I. Breast Density and Parenchymal Patterns as Markers of Breast Cancer Risk: A Meta-analysis. Cancer Epidemiol Biomarkers Prev. 14. Juni 2006;15(6):1159–69. doi:10.1158/1055-9965.EPI-06-0034
27. Mann RM, Athanasiou A, Baltzer PAT, Camps-Herrero J, Clauser P, Fallenberg EM, u. a. Breast cancer screening in women with extremely dense breasts recommendations of the European Society of Breast Imaging (EUSOBI). Eur Radiol. Juni 2022;32(6):4036–45. doi:10.1007/s00330-022-08617-6 PubMed PMID: 35258677; PubMed Central PMCID: PMC9122856.
28. Comstock CE, Gatsonis C, Newstead GM, Snyder BS, Gareen IF, Bergin JT, u. a. Comparison of Abbreviated Breast MRI vs Digital Breast Tomosynthesis for Breast Cancer Detection Among Women With Dense Breasts Undergoing Screening. JAMA. 25. Februar 2020;323(8):746–56. doi:10.1001/jama.2020.0572
29. Ohuchi N, Suzuki A, Sobue T, Kawai M, Yamamoto S, Zheng YF, u. a. Sensitivity and specificity of mammography and adjunctive ultrasonography to screen for breast cancer in the Japan Strategic Anti-cancer Randomized Trial (J-START): a randomised controlled trial. The Lancet. 23. Januar 2016;387(10016):341–8. doi:10.1016/S0140-6736(15)00774-6 PubMed PMID: 26547101.
30. Hernström V, Josefsson V, Sartor H, Schmidt D, Larsson AM, Hofvind S, u. a. Screening performance and characteristics of breast cancer detected in the Mammography Screening with Artificial Intelligence trial (MASAI): a randomised, controlled, parallel-group, non-inferiority, single-blinded, screening accuracy study. The Lancet Digital Health. 1. März 2025;7(3):e175–83. doi:10.1016/S2589-7500(24)00267-X PubMed PMID: 39904652.
info@gynäkologie
- Vol. 16
- Ausgabe 2
- April 2026