- Point of care Ultraschall: Behandle die Arterien, nicht die Risikofaktoren
Point-of-Care Karotis-Ultraschall gestattet, strahlungsfrei, kostengünstig und reproduzierbar die Risikostratifizierung zu personalisieren, was im klinischen Alltag ein häufiges Problem darstellt. Liegen Karotis-Plaques vor, ist in der Regel eine intensivere sekundärpräventive Behandlung der kardiovaskulären Risikofaktoren, insbesondere auch der Lipide, indiziert. Der hier vorgestellte CTPA-Test (carotid total plaque area) ist schnell erlernbar, benötigt zur Quantifizierung der Plaquelast keine Software und die visuelle Darstellung der atherosklerotischen Plaques verbessert die Therapieadhärenz. Die Effekte der Prävention werden zudem anhand der Abnahme der Plaquelast schon nach 3-6 Monaten sichtbar und sind damit ein stark motivierendes Therapieziel. Der Artikel empfiehlt daher, CTPA als primäre bildgebende Methode zur Risikostratifizierung frühzeitig zu verwenden, zumal Karotisplaque Jahre vor dem Auftreten von Koronarverkalkungen nachweisbar sind. Zudem eignen sich Koronarverkalkungen aus verschiedenen Gründen (Kosten, Strahlenbelastung, Zunahme der Koronarverkalkungen unter Statinbehandlung) nicht als Erfolgskontrolle der präventiven Therapien. Damit ist die CTPA-Methode die einzige, welche als Point-of-Care Management Tool der Atherosklerose zurzeit verfügbar ist.
Point-of-care carotid ultrasound allows for personalized risk stratification in a radiation-free, cost-effective, and reproducible manner, which is a common challenge in everyday clinical practice. If carotid plaques are present, more intensive secondary preventive treatment of cardiovascular risk factors—particularly lipid management—is generally indicated. The CTPA (carotid total plaque area) test presented here is easy to learn, requires no software for quantifying plaque burden, and the visual representation of atherosclerotic plaques improves treatment adherence. Furthermore, the effects of prevention become visible as early as 3–6 months based on the reduction in plaque burden, making this a highly motivating treatment goal. The article therefore recommends using CTPA as the primary imaging method for early risk stratification, especially since carotid plaques can be detected years before the onset of coronary calcifications. Furthermore, coronary calcifications are not suitable for monitoring the success of preventive therapies for various reasons (cost, radiation exposure, increased incidence of coronary calcifications under statin treatment). Thus, the CTPA method is currently the only point-of-care management tool for atherosclerosis available.
Keywords: Point-of-Care-Ultraschall, Kardiovaskuläre Prävention, Risikostratifizierung, Karotis-Atherosklerose
Einleitung
Die kardiovaskuläre Prävention befindet sich an einem Wendepunkt. Während traditionelle Ansätze primär auf die Kontrolle von Risikofaktoren wie Bluthochdruck, erhöhtem Cholesterin oder Diabetes fokussieren (1), zeigen Forschungsergebnisse eine fundamentale Limitation dieser Strategie: Risikofaktoren sind statistische Surrogatmarker, die das tatsächliche Erkrankungsausmass der Gefässwand oft unzureichend abbilden (2–4), und die verwendeten Motivationsmethoden sind gegenüber der Reaktanz zur Korrektur von Laborwerten und Lebensstil häufig machtlos (5, 6).
Der Point-of-Care-Ultraschall (POCUS) der Karotiden ermöglicht demgegenüber eine direkte, unmittelbare Visualisierung der Atherosklerose – jener pathophysiologischen Realität, die letztlich über das kardiovaskuläre Schicksal entscheidet – und weist eine Reihe von entscheidenden Vorteilen gegenüber dem Screening-CT mit Bestimmung des Koronarkalks (CAC-Scan ohne Röntgen-Kontrastmittel) auf.
Das etablierte SCORE2/-OP-Modell, das in der Schweiz gemäss AGLA-Leitlinien zur Risikostratifizierung eingesetzt wird (7), basiert auf epidemiologischen Daten und berechnet statistische Wahrscheinlichkeiten. Dabei zeigt sich jedoch ein systematisches Problem: Die meisten kardiovaskulären Ereignisse ereignen sich bei Personen im niedrigen bis mittleren Risikobereich (3, 4, 8, 9).
Dieser Befund deutet auf eine strukturelle Unterdiagnostik hin, die insbesondere jüngere Patienten und Frauen betrifft. Der Paradigmenwechsel hin zur bildbasierten Prävention – «treating arteries instead of risk factors» (9) – eröffnet neue therapeutische Perspektiven, verbessert die diagnostische Präzision und erhöht die Adhärenz zu präventiven Empfehlungen.
Im Folgenden geben wir eine kurze Forschungsübersicht zu eigenen und internationalen Arbeiten:
a) Karotis-Plaques sind häufig vor dem Auftreten von Koronarverkalkungen vorhanden; b) klinische Implikationen gemäss den neuesten Empfehlungen der Amerikanischen Herzgesellschaften (Karotis-Plaques sollten auch ohne Nachweis von Koronarverkalkungen intensiv präventiv behandelt werden (10); c) Kasuistik; d) Berechnung des Risikos anhand von SCORE2-/OP und Karotis-Plaques oder Koronarverkalkungen; e) Vorstellung der CTPA-Methode und Risikokategorisierung anhand von Karotis-Plaques und Koronarverkalkungen; f) Vorteile von CTPA gegenüber dem CT-Test (Koronarverkalkungen).
Karotis-Atheromatose erscheinen vor Koronarverkalkungen
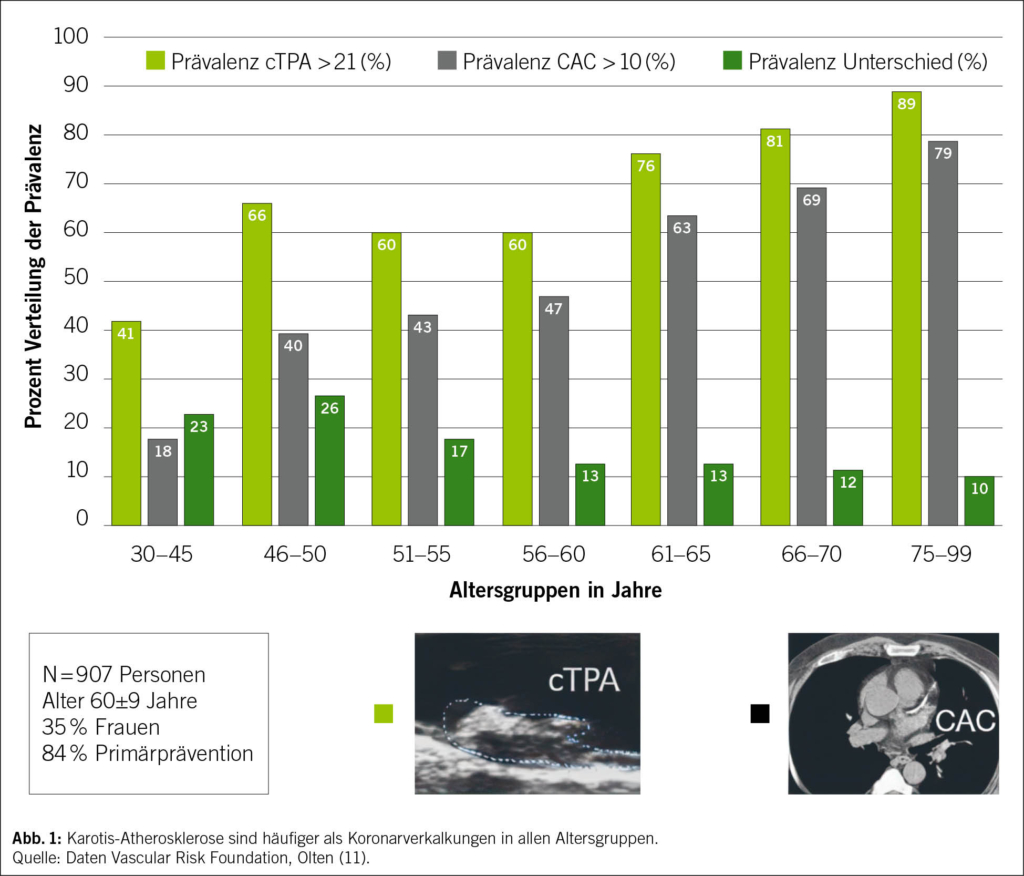
Die zeitliche Sequenz der Atherogenese an verschiedenen Gefässlokalisationen ist von entscheidender präventivmedizinischer Bedeutung. Mehrere Studien belegen übereinstimmend, dass Karotis-Plaques dem Auftreten von Koronarkalk chronologisch vorausgehen – teilweise um Jahre bis Jahrzehnte (Abb. 1).
• Gudmundsson stratifizierte weibliche und männliche Probanden nach Koronarkalk (CAC) und Karotisatheromatose (cTPA-Plaqueflächensumme). Ohne CAC wurde bei 36 % der Frauen und 19 % der Männer eine Karotisplaque festgestellt (Chi2 = 5.01, p = 0.02 für den Geschlechtsunterschied), während nur bei 5.5 % der Frauen und 4.6 % der Männer keine Karotisplaque bei CAC > 0 festgestellt wurde. Eine signifikante Menge an CAC (z. B. Agatston Score CAC ≥ 100) ohne Karotisplaque war bei 1.4 % der Frauen und 1.6 % der Männer vorhanden (12), und die Ergebnisse unter Verwendung der Fläche unter der Kurve (AUC) und der Netto-Reklassifizierungsverbesserung für kardiovaskuläre Ereignisse waren für cTPA und CAC in 3 Modellen, die um Kovariaten bereinigt wurden, vergleichbar.
• In der PESA-Studie, in der 4066 Patienten auf das Vorhandensein von Karotisplaques und Koronarkalk untersucht wurden, stratifiziert nach Geschlecht und mit einem Durchschnittsalter von 45.8 ± 4.3 Jahren, wurde bei 36 % der Männer (24 % der Frauen) das Vorhandensein von Karotisplaques festgestellt, aber CAC wurde nur bei 25 % der Männer und 5 % der Frauen mit familiärer Hypercholesterinämie gefunden (13).
• Bei Patienten mit familiärer Hypercholesterinämie berechneten die Autoren das Durchschnittsalter für das Auftreten von Karotisplaques, Koronarplaques und Koronarkalk und fanden Werte von 17, 26 und 31 Jahren für männliche und 30, 36 und 40 Jahren für weibliche Patienten (14). Daher traten bei familiärer Hypercholesterinämie koronare Verkalkungen bei Männern 14 Jahre später und bei Frauen 10 Jahre später als Karotisplaques auf. Karotisplaques sind auch mit einer höheren Inzidenz der Entwicklung von Koronarkalk in der Zukunft verbunden (15).
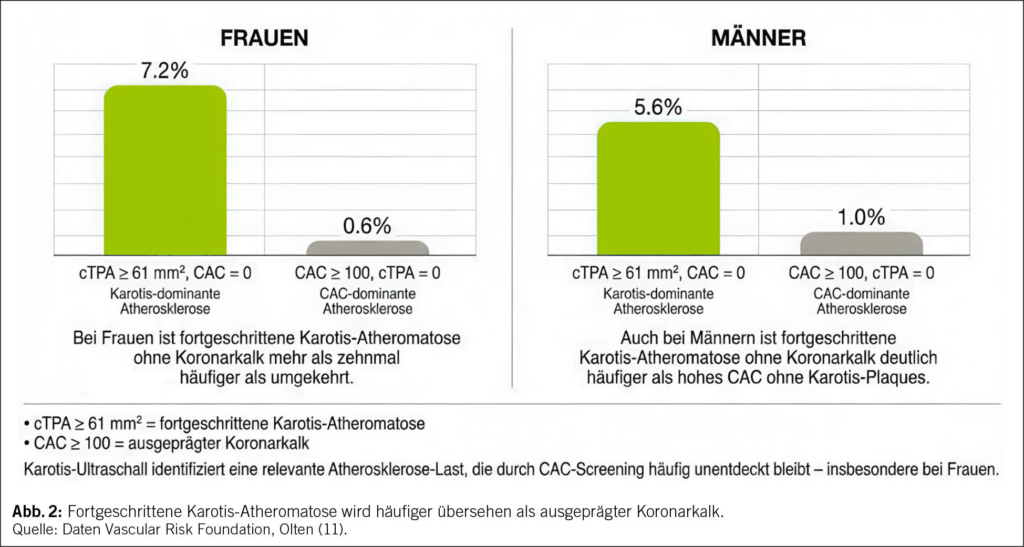
• In einer eigenen Arbeit (11) haben wir bei 907 Personen CAC mit cTPA verglichen (mittleres Alter 60±9 Jahre, 35 % Frauen, 12 % Diabetes mellitus Typ II, 28 % Raucherinnen und Raucher, 84 % Primärprävention) und beobachtet, dass insbesondere bei Frauen häufiger (23 %) eine cTPA > 21 mm2 vorlag als CAC (bei den Männern waren es 17 %), während bei Frauen und Männern CAC > 10 ohne Karotis-Atheromatose nur bei 2.5 % bzw. 2.9 % gefunden wurde (p < 0.01). Auch bei fortgeschrittener Karotis-Atheromatose wiesen 7.2 % der Frauen eine cTPA > 61 mm2 ohne Koronarverkalkungen auf (Männer 5.6 %), während CAC > 100 ohne Karotis-Atheromatose nur bei 0.6 % der Frauen und nur 1.0 % der Männer gefunden wurde (Abb. 2).
Klinische Implikationen: Sekundär- statt Primärprävention
Die frühere Manifestation der Karotis-Atherosklerose eröffnet ein diagnostisches Zeitfenster für präventive Interventionen, bevor koronare Verkalkungen eintreten. Dies ist von besonderer Relevanz, da Koronarkalk bereits einen fortgeschrittenen Heilungsprozess nach vorangegangenen Plaque-Rupturen repräsentiert. Patienten mit CAC = 0, aber nachweisbarer Karotis-Atherosklerose weisen höchstwahrscheinlich bereits nicht verkalkte koronare Plaques auf – jene vulnerablen, lipidreichen Läsionen, die für akute kardiovaskuläre Ereignisse verantwortlich sind und die betroffenen Personen in die Sekundärprävention platzieren. Deswegen sollte gemäss den neuesten US-amerikanischen Empfehlungen selbst bei fehlenden Koronarverkalkungen eine LDL-Behandlung erfolgen (10). Personen mit relevanter Atherosklerose sollten mit den Zielwerten der Sekundärprävention präventiv behandelt werden. Die LDL-Senkung führte bei Patienten mit Atherosklerose oder Diabetes und ohne vorherigen Myokardinfarkt oder Schlaganfall zu einem geringeren Risiko für erste kardiovaskuläre Ereignisse als Placebo, wie die Vesalius-Studie kürzlich bestätigte (16). Damit ist auch erwiesen, dass Personen im Risikobereich der Sekundärprävention aufgrund einer bekannten Atherosklerose ohne vorherigen Herzinfarkt oder Hirnschlag durch eine rechtzeitige LDL-Senkung vor solchen Ereignissen geschützt werden können. Diese Wissenslücke wurde durch die Vesaliusstudie geschlossen und entspricht den wissenschaftlichen Erwartungen.
Kasuistik
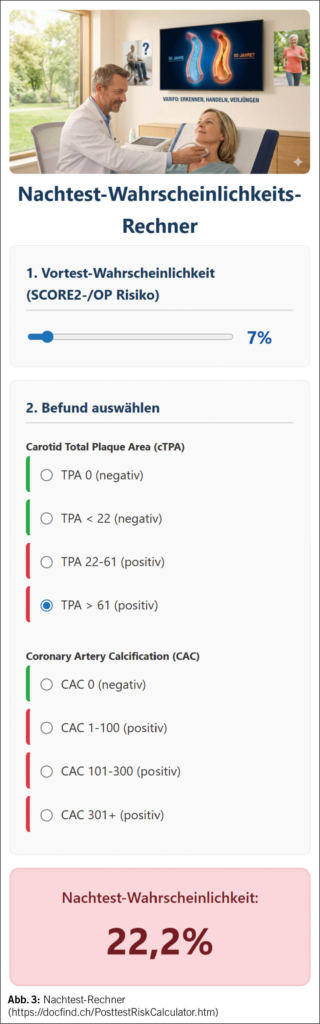
Eine 62-jährige sportliche und gesunde Nichtraucherin meldet sich zur präventiven Untersuchung, weil ihr jüngerer Bruder kürzlich einen Stent benötigte, obwohl auch er Nichtraucher ist. Auch der Vater erlitt im Alter von 52 Jahren bereits einen Herzinfarkt, er war jedoch stark übergewichtig und Typ II Diabetiker. Die Patientin erhält nun einen medizinischen Check-up. Hier die relevanten Befunde: Blutdruck 124/78 mm Hg, Herzfrequenz 62/min, Cholesterin 6.2 mmol/l, HDL 2.2 mmol/l, LDL 3.5 mmol/l, TG 1.0 mmol/l, Lp(a) 645 mg/l (Norm -300). Aufgrund dieser Daten ergibt sich ein kardiovaskuläres SCORE-2-Risiko von 3.2 % in 10 Jahren. Infolge des erhöhten Lp(a) wird noch ein experimenteller, von der Europäischen Herzgesellschaft empfohlener Nachtest-Rechner verwendet (www.lpaclinicalguidance.com/). Dieser berechnet für die nächsten 18 Jahre ein Risiko von 4.6 %, mit Lp(a) ein Risiko von 6.6 %. Aufgrund dieser nicht sehr hohen Risiken und wegen befürchteter Statin-Nebenwirkungen sowie ohnehin nicht hohem LDL-Cholesterin möchte die Patientin sich nicht behandeln lassen. Sie willigt aber ein, die Halsschlagader auf Plaque untersuchen zu lassen. Im POCUS des Hausarztes sieht die Patientin eine Plaqueflächen-Summe von 66 mm2, was einem Arterienalter einer 70-Jährigen entspricht (17). Anhand des Bayes-Theorems bei positivem Testergebnis (Sensitivität 82 %, Spezifität 78 %) und der Berechnung der Nachtest-Wahrscheinlichkeit nach der Formel PTP pos: (PV x SE)/[PV x SE + (1 – PV) x (1 – SP)] steigt das Risiko von 7 % auf 22 % (Abb. 3) (18). Aufgrund der vorhandenen Atherosklerose befindet sich die Patientin in der Sekundärprävention und sollte das LDL-Cholesterin unter 1.8 mmol/l senken sowie Aspirin cardio 100 mg 1-0-0 erhalten. Sie ist damit einverstanden und erwartet eine Regression der Karotis-Atheromatose in 6 Monaten anlässlich der Nachkontrolle.
Einfache Point-of-Care-Messungen
Der POCUS der Karotiden vereint mehrere methodische Vorteile, die ihn für die breite klinische Anwendung prädestinieren. Die oberflächliche anatomische Lage der Arteria carotis communis, interna und externa ermöglicht eine hochauflösende B-Bild-Darstellung mit linearen Hochfrequenzschallköpfen (7–15 MHz). Die standardisierte Untersuchung erfasst das gesamte extrakranielle Karotissystem vom Schlüsselbein bis zum Kieferwinkel, einschliesslich der Bifurkation und des Bulbus – Prädilektionsstellen der Atherogenese.
Die quantitative Erfassung erfolgt mittels Messung der gesamten Plaquefläche (carotid Total Plaque Area, CTPA). Dabei wird jede Plaque – definiert als fokale Intima-Media-Verdickung ≥ 1.0 mm – longitudinal abgebildet, die Plaquefläche planimetrisch umfahren und die Summe aller Plaques beider Karotiden berechnet. Diese Methode weist eine exzellente Reproduzierbarkeit auf, wie in Validierungsstudien gezeigt wurde (19). Im Gegensatz zur blossen Intima-Media-Dicke (IMT), die per definitionem keine Atherosklerose misst, sondern «arterial injury» (19, 20), fokussiert CTPA auf die tatsächliche atherosklerotische Last.
Weitere Informationen zu Studien der Vascular Risk Foundation sind auf der Präventionsseite des Bundesamtes für Gesundheit abrufbar (21).
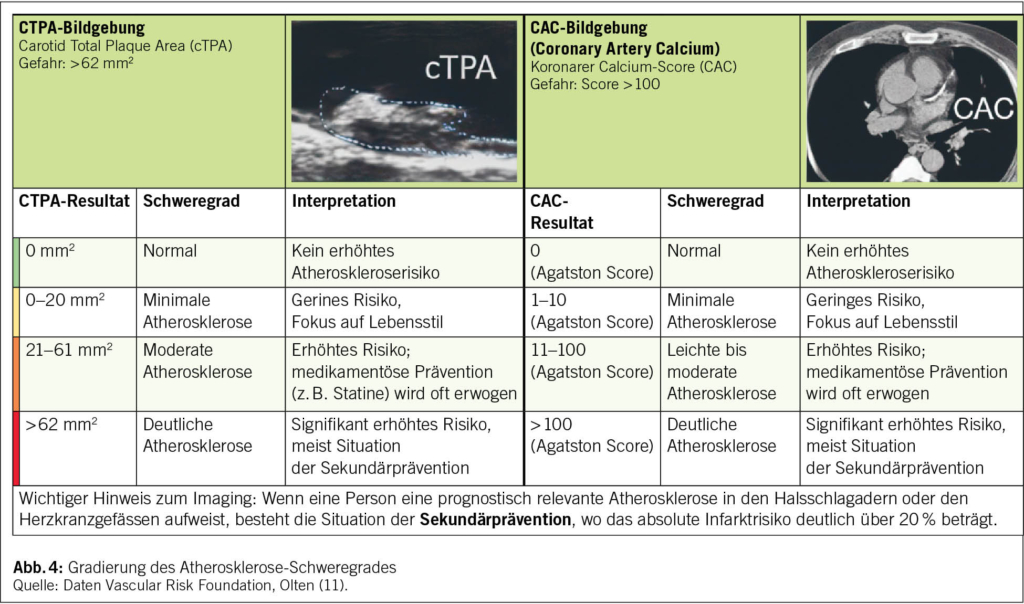
Moderne kompakte Ultraschallgeräte im Tablet-Format ermöglichen die Untersuchung direkt am Krankenbett oder in der Arztpraxis. Nach strukturierter Schulung können Allgemeinmediziner und Internisten reproduzierbare Messungen innerhalb von 1–3 Minuten durchführen und dank der standardisierten Auswertung auch longitudinale Verlaufskontrollen vornehmen. Die Gradierung der Befunde ist in Abb. 4 ersichtlich.
Schlussfolgerungen
Die vorliegenden Daten aus einer Schweizer Kohorte sowie internationale Evidenz konvergieren zu einem klaren Befund: Der Point-of-Care-Ultraschall der Karotiden ist ein überlegenes Instrument zur kardiovaskulären Risikostratifizierung im Vergleich zu konventionellen Risikorechnern und in vielen Situationen auch gegenüber Koronarkalk-CT. Die Vorteile sind vielfältig:
Diagnostisch
Frühere Detektion subklinischer Atherosklerose, insbesondere bei Frauen und jüngeren Patienten. Höhere Sensitivität für behandlungsbedürftige Pathologie als SCORE2/-OP oder Koronarverkalkungen, Neuplatzierung von Erkrankten in die Sekundärprävention.
Therapeutisch
Präzisere Identifikation von Patienten mit Indikation zur intensivierten LDL-Senkung. Möglichkeit zum objektiven Therapiemonitoring und zur individualisierten Steuerung der präventiven Therapieintensität.
Prognostisch
Überlegene Vorhersage kardiovaskulärer Ereignisse. In der ARCO-Studie wurden 95 % der Ereignisse bei den bildbasiert behandelten Patienten erfasst versus 88 % mit SCORE2/-OP. (8)
Praktisch
Strahlungsfrei, beliebig wiederholbar, kostengünstig, am Point-of-Care verfügbar. Keine Kontrastmittel, keine spezialisierte Infrastruktur erforderlich.
Kosten
Verbesserung der Gesundheitsgerechtigkeit durch dezentrale Verfügbarkeit. Reduktion geschlechtsspezifischer Ungleichheiten in der Diagnostik.
Psychologisch
Starker motivationaler Effekt durch Visualisierung und die Erklärung der Plaqueregression (Verjüngung der Arterien!) mit nachweislich verbesserter Patientenadhärenz und Senkung des Reaktanz-Risikos im Gegensatz zu reiner Risikofaktoren-basierter, häufig Angst machender Risikokommunikation.
«Treating arteries instead of risk factors»
Die Implementierung des Konzepts «Treating arteries instead of risk factors» (9) erfordert einen Kulturwandel in der Präventionsmedizin. Statt abstrakte Risikofaktoren zu managen, sollten wir die Atherosklerose als solche diagnostizieren, behandeln und monitorisieren. Der Karotis-POCUS ist das ideale Werkzeug für diesen Paradigmenwechsel: einfach, präzise, patientenfreundlich und kostengünstig. Die Vesaliusstudie (16) hat zudem kürzlich den Beweis erbracht, dass die Behandlung der Atherosklerose «vor dem Infarkt» das relative Risiko um 25 % senkt (erreichte LDL-Senkung hierfür: 1.6 mmol/l).
Die aktuelle Evidenzlage rechtfertigt die Empfehlung, CTPA als primäre bildgebende Untersuchung zur kardiovaskulären Risikobewertung bei Männern und Frauen schon vor dem 40. Lebensjahr einzusetzen. Der Test zur Messung von Koronarverkalkungen behält seinen Stellenwert in speziellen Situationen (sehr hohes Risiko durch Diabetesdauer oder Lp(a), diskordante Befunde bei der CTPA-Messung), sollte aber im Gegensatz zur CTPA Methode nicht primäre Screening-Methode sein.
Die Zukunft der kardiovaskulären Prävention ist bildbasiert, individualisiert und biologisch begründet. Point-of-Care-Ultraschall der Karotiden verkörpert diese Zukunft bereits heute.
Dr. med. Michel Romanens 1
Dr. med. Hermann Lanter 2
Dr. med. Sandor Balint 3
Dr. med. Ansgar Adams 4
1 Facharzt FMH für Kardiologie u. Innere Medizin, Spitalstrasse 9, 4600 Olten
2 Facharzt FMH für Innere Medizin, Spitalstrasse 9, 4600 Olten
3 Facharzt FMH für Innere Medizin, Hauptstrasse 129, 4102 Binningen
4 Arztpraxis Dr. med. Ansgar Adams, BG prevent GmbH, Gesundheitszentrum Koblenz, Bubenheimer Bann 4, D-56070 Koblenz
Copyright
Aerzteverlag medinfo AG
Facharzt FMH für Kardiologie u. Innere Medizin
Spitalstrasse 9
4600 Olten
Arztpraxis Dr. med. Ansgar Adams
BG prevent GmbH
Gesundheitszentrum Koblenz
Bubenheimer Bann 4
D-56070 Koblenz
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Recommendations for EU-wide cardiometabolic health checks. Available at: https://www.escardio.org/news/news-room/recommendations-for-eu-wide-cardiometabolic-health-checks/. Accessed February 7, 2026.
2. Duivenvoorden R., de Groot E., Stroes ESG., Kastelein JJP. Surrogate markers in clinical trials—Challenges and opportunities. Atherosclerosis 2009;206(1):8–16. Doi: 10.1016/j.atherosclerosis.2008.12.009.
3. Romanens M., Szucs T., Sudano I., Adams A. Agreement of PROCAM and SCORE to assess cardiovascular risk in two different low risk European populations. Prev Med Rep 2019;13:113–7. Doi: 10.1016/J.PMEDR.2018.11.019.
4. Romanens M., Sudano I., Adams A., Warmuth W. Advanced carotid atherosclerosis in middle-aged subjects: comparison with PROCAM and SCORE risk categories, the potential for reclassification and cost-efficiency of carotid ultrasound in the setting of primary care. Swiss Med Wkly 2019;149(2930).
5. Georges CMG., Pappaccogli M., Fanelli E., et al. Drug adherence and psychological factors in patients with apparently treatment-resistant hypertension: Yes but which ones? The Journal of Clinical Hypertension 2022;24(11):1436. Doi: 10.1111/jch.14575.
6. Li H., Jia X., Min H., Zhang Y., Wang H., Zhai Y. Relationships between beliefs about statins and non-adherence in inpatients from Northwestern China: a cross-sectional survey. Front Pharmacol 2023;14:1078215. Doi: 10.3389/fphar.2023.1078215.
7. AGLA. SCORE2-/OP Calculator. Available at: https://agla.ch/de/rechner-und-tools/esc-score2-rechner. Accessed October 16, 2025.
8. Romanens M., Adams A., Sudano I., et al. Prediction of cardiovascular events with traditional risk equations and total plaque area of carotid atherosclerosis. Prev Med (Baltim) 2021;147:106525. Doi: 10.1016/j.ypmed.2021.106525.
9. Spence JD., Hackam DG. Treating Arteries Instead of Risk Factors. Stroke 2010;41(6):1193–9. Doi: 10.1161/STROKEAHA.110.577973.
10. Blumenthal RS., Morris PB., Gaudino M., et al. 2026 ACC/AHA/AACVPR/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA Guideline on the Management of Dyslipidemia: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation 2026. Doi: 10.1161/CIR.0000000000001423.
11. Romanens M., Adams A., Szucs TD., Arenja N., Wenger M., Sudano I. Prognostic comparison of cTPA with coronary calcium for cardiovascular risk stratification. Rapid Fire Oral Presentation 2025;(Congress Suisse Society of Cardiology).
12. Gudmundsson EF., Björnsdottir G., Sigurdsson S., et al. Carotid plaque is strongly associated with coronary artery calcium and predicts incident coronary heart disease in a population-based cohort. Atherosclerosis 2022;346:117–23. Doi: 10.1016/j.atherosclerosis.2022.01.018.
13. Fernandez-Friera L., Penalvo JL., Fernandez-Ortiz A., et al. Prevalence, Vascular Distribution, and Multiterritorial Extent of Subclinical Atherosclerosis in a Middle-Aged Cohort: The PESA (Progression of Early Subclinical Atherosclerosis) Study. Circulation 2015;131(24):2104–13.
14. Tada H., Kojima N., Yamagami K., et al. Triple Assessments of Atherosclerosis in Patients With Heterozygous Familial Hypercholesterolemia. JACC: Asia 2025. Doi: 10.1016/J.JACASI.2025.04.011.
15. Mehta A., Rigdon J., Tattersall MC., et al. Association of Carotid Artery Plaque with Cardiovascular Events and Incident Coronary Artery Calcium in Individuals with Absent Coronary Calcification: The Multi-Ethnic Study of Atherosclerosis (MESA). Circ Cardiovasc Imaging 2021;14(4):CIRCIMAGING120011701. Doi: 10.1161/CIRCIMAGING.120.011701.
16. Ndumele CE., Blumenthal RS. VESALIUS and the Anatomy of High-Risk Prevention. New England Journal of Medicine 2025. Doi: 10.1056/NEJME2515447.
17. Romanens M., Ackermann F., Sudano I., Szucs T., Spence JD. Arterial age as a substitute for chronological age in the AGLA risk function could improve coronary risk prediction. Swiss Med Wkly 2014;144:w13967.
18. Romanens M., Ackermann F., Spence JD., et al. Improvement of cardiovascular risk prediction: time to review current knowledge, debates, and fundamentals on how to assess test characteristics. Eur J Cardiovasc Prev Rehab 2010;17(1):18–23.
19. Azarpazhooh MR., Rundek T., Romanens M., et al. Reliability, reproducibility and advantages of measuring carotid total plaque area. Journal of the American Society of Echocardiography 2022. Doi: 10.1016/j.echo.2021.12.016.
20. DRaggi P, Stein J. Carotid intima-media thickness should not be referred to as subclinical atherosclerosis: A recommended update to the editorial policy at Atherosclerosis. Atherosclerosis, 2020; 312, 119-120.
21. Durchbruch in der Prävention: Herz-Kreislauf-Risiken kosteneffizient und ohne Röntgenbestrahlung erkennen. | prevention.ch. Available at: https://www.prevention.ch/article/durchbruch-in-der-prävention-herz-kreislauf-risiken-kosteneffizient-und-ohne-röntgenbestrahlung-erkennen. Accessed February 9, 2026.
der informierte @rzt
- Vol. 16
- Ausgabe 4
- April 2026