- Radiotherapie beim Gallenblasenkarzinom: ein aktuelles Update
Keywords: Gallbladder carcinoma, Radiotherapy, Immunotherapy, Chemotherapy
Einleitung
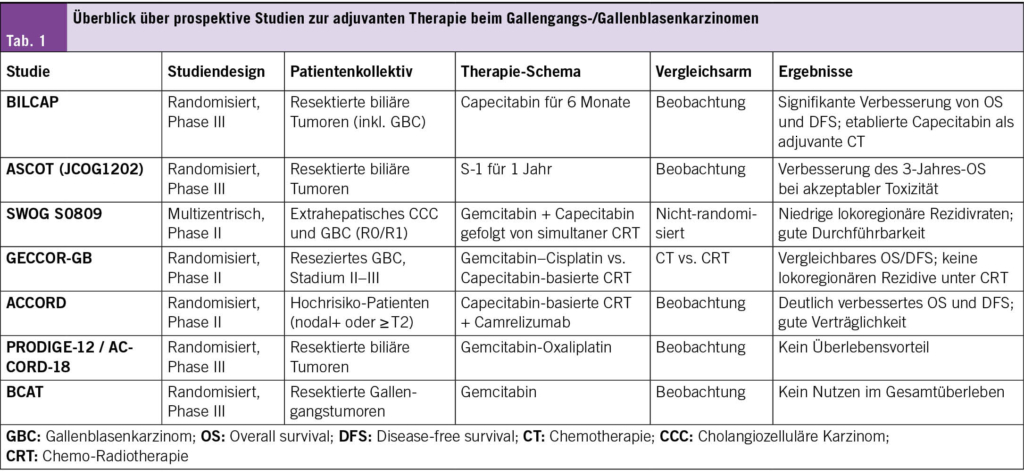
Das Gallenblasenkarzinom ist eine aggressive Erkrankung mit ungünstigen Ergebnissen trotz kurativ intendierter Resektion, was weitgehend auf häufige lokoregionäre und distante Rezidive zurückzuführen ist. Obwohl die adjuvante Radiotherapie (RT) historisch auf der Grundlage retrospektiver Evidenz zur Verbesserung der lokalen Kontrolle eingesetzt wurde, blieb ihr Beitrag zur Verbesserung des Überlebens unklar (1). In den letzten Jahren haben prospektive Studien die adjuvante Chemotherapie (CT), Chemoradiotherapie (CRT) sowie zuletzt die Immuntherapie (IT) beim Gallenblasenkarzinom und anderen biliären Tumoren untersucht und wichtige Erkenntnisse zur Rolle der RT im Kontext der systemischen Therapie geliefert. Dieser Artikel fasst einige zentrale prospektive Studien zusammen, die RT bei Gallenblasen- und biliären Tumoren einsetzten, hebt Überlebens- und Sicherheitsdaten hervor und ordnet die ACCORD-Studie (2) im Kontext früherer Studien wie SWOG S0809 (3), BILCAP (4), ASCOT (5) und GECCOR-GB (6) ein. Eine Übersicht der in diesem Artikel diskutierten Studien ist in Tab. 1 dargestellt.
Adjuvante CRT
SWOG S0809 (3)
Eine multizentrische Phase-II-Studie untersuchte eine adjuvante CRT-Strategie bei biliären Tumoren einschliesslich des Gallenblasenkarzinoms. Die Patienten erhielten zunächst Gemcitabin–Capecitabin, gefolgt von simultanem Capecitabin und RT.
Trotz ungünstiger Risikofaktoren in der Studienpopulation waren die Behandlungsergebnisse für R0- und R1-resezierte Tumoren vergleichbar. Die geringe Rate lokoregionärer Rezidive bei überwiegend distanter Krankheitsprogression spricht dabei für eine wirksame lokale Tumorkontrolle durch die CRT. Das Behandlungsschema erwies sich als gut durchführbar bei akzeptabler Toxizität und unterstützt die Rolle der RT als Bestandteil einer multimodalen adjuvanten Therapiestrategie.
GECCOR-GB (6)
Eine randomisierte Phase-II-Studie bei reseziertem Gallenblasenkarzinom im Stadium II–III verglich eine adjuvante Gemcitabin–Cisplatin-Therapie mit einer Capecitabin-basierten CRT. Beide Ansätze erreichten ein vergleichbares krankheitsfreies und Gesamtüberleben, jedoch eliminierte die CRT lokoregionäre Rezidive und unterstrich damit die Rolle der RT in der lokalen Kontrolle. Die komplette Therapiedurchführung war unter CRT geringer, und Patienten im Stadium III schienen stärker von einer upfront-CT zu profitieren. Insgesamt unterstützt die Studie den Einsatz der RT zur lokoregionären Kontrolle und hebt gleichzeitig die Notwendigkeit hervor, ihre Integration in die systemische Therapie zu optimieren.
Adjuvante CT
Randomisierte Studien zur adjuvanten CT stellen einen wesentlichen Referenzpunkt für kombinierte Therapieansätze dar. In der BILCAP-Studie (4) verbesserte Capecitabin das mediane Gesamtüberleben und das rezidivfreie Überleben im Vergleich zur Beobachtung und etablierte sechs Monate Capecitabin als adjuvanten Therapiestandard. Die ASCOT-Studie (5) zeigte ebenfalls, dass ein Jahr adjuvantes S-1 das 3-Jahres-Gesamtüberleben bei akzeptabler Toxizität verbesserte. Diese Studien etablierten Fluoropyrimidine als effektive adjuvante Therapie und erzielten ein verbessertes Gesamtüberleben ohne RT. Negative Studien wie PRODIGE-12/ACCORD-18 (7) und BCAT (8) zeigten keinen Nutzen Gemcitabin-basierter Regime und unterstreichen, dass nicht alle CT als adjuvante Partner geeignet sind, wodurch Fluoropyrimidine als Rückgrat für Studien zur Kombination von RT und systemischer Therapie gestützt werden.
Neue Ansätze: IT in Kombination mit CRT
Die ACCORD-Studie (2), eine randomisierte Phase-II-Studie bei reseziertem extrahepatischem Cholangiokarzinom und GBC, schloss 93 Hochrisikopatienten (nodal positiv oder T2–T4) ein und verglich Camrelizumab plus Capecitabin-basierte CRT mit Beobachtung. Nach einer medianen Nachbeobachtungszeit von 36 Monaten zeigte ACCORD einen deutlichen Nutzen mit einem 3-Jahres-Gesamtüberleben von 58,2 % gegenüber 30,5 % (HR 0,43) sowie einer Verdopplung des medianen rezidivfreien Überlebens von 13 auf 26 Monate. Die Behandlung war gut verträglich, mit vollständiger Durchführung der CRT, minimalen Verzögerungen der IT, beherrschbarer Toxizität und ohne therapiebedingte Todesfälle.
ACCORD ist die erste prospektive Studie, die zeigt, dass die Hinzunahme einer IT zur adjuvanten CRT die Ergebnisse bei biliären Tumoren signifikant verbessert und auf eine biologische Synergie zwischen RT und PD-1-Blockade hinweist. Da der Kontrollarm jedoch aus Beobachtung bestand und Capecitabin inzwischen als wirksam bekannt ist, müssen die Ergebnisse vorsichtig interpretiert werden. Direkte Vergleiche mit CT allein sind weiterhin erforderlich, und Phase-III-Studien mit aktiven Kontrollarmen werden benötigt, um zu definieren, ob dieser Ansatz einen neuen Standard darstellt.
Rolle der RT
Die aktuelle Evidenz zeigt, dass die RT primär die lokoregionäre Kontrolle verbessert, mit potenziellem Überlebensvorteil, wenn eine effektive systemische Therapie die Fernmetastasierung adressiert. SWOG S0809 (3) zeigte niedrige lokoregionäre Versagensraten und unterstützte den Einsatz der adjuvanten RT zur Kontrolle des Tumorbetts und der Lymphabflussgebiete, was durch GECCOR-GB (6) prospektiv bestätigt wurde, mit keinen lokoregionären Rezidiven nach CRT im Vergleich zu 7 % unter alleiniger CT. Diese Reduktion führte jedoch nicht zu einem überlegenen krankheitsfreien oder Gesamtüberleben, vermutlich da Fernmetastasen die Prognose dominieren. In GECCOR-GB (6) schienen Patienten im Stadium III stärker von intensiver systemischer Therapie als von früher RT zu profitieren, was die Bedeutung der Kontrolle mikrometastatischer Erkrankung unterstreicht. Diese Ergebnisse verdeutlichen die ungelöste Frage der Patientenselektion, da RT für Hochrisikopatienten mit positivem Resektionsrand oder Lymphknotenbefall am vorteilhaftesten sein könnte. Dies wird durch retrospektive Daten gestützt und spiegelt sich in prospektiven Studiendesigns wie ACCORD (2) wider, die ausschliesslich nodal positive oder ≥T2-Erkrankungen einschlossen und einen Überlebensvorteil zeigten. Ob RT bei nodal negativen, randnegativen T2-GBC erforderlich ist, bleibt unklar, und bis randomisierte Vergleiche zwischen CT und CRT vorliegen, müssen Therapieentscheidungen das Risiko lokoregionärer Rezidive gegen zusätzliche Toxizität und logistische Belastungen abwägen.
Sicherheitsprofile
Die adjuvante CRT erhöht die akute Toxizität moderat im Vergleich zur alleinigen CT, insbesondere gastrointestinale Symptome und Zytopenien, wie in den Studien SWOG S0809 (3) und GECCOR-GB (6) beobachtet. Wichtig ist, dass die Hinzunahme der IT in ACCORD (2) die Toxizität nicht wesentlich erhöhte; immunassoziierte Nebenwirkungen waren beherrschbar, mit Therapieunterbrechungen bei nur etwa 13 % der Patienten. Die relativ kurze Dauer der IT könnte die kumulative Toxizität begrenzt haben. Insgesamt zeigen diese Studien, dass die adjuvante CRT bei geeigneten Patienten durchführbar ist, mit akzeptabler Toxizität und potenziellem Überlebensvorteil bei Hochrisiko-GBC.
Kritische Bewertung und zukünftige Perspektiven
Die aktuelle Evidenz unterstützt multimodale adjuvante Therapiekonzepte beim resezierten GBC, jedoch bleibt die optimale Strategie ungeklärt. Sechs Monate Capecitabin, etabliert durch BILCAP (4), stellen den derzeitigen Referenzstandard dar, dennoch existiert keine randomisierte Studie, die CT allein direkt mit CRT verglichen hat. Die zentrale Frage ist, ob die Hinzunahme von RT und nun auch IT einen ausreichenden zusätzlichen Nutzen bietet, um die intensivere Therapie zu rechtfertigen. Obwohl ACCORD (2) beeindruckende Ergebnisse zeigte, erfordert der Beobachtungsarm als Kontrolle eine Bestätigung gegenüber aktiven Vergleichstherapien. Zukünftige Phase-III-Studien sollten CT, CRT und IT-CRT direkt vergleichen, um die individuellen Beiträge von RT und IT zu definieren. Eine verbesserte Patientenselektion ist ebenfalls notwendig, da RT insbesondere für R1- oder nodal positive Erkrankungen relevant sein könnte, während Patienten mit niedrigem Risiko mit CT allein behandelt werden könnten.
Optimale Sequenzierung der Therapie bleibt unklar
SWOG S0809 (3) bevorzugte eine Induktions-CT gefolgt von RT, während GECCOR-GB (6) einen Sandwich-Ansatz verwendete, bestehend aus Capecitabin, gefolgt von simultaner CRT mit Capecitabin und anschliessender weiterer Capecitabin-Gabe, ohne dass sich eine definitive Evidenz zugunsten einer der beiden Strategien ergab. Neue zielgerichtete Substanzen und IT könnten die adjuvante Therapie weiter verändern, wobei die RT weiterhin eine Rolle in der lokalen Kontrolle spielen dürfte. Insgesamt haben Studien der letzten Jahre gezeigt, dass die adjuvante RT die lokoregionäre Kontrolle verbessert und das Überleben steigern kann, wenn sie mit wirksamer systemischer Therapie kombiniert wird. Die ACCORD-Studie (2) legt nahe, dass die Hinzunahme einer IT den Nutzen weiter verstärken könnte, jedoch sind strenge vergleichende Studien, Langzeit-Toxizitätsanalysen und Lebensqualitätsbewertungen erforderlich. Derzeit sollte die adjuvante RT bei Hochrisiko-GBC in erfahrenen Zentren erwogen werden, bis definitive Evidenz ihre präzise Rolle definiert.
Copyright
Aerzteverlag medinfo AG
Universitätsklinik für Radio-Onkologie
Inselspital
Universitätsspital Bern
Freiburgstrasse 18
3010 Bern
Inselspital
Universitätsspital Bern
Universitätsklinik für Radio-Onkologie
Freiburgstrasse
3010 Bern
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Radiotherapie: Prospektive Daten zeigen, dass die adjuvante RT lokoregionäre Rezidive beim GBC reduziert, insbesondere bei Hochrisikopatienten mit positivem Resektionsrand oder Lymphknotenbefall.
- Chemotherapie: Fluoropyrimidin-basierte CT, wie in BILCAP und ASCOT etabliert, verbessert das Überleben gegenüber der alleinigen Operation und stellt den aktuellen adjuvanten Standard dar.
- Chemoradiotherapie: Prospektive Phase-II-Studien zeigen, dass die postoperative CRT durchführbar und wirksam ist, ohne jedoch eine klare Überlegenheit gegenüber CT allein zu belegen, was den Bedarf an Phase-III-Vergleichen unterstreicht.
- Immuntherapie plus Radiotherapie: Die ACCORD-Studie legt nahe, dass die Hinzunahme einer PD-1-Blockade zur Capecitabin-basierten CRT die Ergebnisse bei akzeptabler Verträglichkeit verbessert und eine potenzielle Synergie zwischen RT und IT unterstützt.
- Offene Fragen: Optimale Patientenselektion, Therapiesequenzierung und der zusätzliche Nutzen der RT im Kontext wirksamer systemischer Therapie bleiben ungeklärt und sprechen für einen selektiven, multidisziplinären Ansatz der adjuvanten RT bei Hochrisikopatienten.
1. Lau WY. Gallbladder cancer – A comprehensive review. Surg [Internet]. 2007;6(2):101–10. Available from: http://dx.doi.org/10.1016/S1479-666X(08)80073-X
2. Adjuvant Chemoradiation and Immunotherapy for Extrahepatic Cholangiocarcinoma and Gallbladder Cancer A Randomized Clinical Trial. 2025;11(9):1021–9.
3. Ben-josef E, Guthrie KA, El-khoueiry AB, Corless CL, Zalupski MM, Lowy AM, et al. J OURNAL OF C LINICAL O NCOLOGY SWOG S0809 : A Phase II Intergroup Trial of Adjuvant Capecitabine and Gemcitabine Followed by Radiotherapy and Concurrent Capecitabine in Extrahepatic Cholangiocarcinoma and Gallbladder Carcinoma. 2015;33(24).
4. Primrose JN, Fox RP, Palmer DH, Malik HZ, Prasad R, Mirza D, et al. Capecitabine compared with observation in resected biliary tract cancer ( BILCAP ): a randomised , controlled , multicentre , phase 3 study. :663–73.
5. Nakachi K, Ikeda M, Konishi M, Nomura S, Katayama H, Kataoka T, et al. Articles Adjuvant S-1 compared with observation in resected biliary tract cancer ( JCOG1202 , ASCOT ): a multicentre , open-label , randomised , controlled , phase 3 trial.
6. Adjuvant Gemcitabine Plus Cisplatin and Chemoradiation in Patients With Gallbladder Cancer A Randomized Clinical Trial. 2024;10(8):1116–20.
7. Edeline J, Benabdelghani M, Hammel P, Joly J paul, Boudjema K, Fartoux L, et al. Gemcitabine and Oxaliplatin Chemotherapy or Surveillance in Resected Biliary Tract Cancer ( PRODIGE 12-ACCORD 18-UNICANCER GI ): A Randomized Phase III Study.
8. Ebata T, Hirano S, Konishi M, Uesaka K, Tsuchiya Y, Ohtsuka M, et al. Randomized clinical trial of adjuvant gemcitabine chemotherapy versus observation in resected bile duct cancer. 2018;192–202.
info@onco-suisse
- Vol. 16
- Ausgabe 2
- Mai 2026