- Hépatite C
L’ Organisation mondiale de la santé (OMS) estime que 1,34 million de personnes sont décédées d’ une hépatite virale en 2015 et que 1,75 million ont été nouvellement infectées par le VHC (1). De plus, 71 millions de patients sont infectés par le VHC dans le monde selon l’ OMS. En Suisse, le nombre de personnes chroniquement infectées est estimé actuellement à 36 000-43 000 personnes, ce qui correspond à une prévalence de 0,7 %. Cependant, seul un peu plus de la moitié des porteurs du virus ont été testés. Il faut donc supposer qu’ un grand nombre de patients n’ aient pas encore été diagnostiqués. La morbidité et la mortalité de l’ hépatite C chronique ont dépassé celles du VIH depuis le tournant du millénaire (2). Cet article présente, à travers une perspective historique, les recommandations pour le diagnostic et pour le traitement de l’ hépatite C.
Bien que la prévalence de l’ hépatite C virémique soit en baisse depuis 2000, le pic de morbidité et de mortalité ne sera atteint qu’ en 2030 (3) en raison de l’ évolution naturelle de la maladie et de sa possibilité de séquelles tardives (cirrhose et ses complications, ainsi que carcinome hépatocellulaire). Jusqu’ à l’ introduction des nouveaux traitements appelés antiviraux à action directe (directly acting antivirals, DAA) en 2011 resp. 2014, nous n’ étions pas en mesure de faire face à ce scénario. Toutefois, en 2014, seuls les patients atteints de fibrose avancée (F3) ou de cirrhose (F4) ont pu être traités. Grâce à la collaboration entre le Groupe d’ experts suisse sur l’ hépatite virale (SEVHep), l’ Office fédéral de la santé publique, les associations médicales et les personnes concernées ainsi que les ajustements de prix, une nouvelle ère a pu débuter en octobre 2017. En effet, tous les patients peuvent désormais être traités quel que soit le degré de fibrose. Ainsi, il sera maintenant possible d’ avoir une influence efficace sur les nouvelles infections et les maladies secondaires de l’ hépatite C. La coopération des différents acteurs a conduit à la mise en place de la « Stratégie suisse contre l’ hépatite » visant à réduire à 0 % d’ ici 2030 les nouvelles infections par l’ hépatite C, les carcinomes hépatocellulaires ainsi que les transplantations liées à l’ hépatite C.
Historique de la thérapie de l’ hépatite C
Au début des années 1990, le traitement de l’ hépatite C consistait en une monothérapie à l’ interféron alpha (3 injections par semaine pendant 24-48 semaines), avec des effets secondaires prononcés dans certains cas et un faible taux de guérison (10 %) (4). Depuis la combinaison avec la ribavirine en 1998, le taux de guérison est passé à 30-40 %. La pégylation de l’ interféron en 2001 a prolongé la demi-vie de la substance, facilitant ainsi le traitement et augmentant à nouveau le taux de guérison (45 %). En 2011, les inhibiteurs de la protéase de première génération (bocéprévir et télaprévir) ont été lancés. Ceux-ci inhibent certaines protéines virales du virus de l’ hépatite C (protéase virale NS3-4A) étant importantes pour sa réplication. Il a donc fallu combiner les inhibiteurs de la protéase de première génération avec l’ interféron pégylé et la ribavirine. Ceux-ci ont été limités au génotype 1 et ont parfois entraîné des effets secondaires cutanés graves. Toutefois, le taux de guérison a été amélioré (65 à 75 %). L’ approbation d’ autres substances (inhibiteurs de la polymérase virale NS5B et de la protéine NS5A) a finalement marqué la percée dans le traitement du VHC. En effet, pour la première fois, des thérapies sans interféron pouvaient être appliquées en combinant 2 à 3 agents du type DAA (5). En comparaison avec les thérapies à base d’ interféron, ces thérapies permettent une durée de traitement nettement plus courte (12-24 semaines), avec des taux de guérison considérablement améliorés de 90-100 % et un profil d’ effets secondaires faible.
Diagnostic de l’ hépatite C
Avec la découverte du virus de l’ hépatite C par Qui-Lim Choo, George C. Kuo et Michael Houghton en 1989, le premier test de détection des anticorps a été mis au point et, en 1990, le test de dépistage du virus de l’ hépatite C a également été introduit en Suisse (6). Cela a permis de tester les produits sanguins et de les rendre plus sûrs. L’ hépatite C, tout comme l’ hépatite B et l’ infection par le VIH, est une maladie à déclaration obligatoire en vertu de la Loi sur les épidémies (rapport de laboratoire). Le diagnostic d’ une infection active par le virus de l’ hépatite C est basé sur le test de dépistage des anticorps anti-VHC ainsi que la détection de l’ ARN du VHC dans le sérum par l’ amplification en chaîne par polymérase (« polymerase chain reaction », PCR). La détection des anticorps seule ne suffit pas pour diagnostiquer l’ hépatite C chronique. En effet, environ 20 % des personnes infectées éliminent le virus après la phase aiguë de l’ infection : il s’ agit de l’ hépatite C vécue. Au cours de l’ infection initiale, les anticorps anti-VHC deviennent détectables après sept à huit semaines en moyenne. Le test de détection des anticorps de l’ hépatite C devrait être effectué chez les personnes à risque accru. Il s’ agit notamment des personnes ayant un taux élevé de transaminases ou d’ autres maladies du foie, ayant déjà consommé ou continuant à consommer des drogues par voie intraveineuse ou intranasale, des personnes en hémodialyse, des personnes ayant reçu des produits sanguins ou des transfusions avant juillet 1992, des personnes tatouées, ayant des piercings ou ayant été soumises à des procédures invasives dans des conditions d’ hygiène précaires ainsi que des personnes atteintes du VIH ou de l’ hépatite B. Cela inclut également les partenaires de patients infectés par le VHC, les enfants de mères positives au VHC, les hétérosexuels avec plusieurs partenaires sexuels, les hommes ayant des rapports sexuels avec d’ autres hommes (HSH) ainsi que les personnes ayant des contacts professionnels étroits avec le sang humain. La stratégie suisse de dépistage des hépatites B et C a été révisée en 2013 (7).
Une fois le diagnostic du VHC posé, le patient devrait être dirigé vers un spécialiste pour obtenir des éclaircissements. Les examens complémentaires comprennent des examens de laboratoire, une échographie du foie, une élastographie du foie et éventuellement une biopsie du foie. Ces examens servent à la détermination de la fibrose hépatique (stadification de la fibrose avec F0 à F4) et de la fonction hépatique qui décident de l’ urgence du traitement du VHC. En outre, les patients seront examinés pour détecter la présence de manifestations dites extrahépatiques de l’ hépatite C (p.ex. fatigue prononcée, douleurs articulaires, cryoglobulinémie mixte et vasculite leucocytoclastique, maladies lymphoprolifératives associées au VHC et maladies rénales, etc.), pouvant survenir indépendamment du stade de la fibrose et influencer la décision thérapeutique.
Traitement de l’ hépatite C
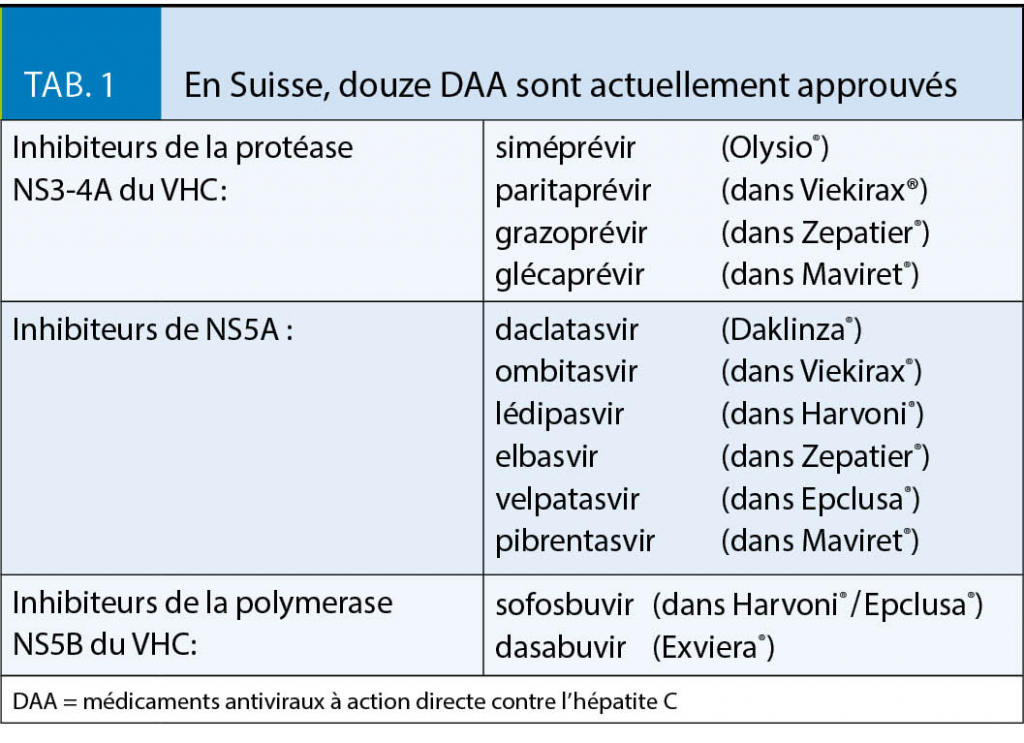
Dans le cas de l’ hépatite C, contrairement au VIH et au VHB (objectif thérapeutique : suppression de la virémie), l’ élimination du virus peut être visée. L’ ARN négatif du VHC, 12 semaines après la fin du traitement, est appelé « réponse virologique soutenue », SVR12 (« sustained virologic response »). 99 % des patients ayant atteint le résultat SVR12 restent guéris même 5 ans après. C’ est pour cette raison que le SVR12 a été accepté comme marqueur de substitution pour la guérison de l’ hépatite C par les autorités d’ enregistrement. Avant le traitement du VHC, il faut toujours exclure la présence d’ une co-infection par le VHB ou le VIH. Tout abus d’ alcool et tout syndrome métabolique doivent être recherchés et traités. Au cours du traitement de l’ hépatite C chez des patients co-infectés par le VHC et le VHB, des réactivations de l’ hépatite B en partie fatales ont parfois été rapportées. Un patient positif à l’ AgHBs doit donc aussi être accompagné par un spécialiste expérimenté durant le traitement de l’ hépatite C. En effet, le traitement de l’ infection à VHB est en général nécessaire. Les patients qui ne sont que des anti-HBc positifs (constellation « anti-HBc-only ») doivent être strictement surveillés, puisque que la réactivation du VHB est également possible dans cette situation. Tous les patients n’ étant pas immunisés contre le VHA / VHB doivent être vaccinés (8). Des recommandations thérapeutiques actualisées peuvent être trouvées auprès des sociétés spécialisées en hépatologie et infectiologie (SASL / SSI) sous forme de recommandations d’ experts (9). Une application (sous forme d’ App) très pratique pour la recherche rapide d’ options thérapeutiques se trouve sur le site www.hcv-advisor.com. Les interactions médicamenteuses peuvent être facilement extraites du Liverpool Interaction Checker à l’ adresse www.hep-druginteractions.org. Le tableau 1 montre les médicaments antiviraux directs actuellement homologués en Suisse pour l’ hépatite C (DAA).
La combinaison choisie pour la durée du traitement dépend du génotype, de la résistance virale, de la fonction rénale, de l’ étendue de la fibrose hépatique, du score de CHILD dans la cirrhose hépatique et de toute tentative de traitement antérieure. Le génotype doit être réévalué si l’ évaluation date depuis longtemps, car l’ anticorps contre l’ hépatite C ne protège pas contre de nouvelles infections.
Les patients atteints d’ insuffisance rénale importante peuvent être traités avec du grazoprevir / elbasvir ou paritaprevir / ombitasvir / dasabuvir (tous éliminés principalement par voie hépatique). Les patients atteints de cirrhose hépatique décompensée (CHILD B / C) peuvent être traités sans inhibiteurs de protéase (9).
Avènement de nouvelles thérapies
D’ autres nouvelles thérapies seront enregistrées dans les mois qui suivent et permettront de guérir les personnes n’ ayant pas pu être guéries du fait de leur résistance aux DAA existants. Les médicaments disponibles en Suisse et les indications actuelles sont continuellement évalués par des experts de SSI, SGG et SASL et sont mis à jour ainsi que publiés sur le site www.sasl.ch
Suivi après un traitement efficace contre l’ hépatite C
La présence d’ anticorps contre le virus de l’ hépatite C ne protège pas contre la réinfection. En effet, les réinfections après une thérapie réussie peuvent être observées en particulier chez les hommes ayant des rapports sexuels avec des hommes et chez les personnes consommant des drogues injectables. Elles peuvent être évitées par une information et une prévention appropriées. Les personnes atteintes d’ hépatite C souffrent souvent d’ autres maladies du foie, telles que la consommation excessive d’ alcool et leurs maladies du foie associées ou la stéatohépatite non alcoolique, doivent être correctement examinées et traitées. Les patients atteints de fibrose avancée ou même de cirrhose avant le traitement doivent probablement être suivis par échographie ou autre imagerie appropriée tous les 6 mois pour le reste de leur vie, car le risque de carcinome hépatocellulaire demeure même après l’ élimination du virus de l’ hépatite C dans cette population (10, 11).
Fondazione Epatocentro Ticino
Via Soldino 5
6900 Lugano
daniel.hagara@hin.ch
Rosengartenstrasse 1d
9000 St. Gallen
thomas.cerny@kssg.ch
Les auteurs ont déclaré avoir aucun conflit d’ intérêts en relation avec cet article.
- Près de 30 ans après la découverte du virus de l’ hépatite C, l’ hépatite C chronique est aujourd’ hui quasiment guérissable à 100 % grâce à une thérapie orale, dont la durée habituelle est de 12 semaines et généralement exempte d’ effets secondaires.
- Avec cette thérapie, la progression de la maladie peut être évitée chez de nombreux individus.
- Il reste le défi de repérer et de traiter en temps opportun les cas pas encore diagnostiqués. La Stratégie suisse contre l’ hépatite (www.hepatitis-schweiz.ch), soutenue par la Confédération suisse, tente de s’ attaquer à ce problème avec l’ objectif à long terme d’ éliminer complètement les hépatites B et C chroniques.
- Le médecin de famille est en charge de la mise en œuvre de la stratégie de dépistage existante, du diagnostic et du traitement des patients avec le spécialiste ainsi que de l’ élimination du virus de l’ hépatite C.
- Il est important d’ assurer un suivi adéquat commençant par des informations individualisées au patient et surveillant en particulier le risque de réinfection, le développement de carcinomes hépatocellulaires et les pathologies hépatiques existantes.
Rérérences :
1. WHO | Global hepatitis report, 2017. Available from: http://www.who.int / hepatitis / publications / global-hepatitis-report2017 / en /
2. Situationsanalyse zu Hepatitis B und C in der Schweiz. 2017. Available from: https://www.bag.admin.ch / bag / de / home / service / publikationen / forschungsberichte / forschungsberichte-uebertragbare-krankheiten / situationsanalyse-hepatitis.html
3. Müllhaupt B et al. Modeling the Haelth and Economic Burden of Hepatitis C Virus in Switzerland. PLoS ONE 10(6): e0125214. https://doi.org / 10.1371 / journal.pone.0125214
4. Davis G L et al. Treatment of chronic hepatitis C with recombinant interferon α. A multicenter randomized, controlled trial. Hepatitis Interventional Therapy Group. N Engl J Med 1989; 321(22):1501-6
5. Solbach P, Wedemeyer H The New Era of Interferon-Free Treatment of Chronic Hepatitis C Viszeralmedizin 2015; 31(4):290-6
6. Choo QL, et al. Isolation of a cDNA Clone Derived from a Blood-borne Non-A, Non-B Viral Hepatitis Genome, Science 1989; 244: 359–362
7. Fretz R et al. Hepatitis B and C in Switzerland – healthcare provider initiated testing for chronic hepatitis B and C infection. Swiss Med Wkly. 2013; 143:w13793.
8. David Semela. Hepatitis C – Diagnostik und Therapie. Therapeutische Umschau (2017), 74(3), 101-108
9. Müllhaupt B et al. Treatment of Chronic Hepatitis C – November 2017 Update, SASL-SSI Expert Opinion Statement. Available from:
https://sasl.unibas.ch / guidelines / SASL-SSI_HepC_EOS20.Nov17.pdf
10. Baumert TF et al. Hepatitis C-related hepatocellular carcinoma in the era of new generation antivirals. BMC Med. 2017; 15: 52-62
11. Cerny A. Screening for liver cancer in high risk patients in Switzerland: Yes, it works, but No, we do not do it systematically! Swiss Med Wkly. 2015;145:w14231
https://doi.org / 10.23785 / Gazette.2019.01.00X
la gazette médicale
- Vol. 8
- Ausgabe 1
- Januar 2019