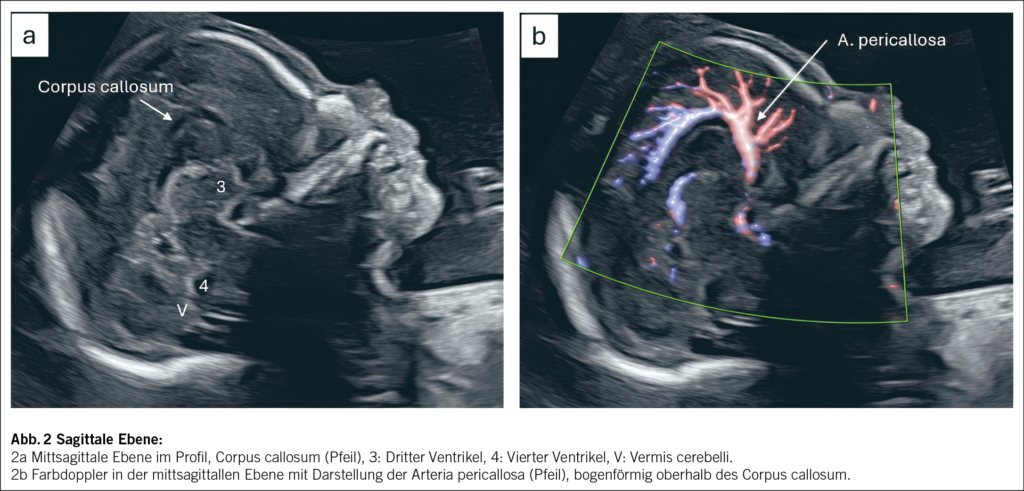
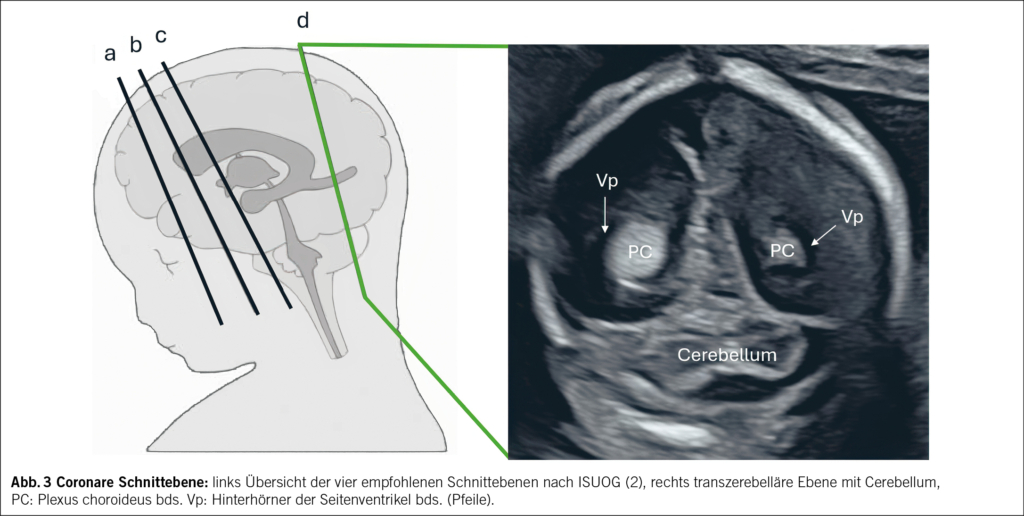
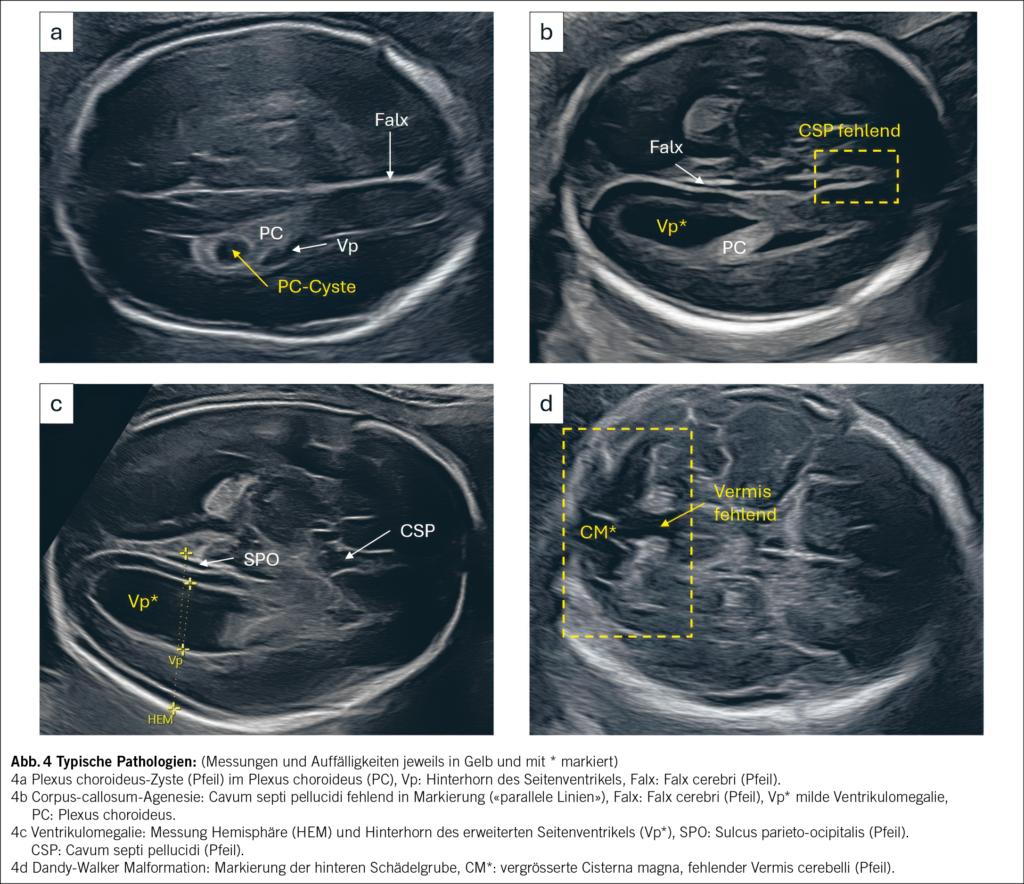
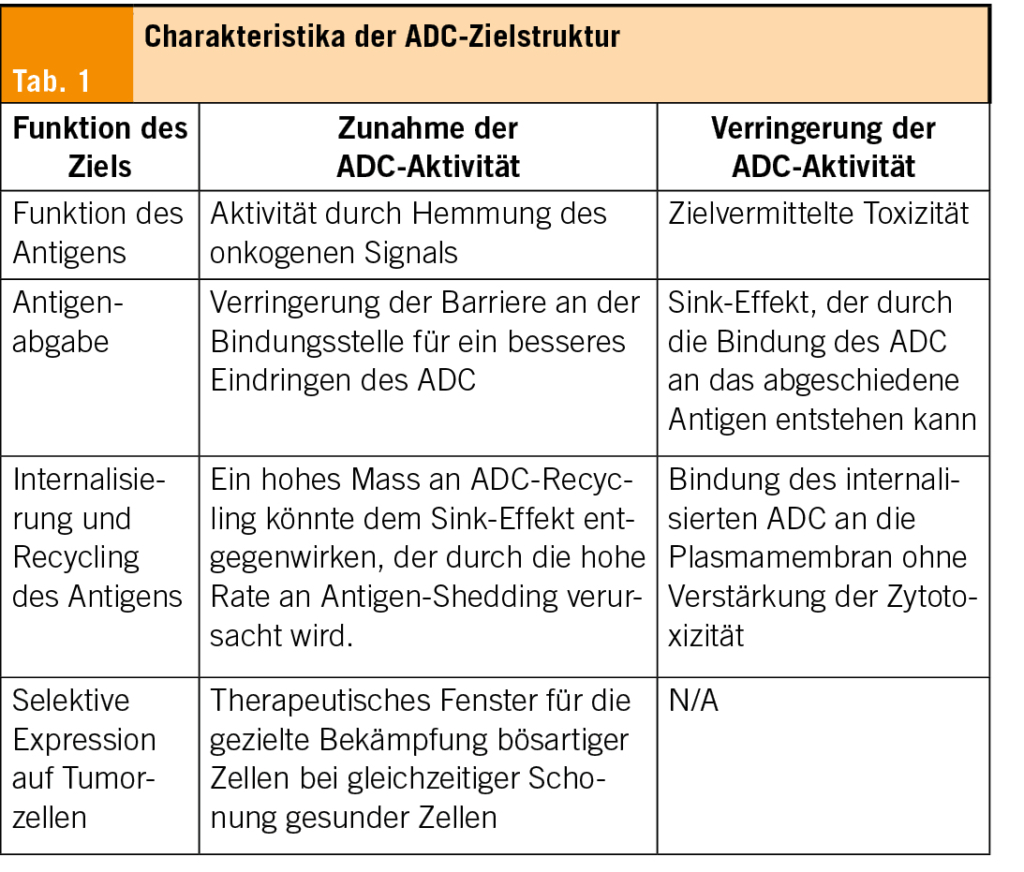
Mitte März fand in Wien die 19. St. Gallen International Breast Cancer Conference (SGBCC25) statt. Prof. Dr. med. Beat Thürlimann, Co-Chair, SGBCC 2025, erklärt die Ziele der SGBCC Konsensus Konferenz.
 Professor Thürlimann, was ist das Besondere am SGB-CC?
Professor Thürlimann, was ist das Besondere am SGB-CC?
nsere Konferenz mit der anschliessenden Konsensuskonferenz ist wirklich einzigartig in der Kongresslandschaft. Wir produzieren oder präsentieren praktisch keine neuen Daten, wir haben uns spezialisiert auf die Umsetzung der wissenschaftlichen Ergebnisse in die Praxis.Die wissenschaftlichen Ergebnisse werden weitgehend in prospektiv randomisierten Studien erarbeitet, mindestens diejenigen, die «practice changing» sind. Und wie wir wissen, sind natürlich solche Studien immer Modelle, die nur eine kleine, gesunde, therapiewillige Patientenpopulation betreffen.
Die Studien sagen uns also eigentlich, was eine bestimmte Behandlung in dieser geprüften Population erreichen kann. Aber sie sagen uns nicht, wie wir einen individuellen Patienten, der vor uns sitzt, in der Praxis behandeln sollen. Das ist die eine Art für die Umsetzung, die wir verbessern wollen. Das andere ist die Fokussierung auf die Kontroverse, also nicht das, was in den Guidelines internationaler Organisationen oder bestimmter Länder zusammengefasst wird.
Sondern wir machen sozusagen genau das Gegenteil: Wir möchten eine Abbildung der Landschaft der Expertenmeinungen geben, dort, wo es eben keine Evidenz gibt, oder nicht diejenige Evidenz, so wie wir uns dies vorstellen, um die Praxis zu ändern. Oder, dort, wo es eine Evidenz gibt, aber die Interpretation der Evidenz und die Extrapolation auf die tägliche Praxis eben umstritten sind, führen wir eine Debatte.
Diese Debatte findet bekanntlich als sogenannte Konsensuskonferenz statt, jeweils am Samstag. Wo gibt es kontroverse Ansichten und wie gehen sie damit in der Praxis um?
Kontroverse Ansichten gibt es natürlich viele, weil wir mit der Fülle der Ergebnisse und Möglichkeiten, die uns die neuen Techniken und die Biotechnologie geben, im wahrsten Sinne des Wortes mehr Fragen als Antworten haben.
Das Zweite ist, dass wir diese Fragen nie alle in großen, prospektiv-randomisierten Studien werden testen können. Zudem ist der Fortschritt der Wissenschaft schneller, als wir regulieren können, eben in Übernahme von Guidelines. Das ist einmal die Landschaft, in der wir uns bewegen. Und inhaltlich ist eines der Hauptanliegen seit bald zehn Jahren die Deeskalation für die grosse Mehrheit und Eskalation für eine gut ausgewählte Minderheit der Patientinnen. Wir versuchen, die Medizin mehr zu personalisieren.
Wo gab es jetzt, wenn Sie etwas herauspicken möchten, kontroverse Ansichten, zu welchen Themen beispielsweise?
Also, es gibt die alten Bestseller, die nicht gelöst sind, vor allem in der Deeskalation. Und hier steht im Vordergrund die loko-regionäre Behandlung mit Chirurgie und Radiotherapie für bestimmte Risikogruppen. Bei der Chirurgie geht es sicher um die Frage, wie weit wir auf die Axillachirurgie ganz verzichten können.
Zwischenzeitlich gab es auch für Niedrigrisikopopulationen zwei wegweisende Studien. Die Frage ist, wie weit können, dürfen oder sollen wir diese Resultate extrapolieren zu den intermediate Risk Patientinnen. Das ist etwas, was man an jedem Tumorboard jede Woche diskutiert und wonach auch viele Patientinnen fragen und sonst vielleicht nicht wagen, den Arzt darüber zu fragen. Darum wäre es gut, das anzusprechen. Wir wissen, dass die Sentinel-Lymphknotenbiopsie ihre Rolle weitgehend verloren hat zur Auswahl der adjuvanten Therapie, mindestens der Systemtherapie. Und zunehmend auch betreffend der Frage der Radiotherapie. Und darum ist das ein sehr wichtiges Thema, das natürlich noch nicht abschliessend gesprochen ist.
Ich kann hier gerade auf die Publikation von Walter Weber verweisen, aus der TAXIS-Studie, die eben gezeigt hat, dass es keinen Zusammenhang gibt mit der Art der Chirurgie in der Axilla und den Findings in der Axilla für die Selektion der adjuvanten Therapien. Und das zeigt, dass wir hier ganz klar auf dem richtigen Weg sind.
Bei der Systemtherapie geht es zum Beispiel um die Frage des weiteren Abbaus der Anthrazykline, insbesondere für höhere Risikogruppen, beispielsweise bei nodal-positiven Karzinomen, die HER2-positiv sind.
Gab es neue, unerwartete Erkenntnisse, Antworten auf Fragen, die Sie bereits jetzt in die tägliche Praxis umsetzen?
Das ist natürlich eine Frage, die jeder Onkologe, jeder Chirurg oder Radio-Onkologe für sich beantworten muss, weil in diesem Graubereich die einen eben die Ergebnisse etwas schneller als andere Ärzte adoptieren und auch implementieren, in ihrer Institution und dann auch im einzelnen Fall.
Hier muss jeder in seiner Umgebung, an seinem Tumorboard Einfluss nehmen, dass beispielsweise diese Deeskalation in vernünftigem Ausmass, aber auch mit vernünftigem Fortschritt eingeführt wird. Ein gutes Beispiel in der Schweiz ist Radiotherapiefraktionierung bei der Bestrahlung der Brust, aber auch bei der Bestrahlung der Lymphknoten.
Und die Frage des Boosts: Hier gibt es auch noch einiges an Potential zur Deeskalationan einigen Institutionen, gerade in der Schweiz, aber vielleicht auch in weiteren Ländern.
Der Konsensus wird im Frühsommer publiziert werden. Ist der Sinn und Zweck eine Anleitung zu geben oder einen Hinweis, wie man in der Therapie oder auch der Diagnostik verfahren kann?
Es ist aber kein starres Gebilde, sondern hier muss man auch flexibel darauf eingehen können. Es war das Ziel seit etwa 2005, dass wir weggekommen sind von diesen Minimal Guidelines, die wir bis dahin betrieben hatten. Damals hatten wir einen Konsens gesucht für das, was nicht umstritten ist, was die Minimal Care für Patienten mit Brustkrebs bedeuten sollte.
Seither wollen wir das Gegenteil machen. Wir wollen uns auf die Kontroverse konzentrieren. Wir begannen das Panel zu befragen, was die Top Ten of Controversy sind. Diese Themen haben wir dann in den Kongress eingebaut und natürlich auch in die Fragen des Konsensus-Meetings.
Es war von Anfang an klar, dass dieses Papier, das wir produzieren, eben keine Guideline sein soll. Ja, wir glauben, dass es nicht einmal eine Public-Health-Instrument sein soll, sondern es soll ein Instrument für den einzelnen Arzt sein. Für die Situation, wo es eben keine Guidelines gibt, um zu sehen, wie er seinen Patienten oder seine Patientin beraten soll, um schliesslich zu einer vernünftigen Entscheidung zu kommen. Die ist oft nicht richtig und nicht falsch, sondern nur vernünftig. Es ist also ein ärztliches Hilfsmittel und kein Public-Health-Tool.
Werfen wir einen Blick in die Zukunft. Können Sie einen Ausblick geben, wohin die Reise bei der Therapie des frühen Mammakarzinoms geht?
Die Reise geht weiter, denn es ist ein kontinuierlicher Prozess. Patientinnen mit frühem Brustkrebs im Stadium 1 und 2 haben sehr gute Überlebenschancen, wenn sie Zugang zur richtigen Behandlung haben. Doch die Herausforderung bleibt zweifach: Erstens bei den Patientinnen in low- und middle-income countries, die den Zugang zu dem Fortschritt haben sollen, den wir auch haben. Und das ist natürlich eine Verantwortung der Regulierer und der Industrie. Und das zweite ist, dass die Patientinnen in diesen Gegenden früher zur Diagnose kommen. Hier müssen wir weiter vorwärts machen.
Gibt es bestimmte Medikamentengruppen, die möglicherweise in naher Zukunft mehr an Bedeutung gewinnen?
Keine Frage, wir werden vermehrt «Targeted Agents» einsetzen, so wie wir es bereits in der vorgeschrittenen Krankheit machen. Diese werden vermehrt in die adjuvante Situation übernommen werden. Es braucht aber noch ein bisschen Arbeit dazu. Dies ist eine Herausforderung, da zumindest in den Industriestaaten die disease-free-survival-Raten schon sehr hoch sind und es darum entsprechend grosse Studien braucht, um in den mittleren und niedrigen Risikopopulationen einen Unterschied zeigen zu können.
Da wird vermutlich auch die künstliche Intelligenz eine wichtige Rolle spielen, bei der Diagnostik und bei der Findung von Therapiemöglichkeiten?
Wir haben eine ganze Session für dieses Thema angesetzt. Und wir haben natürlich die Session bewusst mit Ärzten, mit Care-Givers für Breast-Cancer besetzt und nicht mit Computerspezialisten. Und hier hat uns zum Beispiel Herr Jakob Kather aus Dresden die verschiedenen Optionen gezeigt, in welche Richtung wir AI auch anwenden können.
Das ist beispielsweise wichtig für die Pathologie, wo die AI zur automatisierten Befundung eingesetzt wird und damit Zeit und Aufwand eingespart werden können. Das ist mehr als nur ein Segen, gerade für LMIC, und ein grosser Sprung nach vorne. Die AI kommt nicht nur in der Pathologie oder Radiologie zur Anwendung, wo sie ja teilweise schon etabliert ist, sondern in der Session wurde auch ein Beispiel gezeigt, wie diese Technologie während des Tumorboards angewendet werden kann.
Sie haben vorhin die höheren Raten an längerem krankheitsfreiem Überleben angesprochen. Darf man sagen, dass das frühe Mammakarzinom in vielen Fällen eine behandelbare Erkrankung wurde, wo echte Heilungschancen bestehen?
Also wir können sagen, dass echte Heilungschancen schon seit langem bestehen. Viele Patientinnen werden durch Chirurgie alleine geheilt oder durch Chirurgie und Radiotherapie. Doch wir möchten gute Therapieaussichten in über 90 Prozent der Fälle für alle oder für fast alle Patientinnen erreichen können. Da sind wir aber noch ein Stück davon weg, besonders für Patientinnen, die im Stadium 2 und 3 zur Diagnose kommen.
Wir sind praktisch am Ende unseres Gesprächs. Haben Sie noch etwas mitzuteilen? Eine Take-home-Message? Etwas, was Ihnen besonders am Herzen liegt?
Um im Gebiet der Kontroverse zu bleiben: Es ist oft gut, dass von den behandelnden Ärzten vorgeschlagen wird, vielleicht eine Zweitmeinung einzuholen. Ich mache viele solche Zweitmeinungen und ich sehe, dass, wenn auch die Meinung des Tumorboards bestätigt wird, dies viel Ruhe bei den Patientinnen und den Angehörigen bringt. Das ist billig, gut und schnell, wie kaum eine andere Intervention, die wir bei den Patienten machen können. Das würde ich anregen, vermehrt zu nutzen.
Und: Wir haben im Konsensus-Meeting auch schon abgestimmt, dass Patienten unterstützt werden können, nicht die maximale Therapie zu machen oder davon auszugehen, dass Patientinnen dies ohnehin wünschen, sondern dass es in Ordnung ist, im Rahmen des sogenannten proper treatment Therapien wegzulassen, wenn der absolute Gewinn klein ist. Dies soll im Einzelfall mit der Patientin besprochen werden. Aber wir dürfen nicht davon ausgehen, dass alle Patienten alles machen wollen, nur weil wir so denken oder weil wir zu wenig Interaktion mit dem Patienten haben und stattdessen von Safety First ausgehen und dann eben eine Eskalation der Behandlung machen, von der die Patientin kaum eine Chance hat, zu profitieren.