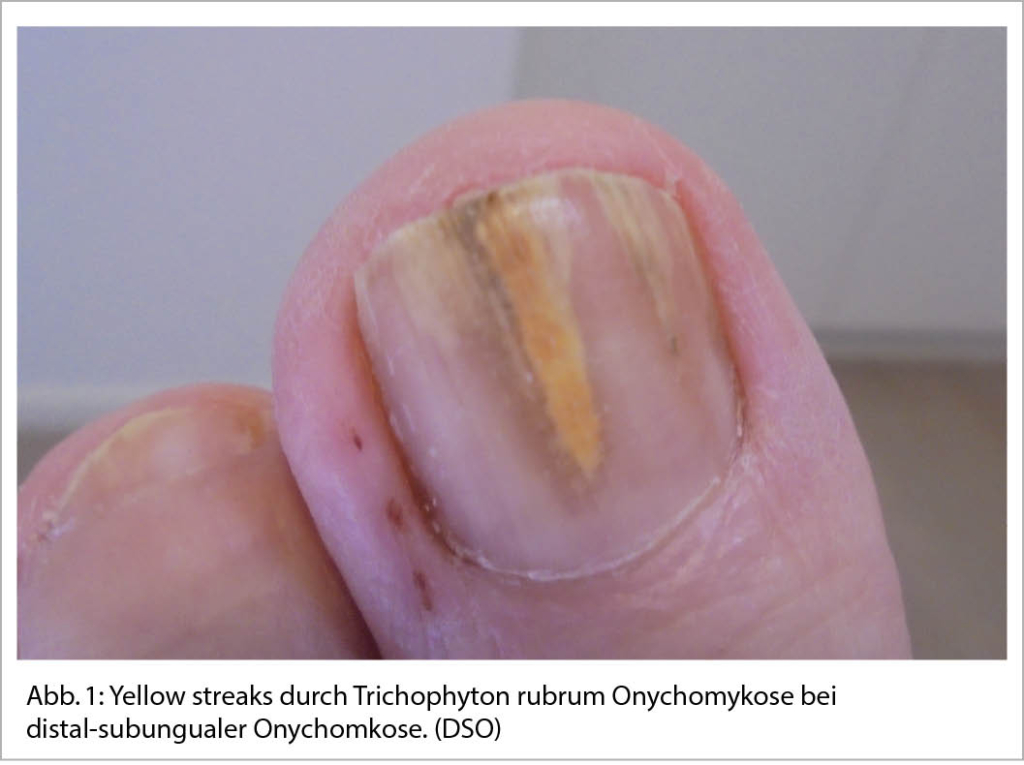
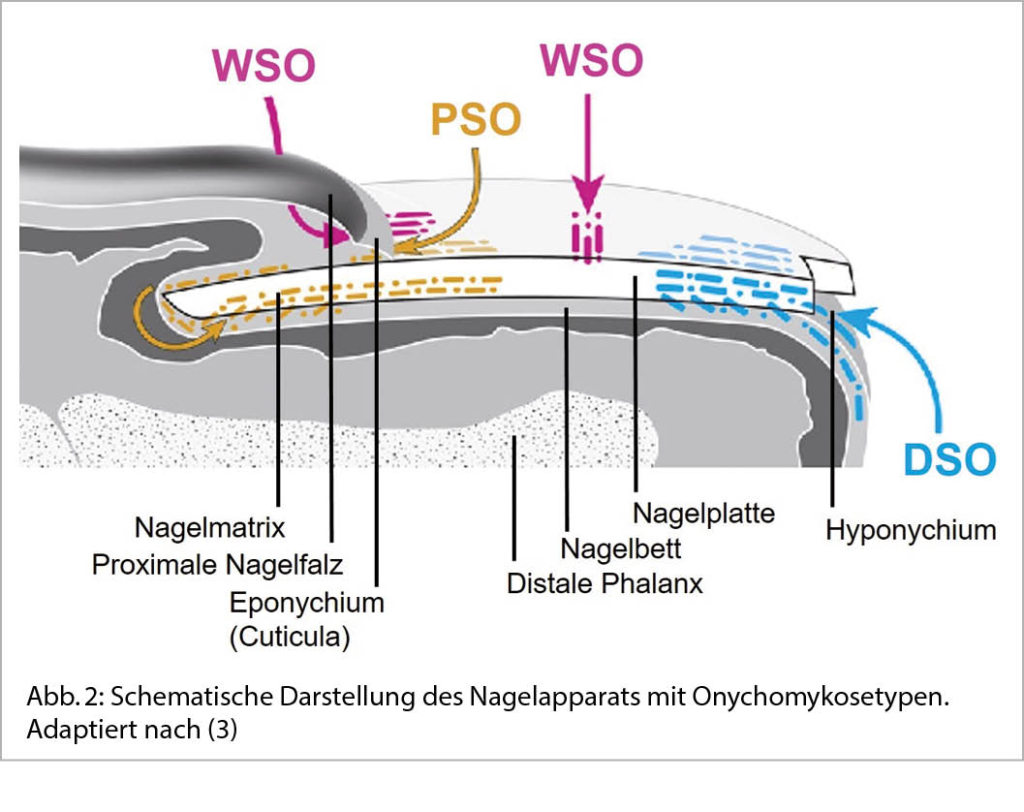
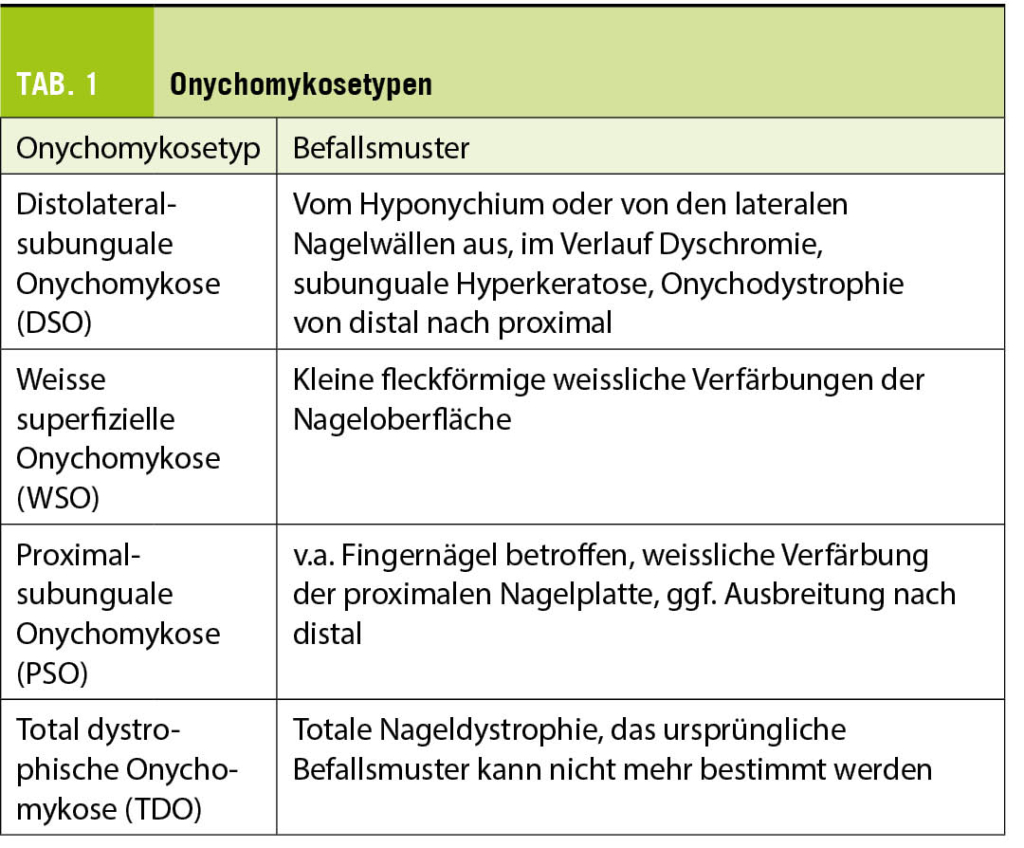
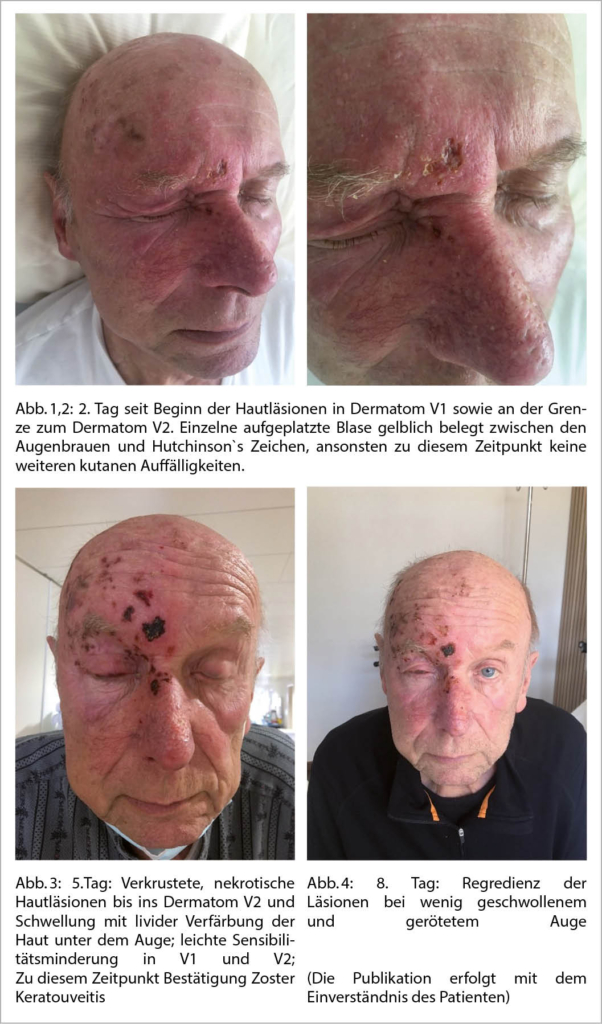
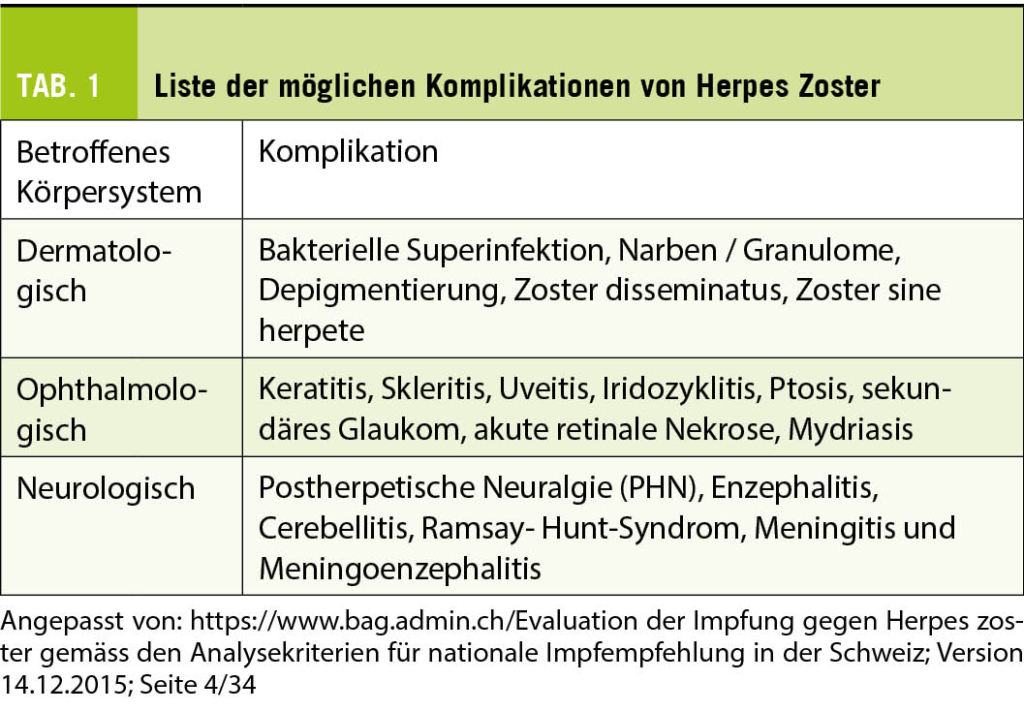
Die Onychomykose ist eine global häufig vorkommende Erkrankung mit einer altersabhängigen Prävalenz von 10% der Allgemeinbevölkerung bis hin zu 50% der > 70-Jährigen und stellt die Hälfte aller Nagelpathologien dar (1). Auslöser sind in den meisten Fällen anthropophile Dermatophyten, hiervon der Grossteil (ca. 80 % der Fälle) durch Trichophyton rubrum (2). Die Onychomykose ist in ihrem klinischen Erscheinungsbild häufig durch gelb-braune flammenförmige Nagelinvasion (yellow streaks, Abb. 1) charakterisiert. Die Unterscheidung in distolaterale-subunguale (DSO), weisse superfizielle (WSO), proximal-subunguale (PSO) sowie total-dystrophische Onychomykose (TDO) ist bezüglich Abklärung und Therapie relevant (Tab. 1, Abb. 2). Die Behandlung der Onychomykose stellt häufig eine Herausforderung dar.
Onychomycosis is a globally common disease with an age-dependent prevalence ranging from 10% of the general population to 50% of >70-year-olds and represents half of all nail pathologies (1). Triggers are in most cases anthropophilic dermatophytes, of which the majority (about 80% of cases) are caused by Trichophyton rubrum (2). The clinical appearance of onychomycosis is often characterized by yellow-brown flame-like nail invasion (yellow streaks, Abb. 1). The differentiation into distolateral-subungual (DSO), white superficial (WSO), proximal-subungual (PSO) and total dystrophic onychomycosis (TDO) is relevant with regard to diagnostics and therapy (Tab. 1, Abb. 2). The treatment of onychomycosis is often challenging.
Key Words: Onychomycosis, anthropophilic dermatophytes, yellow streaks
Einleitung
Die Nagelbeteiligung bei nicht infektiösen Erkrankungen wie Psoriasis, Lichen ruber planus oder Alopezia areata können eine Onychomykose imitieren. Der wichtigste Schritt zur adäquaten Behandlung der Onychomykose ist deshalb der Erregernachweis, um dem Patienten im (eventuell wiederholt) negativen Fall unnötige, langwierige und kostenintensive Behandlungen zu ersparen. Trichophyton rubrum und Trichophyton mentagrophytes sind in Europa derzeit die häufigsten Erreger der Onychomykose (4). Aber auch seltenere Dermatophyten wie z.B. Epidermophyton floccosum können eine dermatophytäre Onychomykose auslösen. Weniger häufig wird eine Onychomykose auch durch Hefepilze oder Schimmelpilze ausgelöst. Hierbei handelt es sich vorwiegend um Candida parapsilosis, Candida albicans, respektive Fusarium spp., Acremonium, oder Scopulariopsis brevicaulis. Letzterer kann zu einer bräunlichen zimtfarbenen Verfärbung durch die Pigmentierung der Pilzsporen im Nagelkeratin führen. All diesen seltenen Erregern ist gemein, dass sie äussert therapieresistent sind und eine hohe Rezidivrate aufweisen. Bei Candida-Onychomykose sollte (wie auch bei einer proximalen subungualen Onychomykose) nach einer Immunsuppression (HIV, hämatologische Neoplasien etc.) gesucht werden.
Diagnostik
Zur Diagnostik der Onychomykose stehen verschiedene Labortechniken zur Verfügung. Eventuell schon begonnene Vortherapien mit topischen Antimykotika sollten über einen Zeitraum von 2 Monaten, systemische Antimykotika über 3 Monate vor der Probenentnahme abgesetzt werden, um einen Erregernachweis zu ermöglichen.
Die Mikroskopie des Direktpräparats (z.B. mit KOH) und die Kultur (z.B. 4% Sabouraud-Glucose-Agar) haben nach wie vor eine hohe Relevanz, letztere gilt weiterhin als Goldstandard. Sie benötigen aber Erfahrung, Zeit und eine geübte Abnahmetechnik. Der erkrankte Nagel sollte vor der Probenentnahme zunächst mit 70-100%igem Alkohol desinfiziert werden, damit eine bakterielle Kontamination der Kultur vermieden wird. Es sollte reichlich betroffenes Nagelmaterial in feinen Spänen gewonnen werden. Neben der subungualen Probengewinnung bei der sehr häufigen disto-lateralen subungualen Onychomykose ist auch die Fräsung des betroffenen Nagelanteils (mit Gewinnung von feinem Nagelspänen) eine sinnvolle diagnostische und auch adjuvante therapeutische Option. Bei weisser superfizieller Onychomykose sollte das oberflächlich betroffene Nagelmaterial mit z.B. einer Kürette gewonnen werden, bei der seltenen proximalen subungualen Onychomykose ist eine Punchbiopsie zur Materialgewinnung zu erwägen. Das Kulturergebnis ist nach ca. 2 – 4 Wochen zu erwarten und kann im Gegensatz zur Direktmikroskopie, Histopathologie (PAS-Färbung) oder modernen Nachweismethoden (PCR oder MALDI-TOF) einen vitalen Erregernachweis erbringen. Die Sensitivität beträgt bei nicht vorbehandelter Onychomykose bei der Histopathologie 82%, bei der Kultur 53% und bei der Direktmikroskopie 48%, bei vorbehandelten Patienten respektive 88%, 33% und 50% (5), weshalb bei negativer Kultur, jedoch persistierendem klinischen Verdacht eine Punchbiopsie zur Nagelentnahme sinnvoll sein kann vor monatelanger antimykotischer Therapie.
Seit einiger Zeit steht auch ein molekularbiologischer DNA-Nachweis mittels PCR zur Verfügung, die das Ergebnis deutlich schneller, im Idealfall bereits innert eines Tages, liefern kann. Hierbei gilt es jedoch zu bedenken, dass die PCR bisher meist nur ein limitiertes, vordefiniertes Erregerspektrum untersucht (das konkrete Spektrum kann von Labor zu Labor variieren und sollte vorab dem Untersucher bekannt sein) und der DNA-Nachweis keine Aussage über die biologische Aktivität und Vitalität der Erreger erlaubt. Die MALDI-TOF-Technik (Matrix-assisted laser desorption time-of-flight-Massenspektrometrie) bleiben spezialisierten Laboratorien vorbehalten und erlauben ebenfalls keine Aussage über die Vitalität des nachgewiesenen Erregers.
Lokaltherapie (topische Therapie)
Zu Beginn der Therapie nach Vorliegen des positiven Kulturergebnisses sollte zunächst der klinisch betroffene Nagelanteil zur Verringerung der Sporen- und Myzellast soweit wie möglich entfernt werden. Hierfür kann bei rein distaler (DSO) Nagelinfektion der Nagel einfach abgeschnitten werden. Sobald der Befall sich weiter nach proximal fortsetzt und die Nagelplatte zudem verdickt ist, ist eine Fräsung zur Abflachung des Nagels und zur Verbesserung der Wirkstoffaufnahme z.B. im Rahmen einer podologischen Behandlung vor Beginn einer Lokaltherapie mit einem antimykotischen Nagellack vorteilhaft. Auch eine Nagelentfernung durch Aufweichung des Nagels mit 40 – 50%iger Harnstoffsalbe ist in Absprache mit dem Patienten zu erwägen (kommerziell erhältlich ± Antimykotikum, in der Schweiz z.B. Onyster® Nagelsalbe oder Canesten® extra Nagelset, in der Regel nicht via Krankenkasse getragen). Es ist darauf zu achten, dass die keratolytische Harnstoffsalbe lediglich auf den Nagel appliziert wird, damit Mazerierung/Entzündungen der umliegenden Haut vermieden werden. Zum Schutz sollte ein Pflaster oder Klebefolie über die Salbe angebracht werden, so dass die Salbe auf dem Nagel verbleibt und die Haut geschützt wird. Die Salbe muss, je nach Nageldicke, ca. 2 Wochen für dünne Nägel und bis zu 4 Wochen für dicke Nägel, kontinuierlich, d.h. ganztägig, angewandt werden, da es bei Absetzen bereits nach wenigen Stunden zu einem erneuten Aushärten des Nagels kommt (ein kurzes Entfernen der Salbe zum Duschen ist unproblematisch). Nach adäquatem Anwendungszeitraum kann der weich gewordene Nagelanteil mit einem mitgelieferten Spatel oder mittels Schere weitgehend entfernt und die Therapie mit einem topischen Antimykotikum (s.u.) fortgesetzt werden.
Eine früher in Lokalanästhesie oft durchgeführte chirurgische Entfernung (Avulsion) des infizierten Nagels mit speziellem extrahierendem Nagelwerkzeug gilt heute als weitgehend obsolet und sollte nur noch in wenigen individuellen Ausnahmefällen eingesetzt werden. Zum einen sind postoperative bakterielle Infektionen der Nagelmatrix und Nagelbetts nicht selten, darüber hinaus bleibt die Nagelmatrix bei Matrixbefall auch nach Nagelextraktion mit Myzel infiziert. Oft werden die Nagelmatrix und das Nagelbett im Rahmen einer Extraktion irreparabel geschädigt und es resultiert ein dauerhaft verformtes Nagelwachstum (permanente Onychodystrophie).
Nach Entfernung der infizierten Nagelanteile sollte die antimykotische Therapie initiiert werden. Als Faustregel gilt, dass bei einem distalen Befall bis zu 50% der sichtbaren Nagelplatte eine alleinige topische Therapie häufig ausreicht. Bei Therapieresistenz oder bei einem Befall von mehr als 50% der Nagelplatte ist die Kombination von topischer mit systemischer Therapie empfohlen (6).
Die Lokaltherapie sollte sowohl den noch bestehenden Nagel, als auch das ggf. durch die Nagelablösung freiliegende Nagelbett sowie die Nagelfalze behandeln. Hierfür stehen für den verbliebenen Nagelanteil Nagellacke und für das freiliegende Nagelbett Cremes mit unterschiedlichen Wirkstoffen zur Verfügung. Die in Europa verbreiteten topischen antimykotischen Breitspektrum-Wirkstoffe (mit Wirksamkeit auf Dermatophyten, Hefen und Schimmelpilze) umfassen vorwiegend Amorolfin, welches als Acryllack eins bis zweimal pro Woche auf den Nagel (nicht jedoch auf die Haut) aufgetragen wird und bei dem vor erneutem Auftragen die vorherige Schicht wieder abgelöst werden muss, sowie Ciclopirox, welches mindestens einmal täglich nach dem Duschen (bei Wasserkontakt häufiger) als meist wasserlöslicher Nagellack (Hydrolack) sowohl auf den Nagel als auch auf die Haut aufgetragen wird, ohne dass die vorherigen Lackschichten entfernt werden müssen. Zur Behandlung des Nagelbetts (nicht jedoch des Nagels) stehen diverse Wirkstoffe in Form von Cremes zur Verfügung (Terbinafin, Miconazol, Ciclopirox, Bifonazol u.a.). Neuere topische Antimykotika wie Efinaconazol (welches sowohl auf dem Nagel als auch auf der Haut angewendet werden kann und eine verbesserte Permeation aufweist), Tavaborol (auch hier mit verbesserter Permeation) oder Tioconazol sind in der Schweiz nicht zugelassen. Andere Medikamente, wie z.B. Luliconazol, ME1111 oder K101 Nail Solution, sind aktuell erst in Entwicklung.
In zwei Studien mit 490 Teilnehmern ergab sich eine qualitativ moderate Evidenz, dass Ciclopirox 8% Hydrolack wirksamer ist als Ciclopirox 8% Acryllack oder Amorolfin 5% Acryllack bezüglich Heilungsrate (7). In einer weiteren Studie, bei der Ciclopirox 8% Hydrolack mit 5% Amorolfin Acryllack bei milder bis moderater Onychomykose verglichen wurden, zeigt sich ebenfalls eine Überlegenheit von Ciclopirox 8% Hydrolack (Komplette Heilungsrate 35% vs. 11.7%) (8).
Systemische Therapie
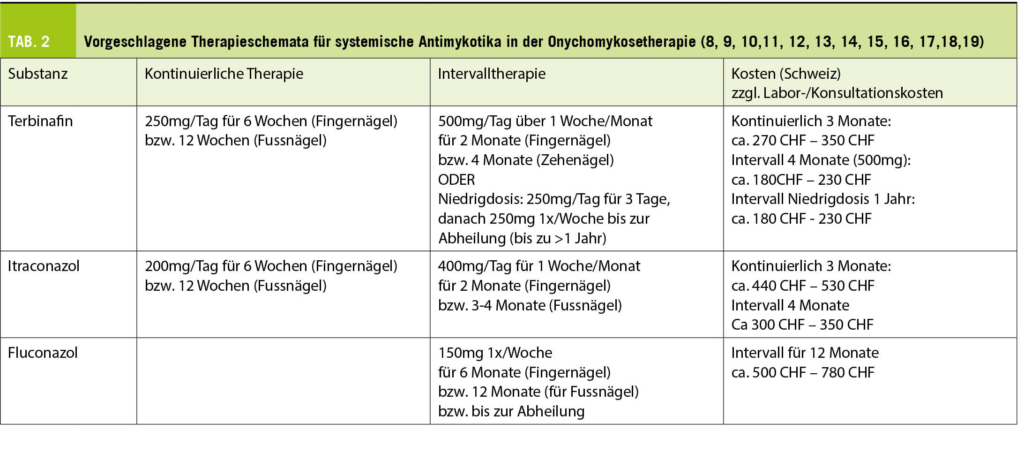
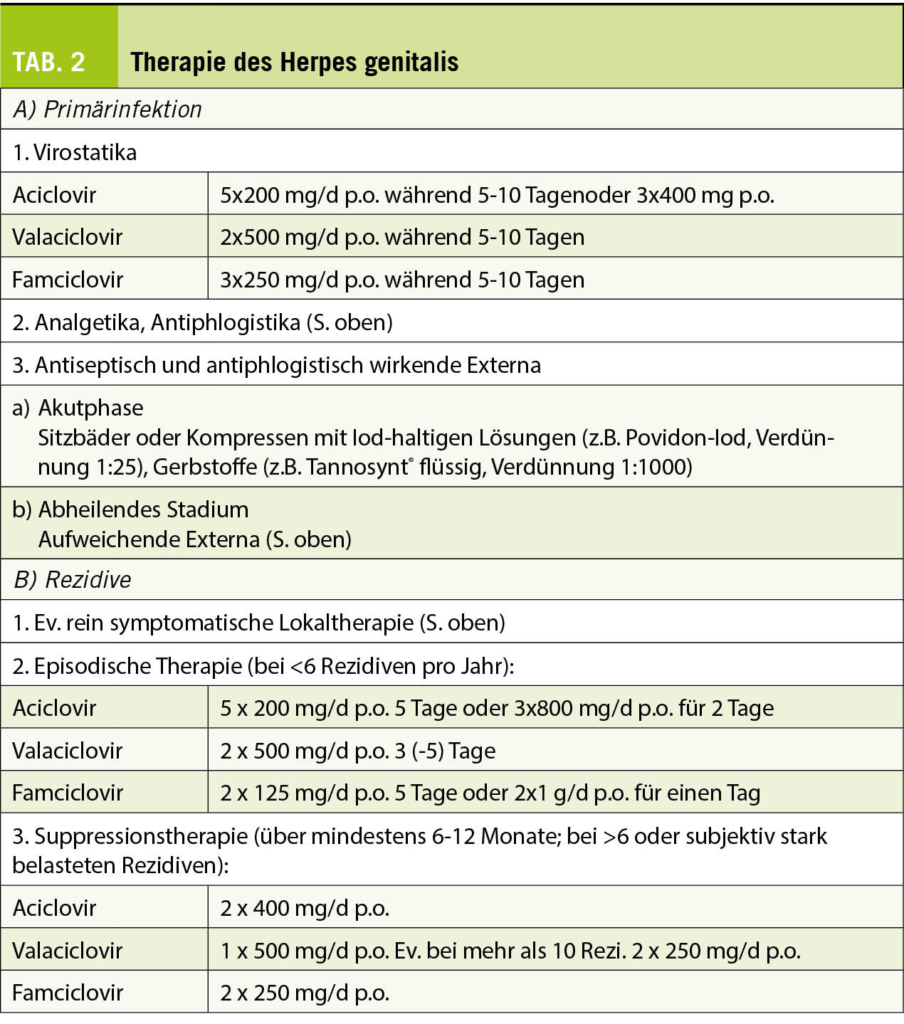
Systemisch wird aufgrund der guten Wirksamkeit und der guten Verträglichkeit meist das fungizide und fungistatische Terbinafin favorisiert. Hierbei gilt es zu beachten, dass Terbinafin nur für Onychomykosen durch Fadenpilze (nicht jedoch Onychomykosen durch Hefen oder Schimmelpilze) empfohlen ist, so dass ein Erregernachweis vor Therapiebeginn vorliegen sollte. Falls es sich um eine Dermatophytose handelt, ist das Allylamin Terbinafin anderen klassendifferenten Wirkstoffen, wie Itraconazol und Fluconazol, bezüglich Wirksamkeit überlegen (9). Die Anwendung einer kontinuierlichen täglichen Einnahme zeigte zumindest keine konsistenten Vorteile gegenüber einer günstigeren und besser verträglichen Intervalltherapie (9) (Tabelle 2). Man geht davon aus, dass dies durch die lange Verweildauer und Akkumulation von Terbinafin in der Nagelmatrix zu erklären ist.
Häufig eingesetzte systemische Breitspektrum-Antimykotika (mit Wirksamkeit auch gegenüber Hefen und einigen Schimmelpilzen) sind die Azole Itraconazol sowie Fluconazol. Bei beiden Wirkstoffen ist allerdings häufiger mit Nebenwirkungen und Interaktionen zu rechnen als bei Terbinafin.
Das fungistatische Itraconazol penetriert ebenfalls schnell in die Nagelplatte und bleibt auch noch über einen Zeitraum bis zu 6 – 9 Monaten nach Einnahme nachweisbar. Die Wirksamkeit auf Dermatophyten ist geringer als bei Terbinafin (10). Es benötigt jedoch zur intestinalen Aufnahme ein saures gastrales Milieu, so dass es bei gleichzeitiger Einnahme von Protonenpumpenhemmern oder bei anderweitiger Achlorhydrie schlecht absorbiert werden kann. Die Aufnahme kann durch Getränke mit einem sauren pH-Wert wie z.B. Orangensaft (nicht Grapefruitsaft aufgrund der einige Tage andauernden irreversiblen CYP3A4 Hemmung) gefördert werden. Itraconazol darf zudem nicht zusammen mit Statinen aufgrund des Risikos einer Rhabdomyolyse gegeben werden. Auch die zeitgleiche Einnahme von Chinidin sollte aufgrund des erhöhten Risikos für ventrikuläre Tachykardien vermieden werden. Aufgrund der Eigenschaften von Itraconazol als Substrat und Inhibitor des hepatischen Enzyms CYP3A4 und von Arzneistoff-Transporter-Glykoproteinen zeigt der Wirkstoff ein grosses Interaktionspotential. Eine individuelle Evaluation in Zusammenschau mit der Medikamentenliste des zu behandelnden Patienten ist in jedem Fall notwendig. Bei Herzinsuffizienz und/oder Lebererkrankungen ist es kontraindiziert.
Das fungistatische Fluconazol penetriert die Nagelplatte langsamer (innerhalb von 2 Wochen) und persistiert bis 3-6 Monate nach Therapieende im Nagel. Studiendaten zeigen jedoch, dass Fluconazol sowohl Itraconazol als auch Terbinafin bzgl. Wirksamkeit bei Dermatophyteninfektionen unterlegen ist (10). Das Interaktionspotential ist kleiner als bei Itraconazol, muss jedoch auch individuell evaluiert werden.
Andere Antimykotika wie VT-1161 werden aktuell in klinischen Studien untersucht.
Für alle systemischen Antimykotika werden Laborkontrollen, insbesondere Leberwertkontrollen vor Therapiestart und nach 4-6 Wochen Therapie empfohlen. Zudem müssen zwingend Interaktionschecks mit der Begleitmedikation durchgeführt werden.
Es gilt generell, dass die Kombination von Lokal- und Systemtherapie effektiver ist, als die Monotherapie (11). Wir empfehlen dennoch die Erwartungshaltung der Patienten nicht zu hoch zu halten, da die in Studien erhobenen Heilungsraten von Terbinafin, Itraconazol und Fluconazol klinisch bei 81.3%, 77.8% und 37.5% bzw. mykologisch bei 75%, 61.1% und 31.2% lagen (10).
Zusammenfassend ist die systemische Therapie nur zu vertreten, wenn ein klarer Erregernachweis, idealerweise mittels Kultur, erfolgt ist und eine kombinierte Therapie aus Erregerlast-Entfernung sowie adäquater kombiniert topisch-systemischer Therapie durchgeführt wird und der Therapieerfolg genau (foto-)dokumentiert wird. Ein Therapieabbruch sollte nach adäquater Frist, z.B. nach 6 Monaten, erwogen werden, wenn kein Ansprechen erkennbar ist. In diesem Fall sollte die Prüfung von Differenzialdiagnosen, insbesondere in Hinblick auf Malignome des Nagelapparats mit allfälliger sekundärer Onychomykose, erfolgen.
Nicht-medikamentöse Behandlungsoptionen wie Laser, photodynamische Therapie PDT oder Iontophorese sind zwar beschrieben, jedoch fehlen hierzu verlässliche Studiendaten um einen breiten Einsatz zu rechtfertigen. Zudem sind diese keine Pflichtleistungen der Krankenkassen. Die Therapien können in Einzelfällen erwogen werden, in denen eine antimykotische Pharmakotherapie aus bestimmten Gründen kontraindiziert ist, oder bei jenen Patienten, bei denen die bisherigen Therapien nicht erfolgreich waren.
Voraussichtlich Mitte 2022 wird es eine Überarbeitung der AWMF (Arbeitsgemeinschaft der wissenschaftlichen medizinische Gesellschaften) Leitlinie zur Onychomykose geben (4, 19), bei welcher einer der Autoren (JM) aktiv als Vertreter der Schweiz involviert ist.
Copyright bei Aerzteverlag medinfo AG
Universitätsspital Zürich
Dermatologische Klinik
Rämistrasse 100
8091 Zürich
Polipraxis Herisau
Dermatologie
Gossauerstrasse 24
9100 Herisau
Kantonsspital St. Gallen
Rorschacher Strasse 95
Haus 20
9007 St. Gallen
antonio.cozzio@kssg.ch
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert
1. Thomas J. Toenail onychomycosis: an important global disease burden. J Clin Pharm Ther. oct 2010;35(5):497-519.
2. Sigurgeirsson B, Baran R. The prevalence of onychomycosis in the global population – A literature study. J Eur Acad Dermatol Venereol JEADV. 28 nov 2013
3. Baran R, Hay RJ. Nouvelle classification clinique des onychomycoses [New clinical classification for onychomycoses]. J Mycol Med. 2014 Dec;24(4):247-60.
4. https://dmykg.ementals.de/wp-content/uploads/2015/08/Onychomykose.pdf, accessed on 26/03/2022
5. Wilsmann-Theis D, Sareika F, Bieber T, Schmid-Wendtner MH, Wenzel J. New reasons for histopathological nail-clipping examination in the diagnosis of onychomycosis. J Eur Acad Dermatol Venereol. 2011 Feb;25(2):235-7
6. Lecha M, Effendy I, Feuilhade de Chauvin M, Di Chiacchio N, Baran R; Taskforce on Onychomycosis Education. Treatment options–development of consensus guidelines. J Eur Acad Dermatol Venereol. 2005 Sep;19 Suppl 1:25-33
7. Foley K, Gupta AK, VersteegS, et al. Topical and device-based treatments forfungal infections of the toenails. Chochrane Database Syst Rev 2020; 1: CD012093
8. Iorizzo M, Hartmane I, Derveniece A, Mikazans I. Ciclopirox 8% HPCH Nail Lacquer in the Treatment of Mild-to-Moderate Onychomycosis: A Randomized, Double-Blind Amorolfine Controlled Study Using a Blinded Evaluator. Skin Appendage Disord. 2016 Feb;1(3):134-40.
9. de Sá DC, Lamas AP, Tosti A. Oral therapy for onychomycosis: an evidence-based review. Am J Clin Dermatol. 2014 Feb;15(1):17-36. doi: 10.1007/s40257-013-0056-2.
10. Arca E, Taştan HB, Akar A, Kurumlu Z, Gür AR. An open, randomized, comparative study of oral fluconazole, itraconazole and terbinafine therapy in onychomycosis. J Dermatolog Treat. 2002 Mar;13(1):3-9.
11. Effendy I, Mayer J, Nenoff P, et al. Kombinationstherapie von schweren Onychomykosen – Empfehlungen eines Expertengremiums. Akt Dermatol 2020; 46(07): 311-318
12. Drake LA, Shear NH, Arlette JP, Cloutier R, Danby FW, Elewski BE, Garnis-Jones S, Giroux JM, Gratton D, Gulliver W, Hull P, Jones HE, Journet M, Krol AL, Leyden JJ, Maddin SC, Ross JB, Savin RC, Scher RK, Sibbald GR, Tawfik NH, Zaias N, Tolpin M, Evans S, Birnbaum JE, et al. Oral terbinafine in the treatment of toenail onychomycosis: North American multicenter trial. J Am Acad Dermatol. 1997 Nov;37(5 Pt 1):740-5
13. Iorizzo M, Piraccini BM, Tosti A. Today’s treatments options for onychomycosis. J Dtsch Dermatol Ges. 2010 Nov;8(11):875-9.
14. Tosti A, Piraccini BM, Stinchi C, Venturo N, Bardazzi F, Colombo MD. Treatment of dermatophyte nail infections: an open randomized study comparing intermittent terbinafine therapy with continuous terbinafine treatment and intermittent itraconazole therapy. J Am Acad Dermatol. 1996 Apr;34(4):595-600.
15. Darkes MJ, Scott LJ, Goa KL. Terbinafine: a review of its use in onychomycosis in adults. Am J Clin Dermatol. 2003;4(1):39-65.
16. Scher RK, Breneman D, Rich P, Savin RC, Feingold DS, Konnikov N, Shupack JL, Pinnell S, Levine N, Lowe NJ, Aly R, Odom RB, Greer DL, Morman MR, Bucko AD, Tschen EH, Elewski BE, Smith EB. Once-weekly fluconazole (150, 300, or 450 mg) in the treatment of distal subungual onychomycosis of the toenail. J Am Acad Dermatol. 1998 Jun;38(6 Pt 2):S77-86.
17. Rigopoulos D. Onychomycosis: Diagnosis and effective Management, First Edition. Edited by Dimitris Rigopoulos, Boni Elewski and Bertrand Richert. Hoboken, NJ: Wiley; 2018.
18. Baran R. Baran & Dawber`s Diseases of the Nails and their Management. Fifth edition. Hoboken, NJ: Wiley-Blackwell 2019.
19. https://www.awmf.org/leitlinien/detail/anmeldung/1/ll/013-003.html, accessed on 26/03/2022