Die Abklärung, Triage und Behandlung von Notfallpatientinnen und Notfallpatienten mit kardiologischen Problemen in der Praxis ist herausfordernd, interessant und dankbar. Mit Anamnese, Status, EKG und wenigen Labortests kann die Diagnose oft gestellt und eine Therapie eingeleitet werden. Instabile Patienten müssen rasch verlegt werden, bei allen anderen hat man Zeit, um einen Therapieplan zu erstellen. Viele kardiologische Notfälle können ambulant betreut werden. Die Zusammenarbeit mit einer Kardiologin oder einem Kardiologen des Vertrauens erleichtert der Hausärztin oder dem Hausarzt die Arbeit und macht die Abläufe effizient.
The assessment, triage, and treatment of emergency patients with cardiological problems in practice is challenging, interesting, and rewarding. With a medical history, physical examination, ECG, and a few laboratory tests, a diagnosis can often be made, and therapy can be initiated. Unstable patients must be transferred quickly, while for all others, there is time to create an treatment plan. Many cardiological emergencies can be managed on an outpatient basis. Collaborating with a trusted cardiologist makes the work easier for the primary care provider and streamlines the processes.
Keywords: Cardiac emergency, Primary care triage, ECG and biomarker diagnostics, Acute cardiovascular treatment
Einleitung
Die Abklärung, Triage und Behandlung kardiologischer Notfälle in der hausärztlichen Praxis stellt eine klinisch anspruchsvolle, aber zugleich lohnende Aufgabe dar. Bereits mit Anamnese, klinischem Status, Ruhe-EKG und gezielter Labordiagnostik lassen sich in vielen Fällen richtungsweisende Diagnosen stellen und therapeutische Massnahmen einleiten.
In der Folge werden Überlegungen und mögliche Vorgehensweisen zur Abklärung generell sowie zur Abklärung und Therapie spezifischer Krankheiten aufgezeigt.
Die Referenzen sind hauptsächlich die Richtlinien der Europäischen Herzgesellschaft ESC. Diese sind informativ, ansprechend und frei erhältlich.
Abklärung
Anamnese
Patienten mit akuten Thorax- und Oberbauchbeschwerden aller Art (Dyspnoe, Schmerzen, Druck, Brennen), Palpitationen, akutem Schwindel und Synkopen sowie Patienten mit hohem Blutdruck werden als kardiologischer Notfall behandelt. Dabei lohnt es sich, trotz des hektischen Praxisalltags, die Anamnese, d.h. detaillierte Angaben zum jetzigen Leiden, nicht zu überspringen und auch nicht zu delegieren. Die persönliche Anamnese fördert zudem oft Unerwartetes zu Tage und hilft entscheidend bei der Beurteilung eines akuten Problems.
Status
Der Status ermöglicht die erste Triage und gilt der Frage, ob der Patient klinisch stabil ist oder nicht. Brady- und tachykarde Rhythmusstörungen können bereits im Status erfasst oder weitgehend ausgeschlossen werden. Der Blutdruck soll an beiden Oberarmen gemessen und die Herzauskultation nicht nur im Liegen, sondern auch im Sitzen nach der Exspiration durchgeführt werden, weil man so z.B. die Aorteninsuffizienz besser hört. Zur Beurteilung der Halsvene wird der Patient im Liegen bei 0° und bei 45° untersucht. Dies erfordert eine entsprechend gute Liege.
Instabile Patienten werden mit einer Infusion versehen und mit dem Rettungsdienst (Tel. 144) verlegt.
EKG
Das EKG dient der Diagnostik von Myokardinfarkt und von Rhythmusstörungen sowie der Risikostratifizierung und sollte immer angefertigt werden. Dabei ist auf eine korrekte Platzierung der Elektroden zu achten, da sonst Fehldiagnosen drohen (1).
Die P-Wellen, gelegentlich diskret versteckt und schwierig zu entdecken, führen bei Rhythmusstörungen fast immer zur Diagnose, sowohl bei brady- als auch bei tachykarden Rhythmusstörungen.
Beim Verdacht auf ein akutes koronares Syndrom (ACS) ist das EKG unabdingbar zur Risikostratifizierung. Thoraxschmerzen in Kombination mit einer ST-Hebung ist definitionsgemäss ein ST-Hebungs-Myokardinfarkt (STEMI) und erfordern eine unverzügliche invasive Abklärung mit Revaskularisation in einem dafür vorgesehenen Zentrum. ST-Hebungen erscheinen bisweilen diskret und sollen nicht übersehen werden. Eine ST-Hebung in V1 deutet auf einen Verschluss des proximalen RIVA hin und ist prognostisch besonders ungünstig.
Andere EKG-Veränderungen wie ein Blockbild, speziell ein Linksschenkelblock, oder ein Schrittmacher-EKG machen die Interpretation vor allem beim ACS schwierig. Alte EKGs helfen hierbei, sind aber nicht immer verfügbar. Im Zweifelsfalle sollten Patienten mit schwierig interpretierbarem EKG wie ein STEMI behandelt werden (2). Ein normales EKG schliesst ein höchstes Risiko aus.
Troponin-Test
Der Troponin-Test hilft bei der Beurteilung, ob die Thoraxbeschwerden die Folge eines Myokardinfarktes sind oder nicht (2). Heute werden nur noch Tests verwendet, welche das high sensitive Troponin (hsTn) messen. Ein wiederholt normaler Test (d. h. ein Troponinwert unter der 99. Perzentile) schliesst einen Myokardinfarkt, nicht aber eine Angina pectoris aus, ein positiver Test wiederum macht einen Myokardinfarkt wahrscheinlich. Algorithmen mit seriell gemessenen Troponinwerten wurden entwickelt und zur Diagnostik des ACS empfohlen («rule in» und «rule out», Abb. 1). Die Cut-offs für die Tests sind Assay-spezifisch und können beim Hersteller des Tests in Erfahrung gebracht werden. Patienten, welche einen Non-STEMI haben («rule in»), brauchen eine beschleunigte invasive Abklärung in einer Institution mit Herzkatheterlabor. Patienten, welche weder die Kriterien für «rule in» noch für «rule out» erfüllen, müssen weiter kardiologisch abgeklärt werden. Spätestens hier lohnt es sich, die Anamnese zu vertiefen und weitere Tests anzuschliessen, um die Ursache der Erkrankung zu erfahren. Dabei hat die Echokardiographie einen hohen Stellenwert, können mit dieser Untersuchung doch nicht nur detailliert die Herzklappen und die Funktion des linken Ventrikels untersucht, sondern auch Perikard und Grösse der Vorhöfe beurteilt und die Druckverhältnisse im System- und Lungenkreislauf abgeschätzt werden, was häufig zur Diagnose führt. Eine echokardiographische Untersuchung ist in der Regel rasch, d.h. innerhalb weniger Tage, erhältlich.
Natriuretische Peptide
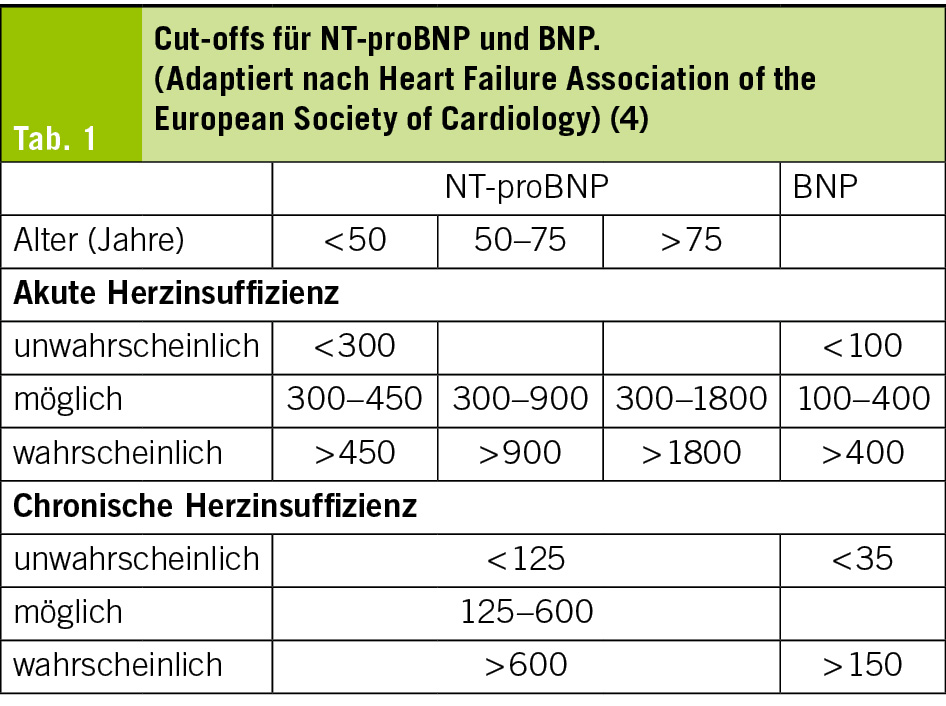
Dieser Test kann bei der Diagnostik von Herzinsuffizienz helfen, wobei er stets im Zusammenhang mit der Anamnese und dem Status verwendet werden soll. Es gilt: Je höher der gemessene Wert, desto höher ist die Wahrscheinlichkeit, dass eine Herzinsuffizienz vorliegt (Tab. 1). Ein fortgeschrittenes Alter und eine Niereninsuffizienz können die Natriuretischen Peptide erhöhen und die Verlässlichkeit des Testes beeinträchtigen. Bei Patienten mit Adipositas hingegen werden eher tiefere Natriuretische Peptide gemessen als bei Patienten mit Normalgewicht (3, 4).
D-Dimer-Test
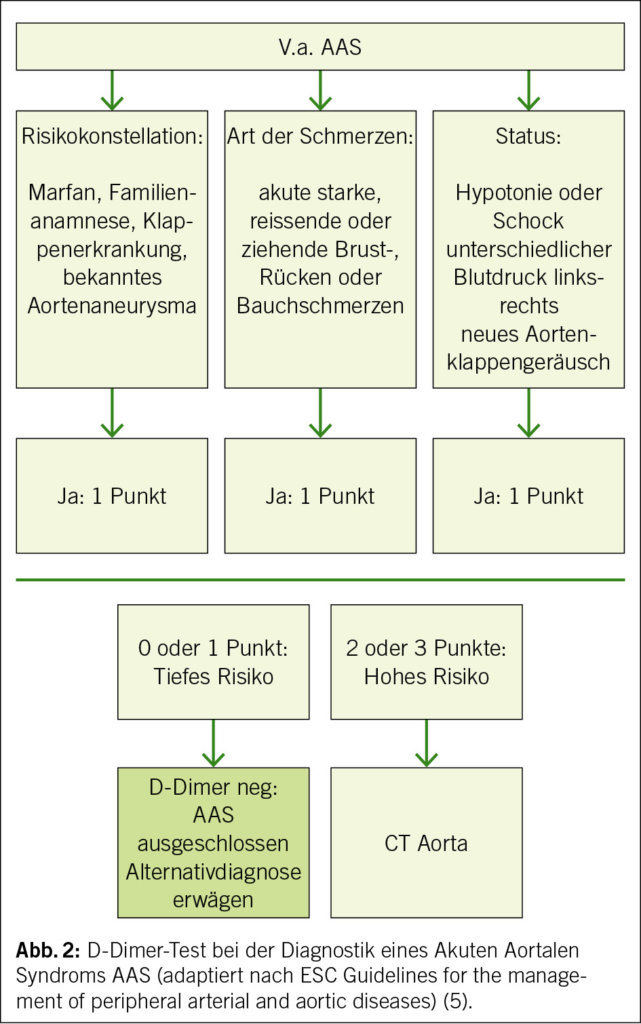
Der D-Dimer-Test, hilfreich für den Ausschluss von venösen thromboembolischen Erkrankungen, hilft auch bei der Diagnostik des akuten aortalen Syndroms (AAS), d.h. der Aortendissektion. Besteht keine hohe Vortestwahrscheinlichkeit für ein AAS, so schliesst ein normaler D-Dimer-Test ein akutes aortales Syndrom weitgehend aus (Abb. 2) (5).
Weitere Laboruntersuchungen
Abgesehen vom Troponintest können beim kardiologischen Notfall weitere Laboruntersuchungen sinnvoll sein. Neben dem Blutbild sind dies Werte zur Bestimmung der Nierenfunktion wie Kreatinin, die Elektrolyte, Werte zur Bestimmung der Leberfunktion wie Transaminasen, Bilirubin und INR sowie TSH und CRP. Mit Hilfe dieser Werte können einerseits Alternativdiagnosen gestellt oder vermutet werden, anderseits werden diese Werte gebraucht, um zum Beispiel im Zuge der Therapie einer Herzkrankheit die Auswahl der Medikamente zu machen oder die korrekte Dosis eines Medikaments zu bestimmen.
Nitroglycerin
Nitroglycerin eignet sich nicht als Test zur Diagnostik bei akuten Thoraxschmerzen, weil die Besserung von Thoraxschmerzen auf Nitroglycerin kein spezifisches Zeichen für ein ACS ist (6).
Therapieplan
Konnte die Diagnose zu diesem Zeitpunkt bereits bestimmt werden, wird ein Therapieplan erstellt.
ACS
Beim ACS ist dies die Revaskularisation der Koronararterien. Im Falle eines STEMI die sofortige Revaskularisation, was die Überwachung des Patienten und die unverzügliche Zuweisung zur Koronarangiographie an ein entsprechendes Zentrum erfordert. Im Falle eines Non-STEMI sollte die Koronarangiographie innert 24 Stunden stattfinden und der Patient bis zu diesem Zeitpunkt überwacht werden (2).
Der lokale Rettungsdienst (Telefonnummer 144) ist rasch vor Ort in der Praxis und erfahrungsgemäss bei der Auswahl eines entsprechenden Zentrums behilflich.
Sauerstoff ist Patienten mit einer reduzierten peripheren Sauerstoffsättigung (SO2 < 90 %) vorbehalten. Intravenöse Opiate (z. B. Morphin 1–3 mg als Bolus i.v.) können schmerzlindernd und anxiolytisch wirken. Eine antiischämische Therapie mit Nitroglycerin (Spray 1–3 Hübe oder Nitroglycerinkapsel) kann schmerzlindernd wirken und bewährt sich vor allem bei hypertensiven Patienten. Patienten mit Hypotonie sollten keine Nitrate erhalten. Aspirin (150–300 mg p.o. oder 500 mg i. v.) soll noch vor Ort appliziert werden, hingegen wird die Gabe von anderen Plättchenhemmern (P2Y12-Rezeptor-Blocker) vor der Koronarangiographie nicht empfohlen.
Hypertensiver Notfall
Definitionsgmäss liegt ein hypertensiver Notfall (engl. hypertensive emergency) vor, wenn der Blutdruck mindestens 180/110 mmHg beträgt und ein Endorganschaden (Gehirn, Herz-Kreislaufsystem oder Nieren) dokumentiert ist. Ein solcher äussert sich z.B. in Atemnot, Kopfschmerzen, Sehstörungen, selten neurologischen Defiziten oder Somnolenz. In dieser Situation ist der Blutdruck rasch zu senken, vorzugsweise mit i.v. applizierten Antihypertensiva in einem Spital. Fehlen solche Symptome, spricht man von hypertensiver Entgleisung (hypertensive urgency) (7). Bei der hypertensiven Entgleisung ist in der Regel keine Hospitalisation nötig. Zur Therapie eignen sich die üblichen Antihypertensiva wie ACE-Hemmer und Kalziumantagonisten, wobei Captopril und Nifedipin am besten untersucht wurden (8). Praktisch sind Nitrate. Nitroglycerinspray, -kapseln und Nitroglycerinpflaster wirken rasch und sind gut zu dosieren. Im Falle des Pflasters kann die Wirkung zudem schnell rückgängig gemacht werden durch das Entfernen desselben, sollte dies wegen einer zu raschen Blutdrucksenkung notwendig sein.
Herzinsuffizienz
Bei der Herzinsuffizienz muss immer die Ursache derselben eruiert werden. Myokardischämie, Rhythmusstörungen, arterielle Hypertonie, Klappenvitien oder Kardiomyopathien zum Beispiel können zu Herzinsuffizienz führen. Im Falle einer Stauung der Halsvene und Ödemen sind Schleifendiuretika (je nach Dringlichkeit z.B. Furosemid 20–40 mg i.v. oder Torasemid 5–20 mg p.o.) fast immer richtig. Oligosymptomatische Patienten oder Patienten, welche notfallmässig erscheinen, obwohl sie bereits seit einiger Zeit Beschwerden haben, können durchaus auch in Zusammenarbeit mit einer kardiologischen Praxis ambulant behandelt werden. Dies erfordert etwas Zeit und Geduld von Seiten des Arztes und des Patienten, müssen solche Patienten doch kurzfristig und regelmässig gesehen werden, um die Abklärung zu begleiten und den Therapieerfolg zu überwachen.
Tachykarde Rhythmusstörungen
Während Schmalkomplextachykardien wie Reentry-Tachykardien und Vorhofflattern fast immer eine Konversion (mit Adenosin i.v. bzw. einer Elektrokardioversion) und eine Rhythmuskontrolle erfordern, kann das tachykarde Vorhofflimmern oft medikamentös in ein normokardes Vorhofflimmern überführt werden (Frequenzkontrolle). Hierfür eignen sich Betablocker gut, z. B. Bisoprolol 2.5 bis 10 mg p.o, allenfalls in Kombination mit sogenannten Nicht-Dihydropyridin-Kalziumangonisten (Verapamil oder Diltiazem) oder Glycosiden (Digoxin). Bis zur kardiologischen Abklärung und allfälligen Konversion kann bereits bei der Diagnosestellung eine Antikoagulation mit einem DOAC begonnen und, falls eine Herzinsuffizienz vorliegt, ein Schleifendiuretikum verschrieben werden.
Bei stabilen Patienten mit regelmässiger Schmalkomplextachykardie ist es nie falsch, vagale Manöver durchzuführen oder Adenosin 6–12 mg i.v. zu applizieren zur Terminierung derselben oder zur Demaskierung eines Vorhofflatterns.
Breitkomplextachykardien weisen auf eine strukturelle Herzerkrankung hin und erfordern in der Regel eine rasche Abklärung und Therapie, weshalb eine unverzügliche Verlegung in ein Spital in der Regel sinnvoll ist.
Bradykarde Rhythmusstörungen
Symptomatische bradykarde Rhythmusstörungen erfordern die rasche Implantation eines Herzschrittmachers, es sei denn, es gibt eine behandelbare Ursache wie eine bradykardisierende Therapie oder eine Niereninsuffizienz mit Elektrolytstörung. Vor jeder Schrittmacherimplantation sollte eine Echokardiographie durchgeführt werden.
Synkopen
Die Anamnese ist das wichtigste Hilfsmittel bei der Abklärung von Synkopen. Diese ist exakt zu erheben und führt bei orthostatischen (z. B. nach dem Aufstehen vom Bett) und neurokardiogenen, d. h. vasovagalen oder situativen Synkopen (z. B. im Rahmen von Schmerzen bzw. der Miktion oder eines Hustens) meistens schon zur Diagnose. Unangekündigte Synkopen («ohne Prodromi»), speziell wenn dabei ernsthafte Verletzungen auftreten, brauchen rasch weitere Abklärungen mittels Langzeit-EKG bzw. eines Loop-Recorders und einer Echokardiographie. Das EKG gibt bereits wichtige Hinweise: Findet sich eine Bradykardie, ein Schenkelblock oder viele Extrasystolen, macht dies die Diagnose einer rhythmogenen Synkope wahrscheinlicher. Die Patienten sollten auf das Autofahren verzichten, bis die in der Regel ambulanten Abklärungen beendet sind, die definitive Diagnose bekannt und das Problem gelöst ist, z. B. mit einem Herzschrittmacher.
Perikarditis und Myokarditis
Die Peri- und Myokarditis sind immunologische Phänomene und treten typischerweise 2–3 Wochen nach einem viralen Infekt auf. Die Anamnese unterscheidet sich bisweilen kaum von derjenigen des ACS.
Die Perikarditis verursacht typischerweise einen lageabhängigen Thoraxschmerz (verstärkt im Liegen, speziell in Links-Seitenlage) und geht mit einem normalen Troponintest einher. Gelegentlich hört man ein Perikardreiben, was knarrend klingt wie das Gehen auf Schnee. Die Therapie ist symptomatisch mit nichtsteroidalen Antirheumatika (NSAR, z. B. Ibuprofen 4 x 600 mg p.o.) und Colchicin (1 bzw. 2 x 0.5 mg p.o., je nachdem, ob das Körpergewicht unter oder über 70 kg ist). Die Prognose ist gut, Patienten mit Perikarditis werden meist ambulant behandelt (9).
Bei der Myokarditis ist der Troponintest pathologisch erhöht. Die Diagnose der Myokarditis erfordert üblicherweise weitere Tests, neben einer Echokardiographie z.B. ein MRI oder eine Koronarangioraphie zum Ausschluss eines Verschlusses der Koronararterien.
Medikamentennebenwirkungen
Solche sind häufig, auch kardiale, weshalb eine genaue Medikamentenanamnese unumgänglich ist. Speziell bei Hypotonie (Antihypertensiva), Hypertonie (NSAR, Steroide z. B.) und Rhythmusstörungen (Antiarrhythmika, Psychopharmaka) ist an eine der genannten Substanzklassen zu denken.
Nicht-kardiale Diagnosen
Speziell Asthma bronchiale und Dyspepsie sind häufige Erkrankungen und manifestieren sich oft ähnlich wie kardiale Erkrankungen. Auch sog. «muskuloskelettale» Syndrome sind häufig und lassen sich vom geübten Praktiker von kardialen Syndromen differenzieren. Es lohnt sich, die Differentialdiagnose bei Notfällen weit zu fassen und die Verdachtsdiagnose immer wieder zu hinterfragen.
Unklare Beschwerden
Nicht selten kann trotz der oben genannten Abklärungen keine spezifische Diagnose gestellt werden. Konnten die oben genannten Krankheiten ausgeschlossen werden, handelt es sich prinzipiell um ein günstiges Phänomen, und der Patient kann beruhigt werden. Eine Folgekonsultation ist dann sinnvoll, um über den Verlauf zu erfahren und ggf. weitere Abklärungen zu machen.
Spezifische Bedingungen
Es ist nützlich, das Risiko zu kennen, das die verschiedenen spezifischenBedingungen mit sich bringen.
Alter:
Generell gilt, dass das kardiovaskuläre Risiko mit dem Alter steigt. Alte Leute haben ein höheres Risiko als junge Leute und erfordern besondere Aufmerksamkeit.
Bei Frauen:
Patientinnen haben bekanntermassen nicht nur andere Krankheiten als Patienten, sondern auch andere Manifestationen der gleichen Erkrankungen. Besonders beim ACS sind sogenannte atypische Manifestationen häufig. Frauen werden auch häufiger als Männer unterdiagnostiziert (10).
Frauen vor der Menopause sind weitgehend vor Myokardinfarkt geschützt, ein ACS ist bei ihnen sehr selten. Nach der Menopause gleicht sich das Risiko der Frauen demjenigen der Männer an.
Ein spezieller Risikofaktor für die koronare Herzerkrankung und Klappenerkrankungen ist die Bestrahlung der linken Brust, weshalb diese Information bekannt sein muss (11). Rhythmusstörungen, eine arterielle Hypertonie, Kardiomyopathien und auch Koronardissektionen treten bei Schwangeren häufiger auf als bei Nicht-Schwangeren (12).
Psychiatrische Patienten
Patienten mit psychiatrischen Erkrankungen erfordern besondere Aufmerksamkeit, weil die Anamnese bisweilen erschwert ist. Psychiatrische Leiden gelten zudem als Risikofaktor für kardiovaskuläre Erkrankungen (13).
Zusammenarbeit mit dem Spezialisten
Tipp: Die Zusammenarbeit mit einem Kardiologen des Vertrauens erleichtert dem Grundversorger die Arbeit und macht die Abläufe effizient. Mit den heutigen Kommunikationswegen ist es auch kein Problem mehr, einen Befund rasch auszutauschen, um einen konsiliarischen Rat zeitnah einzuholen.
Copyright
Aerzteverlag medinfo AG
alfaré │ debrunner │ seebach
praxisgemeinschaft
Poststrasse 2
8610 Uster
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Harringan RA. Electrocardiographic Electrode Misplacement, Misconnection, and Artifact. J Emerg Med 2012;43(6):1038-1044.
2. 2023 ESC Guidelinies for the management of acute coronary syndromes. Eur Heart J 2023;44:3720-3826.
3. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021;42:3599-3726.
4. Mueller C. Heart Failure Association of the European Society of Cardiology practica. Guidance on the use of natriuretic peptide concentrations. Eur J Heart Fail 2019;21(6):715-731.
5. 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases, Eur Heart J 2024;45;3538-3700.
6. Henrikson CA. Chest pain relief by nitroglycerin does not predict active coronary artery disease. Ann Intern Med 2003;139:979-986.
7. 2024 ESC Giudelines for the management of elevated blood pressure and hypertension. Eur Heart J 2024;45:3912-4018.
8. Campos C. Pharmacologic Treatment of Hypertensive Urgency in the Outpatient Setting: A Systematic Review. J Gen Intern Med 2018;33(4):539-550.
9. 2015 ESC Guidelines for the diagnosis and management of pericardial diseases. Eur Heart J 2015;36(42):2921-2964.
10. Haider A et al. Sex and gender in cardiovascular medicine: presentation and outcomes of acute coronary syndrome. Eur Heart J 2020; 41:1328–1336.
11. Darby S. Risk of ischemic heart disease in women after radiotherapy for beast cancer. N Engl J Med 2013; 368(11):987-998.
12. 2018 ESC Guidelinies for the management of cardiovascular diseases during pregnancy. Eur Heart J 2018; 39:3165-3241.
13. Nielsen RE. Cardiovascular disease in patients with severe mental illness. Nat Rev Cardiol 2021;18(2):136-145.