- 25. Zürcher Herzkurs – Cardiology Today, Teil 2
Der traditionelle Zürcher Herzkurs fand in diesem Jahr zum 25. Mal statt. Das von Prof. Franz Wolfgang Amann und Prof. Christian Schmied (HerzGefässMedizin Hirslanden, Klinik im Park) zusammengestellte Programm stiess auf grosses Interesse, was sich in einer Rekordbeteiligung widerspiegelte. Aus dem breit gefächerten Programm werden in diesem zweiten Teil drei Referate vorgestellt.
LDL-Cholesterin oder Lipoprotein(a) – worauf kommt es in der Praxis an?

Prof. Stephen Gloekler vom Diagnostischen und Therapeutischen Herzzentrum Zürich gab zunächst einen Überblick über die Lipoproteine, deren Metabolismus und Grössenverhältnisse. Anschliessend erläuterte er die Grundlagen der Atherosklerose als chronisch inflammatorischen Prozess, der wesentlich durch Lipide angetrieben wird. Anhand intrakoronarer Bildgebung verdeutlichte er die zentrale Rolle von LDL-Cholesterin als kausalen Faktor der Atherosklerose.
Risikostratifizierung in der klinischen Praxis
Für die kardiovaskuläre Risikostratifizierung stehen im klinischen Alltag verschiedene validierte Instrumente zur Verfügung. Bei mutmasslich gesunden Personen im Alter von 20 bis 69 Jahren kann der AGLA-Score eingesetzt werden, während für ältere Personen SCORE2 beziehungsweise SCORE2-OP zur Anwendung kommen. Für Patienten mit Diabetes ohne manifeste atherosklerotische kardiovaskuläre Erkrankung und ohne Endorganschäden steht ein spezifischer SCORE2-Diabetes-Rechner zur Verfügung. Diese Instrumente sind allerdings nicht geeignet für Patienten mit bereits manifester koronarer Herzkrankheit, Diabetes mit Organschaden, Niereninsuffizienz oder anderen Hochrisikokonstellationen.
Wer gehört zur Hochrisikogruppe?
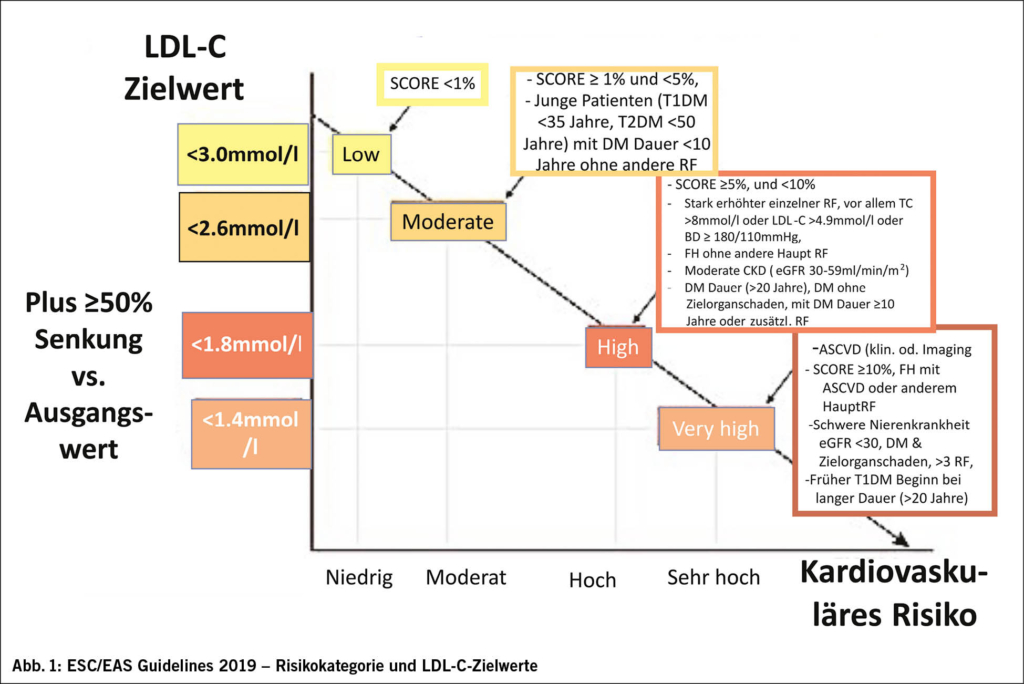
Ein sehr hohes kardiovaskuläres Risiko liegt insbesondere bei Patienten mit dokumentierter atherosklerotischer kardiovaskulärer Erkrankung vor, sei diese klinisch manifest oder bildgebend eindeutig nachgewiesen. Dazu zählen unter anderem Patienten mit chronischem Koronarsyndrom, nach koronarer Revaskularisation oder mit signifikanten Plaques in der Koronarangiografie, im CT oder in der karotiden oder femoralen Gefässbildgebung. Ebenfalls dieser Risikokategorie zuzuordnen sind Patienten mit Diabetes mellitus und Endorganschaden, mit schwerer chronischer Nierenerkrankung bei einer eGFR unter 30 ml/min/1,73 m² oder mit familiärer Hypercholesterinämie in Kombination mit ASCVD oder einem weiteren Hauptrisikofaktor.
Von einem hohen Risiko spricht man zudem bei stark erhöhten Einzelrisikofaktoren wie einem Gesamtcholesterin von mehr als 8 mmol/l, einem LDL-Cholesterin über 4,9 mmol/l oder einem Blutdruck von mindestens 180/110 mmHg. Auch Patienten mit Diabetes mellitus ohne Endorganschaden oder mit chronischer Nierenerkrankung bei einer eGFR zwischen 30 und 59 ml/min/1,73 m² fallen häufig in diese Kategorie. Moderates Risiko besteht unter anderem bei jüngeren Patienten mit Typ-1- oder Typ-2-Diabetes von kurzer Dauer ohne weitere Risikofaktoren sowie bei Personen mit intermediärem berechnetem 10-Jahresrisiko. Niedriges Risiko liegt schliesslich bei entsprechend niedrigen SCORE2- oder SCORE2-OP-Werten vor.
Verdacht auf familiäre Hypercholesterinämie
Bei Verdacht auf eine familiäre Hypercholesterinämie können der AGLA-FH-Score oder die Dutch Lipid Clinic Network-Kriterien herangezogen werden. In diese Beurteilung fliessen unter anderem die Familienanamnese mit vorzeitiger koronarer Herzkrankheit oder Xanthomen, die persönliche Anamnese, klinische Zeichen wie Sehnenxanthome oder ein Arcus lipoides vor dem 45. Lebensjahr, die Höhe des LDL-Cholesterins sowie der genetische Nachweis einer pathogenen Mutation ein. Je nach erreichter Punktzahl gilt eine familiäre Hypercholesterinämie als unwahrscheinlich, möglich, wahrscheinlich oder definitiv.
Lebensstil als Grundlage jeder Therapie
Die Basis jeder lipidsenkenden Therapie bleibt ein konsequent gesundheitsfördernder Lebensstil. Dazu gehören eine Gewichtsreduktion bei Übergewicht, eine Reduktion gesättigter Fettsäuren zugunsten ungesättigter Fettsäuren, eine ballaststoffreiche Ernährung sowie die Reduktion von Zucker und Alkohol, insbesondere bei Hypertriglyzeridämie. Hinzu kommen regelmässige körperliche Aktivität, die Reduktion sitzender Zeiten und ein konsequenter Nikotinverzicht. Entscheidend ist dabei ein möglichst früher Therapiebeginn mit nachhaltiger Umsetzung.
Die Bedeutung der kumulativen LDL-Exposition
Ein wichtiges Konzept ist die kumulative Expositionshypothese. Mit zunehmender Dauer und Höhe der LDL-Exposition wird mehr Cholesterin in der Arterienwand eingelagert. Dadurch nimmt die atherosklerotische Plaquelast kontinuierlich zu, was das Risiko akuter kardiovaskulärer Ereignisse erhöht. Das ASCVD-Risiko hängt somit nicht nur von der Höhe des LDL-Cholesterins, sondern auch von der Dauer der Exposition ab.
Medikamentöse Optionen zur LDL-Senkung
Zur Senkung des LDL-Cholesterins stehen heute verschiedene Substanzklassen zur Verfügung. Statine hemmen die hepatische Cholesterinsynthese und führen über eine vermehrte Expression von LDL-Rezeptoren zu einer LDL-Senkung von etwa 30 bis 55 %. Ezetimib hemmt die enterale Cholesterinresorption im Dünndarm und senkt das LDL-Cholesterin um etwa 15 bis 25 %. PCSK9-Inhibitoren erhöhen durch Hemmung von PCSK9 die Verfügbarkeit von LDL-Rezeptoren und erreichen eine Reduktion um etwa 50 bis 60 %. Auch siRNA-basierte Therapien, welche die hepatische PCSK9-Synthese hemmen, zeigen Senkungen in der Grössenordnung von 45 bis 55 %.
Weitere Optionen sind Bempedoinsäure mit einer LDL-Senkung von etwa 15 bis 25 %, Gallensäurebinder mit einer Senkung von etwa 10 bis 25 %, Lomitapid mit einer Reduktion von 40 bis 50 % sowie Evinacumab, das über eine Hemmung von ANGPTL3 den Lipoproteinabbau fördert und zu einer LDL-Senkung von etwa 45 bis 55 % führt. In besonders schweren Fällen kann eine Lipoproteinapherese eingesetzt werden, mit der LDL und Lipoprotein(a) physikalisch aus dem Blut entfernt werden.
Verlaufskontrollen und praktische Umsetzung
Bis zum Erreichen des Therapieziels werden erste Kontrollen nach vier Wochen und anschliessend weitere Kontrollen in vierwöchigen Abständen empfohlen. Nach stabiler Zielwerterreichung genügen in der Regel jährliche Verlaufskontrollen. Im Labor sollten Lipidprofil, ALAT, ASAT und CK bestimmt werden. Lipoprotein(a) sollte einmal im Leben gemessen werden.
Lipoprotein(a) als zusätzlicher Risikofaktor
Lipoprotein(a), kurz Lp(a), ist ein LDL-ähnliches Partikel, das aus ApoB, Cholesterin und Apo(a) besteht. Apo(a) ist ein plasminogenähnliches Protein, das kovalent an ApoB gebunden ist. Lp(a) ist nicht nur atherogen wie LDL, sondern weist zusätzlich thrombogene und proinflammatorische Eigenschaften auf. Aufgrund der strukturellen Ähnlichkeit zu Plasminogen kann es prothrombotisch wirken. Zudem ist ein erhöhtes Lp(a) mit einem gesteigerten kardiovaskulären Risiko assoziiert, selbst bei normalen LDL-Werten. Insgesamt resultiert daraus eine besonders aggressive Form der Gefässschädigung.
Klinische Konsequenzen
Die kardiovaskuläre Prävention basiert auf einer strukturierten Risikostratifizierung und einer konsequenten Beeinflussung modifizierbarer Risikofaktoren. LDL-Cholesterin sollte bestimmt, behandelt und kontrolliert werden. Lipoprotein(a) sollte einmalig gemessen werden. Bei erhöhtem Lp(a) ist eine besonders konsequente Kontrolle klassischer Risikofaktoren angezeigt, einschliesslich einer intensiven LDL-Senkung. In ausgewählten Fällen kommen PCSK9-Inhibitoren oder eine Lipoproteinapherese infrage.
Hot Topic Kardiomyopathie
Genetische Grundlagen der hypertrophen Kardiomyopathie

Dr. Judith Schwaiger von der Hirslanden Klinik im Park ging auf die hypertrophe Kardiomyopathie und insbesondere auf die hypertrophe obstruktive Kardiomyopathie ein. Etwa 40 bis 60 % der linksventrikulären Hypertrophien bei HCM sind auf Mutationen in Sarkomerprotein-Genen zurückzuführen. Bei 25 bis 30 % bleibt die Ursache unklar, und bei 5 bis 10 % liegen andere Ursachen zugrunde.
Pathophysiologie und klinische Folgen
Die Sarkomerdysfunktion ist die Hauptursache der genetisch bedingten HCM. Mutationen in Proteinen des Sarkomers, des molekularen Motors des Herzens, führen zu einer abnormalen Kontraktilität, gestörter Relaxation, erhöhter myokardialer Steifigkeit und Fibrose. Die Folgen sind Hyperkontraktilität, eine dynamische linksventrikuläre Ausflusstraktobstruktion sowie eine diastolische Dysfunktion. Klinisch manifestiert sich dies unter anderem durch Palpitationen, Synkopen und ein erhöhtes Risiko für plötzlichen Herztod.
Die Rolle der Stressechokardiographie
Die Stressechokardiographie dient bei HCM der Beurteilung einer Obstruktion im linksventrikulären Ausflusstrakt unter körperlicher oder pharmakologischer Belastung. Sie hilft bei der Einschätzung des Obstruktionsgrades und der Krankheitsausprägung und ist damit für die Therapieplanung zentral.
HCM ist heute behandelbar
Die HCM ist keine einheitliche Erkrankung, sondern zeigt unterschiedliche klinische Verläufe. Ein Teil der Patienten bleibt lange stabil und hat eine nahezu normale Lebenserwartung. Andere entwickeln Komplikationen wie plötzlichen Herztod, progrediente Herzinsuffizienz bei obstruktiver Form, Endstadien einer nicht obstruktiven Verlaufsform oder Vorhofflimmern mit entsprechend erhöhtem Schlaganfallrisiko. Je nach klinischem Bild kommen Medikamente, ICD-Therapie, Septummyektomie, Katheterablation, Antikoagulation oder in fortgeschrittenen Fällen eine Herztransplantation infrage.
LVOT-Obstruktion als therapeutisch relevantes Merkmal
Eine Obstruktion des linksventrikulären Ausflusstrakts kann in Ruhe oder erst unter Provokation auftreten und ist ein zentrales Merkmal der HOCM. Ihre Identifikation ist entscheidend für die Symptomkontrolle, die Prognoseeinschätzung und die Wahl der Therapie.
Mavacamten als neue Therapieoption
Mavacamten ist ein oraler, reversibler, allosterischer Inhibitor der kardialen Myosin-Aktin-Interaktion und stellt einen first-in-class-Wirkstoff zur Behandlung der symptomatischen obstruktiven HCM dar. In der EXPLORER-HCM-Studie führte eine 30-wöchige Behandlung mit Mavacamten zu einer signifikanten Reduktion des linksventrikulären Ausflusstrakt-Gradienten, zu einer Verbesserung der Symptome, der Lebensqualität und der NYHA-Klasse. Auch in der VALOR-HCM-Studie zeigte Mavacamten eine anhaltende Wirksamkeit über 56 Wochen. Zudem konnte die Notwendigkeit einer Septumreduktion deutlich gesenkt werden.
Keynote Lecture: Medizinstudium heute – Lernen, Google oder AI?

Prof. Jörg Goldhahn vom Institut für Translationale Medizin der ETH Zürich und Studiendirektor Humanmedizin gab einen Einblick in die aktuellen Herausforderungen des Medizinstudiums und in die Veränderungen durch künstliche Intelligenz.
Wo künstliche Intelligenz bereits relevant ist
Zu den bereits relevanten oder absehbaren Einsatzbereichen zählen die automatisierte Bild- und Datenanalyse einschliesslich EKG und EEG, die Mustererkennung in grossen Datensätzen, die KI-gestützte klinische Entscheidungsunterstützung, die Automatisierung administrativer und logistischer Prozesse, die Integration in klinische Software sowie die In-silico-Arzneimittelentwicklung.
Ersetzt KI den Arzt?
Maschinen, die lernen und sich selbst korrigieren können, erzielen in einzelnen eng umrissenen Aufgabenbereichen bereits bessere Resultate als Menschen. Dennoch wurde betont, dass KI die Arzt-Patienten-Beziehung, klinische Kontextualisierung und zwischenmenschliche Interaktion nicht ersetzen kann. Realistisch ist daher keine Ablösung des Arztberufs, sondern eine schrittweise Integration von KI in klar definierten Anwendungsfeldern, etwa in der Bildanalyse oder Mustererkennung.
Begriffe und Einordnung
Künstliche Intelligenz bezeichnet Technologien, die Maschinen befähigen, Aufgaben mit menschenähnlichen kognitiven Leistungen auszuführen.
Machine Learning ist ein Teilgebiet der KI, bei dem Systeme auf Basis statistischer Verfahren aus Daten lernen. Deep Learning wiederum ist eine spezielle Form des maschinellen Lernens mit mehrschichtigen neuronalen Netzen zur Modellierung komplexer Zusammenhänge.
Auswirkungen auf das Gesundheitswesen
Als besonders einflussreiche Technologien für die digitale Transformation des Gesundheitswesens wurden unter anderem Telemedizin, Gesundheits-Apps, Sensoren und Wearables für Diagnostik und Remote Monitoring, Genomsequenzierung, Spracherkennung und natürliche Sprachverarbeitung, virtuelle und erweiterte Realität, KI-gestützte Bildinterpretation, interventionelle und rehabilitative Robotik sowie prädiktive Analytik genannt.
Konsequenzen für die medizinische Ausbildung
Die Integration von KI erfordert eine Anpassung des Medizinstudiums. Neben einem technologischen Grundverständnis sind insbesondere interprofessionelle Zusammenarbeit, verantwortungsvolle Einführung neuer Technologien, Sensibilität für soziale Gerechtigkeit, Informationskompetenz und kontinuierliche Weiterbildung relevant. Ebenso wichtig bleiben die realistische Einordnung der Möglichkeiten und Grenzen von KI sowie die kompetente Kommunikation gegenüber Patienten. Gerade in den klassischen ärztlichen Kernkompetenzen – klinische Einordnung, Kommunikation, Verantwortung und ethische Reflexion – bleibt die ärztliche Expertise zentral.
riesen@medinfo-verlag.ch