- Akute Diagnostik und Therapie bei Verdacht auf Hirnschlag – ein Leitfaden für Hausärzte
Ein Verdacht auf Hirnschlag ist ein neurologischer Notfall, bei dem rasches Handeln entscheidend ist. Hausärztinnen und Hausärzte spielen eine zentrale Rolle in der Früherkennung und Einleitung geeigneter Massnahmen. Typische Symptome wie plötzliche Lähmungen, Sprach- oder Sehstörungen müssen umgehend erkannt werden. Die Bildgebung (CT oder MRI) dient der Unterscheidung von ischämischem vs. hämorrhagischem Hirnschlag. Bei ischämischem Insult sind intravenöse Thrombolyse und Thrombektomie zentrale Therapien – letztere auch bis zu 48 h nach Symptombeginn in ausgewählten Fällen. Wichtig sind kurze Zeit bis zur Behandlung («time is brain»), prähospitale Triage (z. B. RACE-Score) und Versorgung in Stroke Units. Auch bei Hirnblutung gibt es heute wirksame Therapien im Rahmen eines Care-Bundles. In der Nachsorge sind Hausärztinnen und Hausärzte zentral für Sekundärprävention, TIA-Abklärung und die Umsetzung der «Life’s Essential 8» zur Förderung eines gesunden Lebensstils.
Suspicion of stroke is a neurological emergency requiring rapid action. General practitioners play a key role in early recognition and initiating urgent care. Sudden weakness, speech or visual disturbances must be identified as possible stroke. Diagnosis is made by CT or MRI to distinguish ischemic from hemorrhagic stroke. In ischemic stroke, thrombolysis or early antithrombotic therapy is key; thrombectomy is used for large artery occlusions, sometimes up to 48 hours post-onset. Critical are fast detection and treatment (“time is brain”), prehospital triage (e.g., RACE score), and care in stroke units. For intracerebral hemorrhage, effective therapies now exist within a structured care bundle. GPs are central in follow-up: secondary prevention, outpatient TIA workup, and promoting healthy lifestyle habits via the “Life’s Essential 8.”
Keywords: Akuter Hirnschlag, Thrombolyse, Thrombektomie, Stroke Unit, Rettungskette
Einleitung
Hirnschläge gehören zu den häufigsten medizinischen Notfällen, mit einer Lebenszeitprävalenz von 25 % («one in four») (1). In der Schweiz sind sie die zweithäufigste Todesursache und die häufigste Ursache einer bleibenden Behinderung im Erwachsenenalter (2). Ein Hirnschlag – veraltet (apoplektischer) Insult – entsteht entweder durch eine plötzliche Durchblutungsstörung im Gehirn (ischämischer Hirnschlag, ca. 80 % der Fälle) oder durch eine Hirnblutung (hämorrhagischer Hirnschlag, ca. 15–20 %). Unbehandelt führt ein Hirnschlag rasch zu einem Absterben von Hirngewebe – es gilt: «Time is brain», da pro Minute bis zu ~1.9 Millionen Neuronen zugrunde gehen (3). Entsprechend ist die Zeit bis zum Behandlungsbeginn kritisch für den neurologischen Outcome.
In der Abklärung und Behandlung des Hirnschlags wurden in den vergangenen Jahrzehnten enorme Fortschritte erzielt, die eine massgeschneiderte Behandlung medikamentös oder interventionell teils noch bis 48 Stunden nach Symptombeginn ermöglichen. Diese Therapien können einerseits die Behinderung durch den Hirnschlag selbst dramatisch reduzieren, andererseits aber auch durch rasche Abklärung und schnellstmögliche Einleitung der adäquaten Sekundärprophylaxe frühe Rezidive verhindern.
Hausärzte sind teilweise die ersten medizinischen Kontaktpersonen bei Hirnschlagpatienten – sei es in der Praxis, am Telefon oder im Hausbesuch. Daher ist es essenziell, die typischen Symptome eines akuten Hirnschlags zu erkennen und umgehend die richtigen Schritte einzuleiten. Dieser Artikel gibt einen praxisorientierten Überblick über die Akutdiagnostik und Akuttherapie des Hirnschlags.
Hirnschlagprävention: Schlüsselrolle der Hausarztmedizin
Die wirksamste Hirnschlagtherapie bleibt die Prävention. Durch kontinuierliche Betreuung, Risikofaktorerhebung und individuelle Therapie können theoretisch 90 % der Hirnschläge verhindert werden (4). Die konsequente Blutdruckkontrolle ist dabei der wichtigste Einzelbeitrag: Bereits eine Senkung des systolischen Drucks um 10 mmHg reduziert das Hirnschlagrisiko um ca. 40 % (5). Auch die systematische Detektion von Vorhofflimmern – v.a. bei älteren Patient/-innen – gewinnt an Bedeutung (6). Neben dem Ruhe-EKG und Langzeit-EKG ermöglichen inzwischen auch neue Technologien wie Smartwatches eine niedrigschwellige Rhythmusüberwachung, müssen jedoch dann noch ärztlich mit entsprechender Expertise verifiziert werden. Bei metabolischen Hochrisikopatienten mit Typ-2-Diabetes sind neben den etablierten Therapien GLP-1-Rezeptoragonisten evidenzbasiert kardiovaskulär protektiv (7). Zudem ist bei Patienten mit manifester Atherosklerose (z. B. KHK oder pAVK) eine strikte LDL-Zielwertkontrolle nach AGLA-Guidelines (< 1.8 mmol/L bzw. < 1.4 mmol/L bei sehr hohem Risiko) essenziell. Dies erfordert eine regelmässige Überprüfung der Verträglichkeit und der LDL-Zielwerte – falls diese unter konventioneller Therapie nicht erreichbar sind, gelingt dies bei fast allen Patientinnen und Patienten durch den Einsatz einer intensivierten lipidsenkenden Therapie (8). Hochrisikopatient/-innen mit stabiler KHK oder pAVK profitieren zudem vom sogenannten COMPASS-Regime: eine Kombination aus niedrig dosierter Rivaroxaban-Therapie (2.5 mg 2 ×/d) plus ASS, welche laut COMPASS-Studie das Risiko für ischämische Ereignisse signifikant senkt (9). Neben der medikamentösen Prävention spielt die Förderung eines gesunden Lebensstils eine zentrale Rolle. Für die «Life’s Essential 8» – darunter ausgewogene Ernährung, regelmässige körperliche Aktivität, Rauchstopp, guter Schlaf, Gewichtsmanagement, Blutdruck-, Blutzucker- und Cholesterinkontrolle – sind Hausärztinnen und Hausärzte entscheidend, um präventive Strategien nicht nur einzuleiten, sondern auch konsequent umzusetzen und langfristig zu begleiten (10).
Hausärztinnen und Hausärzte spielen auch eine zentrale Rolle in der Edukation von Risikopatient/-innen, indem sie diese gezielt über die typischen Symptome eines Hirnschlags aufklären und zur sofortigen Alarmierung des Rettungsdienstes im Verdachtsfall motivieren – ein entscheidender Beitrag zur Verkürzung der Zeit bis zur Behandlung.
Symptomerkennung und erste Abklärung
Trotz optimierter Prävention bleibt der Hirnschlag sehr häufig. Die Symptome treten in der Regel abrupt (innerhalb von Minuten) auf. Leitsymptome sind akute fokal-neurologische Defizite, die je nach betroffener Hirnregion variieren können. Typisch sind:
• Motorik/Sensibilität: Plötzliche einseitige Lähmung und/oder Taubheitsgefühl (Gesicht, Arm oder Bein). Ein herabhängender Mundwinkel oder herabfallender Arm ist ein klassischer Hinweis. Teilweise können diese Defizite peripher anmuten (z. B. wie eine Fallhand) oder auch eine atypische Verteilung haben (z. B. bilaterale schmerzlose Beinschwäche bei beidseitigem A. cerebri anterior Infarkt).
• Sprach- und Sprechstörungen: Aphasien (fehlendes Sprachverständnis oder -ausdruck, Wortfindungsstörungen) oder Dysarthrie (verwaschene Aussprache).
• Sehstörungen: Plötzlicher Sehverlust inkl. Amaurosis (fugax) oder unilateraler Gesichtsfeldausfall; Doppelbilder v.a. bei Beteiligung der hinteren Zirkulation.
• Koordination/Schwindel: Plötzlicher starker Schwindel mit Gangunsicherheit, Ataxie oder weiteren Hirnstammsymptomen.
Die Anwendung des BEFAST-Tests (Balance-Eyes-Face-Arm-Speech-Time) verbessert die Sensitivität der Hirnschlagerkennung, indem Gleichgewichts- und Sehstörungen einbezogen werden. Bei akutem, anhaltendem Schwindel mit Spontannystagmus kann der HINTS+ Test (Head Impulse, Nystagmus, Test of Skew plus Hörminderung, fokalneurologisches Defizit, can’t walk vs. won’t walk) helfen, eine zentrale Ursache wie einen Hirnstamminfarkt von einer peripheren Vestibulopathie zuverlässig zu unterscheiden – insbesondere bei Patient/-innen ohne andere fokale Ausfälle (11). Bei Verdacht auf einen Hirnschlag – besonders bei Symptombeginn innerhalb der letzten 48 Stunden – ist die sofortige notfallmässige Zuweisung in ein Spital mit zertifizierter Stroke Unit oder Stroke Center zwingend erforderlich, auch wenn die Beschwerden nur vorübergehend waren. Bei anhaltenden Symptomen sollte der Rettungsdienst unmittelbar alarmiert werden.
Präklinisches Management
Folgende präklinische Punkte sind wichtig (12):
• Befolgen des ABCDE-Schemas zur Sicherstellung der Vitalfunktionen (Atemwege, Atmung, Kreislauf, neurologisches Defizit)
• Genaue Dokumentation des Zeitpunkts der ersten Symptome bzw. des Zeitpunkts letztmalig sicherer Gesundheit («last known well»).
• Keine Gabe von Aspirin oder Antikoagulantien vor erfolgter Schädelbildgebung (Blutungsausschluss).
• Messung von Blutzucker (häufiger Stroke Mimic) und Temperatur, aber keine Routinelabors oder EKG abwarten
• Übergabe relevanter Informationen: Aktueller Zustand (GCS, Defizit), Geschätzte Ankunftszeit, Antikoagulation, Medikationsliste, Vorerkrankungen, Patientenverfügung, MR-Kontraindikationen (z. B. Pacemaker) an die aufnehmende Klinik.
• Information zu relevanten Kontraindikationen für die intravenöse Thrombolyse (z. B. kürzlich erfolgte Operationen, Marcoumar-Therapie oder vorbekannte Blutungsneigung)
• Frühzeitige telefonische Vorankündigung im Spital.
• Sauerstoffgabe nur bei SpO₂ < 94 %.
• Blutdrucksenkung präklinisch nur falls > 220/120 mmHg.
• Es gibt aktuell keinen klaren Vorteil einer bestimmten Kopfposition, daher sind 0° bis 30° empfohlen
• Nutzung von Triage-Scores wie RACE zur Erkennung von Grossgefässverschlüssen: schwer betroffene Patient:innen sollten direkt in ein Stroke Center mit Möglichkeit zur Thrombektomie zugewiesen werden.
Vorankündigung und Vorausplanung
Eine frühzeitige Vorankündigung an das Stroke-Team verbessert die Vorbereitung und reduziert Behandlungsverzögerungen. Dies gewährleistet die sofortige Einsatzbereitschaft des Stroke-Teams (Neurologie, Pflege) und das Freihalten des Geräts für die Schädelbildgebung (Neuroradiologie). Bei instabilen oder schwer betroffenen Patient/-innen auch zur Planung einer Schockraumversorgung oder Beizug der Anästhesie (Thrombektomie).
Bei Hochrisikopatienten, insbesondere älteren und multimorbiden Menschen mit vorbestehenden Beeinträchtigungen, ist das vorsorgliche Dokumentieren des Patientenwillens und Übermitteln von Patientenverfügungen an Zentrumsspitäler sinnvoll, um unerwünschte Maximaltherapie zu vermeiden. Falls keine Patientenverfügung vorliegt, ist das Übermitteln einer Telefonnummer eines Familienmitglieds hilfreich.
Differenzialdiagnosen: Stroke-Mimics erkennen
Auch wenn der Verdacht auf einen akuten Hirnschlag naheliegt, sollte bei der Ersteinschätzung eine differenzierte Betrachtung möglicher Alternativdiagnosen erfolgen. Zu den häufigsten sogenannten «Stroke Mimics» zählen Hypoglykämie, epileptische Anfälle mit postiktaler Parese (Todd’sche Parese), Migräne mit Aura, funktionelle neurologische Störungen sowie zerebrale Tumoren oder Infektionen wie z. B. Enzephalitis. Besonders relevant in der Hausarztpraxis ist der Ausschluss einer Hypoglykämie mittels kapillärer Blutzuckermessung, da diese reversibel ist und sofortige Therapie erfordert. Dennoch gilt: Ein Hirnschlag ist eine Ausschlussdiagnose – eine sichere Abgrenzung zu Stroke Mimics ist ohne Bildgebung nicht möglich. Auch bei jungen Patient/-innen ohne klassische vaskuläre Risikofaktoren darf ein Hirnschlag nicht ausgeschlossen werden. Seltene Hirnschlagformen wie eine zerebrale Sinusvenenthrombosen oder embolische Insulte durch ein persistierendes Foramen ovale (PFO) oder eine Halsgefässdissektion (Hornersyndrom?) sind in dieser Altersgruppe relevante Differenzialdiagnosen. Daher sollte auch bei unklarer Klinik und auch bei Fehlen eines vaskulären Risikoprofils die Zuweisung in ein Stroke Spital erfolgen, um eine akute Bildgebung und eine fachärztliche und ggf. interdisziplinäre Beurteilung sicherzustellen.
Bildgebung und Akuttherapie
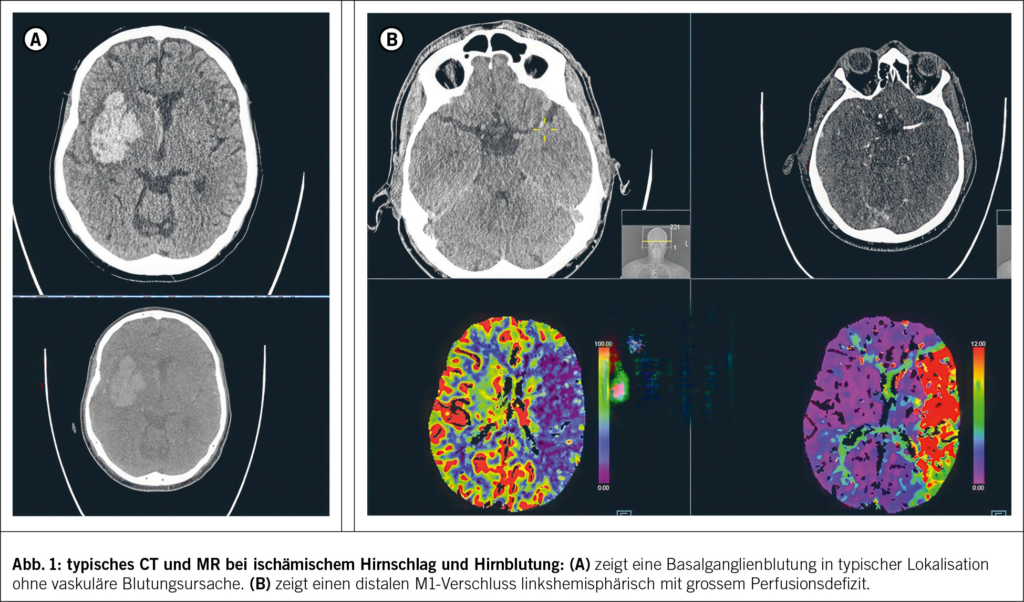
Die Akutdiagnostik erfolgt mittels kranialer CT oder MRI. Während die CT rasch zwischen ischämischem und hämorrhagischem Hirnschlag differenzieren kann, bietet das MRI genauere Gewebebeurteilungen, birgt jedoch den Nachteil von leicht erhöhtem Zeitbedarf und potenziellen Kontraindikationen (Erbrechen, instabiler Patient, ferromagnetische Metallimplantate) (13). Die Entscheidung über die beste Bildgebung muss individuell vom Stroke Spezialisten getroffen werden (Abb. 1).
Therapieoptionen
Intravenöse Thrombolyse: Standard bis 4.5 Stunden nach Symptombeginn bei behinderndem ischämischen Hirnschlag, in ausgewählten Fällen bis zu 48 Stunden nach Symptombeginn abhängig von der Bildgebung (z. B. Wake-Up Strokes). Aufgrund der einfacheren Bolusapplikation und vergleichbarer bis besserer Wirksamkeit erfolgt derzeit vielerorts die Umstellung von Alteplase auf Tenecteplase als routinemässiges Thrombolytikum.
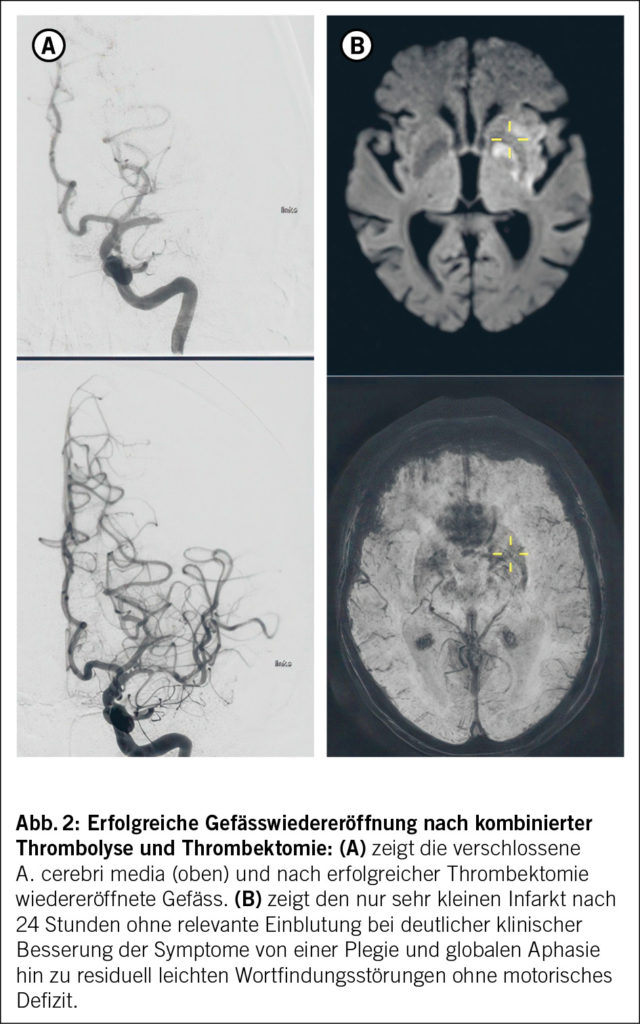
Mechanische Thrombektomie: Indiziert bei grossen intrakraniellen Gefässverschlüssen, Standard bis 6 Stunden nach Symptombeginn, in Einzelfällen bis 48 Stunden abhängig von der Bildgebung. Diese interventionelle Therapie markiert einen Meilenstein in der Schlaganfallbehandlung: Mit einer Number Needed to Treat von nur etwa 3 zählt sie zu den effektivsten medizinischen Therapien überhaupt. Besonders eindrücklich ist das teilweise dramatische Therapieansprechen mit kompletter Rückbildung schwerer neurologischer Defizite. Neuere Studien belegen zudem den Nutzen auch bei Verschlüssen der hinteren Zirkulation (z. B. Basilaristhrombose), bei unklarem Symptombeginn (z. B. Wake-Up-Stroke) sowie bei Patient:innen mit bereits grossem Infarktkern (Abb. 2).
Die aktuelle ELAN-Studie (14) zeigt, dass bei Vorhofflimmer-assoziiertem ischämischem Hirnschlag eine frühzeitige Wiederaufnahme der oralen Antikoagulation – abhängig von Infarktgrösse – sicher und wirksam ist und nicht mit einem erhöhten Blutungsrisiko einhergeht. Lediglich bei Patient/-innen mit einer deutlichen Einblutung ins Infarktareal könnte ein längeres Zuwarten bis zum Wiederbeginn sinnvoll sein (15).
Bei Patien/-innen mit transitorisch ischämischer Attacke (TIA) oder einem leichten bis mittelschwerem ischämischen Hirnschlag (NIHSS ≤ 5), bei denen keine Thrombolyse durchgeführt wird und mit a.e. arteriosklerotischer Genese, stellt die frühzeitige duale Plättchenhemmung mit Clopidogrel und Acetylsalicylsäure (ASS) eine evidenzbasierte Sekundärprävention dar. Die POINT-Studie zeigte, dass die Kombination aus Clopidogrel (600 mg Loading, dann 75 mg/Tag) und ASS (75–100 mg/Tag) innerhalb von 12 Stunden nach Symptombeginn über 90 Tage das Risiko für erneute Hirnschläge signifikant senkt, bei nur minimal erhöhtem Blutungsrisiko (16). Die THALES-Studie bestätigte diesen Nutzen auch für Ticagrelor plus ASS bei leichtem Hirnschlag oder TIA, wobei die Wirkung besonders in den ersten 30 Tagen ausgeprägt war (17). In der Praxis wird daher bei geeigneten Patien/-innen die duale Plättchenhemmung für ca. drei Wochen empfohlen, mit danach Fortführung der Monotherapie. Wichtig ist die sorgfältige Auswahl – Kontraindikationen wie Blutungsrisiko oder bevorstehende operative Eingriffe müssen berücksichtigt werden und das Ereignis sollte eine klare vaskuläre Genese und Symptomatik haben.
Versorgung in spezialisierten Zentren
Die Behandlung in zertifizierten Stroke Units bzw. Stroke Center verbessert signifikant das Outcome. Hier sind multidisziplinäre Teams (Neurologie, Neuroradiologie, Pflege, Physiotherapie) verfügbar. Stroke-Protokolle und Qualitätsstandards (z. B. Schluckabklärung, Antipyrese bei Fieber, Normoglykämie) sichern die Versorgung. Es erfolgt zudem eine standardisierte Abklärung zur Ursachensuche inkl. Vorhofflimmer-Monitoring, kardialer Diagnostik, Darstellung der Halsgefässe, sowie Abklärung eines Persistierenden Foramen Ovale (PFO) oder seltener Ursachen bei entsprechendem Verdacht. Zudem erfolgt eine regelmässige neurologische Überwachung zur frühen Erkennung von Rezidiven oder Komplikationen der Akuttherapie (z. B. die seltene, aber schwerwiegende Einblutung nach Thrombolyse). Falls sich eine symptomatische Gefässstenose zeigt, wird auch in den ersten Tagen eine Revaskularisierung (entweder mittels Carotisendarteriektomie oder Carotis-Stent) durchgeführt.
Die Liste der zertifizierten Stroke Units und Stroke Center ist hier abrufbar: https://www.neurovasc.ch/portrait/stroke-center-stroke-units
Intrazerebrale Blutung: Evidenzbasierter Care-Bundle-Ansatz statt therapeutischem Nihilismus
Während die Prognose der spontanen intrazerebralen Blutung lange als ungünstig galt, hat sich in den letzten Jahren ein Paradigmenwechsel vollzogen: Es existieren mittlerweile mehrere evidenzbasierte Therapiestrategien, die das Outcome signifikant verbessern können, wenn sie frühzeitig und koordiniert angewendet werden (18). Dazu gehört eine rasche Blutdrucksenkung nach erfolgter Bildgebung auf unter 140 mmHg systolisch, wie sie in der INTERACT-4-Studie für Hirnblutungen Wirkung zeigte (19). Allerdings ist präklinisch keine sichere Unterscheidung zwischen ischämischem und hämorrhagischem Hirnschlag möglich. Daher sollten initial die allgemeinen Zielwerte (< 220/110 mmHg) eingehalten werden, da eine Senkung bei ischämischem Infarkt, der die häufigere Ursache darstellt, schädlich ist.
Der sogenannte Care-Bundle-Ansatz umfasst eine Reihe standardisierter, zeitkritischer Interventionen. Dazu gehört die sofortige Revertierung oraler Antikoagulation (z. B. mit Prothrombinkomplexen oder spezifischen Antidots wie Idarucizumab oder Andexanet alfa), sowie die Berücksichtigung neurochirurgischer Verfahren bei geeigneten Patient/-innen. Insbesondere bei lobären Blutungen gewinnt die frühe, minimalinvasive Hämatomausräumung an Bedeutung (20). Ergänzend sind eine konsequente Antipyrese, frühzeitiges Monitoring in der Stroke Unit und die Einleitung einer strukturierten Frührehabilitation entscheidend (21). Die ätiologische Abklärung der Hirnblutung – insbesondere die Differenzierung zwischen zerebraler Amyloidangiopathie (CAA), hypertensiver Genese und anderen vaskulären Ursachen – ist essenziell, da sich daraus entscheidende Unterschiede für die Sekundärprophylaxe und das Blutungsrezidivrisiko ergeben. Daher sollte die akute Bildgebung auch immer mit einer arteriellen und ggf. zusätzlich venösen Angiographie erfolgen. Obwohl die Erholung bei Hirnblutungen etwas länger in Anspruch nimmt, sollten sich Hausärzt:innen bewusst sein, dass ein therapeutischer Nihilismus bei Hirnblutung heute nicht mehr gerechtfertigt ist – stattdessen sollte aktiv eine Zuweisung an spezialisierte Zentren erfolgen, in denen der Care-Bundle-Ansatz etabliert ist.
Ambulante TIA Abklärung
Transitorisch ischämische Attacken sind oft Vorboten eines manifesten Hirnschlags – bis zu 10 % der Betroffenen erleiden innerhalb der ersten Woche einen Hirnschlag, viele davon innerhalb der ersten 48 Stunden. Die rasche Risikostratifizierung erfolgt mithilfe des ABCD²- oder ABCD³-I-Scores, welcher Alter, Blutdruck, klinische Präsentation, Symptomdauer, Diabetes sowie Vorerkrankungen und Bildgebung einbezieht. Bei einem ABCD²-Score < 4 und fehlenden Hochrisikokonstellationen (z. B. Vorhofflimmern, Carotisstenose, Ischämienachweis) kann die Abklärung in einem ambulanten Rahmen erfolgen – vorausgesetzt, sie wird zeitnah (Empfehlung innerhalb von 48 Stunden) organisiert. Dazu gehören ein Echokardiogramm sowie ein Langzeit-EKG (mindestens 72 Stunden) zum Ausschluss von paroxysmalem Vorhofflimmern (6). Hier nimmt der Hausarzt eine Schlüsselrolle ein – er koordiniert den schnellen Zugang zur kardiologischen Diagnostik, idealerweise in Zusammenarbeit mit dem lokalen Stroke Center.
Copyright
Aerzteverlag medinfo AG
Oberarzt, Leiter Neurologisches Notfallteam
Klinik für Neurologie
Inselspital Bern
Rosenbühlgasse 25
3010 Bern
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Hausärztinnen und Hausärzte als Erstbehandler: Frühzeitige Erkennung, korrekte Triage und die Weitergabe relevanter Informationen (Symptombeginn, Medikation, Kontraindikationen) verbessern die Behandlung erheblich.
- BEFAST anwenden: Plötzliche Lähmung, Sprach- oder Sehstörungen sind Warnzeichen – auch wenn vorübergehend – und erfordern eine sofortige notfallmässige Zuweisung in die nächstgelegene Stroke Unit oder ein Stroke Center.
- Sofortige Rettungskette aktivieren: Besonders bei Symptombeginn <48 h und/oder anhaltenden Defiziten. Vorankündigung im Spital beschleunigt die Akutversorgung.
- Blutzuckermessung präklinisch: Hypoglykämie, postiktale Paresen oder Migräne können ähnlich aussehen – aber ein Hirnschlag ist eine Ausschlussdiagnose.
- Keine Therapie ohne Bildgebung: CT oder MRI sind unverzichtbar zur Unterscheidung von ischämischem und hämorrhagischem Schlaganfall. Keine präklinische Gabe von Aspirin oder Blutverdünnern.
- Thrombolyse, Thrombektomie und frühe antithrombotische Therapie sind hocheffektive Therapieoptionen – teilweise noch bis zu 48 Stunden nach Symptombeginn wirksam.
- Patient/-innen in spezialisierte Stroke Units bzw. Stroke Center überweisen.
- Intrazerebrale Blutung aktiv behandeln: Der Care-Bundle-Ansatz ersetzt heute den früher verbreiteten therapeutischen Nihilismus – mit evidenzbasierten, wirksamen Massnahmen.
- TIA ist kein Bagatellereignis: Auch bei transitorischen Symptomen ist eine strukturierte, zeitnahe Abklärung inkl. kardialem Monitoring entscheidend.
1. Collaborators, G. 2021 S. R. F. Global, regional, and national burden of stroke and its risk factors, 1990–2021: a systematic analysis for the Global Burden of Disease Study 2021. Lancet Neurol. 23, 973–1003 (2024).
2. Suisse, C. Nationale Strategie Herz- und Gefässkrankheiten, Hirnschlag und Diabetes, 2017–2024. https://www.neurovasc.ch/fileadmin/user_upload/Nationale_Strategie_Herz-_und_Gefaesskrankheiten__Hirnschlag_und_Diabetes_2017-2024.pdf?utm_source=chatgpt.com (2016).
3. Jung, S. et al. Factors that determine penumbral tissue loss in acute ischaemic stroke. Brain 136, 3554–3560 (2013).
4. O’Donnell, M. J. et al. Global and regional effects of potentially modifiable risk factors associated with acute stroke in 32 countries (INTERSTROKE): a case-control study. Lancet 388, 761–775 (2016).
5. Law, M. R., Morris, J. K. & Wald, N. J. Use of blood pressure lowering drugs in the prevention of cardiovascular disease: Meta-analysis of 147 randomised trials in the context of expectations from prospective epidemiological studies. BMJ 338, 1245 (2009).
6. Meinel, T. et al. Swiss Stroke Society position paper on atrial fibrillation monitoring and management after ischaemic stroke: a shift from understanding the index stroke to preventing the next one. Swiss Med. Wkly. 6, 4170 (2025).
7. Sattar, N. et al. Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of randomised trials. Lancet Diabetes Endocrinol. 9, 653–662 (2021).
8. AGLA. PDF-Pocketguide Prävention der Atherosklerose 2025. (2025).
9. Eikelboom, J. W. et al. Rivaroxaban with or without Aspirin in Stable Cardiovascular Disease. N. Engl. J. Med. 377, 1319–1330 (2017).
10. Lloyd-Jones, D. M. et al. Life’s Essential 8: Updating and Enhancing the American Heart Association’s Construct of Cardiovascular Health: A Presidential Advisory from the American Heart Association. Circulation 146, E18–E43 (2022).
11. S. Jung, T. Meinel, H. Mattle, T. Horvath, D. Seiffge, M. Heldner, P. Bücke, U. Prange, B. V., H. Sarikaya, S. Muth, A. Luczkiewicz, P. Correia, A. Humm, S. Renaud, R. Bühler, J. Gralla, J. Kaesmacher, M., Bühlmann, A. Angelillo-Scherrer, W. Z`Graggen, C. Bassetti, A. Raabe, U. Fischer, M. A. & Bern, S.-T. Stroke Richtlinien des Berner Stroke Netzwerks. https://neurologie.insel.ch/fileadmin/Neurologie/Stroke_Richtlinien_2024_neu.pdf (2024).
12. Kägi, G. et al. Prähospitalphase beim akuten Hirnschlag. Swiss Med. Forum – Schweizerisches Medizin-Forum 21, 322–328 (2021).
13. Fischer, U. et al. Magnetic Resonance Imaging or Computed Tomography for Suspected Acute Stroke: Association of Admission Image Modality with Acute Recanalization Therapies, Workflow Metrics, and Outcomes. Ann. Neurol. 92, 184–194 (2022).
14. Fischer, U. et al. Early versus Later Anticoagulation for Stroke with Atrial Fibrillation. N. Engl. J. Med. 388, 2411–2421 (2023).
15. Rohner, R. et al. Early Versus Late Initiation of Direct Oral Anticoagulants After Ischemic Stroke in People With Atrial Fibrillation and Hemorrhagic Transformation: Prespecified Subanalysis of the Randomized Controlled ELAN Trial. Circulation 150, 19–29 (2024).
16. Johnston, S. C. et al. Clopidogrel and Aspirin in Acute Ischemic Stroke and High-Risk TIA. N. Engl. J. Med. 379, 215–225 (2018).
17. Johnston, S. C. et al. Ticagrelor and Aspirin or Aspirin Alone in Acute Ischemic Stroke or TIA. N. Engl. J. Med. 383, 207–217 (2020).
18. Steiner, T. et al. European Stroke Organisation ( ESO ) and European Association of Neurosurgical Societies ( EANS ) guideline on stroke due to spontaneous intracerebral haemorrhage. (2025) doi:10.1177/23969873251340815.
19. Li, G. et al. Intensive Ambulance-Delivered Blood-Pressure Reduction in Hyperacute Stroke. N. Engl. J. Med. 390, 1862–1872 (2024).
20. Pradilla, G. et al. Trial of Early Minimally Invasive Removal of Intracerebral Hemorrhage. N. Engl. J. Med. 390, 1277–1289 (2024).
21. Ma, L. et al. The third Intensive Care Bundle with Blood Pressure Reduction in Acute Cerebral Haemorrhage Trial (INTERACT3): an international, stepped wedge cluster randomised controlled trial. Lancet 402, 27–40 (2023).
der informierte @rzt
- Vol. 15
- Ausgabe 7
- Juli 2025