- Das geschwollene Bein
Beinödeme sind ein häufiger Vorstellungsgrund in der hausärztlichen und internistischen Praxis. Sie entstehen durch Flüssigkeitsansammlung im Interstitium und können sowohl physiologische Auslöser – wie Hitzeödeme, statische Belastungsödeme, prämenstruelle Veränderungen oder Schwangerschaft – als auch vielfältige pathologische Ursachen haben. Der Artikel beschreibt die wichtigsten Differenzialdiagnosen wie Herzinsuffizienz, nephrotisches Syndrom, Leberzirrhose, tiefe Venenthrombose, chronisch venöse Insuffizienz, postthrombotisches Syndrom und Lymphödem. Für jede Ursache werden typische Anamnese- und Befundkonstellationen, zentrale diagnostische Schritte sowie leitlinienbasierte Therapieoptionen erläutert. Ziel ist die strukturierte ätiologische Einordnung, um frühzeitig angemessene Fachabklärungen und wirksame Behandlungen einzuleiten.
Leg edema is a common reason for presentation in general practice and internal medicine. It results from the accumulation of fluid in the interstitial space and may be caused by physiological factor – such as heat edema, dependent (gravitational) edema, premenstrual or pregnancy related edema as well as a wide range of pathological conditions. The article outlines the most important differential diagnoses, including heart failure, nephrotic syndrome, liver cirrhosis, deep vein thrombosis, chronic venous insufficiency, post-thrombotic syndrome, and lymphedema. For each cause, typical patterns in medical history and clinical findings, key diagnostic steps, and guideline-based therapeutic options are described. The aim is to enable a structured etiological classification to initiate timely specialist evaluation and effective treatment.
Keywords: Beinödeme, Differenzialdiagnostik, Venenerkrankungen, Lymphödem
Einleitung
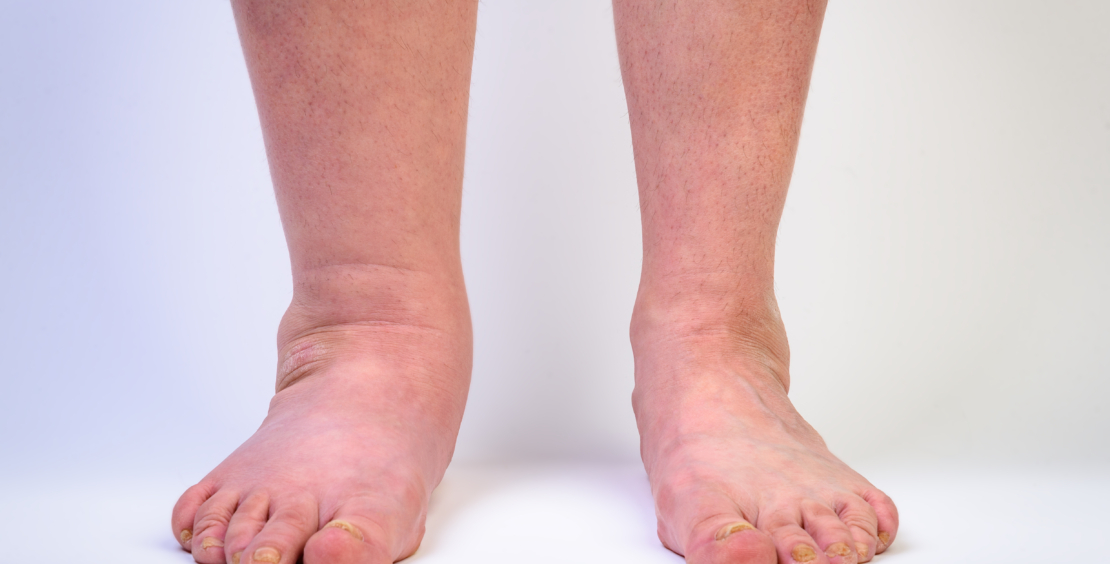
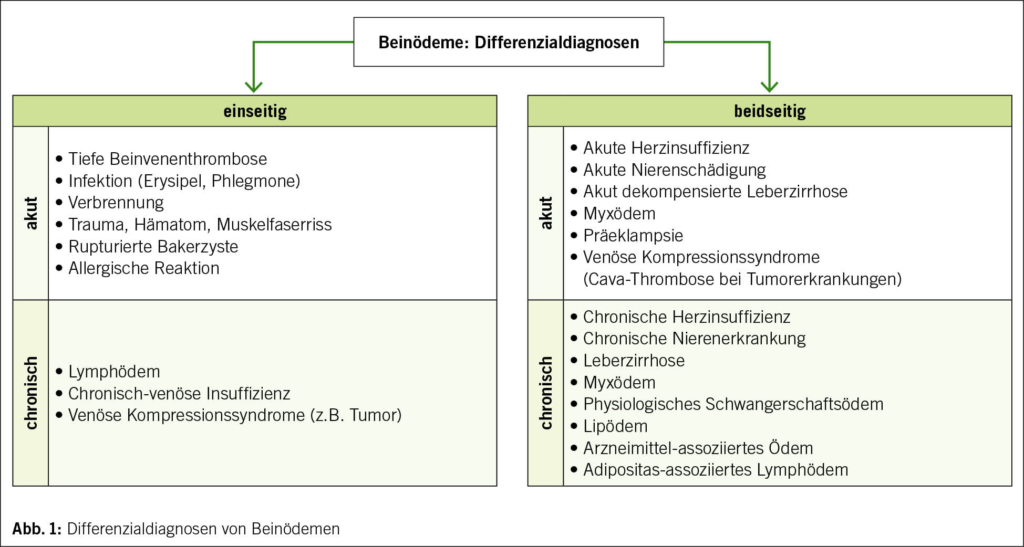
Bein- und Fussödeme sind ein häufiger Konsultationsgrund für Patientinnen und Patienten in der hausärztlichen Praxis. Sie entstehen durch eine Ansammlung von Flüssigkeit im interstitiellen Raum (1). Verschiedene Mechanismen können hierfür verantwortlich sein. Ätiologisch kommen sowohl physiologische Flüssigkeitseinlagerungen als auch eine Vielzahl von Krankheitsbildern in Betracht, die sich als Beinschwellung manifestieren. Zu den physiologischen Ödemen zählen etwa Hitzeödeme, statische Überlastungsödeme nach langem Sitzen oder Stehen, zyklische prämenstruelle Ödeme sowie das physiologische Schwangerschaftsödem. Pathologische Ödeme treten hingegen im Rahmen verschiedener Erkrankungen auf, darunter Herz- und Niereninsuffizienz, Leberzirrhose, chronisch-venöse Insuffizienz, Thrombose, Infektionen oder ein Lymphödem. Das Lipödem wurde zwar historisch zu den Ödemen gezählt, jedoch handelt es sich um eine anlagebedingte Fettverteilungs- und Vermehrungsstörung (1). Einen Überblick ausgewählter Ursachen von Ödemen – orientierend eingeordnet nach der Akuität und Lokalisation ihres Auftretens – gibt Abb. 1.
Die Vielzahl möglicher Differenzialdiagnosen stellt eine relevante Herausforderung im klinischen Alltag dar. Ziel ist es, mittels sorgfältiger Anamnese, klinischer Untersuchung sowie gezielter Labor- und apparativer Diagnostik die ursächliche Pathologie korrekt zu identifizieren, um anschliessend adäquate Behandlungsmassnahmen einzuleiten.
Bei infektiösen Ursachen (z. B. Erysipel oder Phlegmone) stehen neben gezielter Anamnese und klinischer Untersuchung vor allem die labordiagnostische Bestimmung der Entzündungsparameter und die mikrobiologische Diagnostik im Vordergrund. Eine kalkulierte, idealerweise resistogrammgerechte Antibiose stellt die wichtigste therapeutische Massnahme dar. Je nach Befund kann ergänzend eine chirurgische Sanierung erforderlich werden.
Eine kardiale, renale, hepatische oder vaskuläre Ursache von Ödemen erfordert eine umfangreiche diagnostische Aufarbeitung und ein komplexes therapeutisches Management. Diese Krankheitsbilder werden daher im Folgenden genauer dargestellt.
Herzinsuffizienz
Eine Rechtsherzinsuffizienz – etwa infolge pulmonaler Hypertonie, ischämischer Herzerkrankung oder Kardiomyopathie – führt zum Rückstau des Blutes ins venöse System. Der dadurch erhöhte hydrostatische Druck begünstigt den Austritt von Flüssigkeit ins Interstitium und somit die Entstehung von Ödemen. Insbesondere bei fortgeschrittener Herzinsuffizienz können zusätzliche Faktoren wie eine chronische Nierenerkrankung (chronic kidney disease, CKD), Cirrhose cardiaque und Mangelernährung die Symptomatik weiter verstärken.
In der Anamnese sollte nach der Lokalisation, dem zeitlichen Verlauf der Ödeme sowie weiteren kardialen Kardinalsymptomen (Brustschmerzen, Dyspnoe, Orthopnoe, nächtliches Husten, Schwindel, Synkopen, Palpitationen, Herzrasen), Körpergewichtsänderungen und Fieber gefragt werden. Die Labordiagnostik sollte neben Blutbild, Nierenwerten, Elektrolyten, TSH und Transaminasen auch die Bestimmung der natriuretischen Peptide beinhalten (NT-proBNP oder BNP). Falls letztere normwertig sind, kann eine kardiale Genese der Ödeme weitgehend ausgeschlossen werden. Bei erhöhten natriuretischen Peptiden ist eine Überweisung zum Kardiologen zur transthorakalen Echokardiographie indiziert. Diese ermöglicht die Bestätigung der Verdachtsdiagnose, die Klassifikation der Herzinsuffizienz anhand der Auswurffraktion sowie die Gewinnung wichtiger Hinweise zur zugrunde liegenden Ätiologie, wie z. B. Klappenerkrankungen oder strukturellen Myokardschäden.
Neben Allgemeinmassnahmen (Nikotinkarenz, Körpergewichtsnormalisierung, regelmässige körperliche Aktivität) ist oft eine spezifische Behandlung der Grunderkrankung (z. B. Revaskularisation bei KHK, Klappenersatz/-rekonstruktion) möglich. Neben lokaler Kompressionsbehandlung und (Schleifen-)Diuretika zur Flüssigkeitsretention kommen je nach Phänotyp der Herzinsuffizienz als medikamentöse Therapie primär die sog. «phantastischen vier» Wirkstoffgruppen zum Einsatz:
• Herzinsuffizienz mit reduzierter LVEF (HFrEF): SGLT2i (IA), ACEi/ARB/ARNI (IA), MRA (IA), Beta-blocker (IA) (2)
• Herzinsuffizienz mit leicht reduzierter LVEF (HFmrEF): SGLT2i (IA), ACEi/ARB/ARNI (IIb), MRA (IIb), Beta-blocker (IIb) (3)
• Herzinsuffizienz mit erhaltener LVEF (HFpEF): SGLT2i (IA) (3)
Nephrotisches Syndrom
Glomerulonephritiden, diabetische Nephropathie, multiples Myleom, Amyloidose u. a. führen zu einer erhöhten Permeabilität der Kapillaren für Plasmaeiweisse mit Verlust von Proteinen in den Urin. Kompensatorisch wird die Proteinsynthese in der Leber gesteigert. Sobald der Verlust die Synthesekapazität der Leber übersteigt (3–3.5 g/Tag) kommt es zu den klassischen Symptomen des nephrotischen Syndroms.
• Proteinurie > 3.5 g/d
• Hypalbuminämie und Hyperlipoproteinämie
• Ödeme
• Hyperkoagulabilität (1)
Hypothetisch werden zwei wesentliche Mechanismen der Ödembildung angenommen: einerseits die Retention von Natrium und Wasser durch geschädigte Nephrone, andererseits die Senkung des kolloidosmotischen Drucks mit relativer Hypovolämie durch den Verlust von Albumin im Rahmen der erhöhten Kapillarpermeabilität mit konsekutiver Aktivierung des Renin-Angiotensin-Aldosteron-Systems (RAAS) mit wiederum zusätzlicher Natrium- und Wasserretention. Es kommt auch zum Verlust anderer Funktionsproteine wie Immunglobuline oder Antithrombin mit den Folgen einer erhöhten Infektanfälligkeit und einer Thromboseneigung (4).
Die Anamnese sollte u.a. quantitative und qualitative Veränderungen des Urins (z. B. vermehrte Schaumbildung) umfassen. Die klinische Untersuchung zeigt primär oft periorbitale, im Verlauf generalisierte Ödeme. Die Labordiagnostik sollte neben Blutbild, Kreatinin, geschätzter glomerulärer Filtrationsrate (eGFR), Harnstoff, Elektrolyten, TSH und Transaminasen auch die Bestimmung der natriuretischen Peptide beinhalten. Eine Teststreifen-Analyse des morgendlichen Mittelstrahlurins kann als Screeninguntersuchung auf eine Albuminurie – insbesondere auch bei chronischen Erkrankungen, die typischerweise zu einer Nierenschädigung führen (Diabetes mellitus oder arterielle Hypertonie) – erfolgen. Um eine Albuminurie zu bestätigen und zu quantifizieren, sollte nachfolgend immer die Bestimmung der Albumin-/Kreatinin-Ratio (ACR) erfolgen (5). Ein Wert von ≥ 30 mg/g oder ≥ 3 mg/mmol wird als pathologisch angesehen (5). Auf die Bestimmung von ACR und eGFR stützt sich auch das CKD-Klassifikationssystem. Weiterführende diagnostische Methoden umfassen u.a. eine Nierensonographie und eine Nierenbiopsie. Die Therapie der Grunderkrankung steht an erster Stelle, bspw. mittels Immunsuppressiva bei Glomerulonephritiden. Zur Verlangsamung der CKD-Progression kommen ACE-Hemmer und Sartane in der höchsten verträglichen Dosis, sowie SGLT2-Inhibitoren zum Einsatz (5). Eine Proteinaufnahme >1.3 g/kgKG/d und eine Kochsalzaufnahme >5 g/d, Nikotinkonsum und die Einnahme nephrotoxischer Medikamente (z. B. NSAID) sollten vermieden werden (5). Die akute Behandlung der Ödeme erfolgt primär durch die Gabe von Schleifendiuretika, ggf. unter Hinzunahme von Thiaziden oder Thiazidanaloga (z. B. Metolazon) als sequenzielle Nephronblockade.
Leberzirrhose
Verschiedene Auslöser (u.a. kardio-renal, metabolisches Syndrom, toxisch oder infektiös) können zu einer Zerstörung der physiologischen Leberstruktur führen. In der Folge treten eine reduzierte Syntheseleistung der Leber, eine portale Hypertension und die Bildung intrahepatischer portosystemischer Shunts zwischen Portalgefässen und Lebervenen mit konsekutiver Minderperfusion der Leber auf (1).
Mehrere Mechanismen liegen der Ödementstehung zugrunde:
1. Die portale Hypertension bewirkt eine Hypervolämie der Splanchnikusgefässe und eine vermehrte Lymphproduktion (1).
2. Die verminderte Syntheseleistung der Leber führt zur Hypalbuminämie, so dass der kolloidosmotische Druck erniedrigt wird (1).
3. Der resultierende intravasale Volumenmangel bewirkt die Aktivierung des RAAS-Systems, sowie eine gesteigerte Produktion von Antidiuretischem Hormon (ADH) und Katecholaminen. Hierdurch werden renal vermehrt Natrium und Wasser retiniert (1).
Durch die Anamnese sollten unter anderem Risikofaktoren für eine Lebererkrankung evaluiert werden (v.a. Alkoholkonsum, Hepatitiden). In der klinischen Untersuchung können sich neben Aszites, Pleuraergüssen, Ödemen bei gleichzeitig typischerweise kachektischem Habitus die Leberhautzeichen (z. B. Caput medusae, Spider naevi, Teleangiektasien, Lackzunge, Weissnägel, Palmarerythem) zeigen. Labordiagnostisch sollten neben kleinem Blutbild (Thrombozytopenie), Nierenwerten, Elektrolyten, TSH und NT-pro-BNP vor allem Transaminasen, gGT, Albumin, INR, PTT, Antithrombin, Cholinesterase, Bilirubin und eine Hepatitis-Serologie bestimmt werden. Primäre Bildgebung ist eine Sonographie der Leber. Therapeutisch steht – neben der Behandlung der Grunderkrankung – vor allem die symptomatische Behandlung der Ödeme im Vordergrund. Diuretikum der 1. Wahl ist Spironolacton, ggf. in Kombination mit Schleifendiuretika (6). Hepatotoxische Substanzen (insbesondere Alkohol sowie gewisse Medikamente) (1) und eine Kochsalzaufnahme >5 g/d (6) sollten vermieden werden. Hinsichtlich der Ernährung sollte ein ausreichender Eiweissgehalt (1.2–1.5 g/kgKG/d) und Energiegehalt (30–35 kcal/kgKG/d) angestrebt werden (6).
Tiefe Beinvenenthrombose (TVT)
Gemäss der Virchow-Trias können der Entstehung einer Thrombose drei wesentliche Ursachen zugrunde liegen:
1. Schädigung des Endothels: Inflammation, Trauma (1)
2. Veränderung des Blutflusses: Verwirbelung, Verlangsamung (z. B. lokale Stase, Herzinsuffizienz) (1)
3. Veränderung der Zusammensetzung des Blutes: Dysbalance von Gerinnung und Fibrinolyse (1)
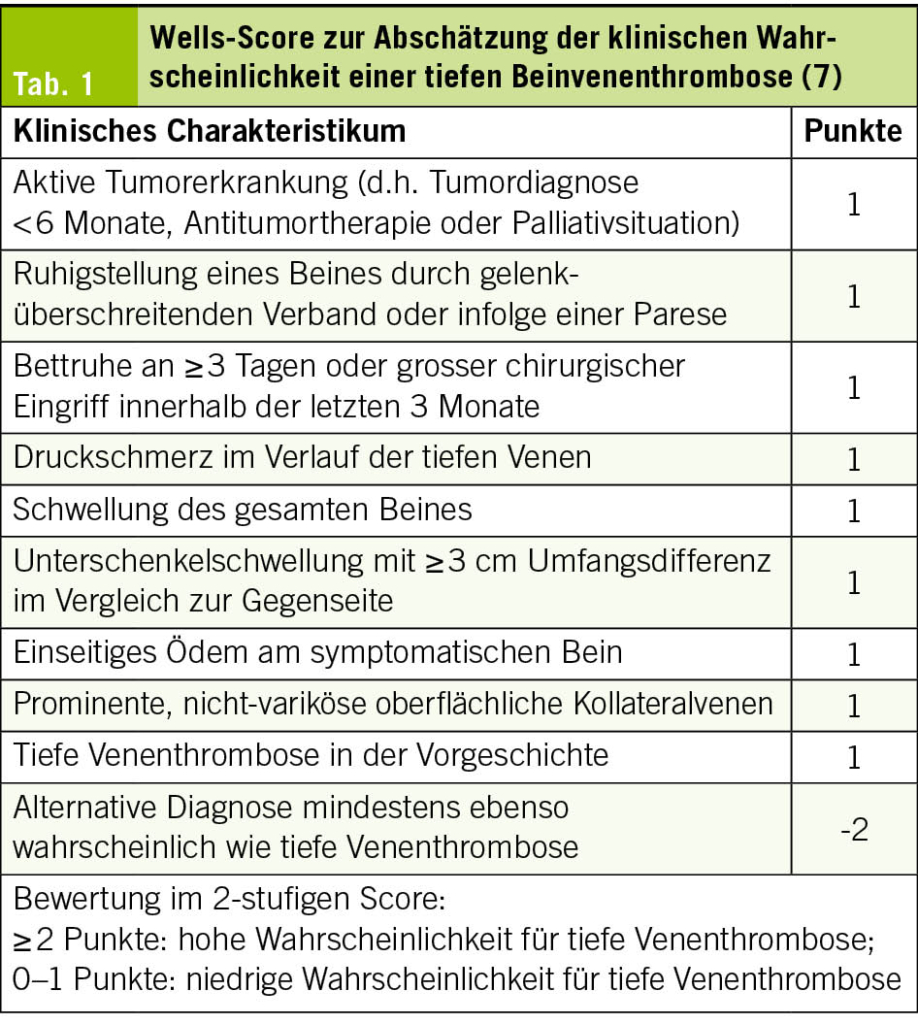
Hinweisend in Anamnese und klinischer Untersuchung sind ein akutes – i.d.R. einseitiges Auftreten, mit Schmerzen, Rötung, Schwellung und harter, gespannter Haut. Als auslösende Faktoren sollten kürzliche Immobilisationen (längere Reisen, Hospitalisationen), die Einnahme hormoneller Kontrazeptiva, Nikotinabusus und bekannte Thrombophilie (auch familiär) erfragt werden. Mittels validierter Scores (z. B. Wells-Score, Tab. 1) kann die klinische Wahrscheinlichkeit für eine TVT abgeschätzt werden. Bei niedriger klinischer Wahrscheinlichkeit (Wells Score 0–1 Punkte) und negativen D-Dimeren gilt eine TVT als ausgeschlossen (7). Bei einem Wells-Score ≥2 Punkte sollte primär eine vollständige Kompressionssonographie des betroffenen Beins erfolgen (7). Sie stellt die Diagnostik der ersten Wahl dar – auch als Bestätigungstest bei positiven D-Dimeren und niedriger klinischer Wahrscheinlichkeit (7). Da bei einer Schwangerschaft die D-Dimere als Ausdruck der physiologischen Aktivierung des Gerinnungssystems physiologisch ansteigen, sollte ein D-Dimer-unabhängiger Vortest verwendet werden, beispielsweise der LEFt-Score (8). Je nach Klinik (Angabe von Dyspnoe/Thoraxschmerzen/EKG-Veränderungen wie Rechtsschenkelblock, Rechtslagetyp, Sinustachykardie) muss an eine Lungenarterienembolie gedacht und diese mittels CT-Angiographie des Thorax ausgeschlossen werden. Die Therapie einer TVT lässt sich in drei Phasen gliedern: Im Rahmen der Initialtherapie (5–21 Tage) und der Erhaltungstherapie (mind. 3–6 Monate) sollte eine therapeutische Antikoagulation erfolgen. Ziel ist die Verhinderung einer Thrombose-Progression und die Verhinderung von Lungenembolien (7). Nach 6 Monaten beginnt die Phase der Sekundärprophylaxe. Hier muss sorgfältig abgewogen werden, ob eine verlängerte oder gar dauerhafte Fortführung der Antikoagulation in therapeutischer oder niedrigerer Dosis erforderlich ist (7). Andernfalls kann diese beendet und ggf. eine medikamentöse Prophylaxe venöser Thromboembolien (VTE) in Risikosituationen etabliert werden. Konstant vorhandene Risikofaktoren – wie eine Thrombophilie oder ein unheilbares Malignom – erfordern im Gegensatz zu nur passager vorhandenen Risikofaktoren – wie einer Immobilisation in Folge eines Langstreckenfluges – i.d.R. eine dauerhafte Fortführung der therapeutischen Antikoagulation. Zur Antikoagulation bei TVT werden grundsätzlich direkte orale Antikoagulanzien (DOAK) gegenüber Vitamin-K-Antagonisten oder niedermolekularen Heparinen bevorzugt, ausser bei substanzspezifischen Kontraindikationen (z. B. Antiphospholipidsyndrom, Schwangerschaft, schwere Niereninsuffizienz) (7). In den letzten Jahren gewinnen minimalinvasive Verfahren zur Rekanalisation iliofemoraler Thrombosen (Entfernung des Thrombus, Behebung einer anatomischen Enge, z. B. bei May-Thurner), mit entsprechender Symptomatik, zunehmend an Bedeutung. Dann sollte auch primär mit einem niedermolekularen Heparin bis zur Klärung des weiteren therapeutischen Vorgehens begonnen werden.
Zu beachten sind die jeweiligen Dosierungsempfehlungen gemäss der gültigen Fachinformationen (z. B. initial höhere Dosis von Rivaroxaban und Apixaban). Die lokale Kompressionstherapie sollte initial mittels eines phlebologischen Kompressionsverbands und bei bereits rückläufiger Beinschwellung mittels eines Kompressionsstrumpfs der Klasse II erfolgen. Auch die Fortführung der Kompressionstherapie sollte nach 3–6 Monaten reevaluiert werden (7). Die Phlegmasie ist die fulminanteste Form einer (meist ilio-femoralen) TVT und stellt einen akuten Gefässnotfall dar. Generell wird zwischen einer Phlegmasia alba dolens und der zyanotischen Phlegmasia cerulea dolens unterschieden. Die letztere kann in eine venöse Gangrän übergehen und benötigt eine umgehende notfallmedizinische Betreuung. Pathophysiologisch führt der nahezu komplette venöse Abflussverschluss zu massivem Gewebsödem, Druckanstieg und sekundär auch zu arterieller Minderperfusion, was klinisch eine akute Extremitäten-Ischämie imitieren kann. Die Soforttherapie umfasst eine therapeutische Antikoagulation, Hochlagerung und konsequente Kompression zur Stabilisierung und Embolie-Prophylaxe sowie – bei geeigneterer Anatomie – eine endovaskuläre Venenintervention zur Wiederherstellung des venösen Abflusses (8).
Chronisch-Venöse Insuffizienz
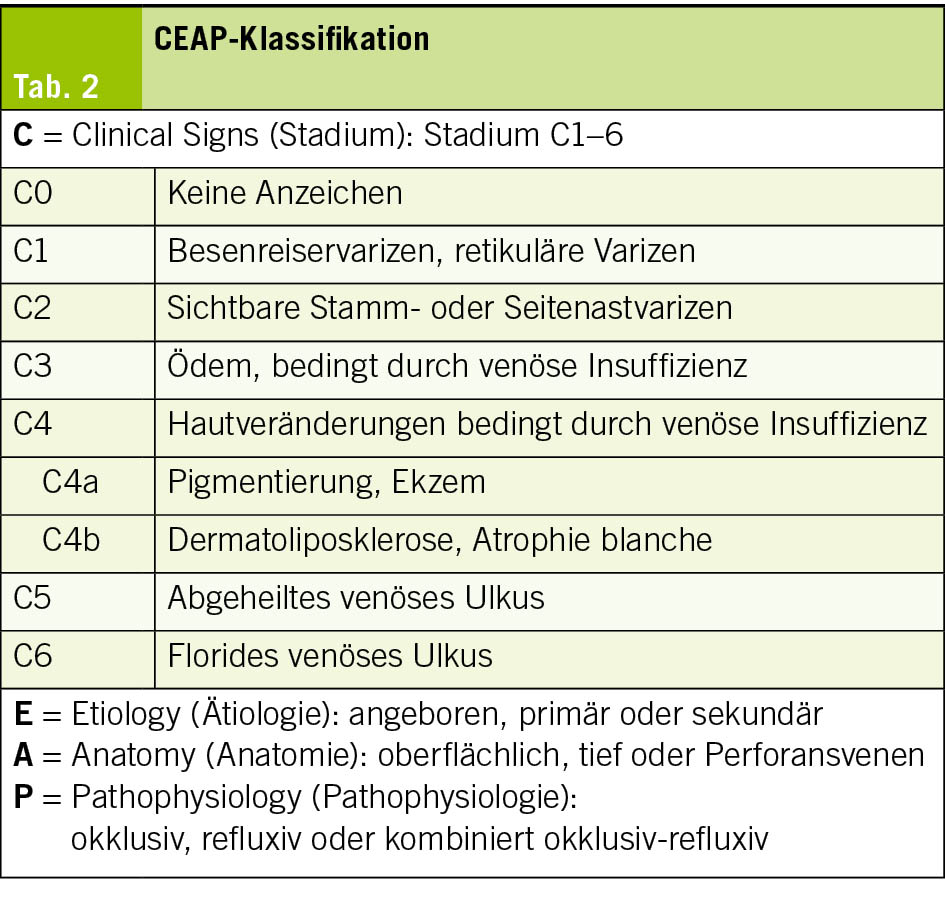
Die chronisch-venöse Insuffizienz entsteht durch eine venöse Hypertonie infolge eines Refluxes (Klappeninsuffizienz) und/oder durch eine venöse Obstruktion (postthrombotisch, Kompression). Im Alltag wird die CEAP-Klassifikation (Tab. 2) zur standardisierten Beschreibung verwendet (9). Klinisch wegweisend sind das Schwere-/ Spannungsgefühl, Schmerzen, das Ödem, Hautveränderungen (Pigmentierung, Dermatoliposklerose, Atrophie blanche, aktive oder abgeheilte Ulzerationen) aber auch Besenreiservarizen/Teleangiektasien, retikuläre Varizen oder bereits im Liegen oder Stehen sichtbare Varizen (10). Ergänzend kann der klinische Schweregrad über den VCSS (Venous Clinical Severity Score) erfolgen. Liegen mit erhöhten Beinen (passiver Rückstrom) und Laufen (aktive Muskelpumpe) wirken sich günstig aus, während Sitzen und Stehen (Stase) zu vermehrter Ödembildung führen. Per Labordiagnostik und Sonographie sollten zunächst andere Ursachen eines Beinödems ausgeschlossen werden. Die klinische Untersuchung erfolgt im Stehen mit Inspektions- und Funktionstests; der Nachweis der Ursache (Reflux/Obstruktion) erfolgt mittels Duplexsonografie (9). Das Fundament der Therapie der chronisch-venösen Insuffizienz bleibt die Kompressionstherapie zur Symptomkontrolle, Ulkusheilung und Rezidivprophylaxe. Bei nachweisbarem Reflux in den Stammvenen oder Perforansvenen existieren endovenöse und chirurgische Verfahren, wobei hier mittlerweile die endovenöse Ablation bei anatomischer Eignung gegenüber den chirurgischen Verfahren vorgezogen wird (11). Phlebektomien und Sklerosierungsverfahren ergänzen hierbei die Intervention. Venoaktive Substanzen (Flavonoide wie z. B. MPFF, Saponine wie z. B. Rosskastaniensamen-Extrakt oder Polysaccharide wie Sulodexid) können Symptome reduzieren, ersetzen aber keine kausale Refluxbehandlung. Ist die chronisch-venöse Insuffizienz bereits soweit fortgeschritten, dass ein venöses Ulcus besteht, sind die effektive Kompressionstherapie und die Varizensanierung essentiell für eine rasche Heilung und zur Verhinderung eines Rezidivs (12).
Postthrombotisches Syndrom
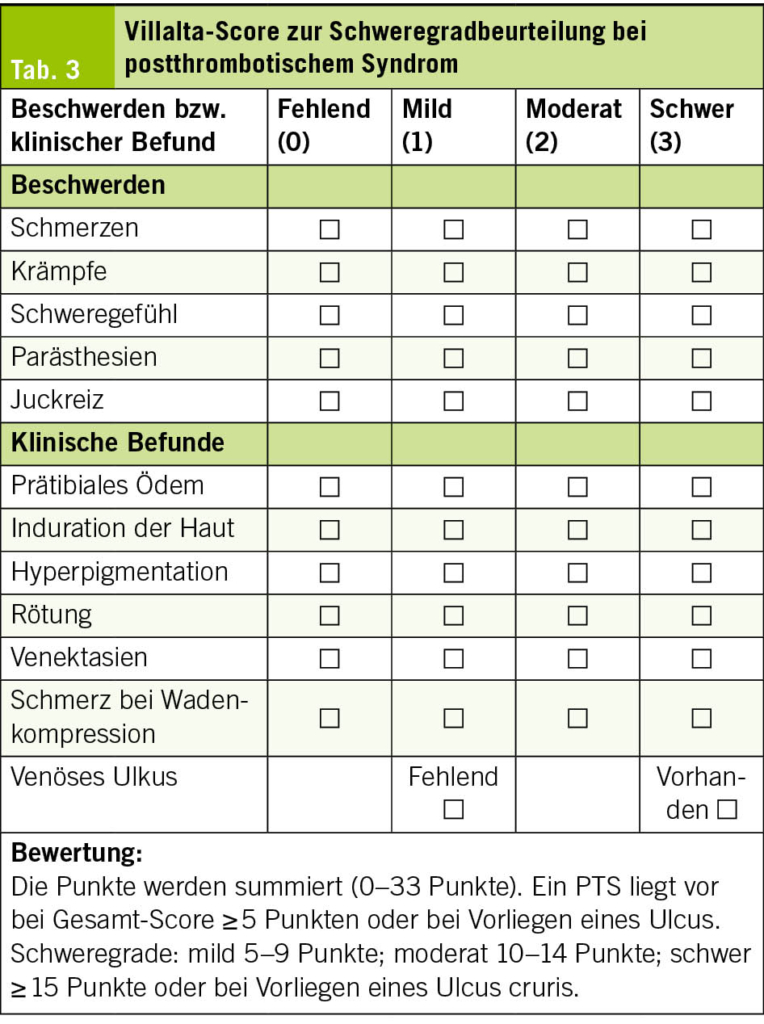
Das postthrombotische Syndrom (PTS) ist eine chronische Spätfolge einer proximalen Beinvenenthrombose (Beckenvenenthrombose, femoro-popliteale Venenthrombose). Das Risiko für die Entstehung eines PTS durch eine distale Beinvenenthrombose (Unterschenkelthrombose, Muskelvenenthrombose) bleibt gering. In Folge der direkten Klappenschädigung durch den Thrombus und/oder durch die anhaltende venöse Obstruktion entsteht eine venöse Hypertonie, welche zu einer chronisch-venösen Insuffizienz führt. In den meisten Fällen entwickelt sich ein PTS innerhalb weniger Monate nach einer symptomatischen Beinvenenthrombose, kann aber auch Jahre nach einem thrombotischen Ereignis auftreten (13). Je nach Patientenkollektiv können 5–10% der Patienten mit einem PTS ein Ulcus cruris entwickeln (14). Das klinische Bild gleicht der chronisch-venösen Insuffizienz. Eine (belastungsabhängige) venöse Claudicatio kann auf eine proximale/zentrale Abflusshinderung hinweisen. Die Beurteilung des PTS-Schweregrades erfolgt mittels des Villalta-Scores (Tab. 3). Der Villalta-Score ist validiert und in den Leitlinien empfohlen (15). Zudem existiert eine patientenberichtete Version (PRV2). Die venöse Claudicatio als ein Schweregrad-relevantes Merkmal wird leider nicht erfasst. Zur Beurteilung eines venösen Refluxes oder einer Obstruktion ist die Duplexsonografie das Mittel der Wahl, wobei sowohl die oberflächlichen als auch die tiefen Beinvenen und Perforansvenen beurteilt werden sollten. Bei einer Beckenvenenthrombose kann eine CT-Venografie/MR-Venografie die Diagnostik ergänzen – vor allem im Hinblick auf eine mögliche Intervention. Hauptpfeiler der Therapie sind – wie bei der chronisch-venösen Insuffizienz – die Symptomkontrolle, die Ulkusprävention sowie die Verhinderung eines Rezidivs. Die Verwendung von Kompressionsstrümpfen ist symptomorientiert. Der Einsatz von Kompressionsstrümpfen zur Prophylaxe eines PTS nach einer TVT ist nach aktueller Evidenz nicht obligat (9, 16). Bei inadäquater Antikoagulation der zugrundeliegenden TVT hingegen besteht ein erhöhtes Risiko für die Entwicklung eines PTS (17). Eine endovaskuläre Rekanalisation der TVT senkt zwar nicht die Inzidenz für ein PTS, kann aber in ausgewählten Fällen den Schweregrad eines PTS positiv beeinflussen (18).
Lymphödem
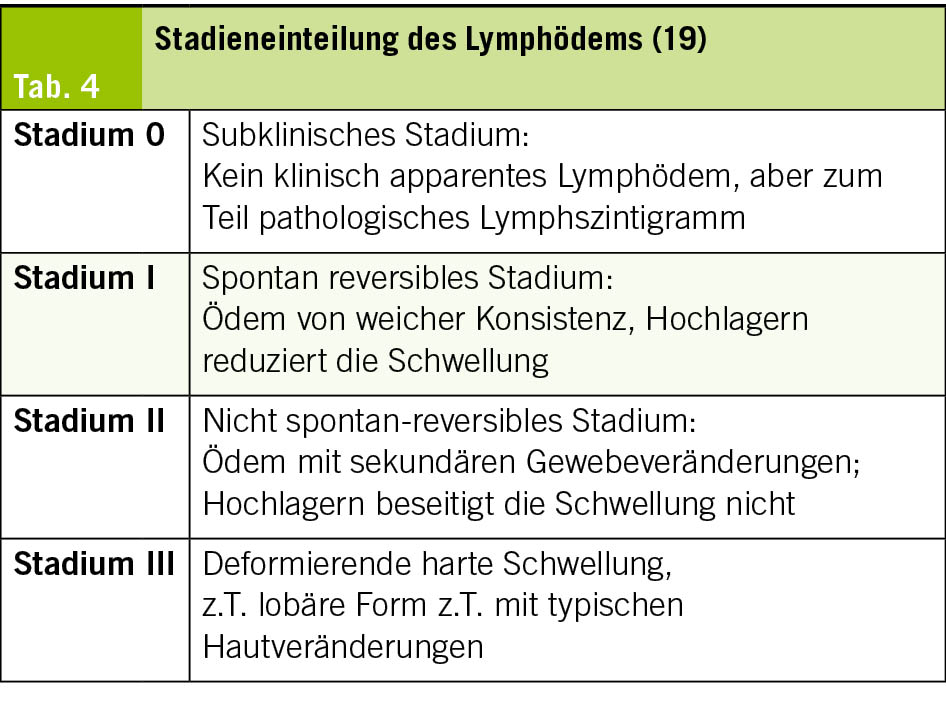
Das Lymphödem ist eine der häufigsten Ursachen chronischer Beinödeme (Tab. 4). Im klinischen Alltag dominiert das sekundäre Lymphödem, welches v.a. nach Operation und Radiatio vorkommt (19). In endemischen Regionen (v.a. Subsahara) ist die Filariose die führende Ursache sekundärer Lymphödeme. Das primäre Lymphödem ist selten und seine Diagnostik bzw. Therapie sollte in Spezialzentren erfolgen. Das weibliche Geschlecht, höheres Alter, Adipositas und wiederholte Operationen sind mit einem höheren Risiko assoziiert. Das Lymphödem kann jedoch auch im Rahmen einer fortgeschrittenen chronisch-venösen Insuffizienz oder immobilitätsbedingt entstehen. Pathophysiologisch liegt eine verminderte Transportkapazität des Lymphsystems in Folge von Fehlbildungen, Funktionsstörungen oder Abflusshinderungen zugrunde, wodurch es zur Zunahme der interstitiellen Flüssigkeit mit – in weiterer Folge – fibrosierenden/sklerosierenden Gewebsumbauten, Schädigung der Hautbarriere, Ulzerationen und rezidivierenden Infekten kommt (20). Typischerweise ist lediglich eine Seite betroffen, oder eine Seite ist deutlicher geschwollen als die Gegenseite. Die Zehen sind – anders als bei venösen Ödemen – mitbetroffen (quaderförmige Schwellung, sog. Kastenzehen sowie ein positives Stemmer-Zeichen) (1). Der zeitliche Verlauf ist langsam progredient. Im initialen Latenzstadium liegt noch keine Schwellung vor. Dann findet sich zunächst eine weiche Schwellung mit eindrückbarer Delle. Bei länger bestehendem Befund kommt es zum fibrotischen Umbau mit Verhärtung. Dann ist das Ödem kaum noch eindrückbar. Im Endstadium stellt sich eine lymphostatische Elephantiasis dar. Per Labordiagnostik und Sonographie sollten zunächst andere Ursachen eines Beinödems ausgeschlossen werden. Rezidivierende Erysipele sind internistische Warnsignale und verschlechtern den klinischen Verlauf eines Lymphödems. Die Tagesfluktuation der Ödemneigung ist – im Gegensatz zur chronisch-venösen Insuffizienz – deutlich geringer ausgeprägt. Unbehandelt drohen bleibende Formveränderungen und erhebliche Lebensqualitätsverluste (21). Die Diagnose eines Lymphödems wird klinisch gestellt und stützt sich auf die Anamnese und den klinischen Befund. Die Duplexsonografie dient dem Nachweis bzw. Ausschluss venöser Abflussstörungen und der Dokumentation eines Phlebo-Lymphödems bei konkomitanter chronisch-venöser Insuffizienz. Eine Lymphszintigrafie kann die Transportstörung objektivieren. Die ICG-Lymphografie erlaubt die Darstellung der Lymphbahnen und den Nachweis von Lymphkollektoren, v.a. im Hinblick auf eine operative Sanierung. Eine standardisierte Einteilung des Lymphödems in Stadien (ISL-Stadium) erleichtert die Verlaufskontrollen und Therapieplanung (19, 21). Hauptpfeiler der Therapie ist wie bei der chronisch-venösen Insuffizienz die Symptomkontrolle, die Hautpflege, die Ulkusprävention sowie die Verhinderung von rezidivierenden Weichteilinfekten. Im Gegensatz zur CVI ist zur Ödemreduktion eine mehrlagige Kompressionsbandagierung in der Initialphase essenziell. Später erfolgt eine Bestrumpfung mittels flachgestrickter Kompressionsstrümpfe der Kompressionsklasse III. Die manuelle Lymphdrainage sowie Bewegungstherapie sind weitere Kernelemente der Therapie des Lymphödems. Eine Kompressionstherapie ist jedoch bei schwerer pAVK, akuter Entzündung, akuter kardialer Dekompensation und malignem Lymphom kontraindiziert. Die komplexe physikalische Entstauungstherapie (KPE) gilt als Goldstandard, wird jedoch in der Schweiz nicht vollumfänglich über die GV übernommen und bedarf in den meisten Fällen einer Zusatzversicherung. In ausgewählten Fällen kommen mikrochirurgische Verfahren (lympho-venöse Anastomosen, vaskularisierter Lymphknoten-Transfer) in spezialisierten Zentren zum Einsatz. Die Evidenz ist jedoch begrenzt und sollte nur bei selektiven Patienten durchgeführt werden (19).
Copyright
Aerzteverlag medinfo AG
Luzerner Kantonsspital, Herzzentrum
Kantonsspital 37
6004 Luzern
KSA Kantonsspital Aarau
Angiologie
Tellstrasse 25
5001 Aarau
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Ödeme können vielfältige Ursachen haben und sowohl physiologisch als auch Symptom einer Erkrankung sein.
- Anamnese, klinische Untersuchung und erste Laboruntersuchungen erlauben bereits in der hausärztlichen Praxis eine ätiologische Eingrenzung.
- Weiterführende Diagnostik sollte bei der entsprechenden Fachrichtung (z. B. Kardiologie, Nephrologie, Angiologie, Gastroenterologie) erfolgen.
1. Herold G. Innere Medizin 2023 eine vorlesungsorientierte Darstellung: unter Berücksichtigung des Gegenstandskataloges für die Ärztliche Prüfung: mit ICD 10-Schlüssel im Text und Stichwortverzeichnis.
Köln: Gerd Herold; 2023.
2. McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599-726.
3. McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023;44(37):3627-39.
4. Nephrotisches Syndrom: AMBOSS SE; 2025 [Available from: https://next.amboss.com/de/article/Mg0MD2?q=nephrotisches%20syndrom.
5. Group KDIGOKCW. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 2024;105(4S):S117-S314.
6. Gerbes AL, Labenz J, Appenrodt B, Dollinger M, Gundling F, Gülberg V, et al. [Updated S2k-Guideline „Complications of liver cirrhosis“. German Society of Gastroenterology (DGVS)]. Z Gastroenterol. 2019;57(5):611-80.
7. Linnemann B, Blank W, Doenst T, Erbel C, Isfort P, Janssens U, et al. Diagnostik und Therapie der tiefen Venenthrombose und Lungenembolie – AWMF-S2k-Leitlinie 2023 [Available from: https:/register.awmf.org/de/leitlinien/detail/065-002.
8. Oncopedia. Prävention und Management der schwangerschaftsassoziierten Thrombose 2025 [Available from: https://www.onkopedia.com/de/onkopedia/guidelines/praevention-und-management-der-schwangerschaftsassoziierten-thrombose/@@guideline/html/index.html.
9. De Maeseneer MG, Kakkos SK, Aherne T, Baekgaard N, Black S, Blomgren L, et al. Editor‘s Choice – European Society for Vascular Surgery (ESVS) 2022 Clinical Practice Guidelines on the Management of Chronic Venous Disease of the Lower Limbs. Eur J Vasc Endovasc Surg. 2022;63(2):184-267.
10. Lurie F, Passman M, Meisner M, Dalsing M, Masuda E, Welch H, et al. The 2020 update of the CEAP classification system and reporting standards. J Vasc Surg Venous Lymphat Disord. 2020;8(3):342-52.
11. Gloviczki P, Lawrence PF, Wasan SM, Meissner MH, Almeida J, Brown KR, et al. The 2023 Society for Vascular Surgery, American Venous Forum, and American Vein and Lymphatic Society clinical practice guidelines for the management of varicose veins of the lower extremities. Part II: Endorsed by the Society of Interventional Radiology and the Society for Vascular Medicine. J Vasc Surg Venous Lymphat Disord. 2024;12(1):101670.
12. Gohel MS, Heatley F, Liu X, Bradbury A, Bulbulia R, Cullum N, et al. A Randomized Trial of Early Endovenous Ablation in Venous Ulceration. N Engl J Med. 2018;378(22):2105-14.
13. Kahn SR, Comerota AJ, Cushman M, Evans NS, Ginsberg JS, Goldenberg NA, et al. The postthrombotic syndrome: evidence-based prevention, diagnosis, and treatment strategies: a scientific statement from the American Heart Association. Circulation. 2014;130(18):1636-61.
14. Prandoni P, Lensing AW, Cogo A, Cuppini S, Villalta S, Carta M, et al. The long-term clinical course of acute deep venous thrombosis. Ann Intern Med. 1996;125(1):1-7.
15. Lattimer CR, Kalodiki E, Azzam M, Geroulakos G. Validation of the Villalta scale in assessing post-thrombotic syndrome using clinical, duplex, and hemodynamic comparators. J Vasc Surg Venous Lymphat Disord. 2014;2(1):8-14.
16. Kahn SR, Galanaud JP, Vedantham S, Ginsberg JS. Guidance for the prevention and treatment of the post-thrombotic syndrome. J Thromb Thrombolysis. 2016;41(1):144-53.
17. van Dongen CJ, Prandoni P, Frulla M, Marchiori A, Prins MH, Hutten BA. Relation between quality of anticoagulant treatment and the development of the postthrombotic syndrome. J Thromb Haemost. 2005;3(5):939-42.
18. Vedantham S, Goldhaber SZ, Julian JA, Kahn SR, Jaff MR, Cohen DJ, et al. Pharmacomechanical Catheter-Directed Thrombolysis for Deep-Vein Thrombosis. N Engl J Med. 2017;377(23):2240-52.
19. AWMF. S2k-Leitlinie Diagnostik und Therapie der Lymphödeme 2017 [Available from: https://register.awmf.org/de/leitlinien/detail/058-001.
20. Nurlaila I, Roh K, Yeom CH, Kang H, Lee S. Acquired lymphedema: Molecular contributors and future directions for developing intervention strategies. Front Pharmacol. 2022;13:873650.
21. The Diagnosis and Treatment of Peripheral Lymphedema: 2023 Consensus Document of The International Society of Lymphology. Lymphology. 2023;56(4):133-51.
der informierte @rzt
- Vol. 16
- Ausgabe 3
- März 2026