- DOKO Basel: Diabetes mellitus – und nun?
Die Behandlung des Typ-2-Diabetes wird zunehmend individueller: Neben dem HbA1c rücken Komorbiditäten, Gewichtsverlauf, kardiorenale Risiken, Nebenwirkungen und auch psychosoziale Aspekte wie die Angst vor Hypoglykämien stärker in den Fokus. An der Donnerstagskonferenz (DOKO) der Klinik für Innere Medizin am Universitätsspital Basel zeigte PD Dr. med. Eleonora Selig anhand mehrerer Fallvignetten, wie sich moderne Diabetestherapien heute differenziert und praxisnah einsetzen lassen.
Fallvignette 1

Zu Beginn präsentierte die Referentin einen Fall aus ihrer eigenen Sprechstunde: ein 43-jähriger Patient mit Typ-2-Diabetes, Erstdiagnose vor zwei Jahren, Übergewicht (BMI 28 kg/m²) und Hypercholesterinämie. Er erhielt Metformin 1000 mg 1-0-1 und Atorvastatin 20 mg 0-0-1. Aktuell lag der HbA1c-Wert bei 7.2 %.
Therapieziele beim Diabetes mellitus
Aus der UKPDS-Studie lässt sich als allgemeines Therapieziel ein HbA1c-Wert von <7 % ableiten. Bei jüngeren Patienten ohne relevante Komorbiditäten sollten Werte unter 6.5 % angestrebt werden, bei älteren multimorbiden Patienten sind Werte <8.0 % meist angemessener. Zudem sollte die Zeit im Zielbereich mehr als 70 % betragen, ohne dass Hypoglykämien auftreten.
Zu den Fallstricken der HbA1c-Bestimmung gehören unter anderem eine verkürzte Erythrozyten-Überlebensdauer, beispielsweise bei Niereninsuffizienz, sowie eine ausgeprägte Glukosevariabilität, die zu irreführenden Werten führen kann.
Dem 43-jährigen Patienten stellte die Referentin einen 73-jährigen Patienten mit Typ-2-Diabetes, kardiovaskulären Risikofaktoren und Niereninsuffizienz gegenüber. Bei diesem Patienten sei ein HbA1c-Wert von 8.0 % oder auch darüber eher angemessen.
Lebensstilintervention und Remission
Als erste therapeutische Massnahme sollte stets eine Änderung der Lebensgewohnheiten empfohlen werden. In der randomisierten kontrollierten DiRECT-Studie führte eine Gewichtsmanagement-Intervention nach zwei Jahren zu einem durchschnittlichen Gewichtsverlust von 7.6 kg; 36 % der Teilnehmer erreichten eine Remission ihres Typ-2-Diabetes. Von den 36 Teilnehmern der Interventionsgruppe, die nach zwei Jahren einen Gewichtsverlust von über 10 kg aufrechterhalten konnten, befanden sich 29 (81 %) in Remission. Auch die verlängerte DiRECT-Intervention war mit einem grösseren aggregierten und absoluten Gewichtsverlust verbunden und deutete auf einen verbesserten Gesundheitszustand über fünf Jahre hin.
Die Ernährungsberatung am Universitätsspital sei sehr kompetent, aufgrund der hohen Auslastung jedoch auf bestimmte Patientengruppen beschränkt, so die Referentin. Dazu gehören Patienten mit Typ-1-Diabetes, pankreopriver Diabetes, Typ-2-Diabetes mit Insulinpumpe oder Basis-Bolus-Therapie und Wunsch nach funktioneller Insulintherapie sowie Patienten nach Transplantation oder mit komplexen internistischen Erkrankungen. In den übrigen Fällen erfolge die Betreuung extern.
Fallvignette 2
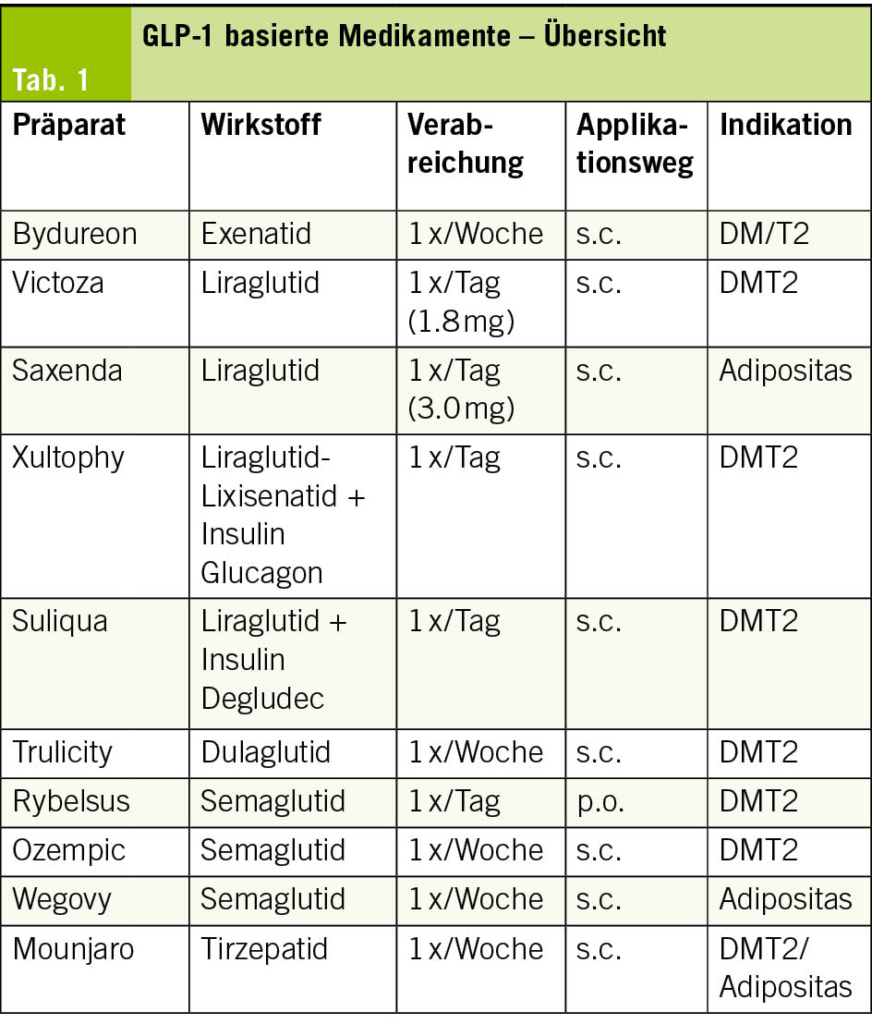
Anschliessend stellte die Referentin eine 53-jährige Patientin mit seit sieben Jahren bestehendem Typ-2-Diabetes vor. Sie litt an arterieller Hypertonie, Adipositas (BMI 33 kg/m²) sowie chronischen Rücken- und Knieschmerzen, jedoch nicht an diabetischen Spätkomplikationen. Die Zuweisung durch den Hausarzt erfolgte bei einem HbA1c-Wert von 10 % unter Janumet® 50/1000 mg 1-0-1. Janumet® wurde abgesetzt und eine Behandlung mit Mounjaro® (GLP-1/GIP-Rezeptoragonist) begonnen.
Die Referentin verwies in diesem Zusammenhang auf die Empfehlungen der Schweizerischen Gesellschaft für Endokrinologie und Diabetologie (SGED), die eine risikoprofilbasierte Therapie empfehlen: Metformin plus SGLT-2-Hemmer bei eGFR >30 ml/min/1.73 m², GLP-1-Rezeptoragonisten bei BMI >28 kg/m² sowie gegebenenfalls DPP-4-Hemmer. Möglich seien auch Kombinationen wie Metformin + GLP-1-RA + SGLT-2-Hemmer, jeweils abhängig von Nierenfunktion, Gewicht und Begleiterkrankungen.
Bei Insulinmangel folgen Basisinsulin oder koformulierte Insuline ein- oder zweimal täglich. Metformin, SGLT-2-Hemmer und GLP-1-RA sollen nach Möglichkeit weitergeführt werden; Sulfonylharnstoffe und DPP-4-Hemmer sollten bei Einsatz eines GLP-1-RA abgesetzt werden.
Kostenübernahme für Mounjaro® bei Typ-2-Diabetes:
• Unzureichend kontrollierter Diabetes mellitus Typ 2 und BMI ≥ 28 kg/m²
• In Monotherapie bei Kontraindikation oder Unverträglichkeit von Metformin.
• In Kombination mit Basalinsulin mit oder ohne Metformin.
• Keine Kombination mit SGLT-2-Hemmern.
• Keine Kombination mit Basis-Bolus
• Umstellung von Ozempic auf Mounjaro möglich, sofern Diabetes nicht kontrolliert ist und BMI ≥ 28 kg/m²
• Rezeptcode für Diabetes: 21977.01.
Wirkung von GLP-1-basierten Medikamenten
GLP-1-basierte Medikamente (Tab. 1) entfalten ihre Wirkung in mehreren Organsystemen. Beschrieben werden unter anderem eine Verbesserung der Insulinsekretion, eine Senkung des HbA1c, Gewichtsverlust, eine Reduktion systemischer Entzündung und der Insulinresistenz sowie günstige Effekte auf Herz, Gefässe, Leber, Niere und obstruktive Schlafapnoe.
Hirn: Substanz-Abusus ↓ , Alzheimer, Parkinson ↓ , Entzündung ↓
Luftwege/Lunge: obstruktive Schlafapnoe ↓
Herz: verbessert HFpEF, Myokardinfarkt ↓
Endokrines Pankreas: Insulin ↑ , Glucagon β, HbA1c ↓
Blutgefässe: Atherosklerose ↓ , Schlaganfall ↓ , periphere arterielle Verschlusskrankheit (PAVK) ↓
Leber: Inflammation ↓ , Fibrose ↓
Niere: chronische Nierenkrankheit
Systemische Effekte: Inflammation ↓ , Insulin-Resistenz ↓ , Gewichtsverlust ↑
Fallvignette 3
Vorgestellt wurde zudem eine 62-jährige Patientin mit Typ-2-Diabetes (Erstdiagnose 2011), Adipositas (BMI 31 kg/m²), diabetischer Retinopathie, Polyneuropathie und Nephropathie. Sie erhielt Metformin und Ozempic®, der HbA1c-Wert lag aktuell bei 8.2 %. Im Raum stand die Frage: Wechsel auf Mounjaro® oder Beginn mit Jardiance®?
GLP-1-RA versus SGLT-2-Hemmer
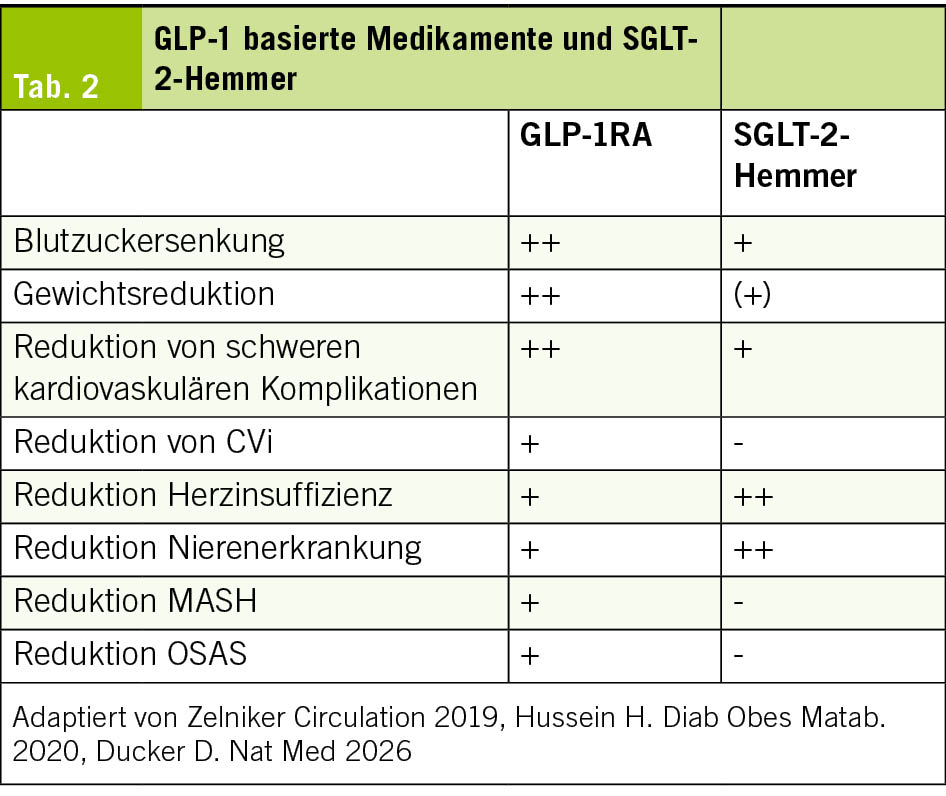
Im Vergleich der Substanzklassen zeigte sich: GLP-1-Rezeptoragonisten senken den Blutzucker und das Gewicht stärker, während SGLT-2-Hemmer Vorteile insbesondere bei Herzinsuffizienz und Nierenerkrankung bieten. Bei schweren kardiovaskulären Ereignissen profitieren Patienten von beiden Klassen, bei Schlaganfällen eher von GLP-1-RA (Tab. 2).
Für die Kombination eines GLP-1-RA mit einem SGLT-2-Hemmer wurden 18 Kohortenstudien mit über 1.1 Millionen Patienten zitiert. Die Kombination reduzierte das Risiko für MACE (RR 0.56), die Gesamt- und kardiovaskuläre Mortalität, Hospitalisationen wegen Herzinsuffizienz sowie renale Endpunkte. Hinweise auf erhöhte Risiken für schwere Hypoglykämien, diabetische Ketoazidosen oder relevante zusätzliche Nebenwirkungen ergaben sich nicht. Die Therapie richte sich nach dem jeweiligen Risikoprofil gemäss SGED-Empfehlungen; das kardiorenal-metabolische Syndrom werde gemäss den ADA Consensus Guidelines 2026 behandelt.
Fallvignette 4
Im nächsten Fall ging es um eine 60-jährige Patientin mit Typ-2-Diabetes, Adipositas (BMI 32 kg/m²) und arterieller Hypertonie. Sie erhielt Metformin und seit neun Wochen neu Ozempic®, zuletzt 1 mg einmal wöchentlich subkutan. Aktuell klagte sie über Bauchschmerzen und Übelkeit. Diskutiert wurden eine Umstellung auf Mounjaro®, eine Umstellung auf Jardiance® oder eine Dosisreduktion von Ozempic® auf 0.5 mg einmal wöchentlich. Zudem müsse eine Pankreatitis ausgeschlossen werden.
Unter GLP-1-RA besteht ein erhöhtes Risiko für Gastroparese (HR 1.59) und Invagination (HR 1.38). Kein erhöhtes Risiko fand sich für akute Pankreatitis, Cholezystitis, Cholezystektomie, biliäre Tumoren, hepatozelluläres Karzinom oder gastrointestinale Karzinome.
Nebenwirkungen von GLP1-Analoga
Zu den häufigen unerwünschten Wirkungen gehören Übelkeit, Durchfall, Obstipation, Erbrechen, akute Nierenschädigung, Gallenblasenerkrankungen, verzögerte Magenentleerung, Aspiration und eine eingeschränkte Darmmotilität. Diskutiert werden ausserdem neuropsychiatrische Ereignisse und Sarkopenie. Weiterhin unklar bleibt der Zusammenhang mit Pankreatitis, Karzinomen, Schilddrüsenkarzinomen und Retinopathie.
Fallvignette 5
Eine weitere Fallbesprechung betraf einen 67-jährigen Patienten, der mit Bauchschmerzen auf die Notfallstation eingeliefert wurde. Zusätzlich bestanden Übelkeit und Erbrechen bei einem Blutzuckerwert von 9 mmol/l. Zunächst wurde er mit Verdacht auf Gastroenteritis entlassen. Am Folgetag stellte er sich erneut vor, nun in deutlich verschlechtertem Zustand mit Erbrechen, Dyspnoe und Verwirrtheit.
In der Anamnese bestanden Typ-2-Diabetes, arterielle Hypertonie und möglicherweise ein Alkoholabusus. Der Patient erhielt Metformin, Jardiance®, Toujeo® 30 E sowie Antihypertensiva. Klinisch zeigte sich ein GCS von 14, Hypotonie, Tachykardie und eine tachypnoische Kussmaul-Atmung bei Afebrilität. Die Laboruntersuchung ergab eine metabolische Ketoazidose unter SGLT-2-Hemmer-Therapie, die auch bei normnahen Blutzuckerwerten auftreten kann. Es wurden die Sick-Day-Rules angewendet.
SGLT2-Hemmer und urogenitale Infektionen
In einer dänischen Kohortenstudie bei Metformin-Anwendern (52 414 unter SGLT-2-Hemmern vs. 27 023 unter GLP-1-RA) mit einem Follow-up von bis zu fünf Jahren zeigte sich unter SGLT-2-Hemmern kein erhöhtes Risiko für Harnwegsinfektionen. Das Risiko für genitale Infektionen war dagegen deutlich erhöht, insbesondere im ersten Jahr (2.0 % vs. 0.7 %; RR 2.95). Im Langzeitverlauf nahm dieses Risiko ab, blieb jedoch weiterhin erhöht (nach fünf Jahren RR 1.64).
Fallvignette 6
Ein weiterer Fall betraf einen 71-jährigen Patienten mit bekanntem Typ-2-Diabetes nach Nierentransplantation. Im Verlauf war es zu Komplikationen in Form eines NSTEMI und einer Pneumonie gekommen.
Blutzuckerentgleisungen im Spital
Hyper- und Hypoglykämien sind im stationären Setting mit einer erhöhten Morbidität und Mortalität assoziiert. Die Vermeidung akuter Stoffwechselentgleisungen verbessert das klinische Outcome, verkürzt die Hospitalisationsdauer und kann Rehospitalisationen reduzieren.
Eine intensive Glukosekontrolle kann bei schwer kranken Patienten gegenüber ausgeprägten Hyperglykämien vorteilhaft sein. Im Vergleich zu moderateren Zielbereichen zeigt sich jedoch kein konsistenter Nutzen; eine zu strenge Blutzuckereinstellung kann vielmehr mit einer erhöhten Mortalität einhergehen. Im klinischen Alltag ist deshalb eine ausgewogene Glukosekontrolle anzustreben, die Hyperglykämien begrenzt und Hypoglykämien vermeidet.
Wie lassen sich Hypoglykämien vermeiden?
Sulfonylharnstoffe und Insulin, insbesondere Mischinsuline, sollten möglichst vermieden werden. Falls eine Basis-Bolus-Therapie notwendig ist, sollte eine kontinuierliche Glukosemessung erfolgen. Das Basalinsulin ist auf den Nüchternblutzucker zu titrieren. Korrekturen mit schnell wirksamem Insulin vor der Bettruhe sollten unterbleiben. Zudem sollte gezielt nach Symptomen gefragt und die Therapie entsprechend angepasst werden. Unter Tresiba® ist das Hypoglykämierisiko geringer als unter Lantus®.
Blutzuckerkontrolle im stationären Bereich
Critically ill:
Bei anhaltender Hyperglykämie (≥10 mmol/l) wird ein Insulinperfusor empfohlen. Die Zielwerte liegen bei 7.8–10.0 mmol/l, gegebenenfalls bei 6.1–7.8 mmol/l, etwa bei Patienten nach herzchirurgischen Eingriffen. Für den 71-jährigen Patienten wurden Zielwerte von 5.8–10.9 mmol/l genannt. Empfohlen wurden zudem eine Anmeldung zur Diabetesberatung und ein Konsil der Endokrinologie.
Non-critically ill:
Bei anhaltender Hyperglykämie (≥10 mmol/l) sollte eine Insulintherapie erwogen werden. Die Zielwerte liegen bei 5.6–10.0 mmol/l; Hypoglykämien sind konsequent zu vermeiden.
Fallvignette 7
Vorgestellt wurde ausserdem eine 37-jährige Patientin mit Typ-2-Diabetes und unzureichender Blutzuckerkontrolle unter Metformin, Ozempic®, Tresiba® 60 E/Tag sowie NovoRapid® etwa 40 E pro Mahlzeit.
Die Zeit in den Zielbereichen zeigte eine ausgeprägte Hyperglykämiebelastung: 29 % der Werte lagen im sehr hohen Bereich (>13.9 mmol/l), 43 % im hohen Bereich (10.1–13.9 mmol/l) und nur 28 % im Zielbereich (3.9–10.0 mmol/l). Hypoglykämien traten nicht auf.
Diskutiert wurden mögliche sekundäre Ursachen sowie praktische Fragen zur Insulinapplikation: Wurde das Insulin korrekt appliziert? Erfolgte ein regelmässiger Wechsel der Pennadeln? Lagen Lipodystrophien vor? Und wurde das Insulin überhaupt gespritzt?
Es zeigte sich, dass Toujeo® in den letzten Wochen nicht appliziert worden war. Als Gründe wurden brennende Schmerzen nach Injektion von 60 E Tresiba® FlexTouch® 100 E/ml sowie die Angst vor Hypoglykämien und entsprechenden Symptomen bereits bei Werten um 6 mmol/l genannt. Als mögliche Alternativen wurden ein Wechsel auf Tresiba® 200 E/ml oder Toujeo® SoloStar® 300 E/ml diskutiert.
Hypoglykämiewahrnehmung und Hypoglykämieangst
Beim gesunden Menschen setzt die Gegenregulation bei einem Blutzuckerwert von etwa 4 mmol/l ein. Nach chronischen Hypoglykämien erfolgt die Reaktion oft erst bei tieferen Werten, bei chronischen Hyperglykämien dagegen bereits bei höheren Werten.
Die Hypoglykämieangst wurde anhand einer Untersuchung bei 385 Patienten mit Typ-2-Diabetes thematisiert. Besonders häufig genannt wurden die Sorge, eine Hypoglykämie nicht zu erkennen, keine Nahrung zur Verfügung zu haben, eine hypoglykämische Episode allein zu erleben, sich benommen oder schwindlig zu fühlen oder in der Öffentlichkeit ohnmächtig zu werden. Ebenfalls relevant waren Ängste vor dauerhaften Gesundheitsschäden, Fehlern oder Unfällen, fehlender Hilfe während einer Hypoglykämie, Konzentrationsstörungen sowie sozialer Blamage.
riesen@medinfo-verlag.ch
- individuelle HbA1c-Ziele
- CGM verbessert Diagnostik und Therapie
- Lebensstilinterventionen können eine Remission ermöglichen
- GLP-1-basierte Medikamente und SGLT2-Inhibitoren nach Komorbiditäten auswählen
- unter GLP-1-basierten Medikamenten vor allem gastrointestinale Nebenwirkungen beachten
- unter SGLT2-Inhibitoren an die seltene euglykämische Ketoazidose denken
- stationäre Hyper- und Hypoglykämieentgleisungen vermeiden
- Hypoglykämieangst aktiv ansprechen
der informierte @rzt
- Vol. 16
- Ausgabe 3
- März 2026