- Immuntherapie bei Krebs
Immunkontrollpunkt-Inhibitoren haben die Behandlung vieler Krebsarten revolutioniert. Diese Immuntherapie ermöglicht bei bestimmten Patienten mit fortgeschrittenem Krebs eine potenzielle langfristige Kontrolle oder sogar Heilung. Trotz der bemerkenswerten Fortschritte profitieren jedoch nur etwa 20 % der Patienten mit fortgeschrittener Erkrankung davon, und langfristig sind es sogar noch weniger. Die manchmal spät auftretenden und potenziell schwerwiegenden Nebenwirkungen erfordern Wachsamkeit und eine schnelle Behandlung in einem Fachzentrum. Eine der grössten Herausforderungen besteht darin, resistente Tumore für die Immuntherapie empfindlicher zu machen. Die Optimierung der Anwendung – in Bezug auf Dosierung, Dauer usw. – ist ein weiteres wichtiges Ziel.
Immune checkpoint inhibitors have transformed the management of many cancers. Immunotherapy can lead to prolonged disease control, and even cure, in some patients with advanced cancer. However, despite these notable advances, only about 20 % benefit from immunotherapy in the advanced setting, and even fewer in the long term. Adverse events, sometimes occurring late and potentially severe, require close monitoring and rapid management in expert centers. Among future challenges is the need to make resistant tumors more sensitive to immunotherapy. Optimizing its use – in terms of dose, duration, etc. – is another important goal.
Keywords: Immune checkpoint inhibitors; anti-tumoral immunity; oncology; PD1; CTLA-4
Einleitung
Obwohl der Begriff Immuntherapie verschiedene Ansätze umfasst, bezieht er sich meist auf Immun-Checkpoint-Inhibitoren, die wir hier beschreiben werden. Diese Immun-Checkpoint-Inhibitoren sind sicherlich der wichtigste Fortschritt in der Onkologie der letzten zwei Jahrzehnte. Bei bestimmten Patienten – beispielsweise bei Lungenkrebs oder Melanomen – hat sie dazu beigetragen, dass ehemals unheilbare metastasierende Erkrankungen langfristig kontrolliert werden können und manchmal sogar von einer Heilung gesprochen werden kann, selbst in ursprünglich extrem fortgeschrittenen Stadien. Diese günstigen Situationen gehören zwar mittlerweile zur täglichen Praxis, sind jedoch auf eine begrenzte Anzahl von Tumorarten beschränkt. Bei fortgeschrittener Erkrankung profitiert nur eine Minderheit der Patienten tatsächlich von der Immuntherapie. Darüber hinaus dürfen die Nebenwirkungen, die durch immunvermittelte Mechanismen praktisch jedes Organ betreffen können, nicht unterschätzt werden. Es ist für den Arzt von entscheidender Bedeutung, diese zu erkennen und zu behandeln. In dieser Arbeit gehen wir auf die biologischen Grundlagen, die klinischen Daten zur Wirksamkeit und Verträglichkeit der Immuntherapie sowie die für die Zukunft der Immuntherapie in Betracht gezogenen Richtungen ein.
Biologische Grundlagen
Jeder Mensch verfügt über eine natürliche Anti-Tumor-Immunität, deren Ziel es ist, abnormale Zellen zu eliminieren. Diese Immunität wird fein reguliert, damit sie weder übermässig noch unzureichend ist, insbesondere dank sogenannter Immun-Checkpoints. Es hat sich gezeigt, dass diese Kontrollpunkte von Krebszellen umgangen werden können, um sich der Immunüberwachung zu entziehen (1).
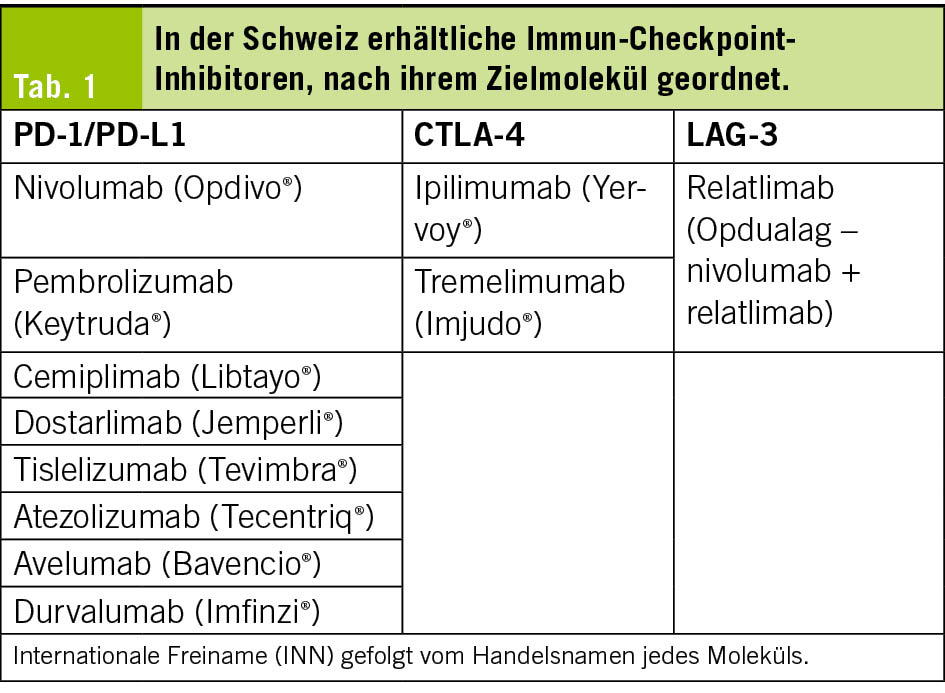
Unter diesen Kontrollpunkten haben vor allem die Interaktion zwischen PD-1 und PD-L1 sowie die zwischen CTLA-4 und Antigen-präsentierenden Zellen die Onkologie revolutioniert (2). Andere Kontrollpunkte wie LAG-3, TIGIT oder TIM-3 sind Gegenstand jüngster Entwicklungen, werden jedoch in diesem Manuskript nicht behandelt (3). Tab. 1 beschreibt die Namen der Moleküle und ihre Zielstrukturen, die in der Schweiz verfügbar sind.
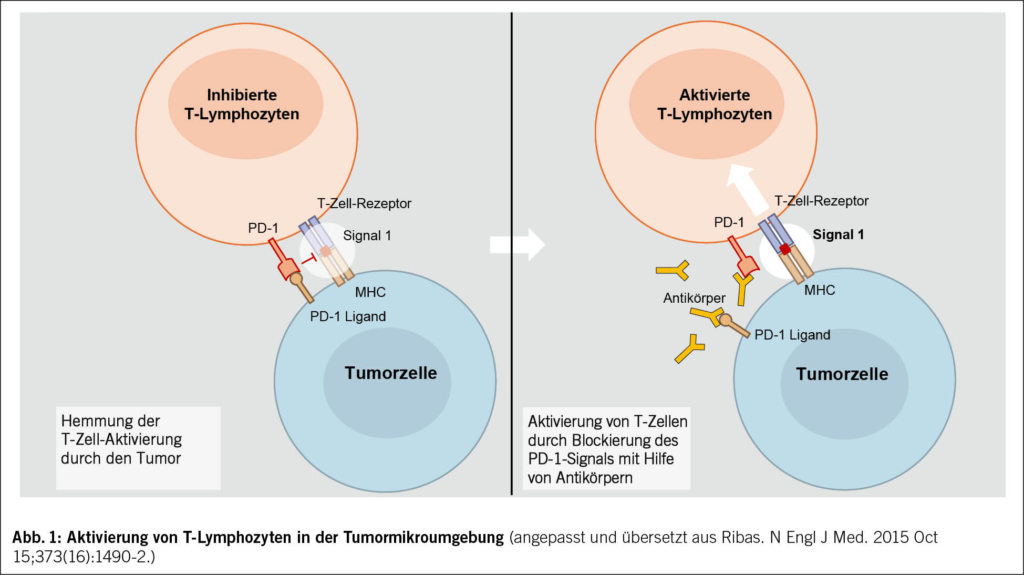
Nehmen wir das Beispiel der Interaktion zwischen PD-1, das auf der Oberfläche von T-Lymphozyten exprimiert wird, und PD-L1, das von Tumorzellen exprimiert wird: Diese Interaktion hemmt die Lymphozyten und verhindert, dass sie ihre zytotoxische Anti-Tumor-Wirkung entfalten. Der Krebs kann sich so, insbesondere durch eine Überexpression von PD-L1, der Immunantwort entziehen und weiter wachsen. Dieser Mechanismus ist in Abb. 1 dargestellt.
Genau an dieser Stelle setzt die Immuntherapie an: Monoklonale Antikörper (monoclonal antibodies – «mab») blockieren diese Interaktion und stellen so die Fähigkeit der T-Lymphozyten wieder her, Krebszellen zu erkennen und zu zerstören. Die Immuntherapie wirkt also nicht direkt gegen den Tumor, sondern indirekt, indem sie die Hemmnisse für die Immunantwort aufhebt (Immun-Checkpoint-Inhibitoren).
Daten zu metastasierten Erkrankungen
Eine umfassende Übersicht über die Daten zur Immuntherapie der letzten zwanzig Jahre würde den Rahmen dieser Arbeit sprengen. Es gibt jedoch eindrucksvolle Beispiele, die das Potenzial dieses neuen Therapieansatzes veranschaulichen.
Das Melanom war früher mit einer sehr schlechten Prognose verbunden, mit einer Lebenserwartung von nur wenigen Monaten in vielen metastasierten Fällen. In diesem Zusammenhang war die Immuntherapie am revolutionärsten. Mittlerweile liegen die 10-Jahres-Ergebnisse der CheckMate 067-Studie vor, in der eine Kombination aus Immuntherapie (Anti-CTLA-4 und Anti-PD-1), Anti-PD-1 allein und Anti-CTLA-4 allein als Erstlinientherapie bei Patienten mit fortgeschrittener oder metastasierter Erkrankung verglichen wurde (4). Bei den Strategien mit Anti-PD-1 (allein oder in Kombination) sind etwa 40 % der Patienten nach 10 Jahren noch am Leben. Bei diesen Patienten kann man wirklich von einer Heilung sprechen.
Auch bei anderen Krebsarten hat die Immuntherapie zu einer radikalen Veränderung der Behandlung geführt.
Beispielsweise wird Lungenkrebs, abgesehen von Sonderfällen, heute bei Metastasen bereits in der Erstlinienbehandlung mit Immuntherapie behandelt, wobei auch hier bei einem Ansprechen des Tumors ein sehr langfristiger Nutzen zu erwarten ist (5, 6, 7).
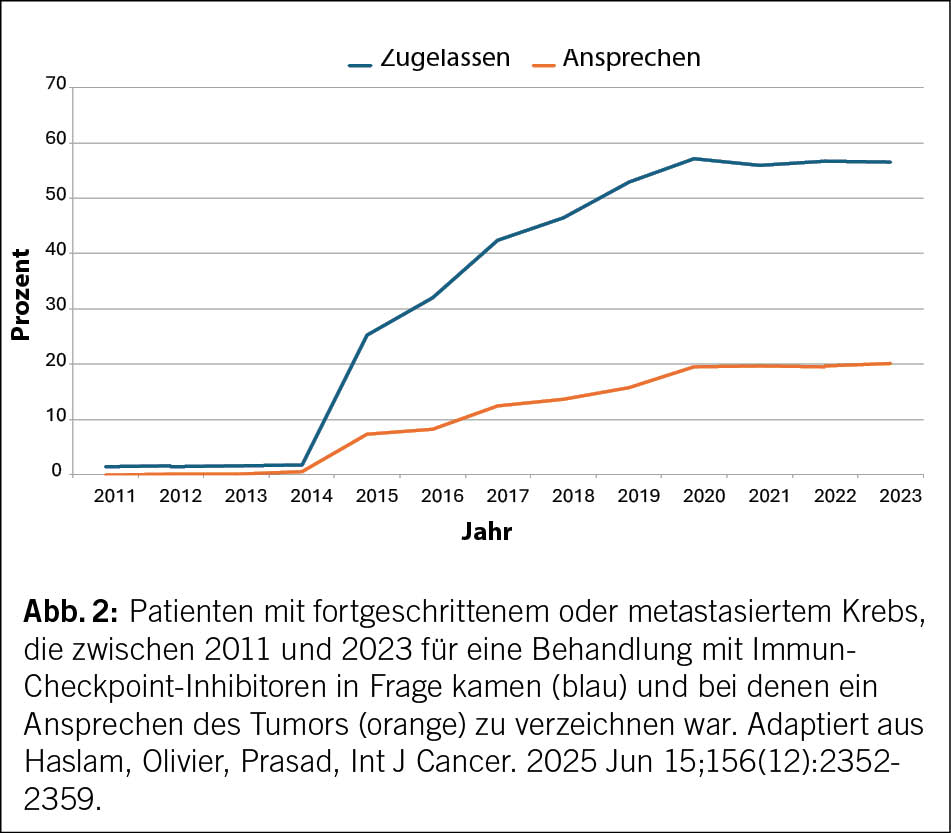
Das Beispiel des Melanoms verdeutlicht aber auch die Grenzen der Immuntherapie: Es handelt sich um eine im Vergleich zu anderen Krebsarten relativ seltene Krebsart im fortgeschrittenen Stadium. Dies erklärt, warum bis heute unter Berücksichtigung der Häufigkeit der einzelnen Krebsarten nur etwa 20 % der Patienten mit fortgeschrittener Erkrankung von einem Ansprechen des Tumors auf die Immuntherapie profitieren (8). Darüber hinaus wird nur ein Bruchteil dieser Patienten einen dauerhaften Nutzen daraus ziehen. Die Entwicklung der Anzahl der Patienten mit fortgeschrittener oder metastasierter Erkrankung, die für die Therapie in Frage kommen, d. h. bei denen eine Indikation für die Therapie vorliegt, und derjenigen, die auf die Therapie ansprechen, ist in Abb. 2 dargestellt. Mit anderen Worten: Obwohl die Immuntherapie für bestimmte Patienten eine Revolution darstellt, kommt sie bisher nur einer Minderheit der Patienten mit fortgeschrittener Erkrankung zugute.
In neoadjuvanter und adjuvanter Situation
Nach den beeindruckenden Ergebnissen, die in bestimmten Situationen bei fortgeschrittener Erkrankung beobachtet wurden, war es logisch, die Auswirkungen der Immuntherapie in früheren Stadien zu untersuchen, insbesondere in neoadjuvanter (vor der Operation) und/oder adjuvanter (nach der Operation) Situation (9, 10).
Bei Lungenkrebs beispielsweise hat eine beträchtliche Anzahl von Phase-3-Studien einen Vorteil hinsichtlich des krankheitsfreien Überlebens gezeigt, und mehrere davon haben auch einen Vorteil hinsichtlich des Gesamtüberlebens aufgezeigt, der mit der Ergänzung der konventionellen perioperativen Chemotherapie durch eine Immuntherapie zusammenhängt (11, 12, 13). Heute kann die Immuntherapie bei vielen Tumorarten perioperativ angeboten werden.
Allerdings sind gewisse Nuancen zu berücksichtigen: Tatsächlich wurden mehrere Studien durchgeführt, die den frühzeitigen Einsatz der Immuntherapie unterstützen, darunter auch in einigen Ländern mit begrenzten Ressourcen. In diesen Ländern hatten die Patienten der Kontrollgruppe, bei denen ein Rezidiv auftrat, nach der klinischen Studie keinen optimalen Zugang zu Behandlungen (10). In diesen Fällen ist es schwierig zu sagen, ob der beobachtete Überlebensvorteil tatsächlich auf die frühzeitige Verabreichung der Immuntherapie zurückzuführen ist oder ob er das Ergebnis einer suboptimalen Behandlung in der Kontrollgruppe zum Zeitpunkt des Rückfalls ist. Ein weiterer wichtiger Punkt betrifft die Toxizität, die in einer Situation, in der die Patienten möglicherweise bereits von ihrer Krankheit geheilt sind, im Rahmen einer echten gemeinsamen medizinischen Entscheidung noch sorgfältiger bewertet werden muss.
Toxizität und Lebensqualität: Erkennen und nicht herunterspielen
Die potenziellen Toxizitäten der Immuntherapie dürfen nicht unterschätzt werden. Obwohl sie nur in wenigen Fällen schwerwiegend sind und oft medizinisch kontrolliert werden können, können bestimmte Toxizitäten zu langfristigen Schäden (14) mit potenziellen Auswirkungen auf die Lebensqualität (15) oder sogar zu tödlichen Nebenwirkungen (16) führen.
Für den Arzt lauten die wichtigsten Botschaften wie folgt:
1. Immuninduzierte Toxizitäten sind Organschäden, die andere Erkrankungen imitieren können, was ihre Diagnose manchmal schwierig macht. Beispielsweise kann eine immunvermittelte Pneumonitis wie eine infektiöse Lungenentzündung erscheinen. Am häufigsten sind die endokrinen Drüsen (Thyreoiditis), die Lunge (Pneumonitis), der Dickdarm (Colitis), die Leber (Hepatitis), die Haut sowie eine ausgeprägte Asthenie betroffen.Seltenere, aber schwerwiegendere Beeinträchtigungen wie Herzmuskelentzündungen oder neurologische Beeinträchtigungen können ebenfalls auftreten (17).
2. Im Gegensatz zur Chemotherapie können die Nebenwirkungen der Immuntherapie erst spät auftreten, mehrere Wochen oder sogar Monate nach Beginn oder sogar nach Beendigung der Behandlung (18).
3. Eine schnell eingeleitete hochdosierte Kortikosteroidtherapie bildet die Grundlage der Erstbehandlung und zielt darauf ab, eine übermässige Immunreaktion zu bremsen. Bei Resistenz können andere Immunsuppressiva erforderlich sein, wie Anti-IL6, Anti-TNF-alpha oder andere Moleküle (19) (20).
4. Die optimale Behandlung dieser Toxizitäten erfordert spezielle Fachkenntnisse. Die frühzeitige Einbeziehung des behandelnden Onkologen ist unerlässlich, um Verzögerungen bei der Diagnose oder Behandlung zu vermeiden.
Zusammenfassend lässt sich sagen, dass die Immuntherapie zwar im Allgemeinen gut verträglich ist, aber schwerwiegende Nebenwirkungen hervorrufen kann. Ihre schnelle Erkennung, ihre Behandlung in einem Fachzentrum und eine klare Information des Patienten und seines Umfelds sind Schlüsselelemente, um die Sicherheit und Wirksamkeit der Behandlung zu gewährleisten.
Herausforderungen für die Zukunft
In Bezug auf die Wirksamkeit bleibt eine zentrale Frage offen: Ist es möglich, dass die Immuntherapie nicht mehr nur einer Minderheit, sondern einer Mehrheit der Patienten zugute kommt? Derzeit werden verschiedene Strategien untersucht, um dieses Ziel zu erreichen, insbesondere durch die gezielte Beeinflussung anderer Immun-Kontrollpunkte oder durch den Versuch, sogenannte «kalte» Krebsarten (die gegen die Immuntherapie resistent sind) in «heisse», d. h. empfindlichere Krebsarten umzuwandeln.
Gleichzeitig besteht eine weitere grosse Herausforderung darin, bereits zugelassene Behandlungen mit einem patientenzentrierten Ansatz zu optimieren (21). Zum Beispiel:
– Sind die derzeit verwendeten Dosierungen wirklich optimal? Einige Studien deuten darauf hin, dass mit deutlich niedrigeren Dosierungen eine vergleichbare Wirksamkeit erzielt werden könnte (22).
– Spielt der Zeitpunkt der Verabreichung eine Rolle? Mehrere vorläufige Daten deuten darauf hin, dass die Verabreichung am Morgen wirksamer sein könnte als am Nachmittag, aber diese Hypothese muss durch strenge randomisierte Studien validiert werden (23).
– Ist die Behandlungsdauer gerechtfertigt? Viele Protokolle sehen eine Immuntherapie über einen Zeitraum von ein bis zwei Jahren vor. Eine Bewertung, ob kürzere Behandlungsdauern eine gleichwertige Wirksamkeit bieten können, würde es ermöglichen, die Toxizität zu begrenzen und gleichzeitig die Kosten für die Gesellschaft erheblich zu senken (24).
Fazit
Immun-Checkpoint-Inhibitoren haben eine echte Revolution in der Onkologie ausgelöst und ermöglichen einigen Patienten eine dauerhafte Kontrolle der Krankheit oder sogar eine Heilung, während ihre Prognose ohne diese Behandlung schnell tödlich gewesen wäre. Dennoch betrifft dies immer noch nur eine Minderheit der Patienten mit fortgeschrittener Erkrankung. Es bleibt eine grosse Herausforderung, zu verstehen, wie der Nutzen der Immuntherapie auf eine grössere Anzahl von Patienten ausgeweitet werden kann. Toxizitäten, also immunvermittelte Organschäden, die mehrere Wochen oder sogar Monate nach Beginn der Behandlung auftreten können, müssen frühzeitig erkannt und unverzüglich behandelt werden (die Kortikosteroidtherapie ist die Behandlung der ersten Wahl), wobei der Onkologe schnell hinzugezogen werden muss. In neoadjuvanten oder adjuvanten Situationen müssen diese Toxizitäten sowie bestimmte methodische Verzerrungen, die manchmal in klinischen Studien auftreten, im Rahmen einer optimalen gemeinsamen medizinischen Entscheidung umfassend berücksichtigt werden.
Copyright
Aerzteverlag medinfo AG
Service d’oncologie
Hôpitaux Universitaires Genève
Rue Gabrielle-Perret-Gentil 4
1205 Genf
Service d’oncologie
Hôpitaux Universitaires Genève
Rue Gabrielle-Perret-Gentil 4
1205 Genf
Timothée Olivier hat keine Interessenkonflikte anzugeben. Alfredo Addeo: Beratungs- oder Gutachtertätigkeit: BMS, Astrazeneca, Boehringer-Ingelheim, Roche, MSD, Pfizer, Eli Lilly, Astellas. Referent: Eli Lilly, Astrazeneca, Regeneron.
- Die Immuntherapie ermöglicht bei bestimmten Krebsarten, einschliesslich in sehr fortgeschrittenen oder metastasierten Stadien, eine dauerhafte Kontrolle oder sogar Heilung – dies ist jedoch auf eine Minderheit der Patienten beschränkt
- Immunvermittelte Nebenwirkungen können spät auftreten und verschiedene Organe betreffen; sie müssen schnell identifiziert und in einem Fachzentrum behandelt werden, wobei eine Kortikosteroidtherapie die erste Wahl ist.
- In neoadjuvanten oder adjuvanten Situationen wird die Immuntherapie zunehmend angeboten, erfordert jedoch eine strenge Bewertung des Nutzen-Risiko-Verhältnisses im Rahmen einer echten gemeinsamen medizinischen Entscheidung.
- Um den Nutzen auf mehr Patienten auszuweiten, werden Möglichkeiten untersucht, resistente Tumoren in Krankheiten umzuwandeln, die empfindlicher auf eine Immuntherapie ansprechen.
- Die Optimierung der Dosis, der Verabreichungsdauer und anderer Faktoren im Zusammenhang mit der bereits angewendeten Immuntherapie könnte möglicherweise deren Toxizität und Kosten reduzieren.
1. Chen DS, Mellman I. Oncology meets immunology: the cancer-immunity cycle. Immunity. 2013 Jul 25;39(1):1–10.
2. Ribas Antoni. Releasing the Brakes on Cancer Immunotherapy. New England Journal of Medicine. 2015;373(16):1490–2.
3. Borgeaud M, Sandoval J, Obeid M, Banna G, Michielin O, Addeo A, et al. Novel targets for immune-checkpoint inhibition in cancer. Cancer Treatment Reviews [Internet]. 2023 Nov 1 [cited 2025 Jun 22];120. Available from: https://www.cancertreatmentreviews.com/article/S0305-7372(23)00107-X/fulltext
4. Wolchok JD, Chiarion-Sileni V, Rutkowski P, Cowey CL, Schadendorf D, Wagstaff J, et al. Final, 10-Year Outcomes with Nivolumab plus Ipilimumab in Advanced Melanoma. New England Journal of Medicine. 2025 Jan 1;392(1):11–22.
5. Garassino MC, Gadgeel S, Speranza G, Felip E, Esteban E, Dómine M, et al. Pembrolizumab Plus Pemetrexed and Platinum in Nonsquamous Non–Small-Cell Lung Cancer: 5-Year Outcomes From the Phase 3 KEYNOTE-189 Study. JCO. 2023 Apr 10;41(11):1992–8.
6. Novello S, Kowalski DM, Luft A, Gümüs M, Vicente D, Mazières J, et al. Pembrolizumab Plus Chemotherapy in Squamous Non–Small-Cell Lung Cancer: 5-Year Update of the Phase III KEYNOTE-407 Study. JCO. 2023 Apr 10;41(11):1999–2006.
7. Desai A, Peters S. Immunotherapy-based combinations in metastatic NSCLC. Cancer Treat Rev. 2023 May;116:102545.
8. Haslam A, Olivier T, Prasad V. How many people in the US are eligible for and respond to checkpoint inhibitors: An empirical analysis. Int J Cancer. 2025 Jun 15;156(12):2352–9.
9. Boydell E, Sandoval JL, Michielin O, Obeid M, Addeo A, Friedlaender A. Neoadjuvant Immunotherapy: A Promising New Standard of Care. Int J Mol Sci. 2023 Jul 24;24(14):11849.
10. Olivier T, Haslam A, Prasad V. Postrecurrence Treatment in Neoadjuvant or Adjuvant FDA Registration Trials: A Systematic Review. JAMA Oncology [Internet]. 2024 Jun 20 [cited 2024 Aug 15]; Available from: https://doi.org/10.1001/jamaoncol.2024.1569
11. Han Y, Xiao X, Qin T, Yao S, Liu X, Feng Y, et al. Efficacy and safety of perioperative immunotherapy combinations for resectable non-small cell lung cancer: a systematic review and network meta-analysis. Cancer Immunol Immunother. 2024 Oct 9;73(12):262.
12. Spicer JD, Garassino MC, Wakelee H, Liberman M, Kato T, Tsuboi M, et al. Neoadjuvant pembrolizumab plus chemotherapy followed by adjuvant pembrolizumab compared with neoadjuvant chemotherapy alone in patients with early-stage non-small-cell lung cancer (KEYNOTE-671): a randomised, double-blind, placebo-controlled, phase 3 trial. The Lancet. 2024 Sep 28;404(10459):1240–52.
13. Forde PM, Spicer JD, Provencio M, Mitsudomi T, Awad MM, Wang C, et al. Overall Survival with Neoadjuvant Nivolumab plus Chemotherapy in Lung Cancer. New England Journal of Medicine [Internet]. [cited 2025 Jun 22];0(0). Available from: https://www.nejm.org/doi/full/10.1056/NEJMoa2502931
14. Ghisoni E, Wicky A, Bouchaab H, Imbimbo M, Delyon J, Gautron Moura B, et al. Late-onset and long-lasting immune-related adverse events from immune checkpoint-inhibitors: An overlooked aspect in immunotherapy. European Journal of Cancer. 2021 May 1;149:153–64.
15. Olivier T, Haslam A, Prasad V. Informative censoring due to missing data in quality of life was inadequately assessed in most oncology randomized controlled trials. Journal of Clinical Epidemiology. 2021 Nov 1;139:80–6.
16. Wang DY, Salem JE, Cohen JV, Chandra S, Menzer C, Ye F, et al. Fatal Toxic Effects Associated With Immune Checkpoint Inhibitors: A Systematic Review and Meta-analysis. JAMA Oncol. 2018 Dec 1;4(12):1721–8.
17. Thouvenin L, Olivier T, Banna G, Addeo A, Friedlaender A. Immune checkpoint inhibitor-induced aseptic meningitis and encephalitis: a case-series and narrative review. Therapeutic Advances in Drug Safety. 2021;12:20420986211004745.
18. Postow Michael A., Sidlow Robert, Hellmann Matthew D. Immune-Related Adverse Events Associated with Immune Checkpoint Blockade. New England Journal of Medicine. 2018 Jan 11;378(2):158–68.
19. Martins F, Sykiotis GP, Maillard M, Fraga M, Ribi C, Kuntzer T, et al. New therapeutic perspectives to manage refractory immune checkpoint-related toxicities. Lancet Oncol. 2019 Jan;20(1):e54–64.
20. Haanen J, Obeid M, Spain L, Carbonnel F, Wang Y, Robert C, et al. Management of toxicities from immunotherapy: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology. 2022 Dec 1;33(12):1217–38.
21. Bouche G, Gilbert D, Quartagno M, Dehbi HM, Merrick S, Doorn-Khosrovani SB van W van, et al. Determining the optimal use of approved drugs in oncology. The Lancet Oncology. 2025 May 1;26(5):e282–94.
22. Patil VM, Noronha V, Menon N, Rai R, Bhattacharjee A, Singh A, et al. Low-Dose Immunotherapy in Head and Neck Cancer: A Randomized Study. JCO. 2023 Jan 10;41(2):222–32.
23. Özdemir BC, Bill R, Okyar A, Scheiermann C, Hayoz S, Olivier T. Chrono-immunotherapy as a low-hanging fruit for cancer treatment? A call for pragmatic randomized clinical trials. J Immunother Cancer. 2025 Mar 3;13(3):e010644.
24. Birkmire J, Haslam A, Olivier T, Fernandez E, Prasad V. Why the duration of cancer treatment requires a closer look: An empirical analysis of recent FDA approvals. JCO. 2025 Jun;43(16_suppl):11022–11022.
der informierte @rzt
- Vol. 16
- Ausgabe 1
- Januar 2026