- Mangelernährung und kardiale Kachexie: Eine unterschätzte Herausforderung bei Herzinsuffizienz
Die chronische Herzinsuffizienz stellt eine der häufigsten kardiologischen Erkrankungen dar und ist stark mit ernährungsassoziierten Begleitsyndromen wie krankheitsbedingter Malnutrition, kardialer Kachexie, Sarkopenie oder Gebrechlichkeit (Frailty) assoziiert. Trotz ähnlicher Pathomechanismen müssen diese Syndrome voneinander abgegrenzt und in der Behandlung rechtzeitig erkannt werden. Hierfür ist jedoch eine Sensibilisierung des klinischen tätigen Personals in der stationären und ambulanten Versorgung sowie eine korrekte Diagnosestellung notwendig. Das Ziel sollte eine strukturierte Integration ernährungsmedizinischer Behandlungsabläufe in der Kardiologie sowie eine enge Zusammenarbeit mit der Ernährungstherapie bei Patienten mit chronischer Herzinsuffizienz sein.
Chronic heart failure is one of the most common cardiological diseases and is strongly associated with nutrition-related comorbidities such as disease-related malnutrition, cardiac cachexia, sarcopenia, and frailty. Despite similar pathomechanisms, these syndromes must be distinguished from one another and recognised in good time during treatment. However, this requires raising awareness among clinical staff working in inpatient and outpatient care, as well as accurate diagnosis. The goal should be the structured integration of nutritional treatment procedures in cardiology and close cooperation with nutritional therapy for patients with chronic heart failure.
Keywords: Herzinsuffizienz, Malnutrition, Kachexie, Sarkopenie, Gebrechlichkeit
Die Herzinsuffizienz ist ein klinisches Syndrom, das auf eine strukturelle oder funktionelle Störung des Herzens zurückzuführen ist und mit erhöhten intrakardialen Drücken und/oder einer unzureichenden Herzleistung in Ruhe oder bei Belastung einhergeht (1). Die Prävalenz der Herzinsuffizienz beträgt etwa 1–3 % der Bevölkerung und steigt aufgrund der vermehrten Häufigkeit von kardiovaskulären Erkrankungen altersabhängig auf bis zu 16 % bei über 80-jährigen Personen an (2). Ein unwillkürlicher Gewichtsverlust und Muskelschwund mit möglichen Folgeerkrankungen wie Malnutrition, Kachexie, Sarkopenie oder Gebrechlichkeit (Frailty) treten insbesondere in fortgeschrittenen Krankheitsstadien der Herzinsuffizienz auf (3). Die frühzeitige Erkennung und Therapie dieser miteinander verknüpften, jedoch per Definition voneinander abzugrenzenden medizinischen Syndrome wird in den aktuellen Herzinsuffizienz-Leitlinien der Europäischen Gesellschaft für Kardiologie hervorgehoben und kann den Krankheitsverlauf sowie die Lebensqualität der Patienten wesentlich beeinflussen.
Pathophysiologische Grundlagen
Ein reduzierter Ernährungszustand und ein zunehmender Muskelverlust bei Herzinsuffizienz-Patienten weisen gemeinsame pathophysiologische Merkmale auf (4). Typische Herzinsuffizienz-Symptome wie eine verstärkte Leistungsintoleranz und Atemnot erhöhen den Energieverbrauch im Körper, während die Nährstoffaufnahme durch ein frühzeitiges Sättigungsgefühl, eine vermehrte Nausea sowie eine gastrointestinale Malabsorption aufgrund von intestinalen Ödemen reduziert ist (5). Häufig empfohlene Nahrungsrestriktionen (z. B. salzreduzierte Kost) und eine Polypharmazie können einen Appetitverlust verstärken. Neurohormonelle Anpassungen und systemische Entzündungsreaktionen, die im Rahmen einer chronischen Herzinsuffizienz im fortgeschrittenen Krankheitsverlauf auftreten, führen zudem zu einem Ungleichgewicht zwischen anabolen und katabolen Stoffwechselprozessen (6). Insbesondere bei Patienten mit fortgeschrittener Herzinsuffizienz und einer «kardialen Kachexie» lassen sich erhöhte inflammatorische Marker und Hormonveränderungen (u.a. CRP, TNF-α, IL-6, Ghrelin, GH/IGF1) nachweisen, die wiederum mit verstärkten katabolen Stoffwechselprozessen, oxidativem Stress und einer vermehrten Proteolyse assoziiert sind (7). Zusammen mit einer reduzierten körperlichen Aktivität und Insulinresistenz können diese Prozesse zusätzlich eine «anabole Resistenz» in der Muskulatur bewirken, durch die eine Muskelproteinsynthese gehemmt und der Muskelabbau verstärkt wird (8).
Häufig vorhandene chronische Begleiterkrankungen (z. B. Diabetes mellitus, Niereninsuffizienz oder COPD) sowie psychosoziale Aspekte (z. B. kognitive Defizite, Depression, soziale Isolation) sind weitere Risikofaktoren für das Auftreten einer Mangelernährung und erhöhen die Vulnerabilität der Patienten. Die Kombination dieser im chronischen Krankheitsprozess häufig auftretenden Faktoren, allen voran der erhöhte Energiebedarf bei gleichzeitig reduzierter Nährstoff- und Proteinaufnahme, die Zunahme kataboler Stoffwechselprozesse sowie die körperliche Inaktivität, führt bei Patienten mit Herzinsuffizienz schliesslich zu einem erhöhten Risiko für die Entwicklung einer krankheitsbedingten Malnutrition, kardialen Kachexie, Sarkopenie und Gebrechlichkeit (4).
Krankheitsbedingte Malnutrition
Eine Mangelernährung (Malnutrition) ist definiert als ein Zustand, der aus einer unzureichenden Zufuhr oder Aufnahme von Energie und Nährstoffen resultiert und mit einer Beeinträchtigung der körperlichen und mentalen Funktionen einhergeht (9). Neben altersbedingten und sozioökonomischen Ursachen ist in unserer Gesellschaft vorwiegend eine «krankheitsbedingte Malnutrition» mit oder ohne Inflammation von Bedeutung. Die Prävalenz der krankheitsbedingten Mangelernährung bei älteren Personen wird abhängig von den verwendeten Assessment-Tools in der Gesamtbevölkerung auf etwa 5 % und bei hospitalisierten Patienten zwischen 20–50 % geschätzt (10). Bei Patienten mit einer Herzinsuffizienz lässt sich ebenfalls bei über 40 % der Patienten eine Mangelernährung feststellen (11). Dabei konnte in mehreren Studien gezeigt werden, dass ein reduzierter Ernährungszustand mit signifikant erhöhten Morbiditäts- und Mortalitätsraten sowie einer reduzierten Lebensqualität der Patienten einhergeht (12, 13, 14). Hingegen gibt es in den letzten Jahren zunehmende Evidenz, dass die Malnutrition auch ein modifizierbarer Risikofaktor ist. In der 2019 veröffentlichten EFFORT-Studie wurde bestätigt, dass bei Patienten mit einem erhöhten Risiko für eine Mangelernährung das Komplikationsrisiko und die 30-Tage-Mortalität durch eine individualisierte Ernährungstherapie signifikant reduziert werden konnte (15). Auch bei Patienten mit akuter Herzinsuffizienz ergab sich durch eine Ernährungsintervention während und nach einem Krankenhausaufenthalt ein prognostischer Benefit (16). Zusätzlich zeigten sich durch eine Ernährungstherapie bei Risikopatienten eine niedrigere Wahrscheinlichkeit für kardiale Ereignisse, kürzere Krankenhausaufenthalte sowie eine geringere Rate an Rehospitalisierungen (17, 18, 19). Letzteres kann insbesondere bei Patienten mit chronischer Herzinsuffizienz gravierenden Einfluss auf deren gesundheitsbezogene Lebensqualität haben.
Screening und Diagnosestellung
Zur Erkennung einer möglichen Mangelernährung wird im ersten Schritt ein systematisches Screening empfohlen (20). Zu diesem Zweck sind in den letzten Jahrzehnten zahlreiche Instrumente entstanden, die neben quantifizierbaren Parametern (z. B. Gewicht, Grösse, BMI, ungewollter Gewichtsverlust) teils auch psychosoziale Risiken für eine Mangelernährung (z. B. psychische Belastungen, Mobilität im Alltag) erfassen. Zwar müssen bei allen Instrumenten die eingeschränkte Aussagekraft und Validität berücksichtigt werden, allerdings können mit denen von der ESPEN (European Society for Clinical Nutrition and Metabolism) empfohlenen Screening-Instrumenten wie MUST («Malnutrition Universal Screening Tool», vorwiegend bei nicht-hospitalisierten Patienten), MNA bzw. MNA-SF («Mini Nutritional Assessment – Short Form», vorwiegend bei älteren Personen ab 65 Jahren) oder NRS-2002 («Nutrition Risk Screening 2002», vorwiegend bei hospitalisierten Patienten) Personen mit einem erhöhten Risiko für eine Malnutrition auf einfache Weise identifiziert werden (21, 22, 23). Bei Herzinsuffizienz-Patienten müssen Fehlinterpretationen aufgrund von Flüssigkeitsretention (Ödeme) beachtet werden. Bisher wurde keines der Instrumente zur Risikoerkennung oder Diagnosestellung einer Malnutrition speziell bei Herzinsuffizienz-Patienten validiert. Zwar können die genannten Screening-Tools selbst bei einer dekompensierten Herzinsuffizienz ein Ernährungsrisiko häufig korrekt erfassen, allerdings scheint die Anwendung multidimensionaler Tools (z. B. MNA-SF) mit Beurteilung von zeitlichen und subjektiven Ernährungsinformationen in dieser Patientengruppe besonders wichtig zu sein (24, 25).
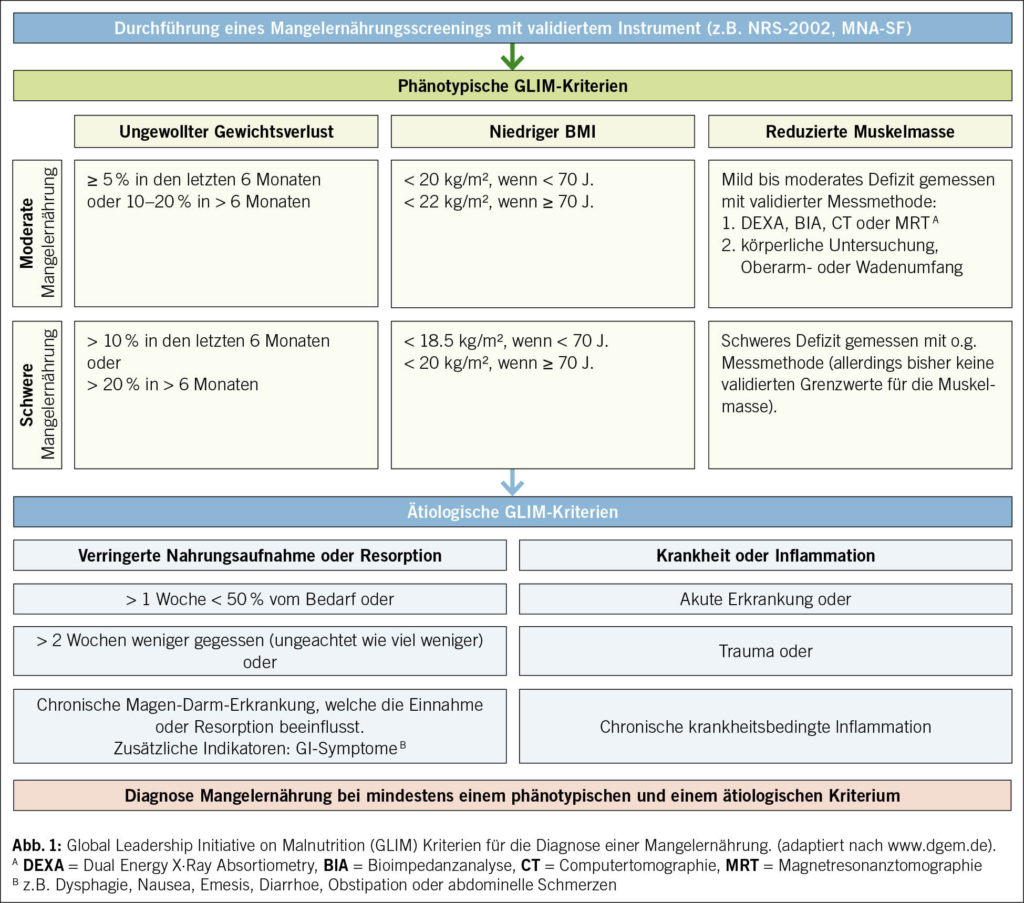
Im Falle eines auffälligen Screenings muss im zweiten Schritt überprüft werden, ob tatsächlich eine Mangelernährung vorliegt. Hierfür wurden im Jahr 2019 die international standardisierten «Global Leadership In Malnutrition» (GLIM)-Diagnosekritierien veröffentlicht (26). Zur Diagnosestellung einer Mangelernährung ist sowohl ein phänotypisches Kriterium (ungewollter Gewichtsverlust, niedriger BMI, reduzierte Muskelmasse) als auch ein ätiologisches Kriterium (reduzierte Nahrungsaufnahme bzw. Malassimilation, Inflammation bzw. hohe Krankheitslast) notwendig. Im dritten Schritt kann daraufhin (anhand der Ausprägung der phänotypischen Kriterien) der Schweregrad der Malnutrition («moderat» oder «schwer») definiert werden. Es ist jedoch zu betonen, dass die GLIM-Kriterien nicht als Ersatz zu einem professionellen Ernährungsassessment dienen, da eine detaillierte Anamnese sowie eine Beurteilung des Ernährungsstatus für die weitere Therapie von Bedeutung sind.
Therapie und Nachsorge
Sobald die Diagnose einer Mangelernährung gestellt und ein ausführliches Ernährungsassessment durchgeführt wurde, sollte eine Ernährungsintervention zur Stabilisierung und Verbesserung des Ernährungszustandes erfolgen. Hierfür wird zunächst die orale Nahrungsaufnahme durch individuell angepasste Haupt- und Zwischenmahlzeiten sowie ggf. durch eine Hinzugabe von angereicherten Lebensmitteln oder oralen Trinknahrungen optimiert (20). Ein Monitoring und Reassessment (alle 24–48 Stunden) ermöglicht die frühzeitige Erkennung von allenfalls notwendigen Therapieanpassungen. Patienten, die durch eine orale Nahrungsaufnahme innerhalb weniger Tage nicht mindestens 75 % des ermittelten Energie- und Proteinbedarfs erreichen, sollten eine zusätzliche enterale Ernährung und bei anhaltend unzureichender Bedarfsdeckung eine zusätzliche parenterale Ernährung erhalten (20).
Zur Abschätzung des individuellen Energiebedarfs ist die Bestimmung des Gesamtenergieverbrauchs (Total Energy Expenditure, TEE) notwendig, der sich aus Grundumsatz (Resting Energy Expenditure, REE), nahrungsinduzierter Thermogenese und aktivitätsabhängigem Energiebedarf zusammensetzt. Da eine indirekte Kalorimetrie zur Messung des Energieumsatzes im klinischen Alltag selten verfügbar ist, werden meist Formeln (z. B. Harris-Benedict-Formel) oder gewichtsadaptierte Schätzungen (z. B. 25–30 kcal/kgKG/Tag) verwendet (20). Diese Schätzungen können eine Ausgangsbasis für eine Ernährungsintervention darstellen, müssen jedoch aufgrund der häufigen Abweichungen vom tatsächlichen Energieverbrauch mit besonderer Vorsicht interpretiert werden (27). Als empfohlene Proteinmenge wird bei polymorbiden Patienten ein Ziel von 1.2–1.5 g/kg Körpergewicht pro Tag angestrebt, sofern keine schwere Nierenfunktionsstörung (eGFR < 30 ml/min/1.73 m2) vorliegt (20, 28). Bereits zu Beginn der Ernährungstherapie sollte zusätzlich eine ausreichende Zufuhr von Mikronährstoffen zur Deckung des Tagesbedarfs gewährleistet und ein laborchemisch dokumentierter Mangel korrigiert werden (20, 29).
Bei der Behandlung einer Mangelernährung muss zudem auf ein mögliches Refeeding-Syndrom geachtet werden. Hierbei handelt es sich um eine lebensbedrohliche Störung des Elektrolyt- und Flüssigkeitshaushaltes, sofern ein Nahrungsaufbau (oral, enteral oder parenteral) zu schnell oder inadäquat erfolgt (9). Der rasche Wechsel von einem katabolen zu einem anabolen Stoffwechsel kann vor allem in den ersten 72 Stunden zu einer schweren Hypophosphatämie (Reduktion > 30 % vom Ausgangswert oder < 0.6 mmol/l), anderen Elektrolytstörungen (u. a. Magnesium- und Kaliummangel) oder Flüssigkeitsverschiebungen führen, die wiederum mit kardiorespiratorischen, hämatologischen und neuromuskulären Funktionsstörungen einhergehen können. Zudem kann sich ein vorbestehender Thiamin-Mangel durch eine Laktatazidose, Wernicke-Enzephalopathie oder auch Herzinsuffizienz («Wet-Beriberi») demaskieren (30). Bei Risikopatienten (BMI < 18.5 kg/m2, Gewichtsverlust > 10 % in den letzten 3–6 Monaten, sehr geringe bzw. fehlende Nahrungsaufnahme > 5 Tage, Alkohol- oder Drogenabusus, vorbestehende Elektrolytstörungen) ist eine Elektrolyt- und Volumenkorrektur, eine Thiamin-Supplementation vor Beginn des Nahrungsaufbaus sowie die Gabe eines Multivitamin- und Spurenelementpräparates von Bedeutung. Die Kalorienzufuhr sollte zudem stufenweise je nach Risiko über 5–10 Tage unter initial täglicher laborchemischer Kontrolle gesteigert werden (30, 31).
Nach Abschluss der Krankenhaus-Behandlung stellt die Fortführung einer ambulanten Therapie bei Patienten mit Ernährungsrisiko oder manifester Malnutrition ein wesentliches Element der Behandlung dar. Das Ziel ist es, das Körpergewicht und den Ernährungsstatus langfristig zu stabilisieren und auf diese Weise den funktionellen Status und die Lebensqualität zu erhöhen (20).
Kardiale Kachexie
Die Kachexie ist als Unterform der krankheitsbedingten Malnutrition zu verstehen und beschreibt ein multifaktorielles Syndrom, das durch einen starken Gewichtsverlust mit Abbau von Muskelmasse und Fettgewebe sowie einer krankheitsbedingten Inflammation gekennzeichnet ist (9). Es tritt vorwiegend bei Patienten mit Organerkrankungen (z. B. Tumorerkrankungen, COPD, chronische Herzinsuffizienz oder Niereninsuffizienz) auf, die im fortgeschrittenen Stadium mit einer katabolen Stoffwechselaktivität einhergehen. Die kardiale Kachexie ist definiert durch einen Gewichtsverlust von mehr als 5 % des Körpergewichts innerhalb von 12 Monaten (oder einem BMI < 20 kg/m2) sowie dem Vorhandensein von mindestens drei weiteren Kriterien (verminderte Muskelkraft, Fatigue, Anorexie, niedriger fettfreier Masse-Index oder abnorme Laborwerte mit Anämie, erhöhten Entzündungsmarkern oder reduziertem Serumalbumin) (32). Die Prävalenz wird bei Herzinsuffizienz-Patienten auf etwa 5–15 % geschätzt, wobei keine eindeutige Korrelation zur linksventrikulären Funktion (LVEF) festzustellen ist (33, 34, 35). Kachektische Patienten weisen eine niedrigere funktionale Kapazität, eine geringere Lebensqualität sowie eine deutlich erhöhte Mortalität auf (36, 37). Aufgrund der chronischen inflammatorischen und katabolen Stoffwechselprozesse kann einer kardialen Kachexie durch Ernährungsinterventionen und körperliche Aktivität nur zum Teil entgegengewirkt werden. In einer Sekundäranalyse der EFFORT-Studie wurde gezeigt, dass Patienten mit einer hohen Inflammation (CRP > 100 mg/l) im Vergleich zu Patienten mit niedrigeren Entzündungsmarkern nicht in gleicher Weise von einer Ernährungstherapie während des Krankenhausaufenthaltes profitieren können (38).
Eine Ernährungsintervention mittels einer kalorien- und proteinreichen Ernährung in Kombination mit einem körperlichen Training stellt dennoch die wichtigste Behandlungsmassnahme für unterernährte oder kachektische Herzinsuffizienz-Patienten dar, um sowohl eine Gewichtstabilisierung als auch eine Verbesserung der kardiorespiratorischen Fitness und funktionalen Kapazität zu erzielen (39, 40). Zum aktuellen Zeitpunkt existieren jedoch keine spezifischen Ernährungsempfehlungen für Patienten mit chronischer Herzinsuffizienz und einer Mangelernährung bzw. kardialen Kachexie. Die kardiologischen Gesellschaften empfehlen bei chronischer Herzinsuffizienz vorwiegend Ansätze einer mediterranen Ernährung oder einer DASH-Diät (Dietary Approaches to Stop Hypertension), da diese am ehesten kardioprotektive und antiinflammatorische Eigenschaften aufweisen (41, 42, 43, 44, 45). Häufigere Mahlzeiten mit kleineren Portionen können zur Vermeidung einer postprandialen Dyspnoe beitragen und die Compliance der Patienten erhöhen. Bei Ödemen sollte eine Flüssigkeitsrestriktion (1.5–2 Liter/Tag) und eine begrenzte Salzaufnahme (ca. 5 g pro Tag) erwogen werden (1). Allerdings bleibt der Nutzen einer Salzrestriktion aufgrund widersprüchlicher Studienergebnisse und allenfalls sogar negativen Auswirkungen (u. a. durch eine verstärkte neurohumerale Aktivierung) umstritten (46, 47, 48). Die Supplementierung von mehrfach ungesättigten Omega-3-Fettsäuren (PUFA) zeigte in einigen Studien ebenfalls positive Effekte auf die linksventrikuläre Funktion, die Rehospitalisierungsrate und die Mortalität, jedoch wurden auch diese Empfehlungen von aufgrund inkonsistenten Studiendaten und einem möglicherweise erhöhten Risiko für das Auftreten von Vorhofflimmern abgeschwächt (49, 50, 51, 52, 53). Bezüglich der Substitution von Mikronährstoffen wird in den aktuellen kardiologischen Leitlinien eine intravenöse Eisengabe bei Herzinsuffizienz-Patienten mit reduzierter linksventrikulärer Funktion (LVEF < 40 %) und einem Eisenmangel (Serum-Ferritin < 100 ng/ml oder 100–299 ng/ml mit TSAT < 20 %) zur Verbesserung der Belastungsfähigkeit und Lebensqualität empfohlen (54, 55). Trotz einzelner vielversprechender Studien zu weiteren Mikronährstoffen oder Nahrungsergänzungen (z. B. Thiamin, Coenzym Q10), kann aufgrund der heterogenen Studiendaten bisher keine klare Empfehlung zur zusätzlichen Mikronährstoff-Substitution bei Herzinsuffizienz-Patienten gegeben werden (56, 57, 58, 59, 60). Hingegen konnte durch eine medikamentöse Therapie mit Betablockern, ACE-Hemmern und Angiotensin-II-Rezeptorantagonisten, unabhängig von einer Verbesserung der linksventrikulären Funktion, ein Gewichtsverlust und die Entwicklung einer kardialen Kachexie verzögert werden (61, 62). Weitere mögliche Therapieoptionen wie z. B. Immunmodulatoren (TNF-α-Hemmer), anabole Hormone (Ghrelin, Testosteron) oder appetitanregende Substanzen werden trotz vereinzelt positiver Ergebnisse in kleineren Studien bisher nicht im klinischen Alltag zur Behandlung der Kachexie eingesetzt (63).
Sarkopenie und Gebrechlichkeit (Frailty)
Bei Patienten mit chronischer Herzinsuffizienz treten neben der Malnutrition und kardialen Kachexie häufig auch eine Sarkopenie und eine vermehrte Gebrechlichkeit (Frailty) auf. Die Sarkopenie ist ein eigenständiges Syndrom, das durch einen progressiven und generalisierten Verlust von Muskelkraft und Muskelmasse (unabhängig von der Fettmasse) gekennzeichnet ist und mit negativen Folgen wie Sturzneigung und Funktionseinschränkungen einhergeht (64). Dieser Verlust tritt im Rahmen von natürlichen Altersprozessen auf, wird jedoch durch krankheitsbedingte entzündliche und hormonelle Prozesse, eine verminderte körperliche Aktivität sowie einer Mangelernährung (insbesondere durch eine unzureichende Proteinzufuhr) verstärkt (65, 66). Die Prävalenz bei Herzinsuffizienz-Patienten wird je nach Einschlusskriterien zwischen 10 % und 69 % geschätzt (67). Sofern nicht bereits typische klinische Zeichen den Verdacht auf eine Sarkopenie nahelegen, wird ein 5-Punkte-Screening (SARC-F) empfohlen, dessen Sensitivität durch eine Messung des Wadenumfangs verbessert werden kann (68, 69). Eine Messung der Handkraft mithilfe eines Dynamometers oder alternativ die Messung der Beinmuskelkraft mithilfe des «Chair-Stand-Test» kann eine Verdachtsdiagnose erhärten (Handkraft < 16 kg für Frauen und < 27 kg für Männer, Chair-Stand-Test < 15 Sekunden) (64). Zur tatsächlichen Diagnosestellung erfolgt anschliessend die Messung der Muskelmasse (appendikuläre Magermasse, ALM), wofür sowohl die Bioelektrische Impedanzanalyse (BIA), die Dual-Röntgen-Absorptiometrie (DXA) als auch bildgebende Verfahren (MRI, CT) eingesetzt werden können. Im Falle eines relativen Skelettmuskelindex (SMI) von < 5.5 kg/m2 bei Frauen bzw. < 7 kg/m2 bei Männern ist eine Sarkopenie bestätigt (64). Die Einordnung des Schweregrades kann durch zusätzliche Funktionsuntersuchungen (Ganggeschwindigkeit, Timed-up-and-go-Test, SPPB oder 400 m-Gehtest) erfolgen (64). Bereits das Vorliegen einer beeinträchtigten Muskelkraft sollte eine Ursachenabklärung und einen Therapiebeginn einleiten. In diesem Zusammenhang konnte in mehreren Studien gezeigt werden, dass vor allem die Kombination aus einem Krafttraining und einer gesteigerten Proteinzufuhr positive Auswirkungen auf die Prävention und Behandlung einer Sarkopenie haben kann (70, 71, 72, 73, 74). Eine Substitution von Proteinen mit einem hohen Leucin-Gehalt (z. B. Molkenprotein) ist möglicherweise mit weiteren positiven Effekten auf die Muskelproteinsynthese assoziiert (75, 76).
Gebrechlichkeit (Frailty) wird häufig als biologisches oder geriatrisches Syndrom betrachtet, das durch den Verlust an körperlichen Funktionen und kognitiven Fähigkeiten gekennzeichnet ist. Als Grundlage dienen vor allem die Phänotyp-Kriterien nach Fried (3 von 5 Kriterien: ungewollter Gewichtsverlust > 5 kg/Jahr, Abnahme der Muskel- bzw. Handkraft, langsame Gehgeschwindigkeit, reduzierte körperliche Aktivität, subjektives Erschöpfungsgefühl) sowie das Defizit-Modell nach Rockwood (Ermittlung eines Frailty-Index anhand von funktionellen, kognitiven und sozialen Einschränkungen) (77, 78). Hierbei ist jedoch zu betonen, dass die Gebrechlichkeit nicht nur als ein physiologischer Altersprozess betrachtet werden sollte. Insbesondere bei Herzinsuffizienz-Patienten besteht sehr häufig ein altersunabhängiger Zustand aus klinischen, funktionalen, kognitiv-psychologischen und sozialen Domänen, die zu einer erhöhten Vulnerabilität gegenüber endogenen oder exogenen Stressoren (z. B. leichte Entzündungen, kleinere Eingriffe, Medikamentenanpassungen) führen (79). Das Vorhandensein einer Gebrechlichkeit ist daher ein zusätzlicher Faktor, der die Prognose von Herzinsuffizienz-Patienten aufgrund erhöhter Morbiditäts- und Mortalitätsraten negativ beeinflusst (80, 81, 82). In der Behandlung ist folglich eine frühzeitige Identifizierung dieser vulnerablen Patientengruppe durch multidimensionale Assessment-Tools (z. B. Clinical Frailty Scale, Essential Frailty Toolset) sinnvoll, um potenziell reversible Faktoren wie Mangelernährung oder Sarkopenie durch individuelle Ernährungsinterventionen und körperliches Training, optimalerweise im Rahmen einer kardialen Rehabilitation, adäquat zu behandeln (83, 84, 85).
Fazit
Zusammenfassend ist es in der Behandlung von chronischen Herzinsuffizienz-Patienten essenziell, dass die Therapie nicht auf interventionelle oder medikamentöse Massnahmen beschränkt bleibt. Die frühzeitige Erkennung einer krankheitsbedingten Mangelernährung sowie häufig assoziierter Begleitsyndrome wie kardiale Kachexie, Sarkopenie oder Gebrechlichkeit (Frailty) sind von wesentlicher Bedeutung für den weiteren Krankheits- und Therapieverlauf. Daher sollte die Einführung von strukturierten Behandlungsabläufen mit Integration von ernährungsmedizinischen Interventionen, die Sensibilisierung und systematische Schulung von klinischem Personal sowie eine enge Zusammenarbeit mit den Fachpersonen der Ernährungstherapie fester Bestandteil in der Behandlung der chronischen Herzinsuffizienz sein.
Copyright
Aerzteverlag medinfo AG
Facharzt Kardiologie und Allgemeine Innere Medizin,
Leitung stationäre kardiovaskuläre Rehabilitation
Zentrum für Rehabilitation & Sportmedizin
Freiburgstrasse 18
3010 Bern
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Malnutrition, Kachexie, Sarkopenie und Frailty sind häufige, oft übersehene Begleitsyndrome der chronischen Herzinsuffizienz und stehen in direktem Zusammenhang mit erhöhter Morbidität, Mortalität und reduzierter Lebensqualität.
- Zur Diagnose einer Mangelernährung sollte ein dreistufiger Ansatz erfolgen: Screening (z.B. MNA-SF, NRS-2002), Diagnosesicherung nach GLIM-Kritierien und anschliessend ein umfassendes Ernährungsassessment zur Therapieplanung.
- Die Kombination aus individualisierter Ernährungstherapie, körperlichem Training und multiprofessionellem Management, idealerweise im Rahmen eines strukturierten Rehabilitationsprogramms, ist essenziell für eine nachhaltige Verbesserung der Lebensqualität und der Prognose von Herzinsuffizienz-Patienten.
1. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021 Sep 21;42(36):3599-3726.
2. Savarese G, Becher PM, Lund LH, Seferovic P, Rosano GMC, Coats AJS. Global burden of heart failure: a comprehensive and updated review of epidemiology. Cardiovasc Res. 2023 Jan 18;118(17):3272-3287.
3. Saitoh M, Ishida J, Doehner W, von Haehling S, Anker MS, Coats AJS, Anker SD, Springer J. Sarcopenia, cachexia, and muscle performance in heart failure: Review update 2016. Int J Cardiol. 2017 Jul 1;238:5-11.
4. Fernández-Pombo A, Rodríguez-Carnero G, Castro AI, et al. Relevance of nutritional assessment and treatment to counteract cardiac cachexia and sarcopenia in chronic heart failure. Clin Nutr. 2021 Sep;40(9):5141-5155.
5. Sandek A, Bauditz J, Swidsinski A, et al. Altered intestinal function in patients with chronic heart failure. J Am Coll Cardiol. 2007 Oct 16;50(16):1561-9.
6. Rahman A, Jafry S, Jeejeebhoy K, Nagpal AD, Pisani B, Agarwala R. Malnutrition and Cachexia in Heart Failure. JPEN J Parenter Enteral Nutr. 2016 May;40(4):475-86.
7. Martins T, Vitorino R, Amado F, Duarte JA, Ferreira R. Biomarkers for cardiac cachexia: reality or utopia. Clin Chim Acta. 2014 Sep 25;436:323-8.
8. Morton RW, Traylor DA, Weijs PJM, Phillips SM. Defining anabolic resistance: implications for delivery of clinical care nutrition. Curr Opin Crit Care. 2018 Apr;24(2):124-130.
9. Cederholm T, Barazzoni R, Austin P, et al. ESPEN guidelines on definitions and terminology of clinical nutrition. Clin Nutr. 2017 Feb;36(1):49-64.
10. Kaiser MJ, Bauer JM, Rämsch C, et al. Mini Nutritional Assessment International Group. Frequency of malnutrition in older adults: a multinational perspective using the mini nutritional assessment. J Am Geriatr Soc. 2010 Sep;58(9):1734-8.
11. Lv S, Ru S. The prevalence of malnutrition and its effects on the all-cause mortality among patients with heart failure: A systematic review and meta-analysis. PLoS One. 2021 Oct 28;16(10):e0259300.
12. Söderström L, Rosenblad A, Adolfsson ET, Saletti A, Bergkvist L. Nutritional status predicts preterm death in older people: a prospective cohort study. Clin Nutr. 2014 Apr;33(2):354-9.
13. Wawrzenczyk A, Anaszewicz M, Wawrzenczyk A, Budzynski J. Clinical significance of nutritional status in patients with chronic heart failure-a systematic review. Heart Fail Rev. 2019 Sep;24(5):671-700.
14. Crogan NL, Pasvogel A. The influence of protein-calorie malnutrition on quality of life in nursing homes. J Gerontol A Biol Sci Med Sci. 2003 Feb;58(2):159-64.
15. Schuetz P, Fehr R, Baechli V, et al. Individualised nutritional support in medical inpatients at nutritional risk: a randomised clinical trial. Lancet. 2019 Jun 8;393(10188):2312-2321.
16. Bonilla-Palomas JL, Gámez-López AL, Castillo-Domínguez JC, et al. Nutritional Intervention in Malnourished Hospitalized Patients with Heart Failure. Arch Med Res. 2016 Oct;47(7):535-540.
17. Hersberger L, Dietz A, Bürgler H, et a.. Individualized Nutritional Support for Hospitalized Patients With Chronic Heart Failure. J Am Coll Cardiol. 2021 May 11;77(18):2307-2319.
18. Gomes F, Baumgartner A, Bounoure L, et al. Association of Nutritional Support With Clinical Outcomes Among Medical Inpatients Who Are Malnourished or at Nutritional Risk: An Updated Systematic Review and Meta-analysis. JAMA Netw Open. 2019 Nov 1;2(11):e1915138.
19. Kaegi-Braun N, Faessli M, Kilchoer F, et al. Nutritional trials using high protein strategies and long duration of support show strongest clinical effects on mortality.: Results of an updated systematic review and meta-analysis. Clin Nutr ESPEN. 2021 Oct;45:45-54.
20. Wunderle C, Gomes F, Schuetz P, et al. ESPEN guideline on nutritional support for polymorbid medical inpatients. Clin Nutr. 2023 Sep;42(9):1545-1568.
21. Kondrup J, Rasmussen HH, Hamberg O, Stanga Z; Ad Hoc ESPEN Working Group. Nutritional risk screening (NRS 2002): a new method based on an analysis of controlled clinical trials. Clin Nutr. 2003 Jun;22(3):321-36.
22. Rubenstein LZ, Harker JO, Salvà A, Guigoz Y, Vellas B. Screening for undernutrition in geriatric practice: developing the short-form mini-nutritional assessment (MNA-SF). J Gerontol A Biol Sci Med Sci. 2001 Jun;56(6):M366-72.
23. van Bokhorst-de van der Schueren MA, Guaitoli PR, Jansma EP, de Vet HC. Nutrition screening tools: does one size fit all? A systematic review of screening tools for the hospital setting. Clin Nutr. 2014 Feb;33(1):39-58.
24. Tevik K, Thürmer H, Husby MI, de Soysa AK, Helvik AS. Nutritional risk screening in hospitalized patients with heart failure. Clin Nutr. 2015 Apr;34(2):257-64.
25. Osório AF, Ribeiro ÉCT, Parahiba SM, Forte GC, Clausell NO, Souza GC. Prognostic value of nutritional screening tools in hospitalized patients with decompensated heart failure: A systematic review and meta-analysis. Nutr Res. 2023 Dec;120:1-19.
26. Cederholm T, Jensen GL, Correia MITD, et al. GLIM criteria for the diagnosis of malnutrition – A consensus report from the global clinical nutrition community. Clin Nutr. 2019 Feb;38(1):1-9.
27. Neelemaat F, van Bokhorst-de van der Schueren MA, Thijs A, Seidell JC, Weijs PJ. Resting energy expenditure in malnourished older patients at hospital admission and three months after discharge: predictive equations versus measurements. Clin Nutr. 2012 Dec;31(6):958-66.
28. Deutz NE, Bauer JM, Barazzoni R,et al. Protein intake and exercise for optimal muscle function with aging: recommendations from the ESPEN Expert Group. Clin Nutr. 2014 Dec;33(6):929-36.
29. Berger MM, Shenkin A, Dizdar OS, et al. ESPEN practical short micronutrient guideline. Clin Nutr. 2024 Mar;43(3):825-857.
30. Friedli N, Stanga Z, Culkin A, et al. Management and prevention of refeeding syndrome in medical inpatients: An evidence-based and consensus-supported algorithm. Nutrition. 2018 Mar;47:13-20.
31. Stanga Z, Brunner A, Leuenberger M, et al. Nutrition in clinical practice-the refeeding syndrome: illustrative cases and guidelines for prevention and treatment. Eur J Clin Nutr. 2008 Jun;62(6):687-94.
32. Evans WJ, Morley JE, Argilés J, Bales C, et al. Cachexia: a new definition. Clin Nutr. 2008 Dec;27(6):793-9.
33. Christensen HM, Kistorp C, Schou M, et al. Prevalence of cachexia in chronic heart failure and characteristics of body composition and metabolic status. Endocrine. 2013 Jun;43(3):626-34.
34. von Haehling S, Anker SD. Prevalence, incidence and clinical impact of cachexia: facts and numbers-update 2014. J Cachexia Sarcopenia Muscle. 2014 Dec;5(4):261-3.
35. Florea VG, Henein MY, Rauchhaus M, et al. The cardiac component of cardiac cachexia. Am Heart J. 2002 Jul;144(1):45-50.
36. Saitoh M, Dos Santos MR, Emami A, Ishida J, et al. Anorexia, functional capacity, and clinical outcome in patients with chronic heart failure: results from the Studies Investigating Co-morbidities Aggravating Heart Failure (SICA-HF). ESC Heart Fail. 2017 Nov;4(4):448-457.
37. Rossignol P, Masson S, Barlera S, et al. Loss in body weight is an independent prognostic factor for mortality in chronic heart failure: insights from the GISSI-HF and Val-HeFT trials. Eur J Heart Fail. 2015 Apr;17(4):424-33.
38. Merker M, Felder M, Gueissaz L, et al. Association of Baseline Inflammation With Effectiveness of Nutritional Support Among Patients With Disease-Related Malnutrition: A Secondary Analysis of a Randomized Clinical Trial. JAMA Netw Open. 2020 Mar 2;3(3):e200663.
39. Deutz NE, Matheson EM, Matarese LE, et al. Readmission and mortality in malnourished, older, hospitalized adults treated with a specialized oral nutritional supplement: A randomized clinical trial. Clin Nutr. 2016 Feb;35(1):18-26.
40. Rozentryt P, von Haehling S, Lainscak M, et al. The effects of a high-caloric protein-rich oral nutritional supplement in patients with chronic heart failure and cachexia on quality of life, body composition, and inflammation markers: a randomized, double-blind pilot study. J Cachexia Sarcopenia Muscle. 2010 Sep;1(1):35-42.
41. Vest AR, Chan M, Deswal A, et al. Nutrition, Obesity, and Cachexia in Patients With Heart Failure: A Consensus Statement from the Heart Failure Society of America Scientific Statements Committee. J Card Fail. 2019 May;25(5):380-400.
42. Estruch R, Ros E, Salas-Salvadó J, et al. Primary Prevention of Cardiovascular Disease with a Mediterranean Diet Supplemented with Extra-Virgin Olive Oil or Nuts. N Engl J Med. 2018 Jun 21;378(25):e34.
43. Hummel SL, Seymour EM, Brook RD, et al. Low-sodium DASH diet improves diastolic function and ventricular-arterial coupling in hypertensive heart failure with preserved ejection fraction. Circ Heart Fail. 2013 Nov;6(6):1165-71.
44. Levitan EB, Lewis CE, Tinker LF, et al. Mediterranean and DASH diet scores and mortality in women with heart failure: The Women’s Health Initiative. Circ Heart Fail. 2013 Nov;6(6):1116-23.
45. Hummel SL, Karmally W, Gillespie BW, et al. Home-Delivered Meals Postdischarge From Heart Failure Hospitalization. Circ Heart Fail. 2018 Aug;11(8):e004886.
46. Philipson H, Ekman I, Forslund HB, Swedberg K, Schaufelberger M. Salt and fluid restriction is effective in patients with chronic heart failure. Eur J Heart Fail. 2013 Nov;15(11):1304-10.
47. Doukky R, Avery E, Mangla A, et al. Impact of Dietary Sodium Restriction on Heart Failure Outcomes. JACC Heart Fail. 2016 Jan;4(1):24-35.
48. Ezekowitz JA, Colin-Ramirez E, Ross H, et al. Reduction of dietary sodium to less than 100 mmol in heart failure (SODIUM-HF): an international, open-label, randomised, controlled trial. Lancet. 2022 Apr 9;399(10333):1391-1400.
49. Tavazzi L, Maggioni AP, Marchioli R, et al. Effect of n-3 polyunsaturated fatty acids in patients with chronic heart failure (the GISSI-HF trial): a randomised, double-blind, placebo-controlled trial. Lancet. 2008 Oct 4;372(9645):1223-30.
50. Oppedisano F, Mollace R, Tavernese A, et al. PUFA Supplementation and Heart Failure: Effects on Fibrosis and Cardiac Remodeling. Nutrients. 2021 Aug 26;13(9):2965.
51. Nicholls SJ, Lincoff AM, Garcia M, et al. Effect of High-Dose Omega-3 Fatty Acids vs Corn Oil on Major Adverse Cardiovascular Events in Patients at High Cardiovascular Risk: The STRENGTH Randomized Clinical Trial. JAMA. 2020 Dec 8;324(22):2268-2280.
52. Lombardi M, Chiabrando JG, Vescovo GM, et al. Impact of Different Doses of Omega-3 Fatty Acids on Cardiovascular Outcomes: a Pairwise and Network Meta-analysis. Curr Atheroscler Rep. 2020 Jul 16;22(9):45.
53. Lombardi M, Carbone S, Del Buono MG, et al. Omega-3 fatty acids supplementation and risk of atrial fibrillation: an updated meta-analysis of randomized controlled trials. Eur Heart J Cardiovasc Pharmacother. 2021 Jul 23;7(4):e69-e70.
54. McDonagh TA, Metra M, Adamo M, et al. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023 Oct 1;44(37):3627-3639.
55. Graham FJ, Pellicori P, Kalra PR, Ford I, Bruzzese D, Cleland JGF. Intravenous iron in patients with heart failure and iron deficiency: an updated meta-analysis. Eur J Heart Fail. 2023 Apr;25(4):528-537. doi: 10.1002/ejhf.2810. Epub 2023 Mar 8. PMID: 36823953; PMCID: PMC10946839
56. Schoenenberger AW, Schoenenberger-Berzins R, der Maur CA, Suter PM, Vergopoulos A, Erne P. Thiamine supplementation in symptomatic chronic heart failure: a randomized, double-blind, placebo-controlled, cross-over pilot study. Clin Res Cardiol. 2012 Mar;101(3):159-64.
57. Keith M, Quach S, Ahmed M, Azizi-Namini P, et al. Thiamin supplementation does not improve left ventricular ejection fraction in ambulatory heart failure patients: a randomized controlled trial. Am J Clin Nutr. 2019 Dec 1;110(6):1287-1295.
58. Mortensen SA, Rosenfeldt F, Kumar A, et al. The effect of coenzyme Q10 on morbidity and mortality in chronic heart failure: results from Q-SYMBIO: a randomized double-blind trial. JACC Heart Fail. 2014 Dec;2(6):641-9.
59. Al Saadi T, Assaf Y, Farwati M, Turkmani K, Al-Mouakeh A, Shebli B, Khoja M, Essali A, Madmani ME. Coenzyme Q10 for heart failure. Cochrane Database Syst Rev. 2021 Feb 3;(2)(2):CD008684.
60. McKeag NA, McKinley MC, Harbinson MT, et al. The effect of multiple micronutrient supplementation on left ventricular ejection fraction in patients with chronic stable heart failure: a randomized, placebo-controlled trial. JACC Heart Fail. 2014 Jun;2(3):308-17.
61. Hryniewicz K, Androne AS, Hudaihed A, Katz SD. Partial reversal of cachexia by beta-adrenergic receptor blocker therapy in patients with chronic heart failure. J Card Fail. 2003 Dec;9(6):464-8.
62. Anker SD, Negassa A, Coats AJ, et al. Prognostic importance of weight loss in chronic heart failure and the effect of treatment with angiotensin-converting-enzyme inhibitors: an observational study. Lancet. 2003 Mar 29;361(9363):1077-83.
63. Rolfe M, Kamel A, Ahmed MM, Kramer J. Pharmacological management of cardiac cachexia: a review of potential therapy options. Heart Fail Rev. 2019 Sep;24(5):617-623.
64. Cruz-Jentoft AJ, Bahat G, Bauer J, et al. Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing. 2019 Jan 1;48(1):16-31.
65. Narici MV, Maffulli N. Sarcopenia: characteristics, mechanisms and functional significance. Br Med Bull. 2010;95:139-59.
66. Bauer J, Biolo G, Cederholm T, et al. Evidence-based recommendations for optimal dietary protein intake in older people: a position paper from the PROT-AGE Study Group. J Am Med Dir Assoc. 2013 Aug;14(8):542-59.
67. Zhang Y, Zhang J, Ni W, et al. Sarcopenia in heart failure: a systematic review and meta-analysis. ESC Heart Fail. 2021 Apr;8(2):1007-1017. doi: 10.1002/ehf2.13255.
68. Malmstrom TK, Morley JE. SARC-F: a simple questionnaire to rapidly diagnose sarcopenia. J Am Med Dir Assoc. 2013 Aug;14(8):531-2.
69. Barbosa-Silva TG, Menezes AM, Bielemann RM, et al. Enhancing SARC-F: Improving Sarcopenia Screening in the Clinical Practice. J Am Med Dir Assoc. 2016 Dec 1;17(12):1136-1141.
70. Deutz NE, Bauer JM, Barazzoni R, et al. Protein intake and exercise for optimal muscle function with aging: recommendations from the ESPEN Expert Group. Clin Nutr. 2014 Dec;33(6):929-36.
71. Peterson MD, Sen A, Gordon PM. Influence of resistance exercise on lean body mass in aging adults: a meta-analysis. Med Sci Sports Exerc. 2011 Feb;43(2):249-58.
72. Cermak NM, Res PT, de Groot LC, Saris WH, van Loon LJ. Protein supplementation augments the adaptive response of skeletal muscle to resistance-type exercise training: a meta-analysis. Am J Clin Nutr. 2012 Dec;96(6):1454-64.
73. Liao CD, Chen HC, Huang SW, Liou TH. The Role of Muscle Mass Gain Following Protein Supplementation Plus Exercise Therapy in Older Adults with Sarcopenia and Frailty Risks: A Systematic Review and Meta-Regression Analysis of Randomized Trials. Nutrients. 2019 Jul 25;11(8):1713.
74. Beckwée D, Delaere A, Aelbrecht S, et al. Exercise Interventions for the Prevention and Treatment of Sarcopenia. A Systematic Umbrella Review. J Nutr Health Aging. 2019;23(6):494-502.
75. Niccoli S, Kolobov A, Bon T, et al. Whey Protein Supplementation Improves Rehabilitation Outcomes in Hospitalized Geriatric Patients: A Double Blinded, Randomized Controlled Trial. J Nutr Gerontol Geriatr. 2017 Oct-Dec;36(4):149-165.
76. Wilkinson DJ, Bukhari SSI, Phillips BE, et al. Effects of leucine-enriched essential amino acid and whey protein bolus dosing upon skeletal muscle protein synthesis at rest and after exercise in older women. Clin Nutr. 2018 Dec;37(6 Pt A):2011-2021.
77. Fried LP, Tangen CM, Walston J, et al. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci. 2001 Mar;56(3):M146-56.
78. Mitnitski AB, Mogilner AJ, Rockwood K. Accumulation of deficits as a proxy measure of aging. ScientificWorldJournal. 2001 Aug 8;1:323-36.
79. Vitale C, Jankowska E, Hill L. Heart Failure Association/European Society of Cardiology position paper on frailty in patients with heart failure. Eur J Heart Fail. 2019 Nov;21(11):1299-1305.
80. Sanders NA, Supiano MA, Lewis EF, et al. The frailty syndrome and outcomes in the TOPCAT trial. Eur J Heart Fail. 2018 Nov;20(11):1570-1577.
81. Bottle A, Kim D, Hayhoe B, et al. Frailty and co-morbidity predict first hospitalisation after heart failure diagnosis in primary care: population-based observational study in England. Age Ageing. 2019 May 1;48(3):347-354.
82. Veronese N, Cereda E, Stubbs B, et a.. Risk of cardiovascular disease morbidity and mortality in frail and pre-frail older adults: Results from a meta-analysis and exploratory meta-regression analysis. Ageing Res Rev. 2017 May;35:63-73.
83. Ng TP, Feng L, Nyunt MS et al. Nutritional, Physical, Cognitive, and Combination Interventions and Frailty Reversal Among Older Adults: A Randomized Controlled Trial. Am J Med. 2015 Nov;128(11):1225-1236.e1.
84. de Vries NM, van Ravensberg CD, Hobbelen JS, Olde Rikkert MG, Staal JB, Nijhuis-van der Sanden MW. Effects of physical exercise therapy on mobility, physical functioning, physical activity and quality of life in community-dwelling older adults with impaired mobility, physical disability and/or multi-morbidity: a meta-analysis. Ageing Res Rev. 2012 Jan;11(1):136-49
85. Richter D, Guasti L, Walker D, et al. Frailty in cardiology: definition, assessment and clinical implications for general cardiology. A consensus document of the Council for Cardiology Practice (CCP), Association for Acute Cardio Vascular Care (ACVC), Association of Cardiovascular Nursing and Allied Professions (ACNAP), European Association of Preventive Cardiology (EAPC), European Heart Rhythm Association (EHRA), Council on Valvular Heart Diseases (VHD), Council on Hypertension (CHT), Council of Cardio-Oncology (CCO), Working Group (WG) Aorta and Peripheral Vascular Diseases, WG e-Cardiology, WG Thrombosis, of the European Society of Cardiology, European Primary Care Cardiology Society (EPCCS). Eur J Prev Cardiol. 2022 Feb 19;29(1):216-227.
der informierte @rzt
- Vol. 16
- Ausgabe 2
- Februar 2026