- Medikamentös induzierte toxische Leberschäden
Medikamentös induzierte Leberschäden (Drug Induced Liver Injury, DILI) stellen eine wichtige Differenzialdiagnose bei erhöhten Leberwerten dar und zählen in der westlichen Welt zu den häufigsten Ursachen eines akuten Leberversagens. Das klinische Spektrum reicht von asymptomatischen Transaminasenerhöhungen bis zu schweren Verläufen mit Ikterus, Koagulopathie und hepatischer Enzephalopathie. Pathophysiologisch werden dosisabhängige, intrinsische von dosisunabhängigen, idiosynkratischen Leberschäden, welche mit variabler Latenz auftreten, unterschieden. Zunehmend relevant sind zudem immuntherapieassoziierte Leberschäden durch Checkpoint-Inhibitoren. Da DILI eine Ausschlussdiagnose ist, kommt einer strukturierten Diagnostik zentrale Bedeutung zu; auch pflanzliche Präparate und Nahrungsergänzungsmittel sind als Auslöser zu berücksichtigen. Therapeutisch steht das frühzeitige Absetzen des auslösenden Medikaments im Vordergrund, ergänzt in ausgewählten Fällen durch spezifische Behandlungsansätze wie N-Acetylcystein oder Kortikosteroide.
Drug-induced liver injury (DILI) represents an important differential diagnosis in patients with abnormal liver tests and is among the most common causes of acute liver failure in Western countries. The clinical spectrum ranges from asymptomatic elevations of transaminases to severe courses with jaundice, coagulopathy, and hepatic encephalopathy. From a pathophysiological perspective, dose-dependent intrinsic liver injury is distinguished from dose-independent idiosyncratic forms, which occur with variable latency. Liver injury associated with immunotherapy, particularly immune checkpoint inhibitors, has become increasingly relevant. As DILI is a diagnosis of exclusion, a structured diagnostic approach is essential, and herbal products as well as dietary supplements should also be considered as potential causative agents. Therapeutic management primarily consists of early discontinuation of the offending drug, supplemented in selected cases by specific treatments such as N-acetylcysteine or corticosteroids.
Keywords: Medikamentöse Leberschäden, Paracetamol, Immuntherapie, pflanzliche Präparate, akutes Leberversagen
Einleitung
Medikamentös induzierte Leberschäden (Drug Induced Liver Injury, DILI) sind eine relevante Ursache akuter und subakuter Leberschädigungen und stellen eine diagnostische Herausforderung dar. Obwohl DILI lange als selten galt (1 : 10 000–1 : 100 000), zeigen populationsbasierte europäische Studien eine jährliche Inzidenz von etwa 14–19 Fällen pro 100 000 Einwohnern (1, 2). Die tatsächliche Häufigkeit dürfte aufgrund nicht erkannter oder nicht gemeldeter milder Verläufe höher liegen.
Das klinische Spektrum reicht von asymptomatischen Transaminasenerhöhungen bis zu schweren Verläufen mit Ikterus, Koagulopathie, hepatischer Enzephalopathie und Multiorganversagen (3). Die oft unspezifische Symptomatik erschwert die frühzeitige Diagnose. Während milde Verläufe nach Absetzen der Medikation meist vollständig ausheilen, sind schwere hepatozelluläre Verläufe mit Ikterus mit einer relevanten Mortalität assoziiert und erfordern eine rasche Risikostratifizierung. In der westlichen Welt ist DILI für etwa die Hälfte der Fälle des akuten Leberversagens verantwortlich (4, 5).
Pathophysiologisch werden direkte (intrinsische) und indirekte (idiosynkratische) Leberschäden unterschieden. Zusätzlich haben immuntherapieassoziierte Leberschäden, insbesondere im Rahmen moderner onkologischer Therapien, deutlich an klinischer Bedeutung gewonnen (6–8).
Intrinsische medikamentöse Leberschäden
Intrinsische medikamentöse Leberschäden sind dosisabhängig, vorhersehbar und treten typischerweise nach kurzer Latenz von Stunden bis wenigen Tagen auf. Sie betreffen einen Grossteil exponierter Personen, sobald eine toxische Dosis überschritten wird. Der klinisch und epidemiologisch wichtigste Vertreter ist die Paracetamol-assoziierte Leberschädigung, die in Europa und Nordamerika eine der häufigsten Ursachen des akuten Leberversagens darstellt (4, 7).
Paracetamol wird in der Leber überwiegend durch Glukuronidierung und Sulfatierung metabolisiert. Ein kleiner Anteil wird über das Cytochrom-P450-Enzymsystem, insbesondere CYP2E1, zu dem hochreaktiven Metaboliten N-Acetyl-p-benzochinonimin (NAPQI) umgewandelt. Unter physiologischen Bedingungen wird NAPQI rasch durch Glutathion entgiftet. Bei Überdosierung oder verminderten Glutathionreserven kommt es zur Akkumulation von NAPQI, was mitochondriale Dysfunktion, oxidativen Stress und hepatozelluläre Nekrose verursacht (8, 9).
Klinisch wird zwischen einer akuten, meist einmaligen toxischen Überdosierung, häufig im Rahmen suizidaler Handlungen, und einer kumulativen Überdosierung über mehrere Tage unterschieden. Die empfohlene maximale Tagesdosis von Paracetamol beträgt bei Erwachsenen 4 g und bei Kindern etwa 60 mg/kg KG. Eine schwere Hepatotoxizität wird ab einer einmaligen Dosis von etwa 150 mg/kg KG beschrieben. Bei wiederholter Einnahme können bereits tägliche Dosen von 4–10 g über mehrere Tage zu schweren Leberschäden führen. Der hepatotoxische Schwellenwert kann durch Faktoren wie chronischen Alkoholabusus, enzyminduzierende Medikamenteninteraktionen (z. B. Isoniazid, Rifampicin), Fasten, systemische Erkrankungen oder einen Glutathionmangel bei Malnutrition oder Anorexie weiter abgesenkt sein.
Der klinische Verlauf ist häufig initial symptomarm mit unspezifischen gastrointestinalen Beschwerden. Ein Anstieg von Transaminasen und Bilirubin tritt meist nach etwa 20 Stunden auf, bei schweren Verläufen kann sich nach 3–4 Tagen ein akutes Leberversagen entwickeln. Typisch sind sehr hohe Transaminasenwerte, teils über 10 000 U/l. Die Labordiagnostik sollte Transaminasen, Lebersyntheseparameter (INR, Bilirubin, Albumin, Faktor V), Kreatinin, Elektrolyte, Laktat, eine arterielle Blutgasanalyse sowie den Paracetamol-Spiegel umfassen. Eine initiale Behandlung auf einer Überwachungs- oder Intensivstation ist zu empfehlen. Neben der Gabe von Aktivkohle (1–2 g/kg KG bei Vorstellung innerhalb von 4 h) stellt die frühzeitige Gabe von N-Acetylcystein (NAC) die zentrale therapeutische Massnahme dar, idealerweise innerhalb der ersten acht Stunden. NAC wirkt als Antidot durch Bereitstellung von SH-Gruppen und verbessert die Prognose auch bei bereits manifester Leberschädigung. In der Regel erfolgt die intravenöse Gabe nach dem Prescott-Schema, bei wiederholter Überdosierung oder unklarer Einnahmeanamnese auch unabhängig vom gemessenen Paracetamol-Spiegel. In schweren Fällen mit akutem Leberversagen ist eine frühzeitige Evaluation zur Lebertransplantation erforderlich. Zur Abschätzung der Transplantationsindikation werden unter anderem die King’s-College-Kriterien herangezogen (4, 10, 11). Durch frühzeitige NAC-Therapie und intensivmedizinische Versorgung kann eine Lebertransplantation in den meisten Fällen vermieden werden.
Idiosynkratische medikamentöse Leberschäden
Idiosynkratische medikamentöse Leberschäden sind nicht dosisabhängig und treten nur bei einem sehr kleinen Anteil exponierter Patienten auf. Die Latenzzeit ist variabel und reicht von wenigen Wochen bis zu mehreren Monaten oder Jahren nach Therapiebeginn. Pathophysiologisch spielen immunvermittelte Mechanismen, genetische Prädispositionen sowie pharmakologische Eigenschaften des jeweiligen Medikaments eine zentrale Rolle (8, 12, 13).
Risikofaktoren und Klinik
Zu den beschriebenen Risikofaktoren zählen höheres Lebensalter, weibliches Geschlecht, Komorbiditäten, Polypharmazie sowie genetische Faktoren, insbesondere Assoziationen mit bestimmten HLA-Allelen (z. B. HLA-B*57:01 oder HLA-DRB1-Varianten) (13–15). Diese sind bislang jedoch nicht ausreichend prädiktiv für eine individuelle Risikostratifizierung. Insgesamt bleibt die Identifikation klarer Risikofaktoren schwierig, da Art und Ausprägung der Leberschädigung stark vom jeweiligen Präparat abhängen.
Klinisch präsentieren sich die Patienten häufig asymptomatisch oder mit unspezifischen Symptomen wie Müdigkeit, Appetitlosigkeit, Übelkeit oder Oberbauchbeschwerden. Idiosynkratische Leberschäden werden in immunallergische Formen mit systemischen Hypersensitivitätszeichen (z. B. Fieber, Exanthem, Lymphadenopathie) und nicht immunallergische Formen unterteilt. In schweren Fällen treten Ikterus, Pruritus und Zeichen der Leberfunktionsstörung auf.
Diagnostik
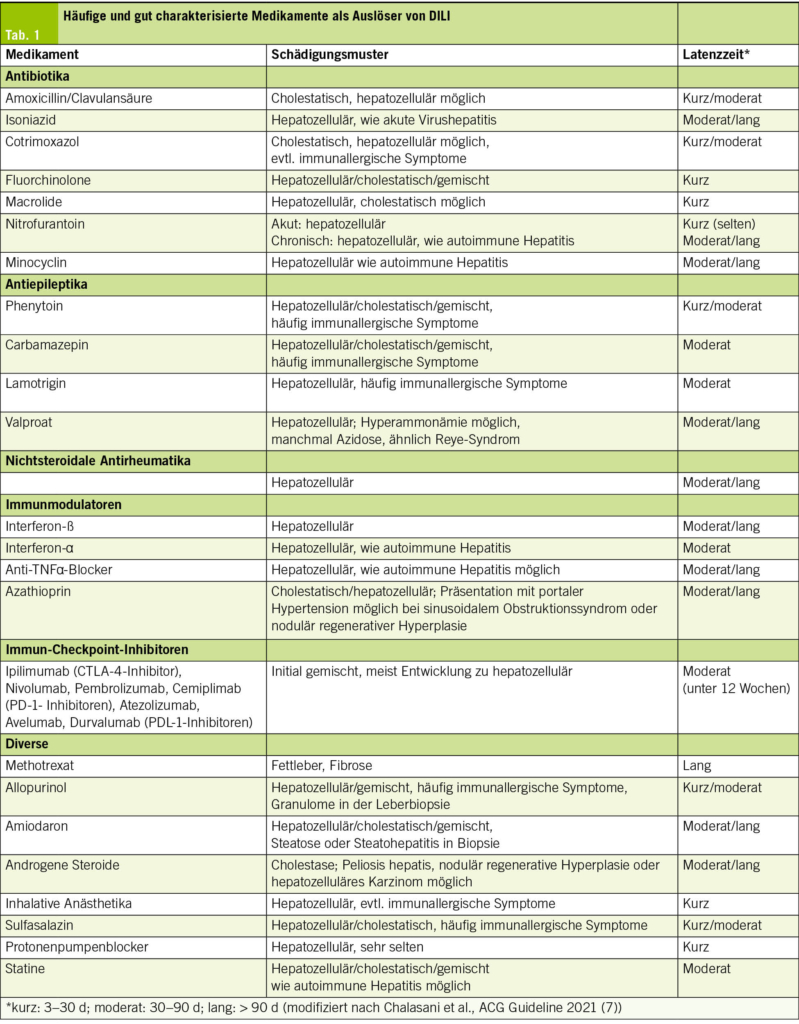
DILI ist eine Ausschlussdiagnose; eine sorgfältige Medikamenten- und Supplementenanamnese ist essenziell und muss auch frei verkäufliche Präparate und pflanzliche Produkte einschliessen. Dabei sollte gezielt nach neu begonnenen Therapien, Dosisänderungen und selbstmedizinierten Substanzen gefragt werden. Eine Übersicht häufiger und gut charakterisierter auslösender Medikamente findet sich in Tab. 1. Die häufigsten Substanzen in einem amerikanischen DILI-Register waren Amoxicillin/Clavulansäure, Isoniazid, Nitrofurantoin, Cotrimoxazol, Minocyclin, Cefazolin, Azithromycin, Ciprofloxacin, Levofloxacin, Diclofenac, Phenytoin, Methyldopa und Azathioprin (absteigende Reihenfolge; (3)). Antibiotika waren auch in einer europäischen Multicenterstudie die häufigsten DILI-Auslöser; als häufigste Einzelpräparate fanden sich Amoxicillin/Clavulansäure, Flucloxacillin, Atorvastatin, Nivolumab/Ipilimumab, Infliximab und Nitrofurantoin (16). Eine umfangreiche Übersicht potenziell hepatotoxischer Arzneimittel ist über die Plattform LiverTox verfügbar (www.ncbi.nlm.nih.gov/books/NBK547852/).
Schädigungsmuster und klinische Bedeutung des R-Werts
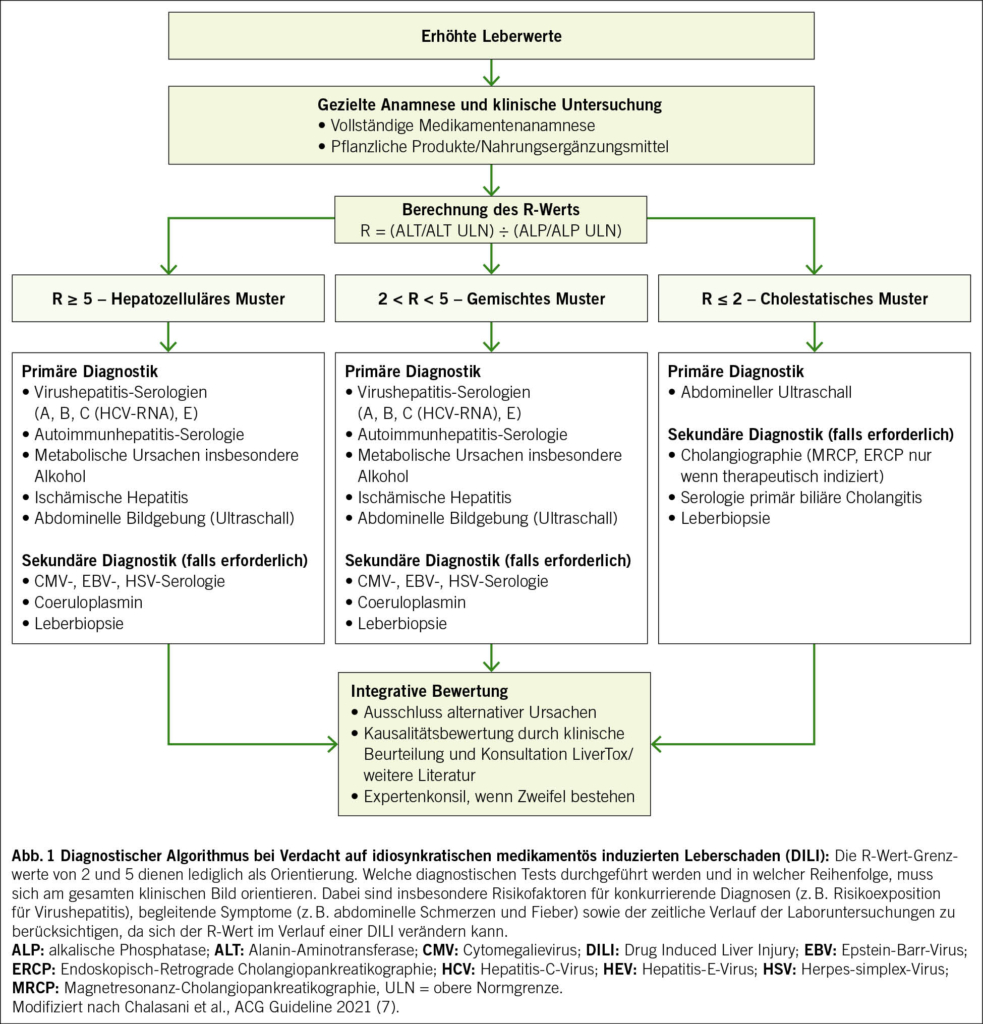
Zur weiteren Einordnung hat sich die Bestimmung des R-Werts etabliert, berechnet aus dem Verhältnis ALT/ULN zu ALP/ULN. Er erlaubt die Einteilung in hepatozelluläre (R ≥ 5), cholestatische (R ≤ 2) und gemischte Schädigungsmuster (R 2–5). Diese Klassifikation besitzt diagnostische und prognostische Relevanz. Hepatozelluläre Muster sind häufiger mit schweren Verläufen assoziiert, insbesondere bei zusätzlichem Ikterus. Cholestatische Verläufe präsentieren sich typischerweise mit Pruritus und zeigen meist einen protrahierten, insgesamt jedoch günstigeren Verlauf. Gemischte Muster vereinen Merkmale beider Entitäten. Entsprechend sollten Differenzialdiagnosen gezielt priorisiert werden, etwa virale Hepatitiden oder ischämische Leberschäden bei hepatozellulärem Muster und biliäre Obstruktionen bei cholestatischem Verlauf (7, 8). Zu beachten ist, dass einzelne Medikamente unterschiedliche Muster verursachen können. Ein strukturiertes diagnostisches Vorgehen ist in Abb. 1 dargestellt.
Therapie und Prognose
Die entscheidende therapeutische Massnahme ist das sofortige Absetzen des auslösenden Medikaments. In der Mehrzahl der Fälle kommt es innerhalb von Wochen bis Monaten zu einer vollständigen Erholung der Leberfunktion. Die Normalisierung der Leberwerte ist auch ein wichtiges Kriterium der Kausalitätsbeurteilung. Der Verlauf der Leberparameter sollte engmaschig kontrolliert werden, angepasst an Schweregrad, Schädigungsmuster und klinische Symptomatik (7, 8). Bei milder Ausprägung kann nach initialer Kontrolle nach 48–72 h und rückläufiger Tendenz eine erneute Kontrolle nach 1–2 Wochen erfolgen, während bei Ikterus oder Gerinnungsstörung eine sehr enge Überwachung erforderlich ist.
Für hepatozelluläre Schädigungsmuster mit gleichzeitigem Ikterus gilt Hy’s Law: Steigt das Gesamtbilirubin auf mehr als das Zweifache der oberen Normgrenze bei deutlich erhöhten Transaminasen, beträgt das Risiko für ein Fortschreiten bis zum akuten Leberversagen etwa 10 % (8). Auch ein rascher Transaminasenanstieg mit klinischer Verschlechterung ist als Warnsignal zu werten und erfordert die frühzeitige Überweisung an ein hepatologisches Zentrum. Bei Gerinnungsstörung oder Zeichen einer hepatischen Enzephalopathie ist eine notfallmässige Hospitalisation erforderlich. Die Indikation zur Lebertransplantation wird u. a. anhand kombinierter Kriterien wie den King’s-College- und Clichy-Kriterien geprüft.
In ausgewählten Situationen kann neben dem Absetzen des Medikaments eine spezifische Therapie notwendig sein. Eine akute Valproat-assoziierte Hepatotoxizität kann durch frühzeitige Gabe von L-Carnitin günstig beeinflusst werden. Leflunomid-induzierte Leberschäden sind meist reversibel, können jedoch selten progredient verlaufen. Aufgrund der langen Halbwertszeit kann eine Auswaschtherapie mit Cholestyramin erforderlich sein (8). Das sinusoidale Obstruktionssyndrom nach hämatologischer Stammzelltransplantation kann in ausgewählten Fällen auf Defibrotide ansprechen (17). Bei akutem Leberversagen mit hepatischer Enzephalopathie Grad 1–2 kann auch bei idiosynkratischer Hepatotoxizität eine intravenöse Gabe von NAC erwogen werden. Immunallergische Symptome stellen keine generelle Indikation für Steroide dar, bei schwerer systemischer Symptomatik kann jedoch ein zeitlich begrenzter Therapieversuch erfolgen.
Eine besondere Subgruppe ist die autoimmun-ähnliche medikamentös induzierte Hepatitis (DI-ALH), beschrieben u. a. für Minocyclin, Nitrofurantoin, Infliximab, Methyldopa oder Hydralazin. Sie weist klinische, serologische und histologische Merkmale einer Autoimmunhepatitis auf. Die Abgrenzung zur primären Autoimmunhepatitis ist diagnostisch anspruchsvoll. In den meisten Fällen bessert sich die Hepatopathie nach Absetzen des Medikaments, eine Persistenz oder Progression ist jedoch möglich. In solchen Fällen kann eine zeitlich begrenzte immunsuppressive Therapie analog zur idiopathischen Autoimmunhepatitis mit Steroiden und ggf. Azathioprin erforderlich sein. Im Gegensatz zur idiopathischen Autoimmunhepatitis treten nach Absetzen der Immunsuppression meist keine Rezidive auf, Nachkontrollen sind jedoch obligat (18).
Eine Reexposition mit einem verdächtigten hepatotoxischen Medikament sollte grundsätzlich vermieden werden, da ein rascheres und schwereres Rezidiv auftreten kann. Eine «Rechallenge» ist nur in Ausnahmefällen vertretbar, etwa bei vitaler Indikation ohne therapeutische Alternative, und erfordert eine sorgfältige Nutzen-Risiko-Abwägung sowie eine umfassende Aufklärung der Patienten (7).
Immuntherapie-vermittelte Leberschäden durch Checkpoint-Inhibitoren
Mit der zunehmenden Anwendung von Immuncheckpoint-Inhibitoren (CTLA-4-, PD-1- und PD-L1-Antikörper) haben immuntherapie-vermittelte Leberschäden deutlich an Bedeutung gewonnen. Diese durch die Interaktion des Medikaments mit dem Immunsystem bedingte Leberschädigung tritt dosisunabhängig bei etwa 1–16 % der behandelten Patienten auf. Das höchste Risiko besteht bei CTLA-4-Antikörpern, insbesondere bei Kombinationstherapien oder Hochdosisregimen (6).
Das klinische Spektrum reicht von milden Transaminasenerhöhungen bis hin zu schweren Hepatitiden mit relevanter Leberfunktionsstörung. Therapeutisch hat sich ein stufenweises Vorgehen etabliert. Bei milden Verläufen stehen engmaschige Kontrollen im Vordergrund, bei moderaten Verläufen wird eine Therapiepause empfohlen, während bei schweren Verläufen der frühzeitige Einsatz systemischer Kortikosteroide indiziert ist. Bei fehlendem Ansprechen kann eine Eskalation mit weiteren Immunsuppressiva, etwa Mycophenolat-Mofetil, erforderlich sein. Dieses Vorgehen entspricht den Empfehlungen internationaler Leitlinien (8, 19) und sollte insbesondere bei höhergradigen Verläufen frühzeitig interdisziplinär abgestimmt erfolgen. Zusätzlich können neben der Hepatopathie weitere immunvermittelte Nebenwirkungen auftreten, die in die therapeutische Gesamtstrategie einzubeziehen sind.
Pflanzliche Produkte und Nahrungsergänzungsmittel
Auch pflanzliche Produkte und Nahrungsergänzungsmittel (Herbal and Dietary Supplements, HDS) konnten als Ursache von DILI identifiziert werden. In den westlichen Ländern wurde ein deutlicher Anstieg HDS-assoziierter Leberschäden beschrieben. Nach Daten eines US-amerikanischen DILI-Registers entfallen etwa 16 % der medikamentös-toxischen Leberschäden auf HDS, während in ostasiatischen Ländern wie China, Korea und Singapur der Anteil auf 27–62 % aller DILI-Fälle geschätzt wird. Diese Präparate werden häufig zur Gewichtsreduktion, Leistungssteigerung oder allgemeinen Gesundheitsförderung eingenommen und nicht immer als relevante Medikation wahrgenommen.
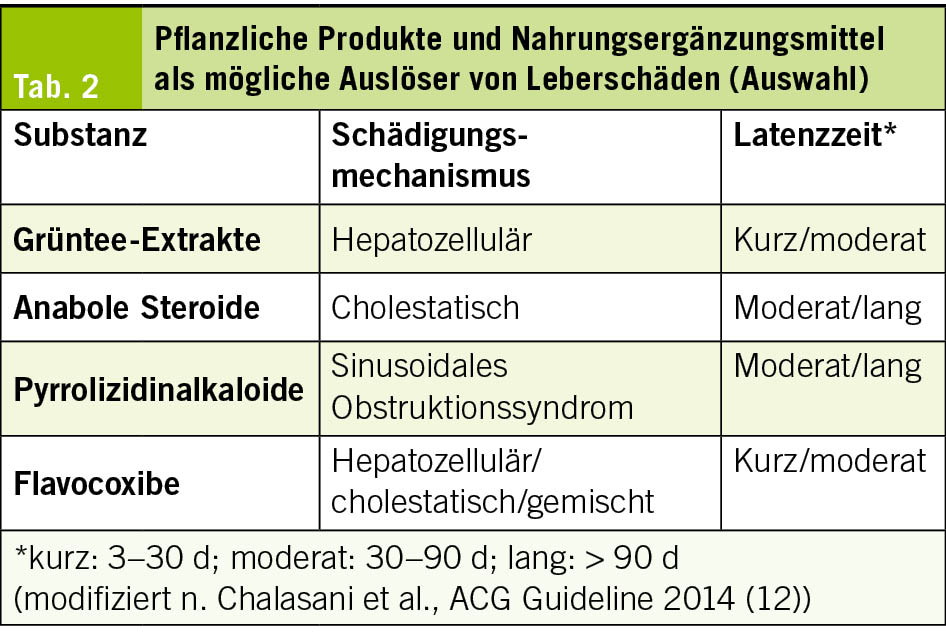
Für die Diagnostik ist eine gezielte Anamnese essenziell. Neben dem Produktnamen sollten Beginn und Dauer der Einnahme, Dosierung, Bezugsquelle sowie die gleichzeitige Einnahme weiterer Präparate erfasst werden. Viele Produkte enthalten mehrere pharmakologisch aktive Substanzen oder sind mit nicht deklarierten Inhaltsstoffen kontaminiert. Da HDS häufig nicht als «Medikamente» wahrgenommen werden, werden sie anamnestisch oft nicht spontan angegeben. Hilfreich kann es sein, Patienten zu bitten, die Präparate oder entsprechende Fotos mitzubringen. Typische Produkte sind in Tab. 2 zusammengefasst. Aktuell sind mehr als 100 Substanzen mit hepatotoxischen Wirkungen beschrieben. Zu den häufigsten Auslösern zählen anabole Steroide, Grüntee-Extrakte sowie Kombinationspräparate zur Gewichtsreduktion. Insbesondere bei pflanzlichen Mischungen ist die Identifikation der verantwortlichen Substanz schwierig. Für einzelne Stoffe bestehen jedoch charakteristische Schädigungsmuster, etwa ein prolongierter, meist selbstlimitierender Ikterus bei anabolen Steroiden oder ein sinusoidales Obstruktionssyndrom durch Pyrrolizidinalkaloide aus der traditionellen chinesischen Medizin. Die Mehrzahl der Substanzen manifestiert sich als unspezifische akute Hepatitis. Eine Übersicht potenziell hepatotoxischer Substanzen ist in der Datenbank LiverTox verfügbar (www.ncbi.nlm.nih.gov/books/NBK547852/).
Das Absetzen führt meist zur Erholung, schwere Verläufe bis hin zum akuten Leberversagen sind jedoch beschrieben (12, 20, 21).
Zusammenfassung
Medikamentös induzierte Leberschäden sind selten, aber klinisch hochrelevant. Eine strukturierte Diagnostik, frühzeitige Risikostratifizierung und das konsequente Absetzen des auslösenden Medikaments sind entscheidend für die Prognose.
Copyright
Aerzteverlag medinfo AG
Facharzt für Innere Medizin und
Gastroenterologie mit Schwerpunkt
Hepatologie (FMH) 1, 2
– Gastropark
Seestrasse 90
8002 Zürich
www.gastropark.ch
– Klinik für Gastroenterologie und Hepatologie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
christoph.juengst@hin.ch
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- DILI (Drug Induced Liver Injury) ist eine wichtige Differenzialdiagnose erhöhter Leberwerte.
- Die Paracetamol-Intoxikation ist der Prototyp des intrinsischen DILI und meist gut durch die rasche Gabe von N-Acetylcystein behandelbar.
- Idiosynkratische DILI können durch eine Vielzahl von Medikamenten ausgelöst werden, sind unvorhersehbar und erfordern eine strukturierte Ausschlussdiagnostik.
- Immuntherapie-vermittelte Leberschäden durch Checkpoint-Inhibitoren nehmen in der klinischen Praxis zu, das Vorgehen richtet sich nach dem Schweregrad der Hepatitis
- Pflanzliche Präparate und Nahrungsergänzungsmittel sind eine relevante und häufig übersehene Ursache von DILI.
1. Sgro C, Clinard F, Ouazir K, Chanay H, Allard C, Guilleminet C, u. a. Incidence of drug-induced hepatic injuries: a French population-based study. Hepatol Baltim Md. August 2002;36(2):451–5.
2. Björnsson ES, Bergmann OM, Björnsson HK, Kvaran RB, Olafsson S. Incidence, presentation, and outcomes in patients with drug-induced liver injury in the general population of Iceland. Gastroenterology. Juni 2013;144(7):1419–25, 1425.e1-3; quiz e19-20.
3. Hoofnagle JH, Björnsson ES. Drug-Induced Liver Injury – Types and Phenotypes. N Engl J Med. 18. Juli 2019;381(3):264–73.
4. Stravitz RT, Lee WM. Acute liver failure. Lancet Lond Engl. 7. September 2019;394(10201):869–81.
5. Andrade RJ, Chalasani N, Björnsson ES, Suzuki A, Kullak-Ublick GA, Watkins PB, u. a. Drug-induced liver injury. Nat Rev Dis Primer. 22. August 2019;5(1):58.
6. Peeraphatdit TB, Wang J, Odenwald MA, Hu S, Hart J, Charlton MR. Hepatotoxicity From Immune Checkpoint Inhibitors: A Systematic Review and Management Recommendation. Hepatol Baltim Md. Juli 2020;72(1):315–29.
7. Chalasani NP, Maddur H, Russo MW, Wong RJ, Reddy KR, Practice Parameters Committee of the American College of Gastroenterology. ACG Clinical Guideline: Diagnosis and Management of Idiosyncratic Drug-Induced Liver Injury. Am J Gastroenterol. 1. Mai 2021;116(5):878–98.
8. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Drug-induced liver injury. J Hepatol. Juni 2019;70(6):1222–61.
9. Ramachandran A, Jaeschke H. Acetaminophen hepatotoxicity: A mitochondrial perspective. Adv Pharmacol San Diego Calif. 2019;85:195–219.
10. Faber K, Reichert C, Rauber-Lüthy Ch. Akute Paracetamolvergiftung. toxinfo suisse 08 2020.
11. Faber K, Reichert C, Rauber-Lüthy Ch. Paracetamolvergiftung: Wiederholte Einnahme. toxinfo suisse 08 2020.
12. Chalasani NP, Hayashi PH, Bonkovsky HL, Navarro VJ, Lee WM, Fontana RJ, u. a. ACG Clinical Guideline: the diagnosis and management of idiosyncratic drug-induced liver injury. Am J Gastroenterol. Juli 2014;109(7):950–66; quiz 967.
13. Fontana RJ, Liou I, Reuben A, Suzuki A, Fiel MI, Lee W, u. a. AASLD practice guidance on drug, herbal, and dietary supplement–induced liver injury. Hepatol Baltim Md. März 2023;77(3):1036–65.
14. Daly AK, Donaldson PT, Bhatnagar P, Shen Y, Pe’er I, Floratos A, u. a. HLA-B*5701 genotype is a major determinant of drug-induced liver injury due to flucloxacillin. Nat Genet. Juli 2009;41(7):816–9.
15. Urban TJ, Daly AK, Aithal GP. Genetic basis of drug-induced liver injury: present and future. Semin Liver Dis. Mai 2014;34(2):123–33.
16. Björnsson ES, Stephens C, Atallah E, Robles-Diaz M, Alvarez-Alvarez I, Gerbes A, u. a. A new framework for advancing in drug-induced liver injury research. The Prospective European DILI Registry. Liver Int Off J Int Assoc Study Liver. Januar 2023;43(1):115–26.
17. Richardson PG, Riches ML, Kernan NA, Brochstein JA, Mineishi S, Termuhlen AM, u. a. Phase 3 trial of defibrotide for the treatment of severe veno-occlusive disease and multi-organ failure. Blood. 31. März 2016;127(13):1656–65.
18. Andrade RJ, Aithal GP, de Boer YS, Liberal R, Gerbes A, Regev A, u. a. Nomenclature, diagnosis and management of drug-induced autoimmune-like hepatitis (DI-ALH): An expert opinion meeting report. J Hepatol. September 2023;79(3):853–66.
19. Haanen J, Obeid M, Spain L, Carbonnel F, Wang Y, Robert C, u. a. Management of toxicities from immunotherapy: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol Off J Eur Soc Med Oncol. Dezember 2022;33(12):1217–38.
20. Navarro VJ, Khan I, Björnsson E, Seeff LB, Serrano J, Hoofnagle JH. Liver injury from herbal and dietary supplements. Hepatol Baltim Md. Januar 2017;65(1):363–73.
21. Zheng E, Sandhu N, Navarro V. Drug-induced Liver Injury Secondary to Herbal and Dietary Supplements. Clin Liver Dis. Februar 2020;24(1):141–55.
der informierte @rzt
- Vol. 16
- Ausgabe 2
- Februar 2026