- Neue Anti-Amyloid-Therapien bei Alzheimer: Was Sie jetzt wissen müssen
Demenzen werden in der Schweiz immer häufiger und zählen zu den führenden Todesursachen. Sie gehören zu den wichtigsten Erkrankungen hinsichtlich verlorener Lebensjahre, da sie reduzierte Lebenserwartung und krankheitsbedingten Verlust an Lebensqualität kombinieren. Die Alzheimer-Krankheit ist mit rund zwei Dritteln aller Fälle die häufigste Ursache einer Demenz. Mit Lecanemab und Donanemab stehen erstmals krankheitsmodifizierende Therapien zur Verfügung, die pathologisches Amyloid-β – ein Protein, das sich bei Alzheimer krankhaft im Gehirn ablagert – gezielt entfernen und den Krankheitsverlauf verlangsamen. Dieser Wandel von rein symptomatischer zu ursächlich wirksamer Behandlung rückt die Früherkennung und präzise Patientenselektion noch stärker in den Vordergrund. Hausärzt/-innen spielen dabei eine entscheidende Rolle, indem sie früheste kognitive Störungen erkennen und Betroffene bei Verdacht auf eine Alzheimer-Krankheit rasch an eine Memory Clinic überweisen. Ein dichtes Netz spezialisierter Memory Clinics sowie einheitliche nationale Empfehlungen sichern in der Schweiz eine koordinierte und leitliniengerechte Einführung dieser neuen Therapien, sobald eine Zulassung auch in der Schweiz erfolgt ist. Die neuen monoklonalen Antikörper stellen einen echten Fortschritt in der Alzheimer-Therapie dar. Sie eröffnen Patient/-innen im Frühstadium erstmals die Möglichkeit, den Krankheitsverlauf zu beeinflussen. Damit gewinnt das Prinzip «time is brain» auch in der Alzheimer-Diagnostik und -Therapie an Bedeutung.
Dementia is becoming increasingly common in Switzerland and is one of the leading causes of death. It is one of the most significant diseases in terms of years of healthy life lost, as it combines reduced life expectancy with a disease-related loss of quality of life. Alzheimer’s disease is the most common cause of dementia, accounting for around two-thirds of all cases. Lecanemab and donanemab are the first disease-modifying therapies available that specifically remove pathological amyloid-ß – a protein that accumulates abnormally in the brain in Alzheimer’s disease – and slow the progression of the disease. This shift from purely symptomatic to causally effective treatment places even greater emphasis on early detection and precise patient selection. Family doctors play a crucial role in this by recognizing the earliest cognitive disorders and quickly referring those affected to a memory clinic if Alzheimer’s disease is suspected. A dense network of specialized memory clinics and uniform national recommendations ensure the coordinated and guideline-compliant introduction of these new therapies in Switzerland as soon as they are approved there. The new monoclonal antibodies represent a real advance in Alzheimer’s therapy. For the first time, they offer patients in the early stages the opportunity to influence the course of the disease. This means that the principle of «time is brain» is also gaining importance in Alzheimer’s diagnosis and therapy.
Keywords: Alzheimer-Krankheit, Anti-Amyloid-Antikörper (Lecanemab/Donanemab), ARIA und MRT-Monitoring
Die Alzheimer-Krankheit ist die häufigste Ursache einer Demenz. Sie nimmt auch in der Schweiz weiter zu und verursacht bereits heute Kosten in Milliardenhöhe. Angesichts der schweren Belastung von Patient/-innen und Angehörigen durch den fortschreitenden Verlust von Selbstständigkeit, Pflegebedürftigkeit und verminderter Lebensqualität besteht ein enormer Bedarf an neuen Therapien, die den Krankheitsverlauf verlangsamen. Was bei Multipler Sklerose oder Krebserkrankungen längst selbstverständlich ist, wird nun auch in der Therapie der Alzheimer-Krankheit Realität: krankheitsmodifizierende Behandlungen. Erstmals stehen monoklonale Antikörper zur Verfügung, die pathologisches Amyloid-β (Aβ) gezielt entfernen und den Krankheitsverlauf nachweislich verlangsamen. Das markiert einen Paradigmenwechsel und rückt die Früherkennung sowie die präzise Patientenauswahl stärker in den Fokus.
Diagnostik und Therapie der Alzheimer-Krankheit in der Schweiz
Die Schweiz verfügt im internationalen Vergleich über ein hervorragendes Netzwerk an Memory Clinics, welche in Zusammenarbeit mit den Hausärzt/-innen sowie weiteren Fachspezialist/-innen die Versorgung der Menschen mit Demenz auf hohem Niveau sicherstellen. Im Verein Swiss Memory Clinics (SMC) sind alle grösseren Memory Clinics der Schweiz (aktuell: 54) organisiert. Alle Mitglieder folgen den gleichen Empfehlungen zur Diagnostik und Therapie, so dass schweizweit ein hoher einheitlicher Standard gewährleistet werden kann, wobei die regionalen Besonderheiten dennoch sehr gut berücksichtigt werden können. Mit der Verfügbarkeit krankheitsmodifizierender Therapien verschiebt sich die Schwelle für eine Überweisung. Ein abwartendes Vorgehen mit Kontrolle nach mehreren Monaten kann heute dazu führen, dass das therapeutische Zeitfenster verpasst wird. Bei neuen kognitiven Beschwerden im Frühstadium sollte daher die zeitnahe Abklärung in einer Memory Clinic niedrigschwellig erfolgen.
Unter der Leitung von SMC wurden in den vergangenen Jahren diverse Empfehlungen publiziert, welche in übersichtlicher Form im Internet frei zugänglich sind (https://www.swissmemoryclinics.ch/qualitaetsentwicklung/qualitaetsstandards/). Es existieren Empfehlungen für die Diagnostik von Demenzerkrankungen in der Schweiz (1, 2), ergänzt durch spezialisierte Empfehlungen für den Einsatz von Biomarkern (3) und PET-Diagnostik (4). 2024 wurden im Auftrag des Bundesamtes für Gesundheit (BAG) Empfehlungen für die Therapie der Demenz in der Schweiz publiziert (5), zudem unter der Führung der Schweizerischen Gesellschaft für Alterspsychiatrie (SGAP) spezifische Empfehlungen für die Therapie von Verhaltenssymptomen (BPSD) (6) und zuletzt auch Anwendungsempfehlungen für die neuen Anti-Amyloid-Antikörper (7).
Aβ als therapeutisches Ziel bei Alzheimer
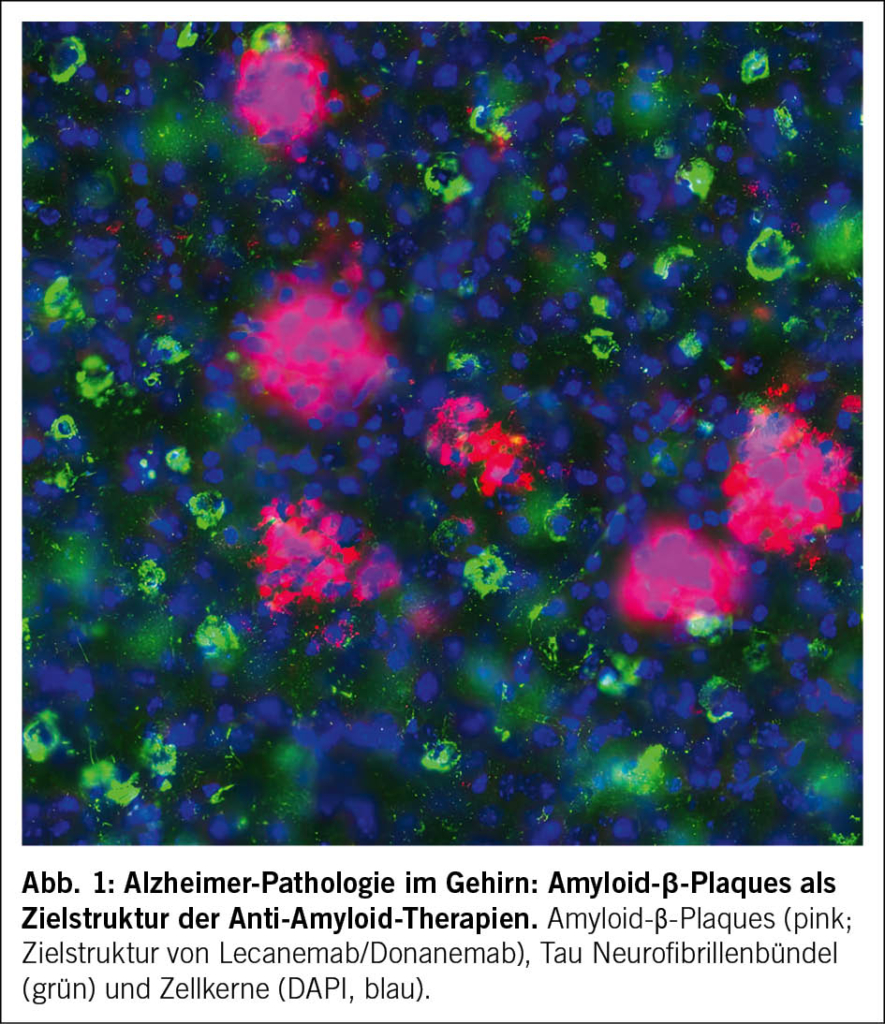
Amyloid (Aβ) und Tau sind die zentralen pathologischen Proteine der Alzheimer-Krankheit. Ihre Ablagerungen in Form von extrazellulären Aβ-Plaques und intrazellulären Tau-Neurofibrillenbündeln schädigen Synapsen und Nervenzellen und treiben die Neurodegeneration voran (8). Diese beiden typischen Proteinablagerungen (Aβ‑Plaques und Tau‑Neurofibrillenbündel) sind in Abb. 1 dargestellt. Die zentrale Rolle von Aβ wird durch genetische Befunde gestützt. Mutationen in den Genen, die an der Aβ-Produktion beteiligt sind, führen zu familiären, früh einsetzenden Formen der Erkrankung, während Varianten, die die Bildung von Aβ verringern, das Erkrankungsrisiko senken (9, 10).
Monoklonale Antikörper gegen Aβ – Wirkprinzip und klinische Bedeutung
Lecanemab ist ein humanisierter monoklonaler Antikörper, der gezielt lösliche protofibrilläre Aβ-Spezies bindet. Diese löslichen Aggregate gelten als besonders neurotoxisch, da sie früh synaptische Dysfunktion auslösen und zur Aktivierung von Mikroglia beitragen (11, 12). Neuere Daten zeigen zudem, dass Lecanemab auch fibrilläres (plaquegebundenes) Aβ bindet (13). Donanemab bindet bevorzugt N-terminal pyroglutamat-modifiziertes Aβ, eine besonders stabile Spezies, die in reifen Plaques angereichert ist. Durch die Bindung fördert Donanemab die Mikroglia-vermittelte Plaque Clearance, was zu einer Reduktion der Plaquelast führt (14).
Lecanemab und Donanemab sind inzwischen in zahlreichen Ländern zugelassen, teils beide, teils nur eine der Substanzen. Die Entscheidung der Swissmedic für die Schweiz steht aktuell (Stand Dezember 2025) noch aus. Diese neuen Therapien markieren einen wichtigen Fortschritt, ersetzen jedoch nicht die bestehenden symptomatischen Behandlungen (Cholinesterasehemmer und Memantin), die weiterhin konsequent angewendet werden sollten. Sie bilden nach wie vor die Grundlage einer modernen, ganzheitlichen Alzheimer-Therapie.
Lecanemab
In der Phase-3-Studie Clarity-AD wurde Lecanemab bei 1795 Personen mit früher Alzheimer-Krankheit, definiert als leichte kognitive Störung oder milde Demenz bei nachgewiesener Aβ-Positivität, untersucht (15). Die Teilnehmenden erhielten 10 mg/kg Lecanemab intravenös alle zwei Wochen oder Placebo über 18 Monate. Lecanemab reduzierte die Aβ-Plaques im Gehirn deutlich, im PET war bei vielen Patient/-innen eine nahezu vollständige Entfernung nachweisbar.
Der primäre klinische Endpunkt, die Veränderung der Clinical Dementia Rating – Sum of Boxes (CDR-SB), einer Skala zur Bewertung kognitiver und alltagspraktischer Fähigkeiten, zeigte eine 0.45-Punkte geringere Zunahme als unter Placebo (p < 0.001), entsprechend einer Verlangsamung der Krankheitsprogression um 27 %. Dies entspricht grob einer Verzögerung um fünf bis sechs Monate über 18 Monate, also einem späteren Übergang in ein schwereres klinisches Stadium. Die Number Needed to Treat (NNT, bezogen auf Verschlechterung im CDR‑Global über 18 Monate) lag bei rund 13 (17). Das heisst: Von 100 vergleichbaren Patient/-innen zeigen über 18 Monate etwa 8 weniger eine solche Verschlechterung als unter Placebo. Auch die sekundären Endpunkte, die die Gedächtnisleistung, die Denkgeschwindigkeit und die Alltagsfunktionen abbilden (z. B. ADAS-Cog14, ADCOMS, ADCS-MCI-ADL), fielen konsistent zugunsten von Lecanemab aus. In einigen Analysen zeigten sich zudem Vorteile in von Patient/-innen und Angehörigen berichteten Endpunkten zur Lebensqualität und Belastung (EQ 5D, QoL AD und das Zarit Burden Interview) (16). Biomarkeranalysen zeigten eine Abnahme von p-Tau181 (CSF und Plasma) und des glialen Aktivierungsmarkers GFAP, während NfL unverändert blieb.
Langzeitdaten über 48 Monate aus einer offenen Verlängerungsphase (18) deuten auf einen anhaltenden klinischen Vorteil hin. Im Vergleich zur unbehandelten ADNI- Kohorte war das Risiko, in ein fortgeschritteneres Krankheitsstadium überzugehen, um 34 %, und das Risiko, von einer leichten kognitiven Störung in eine Alzheimer-Demenz überzutreten, um 56 % reduziert. Etwa die Hälfte der Behandelten zeigte über vier Jahre keinen messbaren kognitiven Abfall.
Donanemab
In der Phase-3-Studie TRAILBLAZER-ALZ-2 wurde Donanemab bei 1736 Personen mit früher Alzheimer-Krankheit (leichte kognitive Störung oder milde Demenz) über 18 Monate untersucht (19). Die Teilnehmenden erhielten Donanemab intravenös einmal monatlich oder Placebo; in den ersten drei Zyklen wurden 700 mg verabreicht, danach 1400 mg bis Studienende. Die Teilnehmenden wurden anhand der Tau-Pathologie im Tau-PET in Gruppen mit niedriger/mittlerer und hoher Tau-Belastung eingeteilt. Donanemab reduzierte die Aβ-Plaques im Gehirn deutlich. Bereits nach 24 Wochen war bei über einem Drittel der Behandelten keine Plaques mehr nachweisbar, nach 18 Monaten bei mehr als 80 %.
In der Gruppe mit niedriger/mittlerer Tau-Belastung verlangsamte Donanemab die Krankheitsprogression hinsichtlich des primären Endpunktes (iADRS, kombiniert Kognition und Alltagsfunktionen) um 35 % gegenüber Placebo. Dies entspricht einer Verzögerung der Krankheitsprogression um rund fünf bis sechs Monate über 18 Monate sowie einer NNT (bezogen auf Verschlechterung im CDR‑Global über 18 Monate) von etwa 10 (17). Das heisst: Von 100 vergleichbaren Patient/-innen zeigen über 18 Monate etwa 10 weniger eine solche Verschlechterung als unter Placebo. Der Nutzen war am grössten bei niedriger oder mittlerer Tau-Belastung; bei fortgeschrittener Tau-Pathologie fiel er geringer aus. Auch die sekundären Endpunkte (CDR-SB, ADCS-iADL, ADAS-Cog13) zeigten eine konsistente Verlangsamung kognitiver und funktioneller Einbussen unter Donanemab. Begleitende Biomarkeranalysen belegten eine deutliche Abnahme von Plasma-p-Tau217 sowie eine stabile oder rückläufige Tau-PET-Signalintensität, was auf eine reduzierte Tau-Propagation hindeuten könnte.
Hervorzuheben ist der treat-to-target-Ansatz. Donanemab wird dabei so lange gegeben, bis im Amyloid-PET keine oder nur noch eine minimale Plaquelast nachweisbar ist, und kann dann pausiert oder beendet werden. In den bisherigen Verlaufsdaten blieb der klinische Vorteil nach Erreichen dieses Ziels über den beobachteten Zeitraum erhalten. Langzeitdaten über bis zu 36 Monate deuten darauf hin, dass sich der Abstand zu unbehandelten Beobachtungskohorten (z. B. ADNI) weiter vergrösserte (20); der Unterschied im CDR-SB nahm von 0.6 nach 18 Monaten auf 1.2 Punkte nach 36 Monaten zu. Eine frühe Behandlung reduzierte damit das Risiko einer klinischen Progression um 27 %.
Wirksamkeit in der Praxis
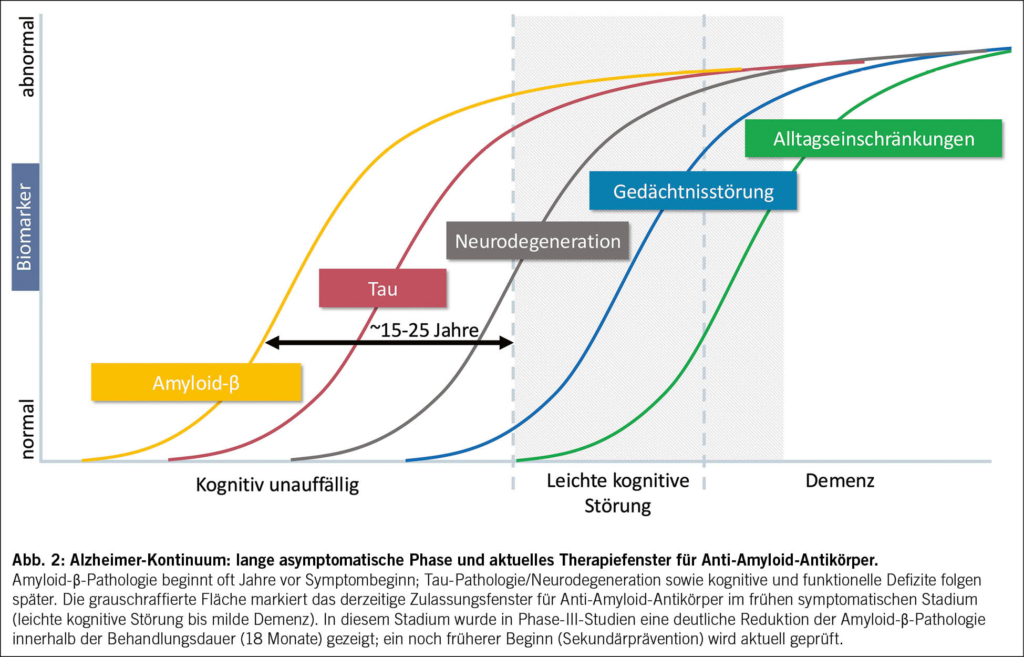
Lecanemab und Donanemab verlangsamen somit den klinischen Verlauf von Alzheimer um etwa ein Viertel bis ein Drittel, was einem Zeitgewinn von rund sechs Monaten über 18 Monate entspricht. Der grösste Nutzen wird bei Patient/-innen im Frühstadium einer Alzheimer-Krankheit erzielt, weshalb eine biomarkerbasierte Frühdiagnostik entscheidend ist. Mit einer NNT von etwa 10 bis 13 und einer Verzögerung des klinischen Verlaufs um 27–36 % liegen die Effektstärken dieser Antikörper in einer ähnlichen Grössenordnung wie jene etablierter Biologika bei anderen chronischen Erkrankungen, etwa bei Multipler Sklerose, Rheumatoider Arthritis oder onkologischen Erkrankungen (25). Angesichts der hohen gesellschaftlichen und pflegerischen Belastung durch Demenz dürfte eine Verzögerung der Krankheitsprogression auch ökonomisch relevant sein. Gleichzeitig wird nur ein kleiner Anteil der Patient/-innen die Kriterien für eine Antikörpertherapie erfüllen (22). Zu beachten ist, dass ein relevanter Teil der Patient/-innen, die aktiv eine Antikörpertherapie anstreben, bei Erstkontakt bereits zu weit fortgeschritten und damit nicht mehr geeignet ist. (26). Für die grosse Mehrheit bleibt eine strukturierte postdiagnostische Versorgung mit Beratung, Behandlung von Begleiterkrankungen und Angehörigenunterstützung zentral. Das Krankheitskontinuum und das derzeitige (internationale) Zulassungsfenster der Anti‑Amyloid‑Antikörper sind in Abb. 2 schematisch dargestellt.
Indikation, Durchführung und Monitoring
Lecanemab und Donanemab sind in der Schweiz derzeit noch nicht zugelassen (Stand Dezember 2025). Für die klinische Vorbereitung dienen die europäischen Zulassungen, internationale Appropriate Use Criteria (22, 23) und die Empfehlungen der Swiss Memory Clinics (7) als Orientierung. Beide Therapien sind für Menschen im Frühstadium der Alzheimer-Krankheit vorgesehen, das heisst bei leichter kognitiver Störung oder milder Demenz im Rahmen einer Alzheimer-Krankheit, wenn eine Aβ-Pathologie nachgewiesen ist und das zerebrale MRT keine relevanten Blutungen, keine superfizielle Siderose und keine ausgeprägte Mikroangiopathie zeigt. Der Nachweis einer Aβ-Pathologie kann über Liquorbiomarker (Aβ42/40-Ratio, p-Tau) oder ein Amyloid-PET erfolgen. Bluttests wie p-Tau217 gewinnen an Bedeutung, sind derzeit aber nur als ergänzende Nachweismethode geeignet. In der Praxis sind grenzwertige Befunde und Unterschiede zwischen Testplattformen zu berücksichtigen, weshalb Blutmarker derzeit vor allem zur gezielten Triage und zur Ergänzung, nicht als alleinige Bestätigung dienen sollten. Da das Risiko für Nebenwirkungen vom APOE-Genotyp abhängt, sollte dieser vor Therapiebeginn bestimmt und besprochen werden. In der EU und in Grossbritannien sind homozygote APOE-ε4-Trägerinnen und -Träger wegen des höheren ARIA-Risikos derzeit nicht zugelassen. Dabei ist zu beachten, dass die ApoE-Genotypisierung lebenslange Risikoinformationen berührt und auch für Angehörige relevant sein kann. Patient/-innen unterscheiden sich deutlich in ihrer Präferenz, genetische Risikoinformationen zu kennen, weshalb eine strukturierte Aufklärung und bei Bedarf genetische Beratung wichtig ist. Eine orale Antikoagulation sowie mehr als vier Mikroblutungen oder eine superfizielle Siderose im MRT schliessen die Therapie aus. Eine Monotherapie mit Thrombozyten-aggregationshemmern (z. B. ASS) ist in der Regel möglich; für eine duale Plättchenhemmung liegen bislang zu wenige Daten vor.
Lecanemab wird alle zwei Wochen als intravenöse Infusion verabreicht (10 mg/kg Körpergewicht, über etwa eine Stunde).
Donanemab wird einmal monatlich über etwa 30 Minuten intravenös infundiert. In der Phase-3-Studie (TRAILBLAZER-ALZ-2) erhielten die Teilnehmenden 700 mg Donanemab für die ersten drei Gaben und anschliessend 1400 mg alle vier Wochen bis Woche 72. In der nachfolgenden TRAILBLAZER-ALZ-6-Studie wurde ein langsames Titrationsschema getestet (350 → 700 → 1050 → 1400 mg), das die Häufigkeit von ARIA-E deutlich senkte bei unveränderter Aβ-Reduktion (24).
In den ersten Zyklen ist bei beiden Therapien eine etwas längere Überwachung vorgesehen, da zu Beginn bei 20–30 % milde Reaktionen auftreten können (z. B. Kopfschmerz, Schüttelfrost, Blutdruckanstieg). Die Behandlung wird beendet, wenn die Erkrankung in eine Demenz mittleren Schweregrades übergeht.
Für beide Anti‑Amyloid‑Therapien ist ein strukturiertes MRT‑Monitoring zur ARIA-Früherkennung obligat; die empfohlenen Zeitpunkte sind jedoch substanzspezifisch. Vor Therapiebeginn ist ein Baseline‑MRT (in der Regel innerhalb der letzten 6 Monate) erforderlich, um vorbestehende Mikroblutungen (insbesondere >4), eine superfizielle Siderose oder relevante Leukoenzephalopathie auszuschliessen. Unter Lecanemab sind gemäss EU‑Fachinformation Kontroll‑MRTs vor der 3., 5., 7. und 14. Gabe vorgesehen; bei Symptomen, die an ARIA denken lassen, sollen jederzeit zusätzliche MRTs erfolgen. Unter Donanemab erfolgen neben dem Baseline-MRT weitere Kontrollen vor der 2., 3., 4. und 7. Gabe; ein zusätzliches MRT nach einem Jahr Therapie (vor der 12. Infusion) ist bei erhöhtem ARIA‑Risiko (z. B. ApoE ε4‑Heterozygotie) und/oder nach vorausgegangenen ARIA‑Ereignissen empfohlen. Die Verlaufskontrollen sollten möglichst am gleichen Scanner und mit identischem Sequenzprotokoll (wenn verfügbar 3‑Tesla) erfolgen, um subtile Veränderungen zuverlässig zu erkennen. Donanemab kann im Rahmen des treat‑to‑target-Ansatzes nach dokumentierter Amyloid‑Clearance pausiert oder beendet werden; gemäss EU‑Zulassung soll die Behandlungsdauer 18 Monate nicht überschreiten.
Nebenwirkungen und Sicherheit
Die neuen krankheitsmodifizierenden Therapien gelten insgesamt als gut verträglich, erfordern jedoch ein strukturiertes Monitoring. Die Aufklärung und Einwilligung sind im Frühstadium nicht trivial, weil Nutzen und Risiken moderat bis relevant sind und die Behandlung für Patient/-innen und Angehörige durch regelmässige Infusionen und MRT-Monitoring belastend sein kann. Zusätzlich kann fehlende Krankheitseinsicht die gemeinsame Entscheidungsfindung erschweren, weshalb eine besonders personenzentrierte Kommunikation und die Einbindung von Angehörigen wichtig sind. Die klinisch wichtigsten Nebenwirkungen sind Infusionsreaktionen und Amyloid-bezogenen Bildgebungsanomalien (amyloid-related imaging abnormalities, ARIA).
Infusionsreaktionen treten vor allem zu Beginn der Behandlung auf, insbesondere in den ersten Infusionszyklen. In den Phase‑III‑Studien wurden akute Infusionsreaktionen unter Lecanemab bei etwa 1 von 4, unter Donanemab bei etwa 1 von 13 Behandelten beobachtet; schwere Reaktionen waren selten (~1.2 % unter Lecanemab, 0.3 % unter Donanemab). Real-World-Daten bestätigen diese Häufigkeit und zeigen, dass Infusionsreaktionen auch ausserhalb von Studien meist mild bis moderat verlaufen (Kopfschmerz, Schüttelfrost, Übelkeit oder Blutdruckanstieg) und gut beherrschbar sind (21, 26). Sie bessern meist nach kurzzeitiger Unterbrechung der Infusion oder symptomatischer Behandlung (z. B. Paracetamol, Antihistaminikum). Eine Standard-Prämedikation mit Antihistaminikum und Paracetamol kann das Risiko zusätzlich senken. Schwere Reaktionen oder Anaphylaxien sind selten (~ 1 %).
ARIA entstehen durch vorübergehende Flüssigkeitseinlagerungen oder Mikroblutungen im Gehirn. Diese sind im MRT gut zu erkennen, weshalb im Verlauf der Behandlung regelmässige MRT-Kontrollen erforderlich sind. Man unterscheidet ARIA-E («E» für edema), die auf vasogene Schwellungen hinweist, und ARIA-H («H» für haemorrhage), die Mikroblutungen oder Hämosiderinablagerungen im MRT beschreibt. ARIA können in Einzelfällen Symptome wie z. B. Kopfschmerzen, Schwindel, Sehstörungen oder Gangunsicherheit verursachen und sind in den meisten Fällen reversibel; seltene schwere Verläufe sind jedoch klinisch relevant und müssen konsequent behandelt werden. Die «80–80–80‑Regel» ist für die Aufklärung hilfreich: Rund 80 % der ARIA treten innerhalb der ersten vier Monate auf, etwa 80 % verlaufen ohne Symptome, und etwa 80 % bilden sich innerhalb von vier Monaten vollständig zurück (17). Das Risiko ist erhöht bei Träger/-innen des APOE-ε4-Gens, insbesondere bei homozygoten Personen, weshalb diese Gruppe in Europa und Grossbritannien derzeit nicht behandelt wird. In einer US-Kohorte lag die ARIA-Häufigkeit bei 44 % der homozygoten, 24 % der heterozygoten und 15 % der nicht-Träger (21). Daher sollte der APOE-Genotyp vor Therapiebeginn bestimmt und mit den Patient/-innen besprochen werden.
In ersten Real-World-Analysen zeigte sich ein vergleichbares Sicherheitsprofil. In einer israelischen Kohorte (n = 86) trat ARIA bei rund 19 % der Behandelten auf, überwiegend mild und asymptomatisch; nur eine Patientin benötigte eine kurzfristige Steroidtherapie (27). In einer Kohorte der Washington University (n = 234) lag die Häufigkeit bei etwa 22 %; die meisten Fälle waren leicht ausgeprägt, 5–6 % symptomatisch, 1 % schwer, ohne Todesfälle oder Makroblutungen (21). Schwere ARIA-Verläufe oder Hirnblutungen >1 cm erfordern den dauerhaften Therapieabbruch. Bei milden oder moderaten Veränderungen kann die Behandlung hingegen nach deren Abklingen in der Regel fortgesetzt werden.
Für die Praxis entscheidend ist die Unterscheidung zwischen ARIA und einem Schlaganfall. Wenn ein Patient unter Antikörpertherapie plötzlich fokal-neurologische Symptome zeigt, wie etwa eine Sprachstörung, Lähmung oder Sehstörung, sollte umgehend ein zerebrales MRT veranlasst werden, nicht nur ein CT, da frühe ARIA-Veränderungen sonst übersehen werden können. Eine intravenöse Thrombolyse ist während einer Antikörpertherapie mit hohen Risiken verbunden, da das Blutungsrisiko deutlich erhöht ist; eine mechanische Thrombektomie ist die Methode der Wahl, sofern eine Gefässokklusion gesichert ist.
Eine Antikoagulation sollte vermieden werden, da sie das Risiko schwerer Hirnblutungen erhöht. Eine einfache Thrombozytenhemmung (z. B. ASS) ist in der Regel möglich, eine duale sollte jedoch nach Möglichkeit unterbleiben. Hypertonie ist ein relevanter modifizierbarer ARIA‑Risikofaktor (mittlerer arterieller Druck >107 mmHg), daher trägt eine konsequente Blutdruckkontrolle wesentlich zur Reduktion des ARIA-Risikos bei (17, 23). Patient/-innen sollten stets eine patient alert card mitführen, die in Notfallsituationen auf die laufende Therapie hinweist.
Zuletzt wird in der Bildgebung gelegentlich eine scheinbare Hirnvolumenabnahme beobachtet (amyloid-related pseudoatrophy). Diese gilt als Folge des Amyloid-Abtransports und der Rückbildung lokaler Entzündungsreaktionen und wird derzeit nicht notwendigerweise als Ausdruck zusätzlicher Schädigung interpretiert (28).
Fazit für die Praxis
Für die ärztliche Praxis ist entscheidend, mögliche Warnzeichen einer ARIA früh zu erkennen und bei Verdacht sofort Kontakt mit der behandelnden Memory Clinic oder dem neurologischen Notfalldienst aufzunehmen. Neu auftretende Symptome wie Kopfschmerzen, Schwindel, Gangunsicherheit, Sehstörungen, Sprachstörungen oder Krampfanfälle erfordern umgehend ein MRT, da ein CT frühe Veränderungen häufig nicht erfasst. Patient/-innen und Angehörige müssen darüber aufgeklärt sein, bei solchen Symptomen unverzüglich die Memory Clinic oder die Notfallambulanz zu kontaktieren. In den bislang publizierten Real‑World‑Erfahrungen zeigten sich keine neuen Sicherheitssignale; die ARIA‑Raten lagen nicht über den in den Zulassungsstudien beobachteten.
Antikoagulation sollte vermieden werden, und eine konsequente Blutdruckkontrolle senkt das Risiko für ARIA deutlich. Bei akuten Schlaganfallsymptomen sollte keine i.v.-Thrombolyse erfolgen, während eine mechanische Thrombektomie bei gesicherter Gefässokklusion in Betracht gezogen werden kann. Patient/-innen sollten stets eine patient alert card mitführen, und die laufende Therapie sollte in der Praxisdokumentation vermerkt sein, damit im Notfall rasch reagiert werden kann. ARIA treten unter Anti‑Amyloid‑Therapien in der Grössenordnung von ~20 % auf; in Zulassungsstudien lagen die Raten je nach Antikörper und Dosierung höher, während frühe Real‑World‑Kohorten bislang um ~20 % berichten. Meist sind ARIA asymptomatisch/mild und reversibel, selten schwer. Infusionsreaktionen sind in der Regel ebenfalls mild und lassen sich durch eine Prämedikation mit Antihistaminikum und Paracetamol gut vermeiden. Real-World-Daten sprechen dafür, dass die Therapien bei konsequentem Monitoring insgesamt sicher und gut handhabbar sind.
Zusammenfassung
Neue krankheitsmodifizierende Therapien markieren einen Wendepunkt in der Alzheimer-Behandlung. Der Weg dahin war lang und von Rückschlägen geprägt. Abb. 3 ordnet die heutigen Anti-Amyloid-Therapien in die wichtigsten Meilensteine ein, von der Erstbeschreibung der Alzheimer‑Krankheit über die Identifikation von Aβ bis zum präklinischen Proof‑of‑concept einer anti-Aβ‑Immunisierung (29) und den zuletzt erfolgreichen Phase‑III‑Studien mit ersten internationalen Zulassungen. Zwischen dem ersten Plaque‑Clearing im Tiermodell und der klinischen Anwendung beim Menschen lagen demnach über zwei Jahrzehnte. Erste Erfahrungen aus Ländern mit bereits zugelassenen Antikörpern zeigen, dass die Anwendung in spezialisierten Memory Clinics sicher und effektiv möglich ist, bei gleichzeitig ähnlichen oder sogar geringeren Nebenwirkungsraten als in den Zulassungsstudien (21). Entscheidend bleiben die sorgfältige Patientenselektion, die enge interdisziplinäre Zusammenarbeit und ein strukturiertes Monitoring. Direkte Head‑to‑Head‑Vergleichsstudien fehlen; die derzeitigen Sicherheits‑ und Wirksamkeitsvergleiche zwischen Lecanemab und Donanemab beruhen auf indirekten Vergleichen und sind daher mit methodischer Unsicherheit behaftet. Für die Umsetzung sind neben den Medikamentenkosten vor allem Infrastruktur und Personal relevant, etwa für regelmässige Infusionen, häufige MRT-Kontrollen, Biomarkerbestätigung, ApoE-Testung und Beratung. Diese Investitionen müssen so geplant werden, dass andere zentrale Bereiche der Demenzversorgung nicht verdrängt werden. Je früher eine geeignete Therapie bei passenden Patient/-innen beginnt, desto grösser ist der potenzielle Nutzen – «time is brain» gewinnt damit auch bei der Alzheimer‑Versorgung zusätzlich an Relevanz. Diese Therapien eröffnen reale Chancen für Betroffene im Frühstadium, vergleichbar mit dem Beginn der modernen MS-Therapie vor 25 Jahren, die heute mehr als 20 hochwirksame Optionen umfasst. Jetzt gilt es, Erfahrungen zu sammeln, Strukturen zu schaffen und offene Fragen zu klären, insbesondere zu Langzeitnutzen, optimaler Patientenselektion und Sicherheit im Versorgungsalltag.
Copyright
Aerzteverlag medinfo AG
– Departement für Demenzielle Erkrankungen, Universitäre Altersmedizin Felix Platter, Universität Basel
– Departement Biomedizin, Universität Basel
– Departement Klinische Forschung, Universität Basel
– UK Dementia Research Institute at University College London
– Universitätsklinik für Neurologie, Inselspital Bern
– Neuro im Zentrum, St. Gallen
Departement für Demenzielle Erkrankungen
Universitäre Altersmedizin Felix Platter
Universität Basel
Die Autorenschaft hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Die monoklonalen Antikörper Lecanemab und Donanemab entfernen pathologisches Amyloid-β aus dem Gehirn und verlangsamen den Krankheitsverlauf von Alzheimer im Frühstadium nachweislich; sie bewirken jedoch keine Heilung oder einen Stopp der Erkrankung.
- Geeignet sind Patient/-innen mit leichter kognitiver Störung oder milder Demenz, nachgewiesener Amyloid-Pathologie und ohne relevante vaskuläre oder hämorrhagische Läsionen im Gehirn.
- Therapien entfalten den grössten Nutzen in frühen Krankheitsstadien. Offene Verlängerungsdaten und Beobachtungsdaten deuten darauf hin, dass ein klinischer Vorteil mit längerer Behandlungsdauer erhalten bleiben kann. Daher sind das frühzeitige Erkennen von Gedächtnis- und anderen kognitiven Störungen und die enge Zusammenarbeit zwischen Hausärzt/-innen und Memory Clinics entscheidend, um Betroffene rasch einer spezialisierten biomarkergestützten Abklärung zuzuführen.
- Bei klarer Indikation und regelmässigem MRT-Monitoring sind die Therapien sicher anwendbar; erste Real-World-Daten legen eine gute Sicherheit und Handhabbarkeit im klinischen Alltag nahe.
- Memory Clinics entwickeln sich von rein diagnostischen und supportiven Angeboten zu einem aktiven therapeutischen Setting. Das ist ein Paradigmenwechsel in der klinischen Versorgung von Alzheimer, der auch Impulse für Diagnostik und Therapie bei anderen Demenzursachen geben dürfte.
1. Bürge M, Bieri G, Brühlmeier M, Colombo F, Demonet JF, Felbecker A, Georgescu D, Gietl A, Brioschi Guevara A, Jüngling F, Kirsch E, Kressig RW, Kulic L, Monsch AU, Ott M, Pihan H, Popp J, Rampa L, Rüegger-Frey B, Schneitter M, Unschuld PG, von Gunten A, Weinheimer B, Wiest R, Savaskan E. Recommendations of Swiss Memory Clinics for the Diagnosis of Dementia. Praxis (Bern 1994). 2018 Apr;107(8):1-17. German. doi: 10.1024/1661-8157/a003374. PMID: 31589108.
2. Popp J, Meyer-Heim T, Bürge M, Ehrensperger MM, Felbecker A, Pihan H, et al. Die Empfehlungen der Swiss Memory Clinics für die Diagnostik der Demenzerkrankungen – ein Update. Praxis (Bern 1994). 2025;114(4):127–136. doi:10.23785/PRAXIS.2025.04.002. PMID: 40336391.
3. Popp J, Georgescu D, Bürge M, Mundwiler-Pachlatko E, Bernasconi L, Felbecker A. Biomarker in der Diagnostik kognitiver Störungen – Empfehlungen der Swiss Memory Clinics. Praxis (Bern 1994). 2022;111(13):738–744. doi:10.1024/1661-8157/a003913. PMID: 36221969.
4. Juengling FD, Allenbach G, Bruehlmeier M, Klaeser B, Wissmeyer MP, Garibotto V, et al. Appropriate use criteria for dementia amyloid imaging in Switzerland-mini-review and statement on behalf of the Swiss Society of Nuclear Medicine and the Swiss Memory Clinics. Nuklearmedizin. 2021;60(1):7–9. doi:10.1055/a-1277-6014. PMID: 33080626.
5. Klöppel S, Meyer-Heim T, Ehrensperger M, Rüttimann A, Weibel I, Schnelli A, et al. Die Empfehlungen der Swiss Memory Clinics für die Therapie der Demenzerkrankungen. Praxis (Bern 1994). 2024;113(8):187–194. doi:10.23785/PRAXIS.2024.08.003. PMID: 39508540.
6. Savaskan E, Georgescu D, Becker S, Benkert B, Blessing A, Bürge M, et al. Recommendations for the diagnostic and therapy of behavioural and psychological symptoms of dementia (BPSD). Praxis (Bern 1994). 2024;113(2):34–43. PMID: 38536191.
7. Felbecker A, Rouaud O, Lathuiliere A, Allali G, Sollberger M, Meyer-Heim T, Monsch AU, Lövblad KO, Becker S, Barro-Belaygues N, Popp J, Bürge M, Lindheimer K, Gietl A, Jung HH, Georgescu D, Meyer R, Frisoni GB. Anti-Amyloid Monoclonal Antibodies for the Treatment of Alzheimer Disease: Intersocietal Recommendations for Their Appropriate Use in Switzerland. Neurodegener Dis. 2025;25(3):114-125. doi: 10.1159/000545799. Epub 2025 Apr 14. PMID: 40222353.
8. Busche MA, Hyman BT. Synergy between amyloid-ß and tau in Alzheimer‘s disease. Nat Neurosci. 2020 Oct;23(10):1183-1193. doi: 10.1038/s41593-020-0687-6. Epub 2020 Aug 10. PMID: 32778792; PMCID: PMC11831977.
9. Selkoe DJ, Hardy J. The amyloid hypothesis of Alzheimer‘s disease at 25 years. EMBO Mol Med. 2016 Jun 1;8(6):595-608. doi: 10.15252/emmm.201606210. PMID: 27025652; PMCID: PMC4888851.
10. Jonsson T, Atwal JK, Steinberg S, Snaedal J, Jonsson PV, Bjornsson S, Stefansson H, Sulem P, Gudbjartsson D, Maloney J, Hoyte K, Gustafson A, Liu Y, Lu Y, Bhangale T, Graham RR, Huttenlocher J, Bjornsdottir G, Andreassen OA, Jönsson EG, Palotie A, Behrens TW, Magnusson OT, Kong A, Thorsteinsdottir U, Watts RJ, Stefansson K. A mutation in APP protects against Alzheimer‘s disease and age-related cognitive decline. Nature. 2012 Aug 2;488(7409):96-9. doi: 10.1038/nature11283. PMID: 22801501.
11. Rajani RM, Ellingford R, Hellmuth M, Harris SS, Taso OS, Graykowski D, et al. Selective suppression of oligodendrocyte-derived amyloid beta rescues neuronal dysfunction in Alzheimer’s disease. PLoS Biol. 2024;22(7):e3002727. doi:10.1371/journal.pbio.3002727.
12. Busche MA, Chen X, Henning HA, Reichwald J, Staufenbiel M, Sakmann B, Konnerth A. Critical role of soluble amyloid-β for early hippocampal hyperactivity in a mouse model of Alzheimer‘s disease. Proc Natl Acad Sci U S A. 2012 May 29;109(22):8740-5. doi: 10.1073/pnas.1206171109. Epub 2012 May 16. PMID: 22592800; PMCID: PMC3365221.
13. Butler PM, Francis A, Meunier AL, Anderson AK, Hennessey EL, Miller MB, et al. Anti-amyloid antibody equilibrium binding to Aß aggregates from human Alzheimer disease brain. bioRxiv. 2025:2025.05.20.654902. doi:10.1101/2025.05.20.654902.
14. Kang C. Donanemab: first approval. Drugs. 2024;84:1313–1318. doi:10.1007/s40265-024-02087-4.
15. Van Dyck CH, Swanson CJ, Aisen P, Bateman RJ, Chen C, Gee M, et al. Lecanemab in early Alzheimer’s disease. N Engl J Med. 2023;388(1):9–21. doi:10.1056/NEJMoa2212948.
16. Cohen S, van Dyck CH, Gee M, Doherty T, Kanekiyo M, Dhadda S, Li D, Hersch S, Irizarry M, Kramer LD. Lecanemab Clarity AD: Quality-of-Life Results from a Randomized, Double-Blind Phase 3 Trial in Early Alzheimer‘s Disease. J Prev Alzheimers Dis. 2023;10(4):771-777. doi: 10.14283/jpad.2023.123. PMID: 37874099.
17. Fox NC, Belder C, Ballard C, Kales HC, Mummery C, Caramelli P, et al. Treatment for Alzheimer’s disease. Lancet. 2025;406:1408–1423.
18. Van Dyck CH, Sperling R, Li D, Kanekiyo M, Dhadda S, Hersch S, et al. The Lecanemab Clarity AD open-label extension in early Alzheimer’s disease: initial findings from the 48-month analysis. Presented at: Alzheimer’s Association International Conference (AAIC); 2025 Jul 27–31; Toronto, Canada.
19. Sims JR, Zimmer JA, Evans CD, Lu M, Ardayfio P, Sparks J, Wessels AM, Shcherbinin S, Wang H, Monkul Nery ES, Collins EC, Solomon P, Salloway S, Apostolova LG, Hansson O, Ritchie C, Brooks DA, Mintun M, Skovronsky DM; TRAILBLAZER-ALZ 2 Investigators. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA. 2023 Aug 8;330(6):512-527. doi: 10.1001/jama.2023.13239. PMID: 37459141; PMCID: PMC10352931.
20. Zimmer JA, Sims JR, Evans CD, Nery ESM, Wang H, Wessels AM, Tronchin G, Sato S, Raket LL, Andersen SW, Sapin C, Paget MA, Gueorguieva I, Ardayfio P, Khanna R, Brooks DA, Matthews BR, Mintun MA; Alzheimer’s Disease Neuroimaging Initiative. Donanemab in early symptomatic Alzheimer‘s disease: results from the TRAILBLAZER-ALZ 2 long-term extension. J Prev Alzheimers Dis. 2025 Dec 1:100446. doi: 10.1016/j.tjpad.2025.100446. Epub ahead of print. PMID: 41330788.
21. Paczynski M, Hofmann A, Posey Z, Gregersen M, Rudman M, Ellington D, Aldinger M, Musiek ES, Holtzman DM, Bateman RJ, Long JM, Ghoshal N, Carr DB, Dow A, Namazie-Kummer S, Jana N, Xiong C, Morris JC, Benzinger TLS, Schindler SE, Snider BJ. Lecanemab Treatment in a Specialty Memory Clinic. JAMA Neurol. 2025 Jul 1;82(7):655-665. doi: 10.1001/jamaneurol.2025.1232. Erratum in: JAMA Neurol. 2025 Jul 1;82(7):754. doi: 10.1001/jamaneurol.2025.2446. PMID: 40354064; PMCID: PMC12070285.
22. Cummings J, Apostolova L, Rabinovici GD, Atri A, Aisen P, Greenberg S, Hendrix S, Selkoe D, Weiner M, Petersen RC, Salloway S. Lecanemab: Appropriate Use Recommendations. J Prev Alzheimers Dis. 2023;10(3):362-377. doi: 10.14283/jpad.2023.30. PMID: 37357276; PMCID: PMC10313141.
23. Rabinovici GD, Selkoe DJ, Schindler SE, Aisen P, Apostolova LG, Atri A, Greenberg SM, Hendrix SB, Petersen RC, Weiner M, Salloway S, Cummings J. Donanemab: Appropriate use recommendations. J Prev Alzheimers Dis. 2025 May;12(5):100150. doi: 10.1016/j.tjpad.2025.100150. Epub 2025 Mar 27. PMID: 40155270; PMCID: PMC12180672.
24. Wang H, Serap Monkul Nery E, Ardayfio P, Khanna R, Otero Svaldi D, Gueorguieva I, Shcherbinin S, Andersen SW, Hauck PM, Engle SE, Brooks DA, Collins EC, Fox NC, Greenberg SM, Salloway S, Mintun MA, Sims JR. Modified titration of donanemab reduces ARIA risk and maintains amyloid reduction. Alzheimers Dement. 2025 Apr;21(4):e70062. doi: 10.1002/alz.70062. Erratum in: Alzheimers Dement. 2025 Aug;21(8):e70576. doi: 10.1002/alz.70576. PMID: 40172303; PMCID: PMC11963282.
25. Frisoni GB, Ribaldi F, Aho E, Brayne C, Walsh S, Ciccarelli O, et al. The new clinical landscape in Alzheimer’s disease: controversies and future directions. Part 3. Lancet. 2025;406:1424–1442. doi:10.1016/S0140-6736(25)01389-3.
26. Rubin R. Treating Alzheimer Disease With Antiamyloid Therapies-The Real-World Experience Grows. JAMA. 2025 Sep 23;334(12):1041-1044. doi: 10.1001/jama.2025.14180. PMID: 40844810
27. Bregman N, Nathan T, Shir D, Omer N, Levy MH, Bar David A, et al. Lecanemab in clinical practice: real-world outcomes in early Alzheimer’s disease. Alzheimers Res Ther. 2025;17:119. doi:10.1186/s13195-025-01763-1.
28. Belder CRS, Boche D, Nicoll JAR, Jaunmuktane Z, Zetterberg H, Schott JM, Barkhof F, Fox NC. Amyloid-related iatrogenic atrophy of the brain: data transparency is an urgent safety priority – Authors‘ reply. Lancet Neurol. 2025 Mar;24(3):190. doi: 10.1016/S1474-4422(25)00030-4. PMID: 39986300.
29. Schenk D, Barbour R, Dunn W, Gordon G, Grajeda H, Guido T, Hu K, Huang J, Johnson-Wood K, Khan K, Kholodenko D, Lee M, Liao Z, Lieberburg I, Motter R, Mutter L, Soriano F, Shopp G, Vasquez N, Vandevert C, Walker S, Wogulis M, Yednock T, Games D, Seubert P. Immunization with amyloid-beta attenuates Alzheimer-disease-like pathology in the PDAPP mouse. Nature. 1999 Jul 8;400(6740):173-7. doi: 10.1038/22124. PMID: 10408445.
der informierte @rzt
- Vol. 16
- Ausgabe 1
- Januar 2026