- Sekundäre Kopfschmerzen
Die korrekte Einordnung von Kopfschmerzen im klinischen Alltag gestaltet sich aufgrund der Vielzahl an Differenzialdiagnosen oft als herausfordernd. Besonders wichtig ist dabei die Unterscheidung zwischen den häufigeren primären Kopfschmerzen, bei denen der Kopfschmerz die eigentliche Erkrankung darstellt, und den sekundären Kopfschmerzen, die teilweise lebensbedrohliche Ursachen haben können. Die diagnostischen Entscheidungswege beginnen daher mit der Identifizierung von sekundären Kopfschmerzen.
In clinical practice, correctly diagnosing headaches can be challenging due to the many differential diagnoses. It is particularly important to differentiate between the more common primary headache types, where the headache itself is the main condition, and secondary headaches, which may have potentially lifethreatening causes. The diagnostic approach initially focuses on identifying secondary headaches.
Keywords: Secondary headaches, primary headaches, red flags, green flags
Überblick
Viele Erkrankungen können sich durch Kopfschmerzen äussern. Kopfschmerzen zählen zu den häufigsten Beschwerden, die zur Vorstellung beim Arzt führen. Epidemiologisch gesehen, liegt in der Europäischen Union die Ein-Jahres-Prävalenz von Kopfschmerzen bei 79 % (1). Neben der erheblichen psychischen Belastung und der Beeinträchtigung der Lebensqualität können Kopfschmerzen auch die Arbeitsleistung deutlich mindern (2). Die Internationale Kopfschmerzgesellschaft (IHS) unterscheidet in der aktuellen Kopfschmerzklassifikation 276 verschiedene Kopfschmerzerkrankungen (3). Migräne ist eine der häufigsten Erkrankungen. Etwa 1.1 Milliarden Menschen weltweit sind von Migräne betroffen (4). Unter den neurologischen Erkrankungen löst sie die höchste Erkrankungslast aus (5). Viele Patienten mit Migräne stellen sich notfallmässig vor, v. a. bei erstmaligem Auftreten einer Aura.
Primär versus sekundär
Bei der Vorstellung von Kopfschmerzpatienten steht oft die Frage nach der Ursache der Beschwerden im Mittelpunkt. Viele Betroffene erhoffen sich durch die Behandlung nicht nur eine Linderung der Symptome, sondern auch die vollständige Beseitigung der Ursache und damit eine Heilung ihrer Erkrankung. Tatsächlich stellt die Unterscheidung zwischen primären und sekundären Kopfschmerzen eine grosse Herausforderung dar, da Kopfschmerzerkrankungen heterogen sind. Das Ziel ist zunächst, einen potenziell bedrohlichen sekundären oder symptomatischen Kopfschmerz mit einer hohen Sensitivität zu identifizieren (6). Während primäre Kopfschmerzen wie Migräne eine eigenständige Erkrankung darstellen, ist bei sekundären oder symptomatischen Kopfschmerzen eine andere Erkrankung zugrunde liegend. Die WHO schätzte im Jahr 2021, dass bis zu 18 % der Patienten, die sich mit Kopfschmerzen vorstellen, an einem sekundären Kopfschmerz leiden (6). In einer norwegischen populationsbasierten Studie betrug die Ein-Jahres-Prävalenz von sekundären Kopfschmerzen in der Altersgruppe zwischen 30 und 44 Jahren hingegen nur 2.14 %. Der überwiegende Anteil dieser Patienten hatte einen Medikamentenübergebrauchskopfschmerz, welcher keinen Notfall darstellt und rein durch die Anamnese diagnostiziert werden kann (7). Dementsprechend ist davon auszugehen, dass nur wenige Menschen, die sich in dieser Altersspanne mit Kopfschmerzen vorstellen, tatsächlich an einem potenziell gefährlichen sekundären Kopfschmerz leiden. Da die Ursache von sekundären Kopfschmerzen eine hohe Morbidität oder gar Mortalität haben kann, müssen sie zuverlässig und ggf. schnell erkannt werden. Besteht aufgrund der Anamnese und klinischen Untersuchung bereits der Verdacht auf einen sekundären Kopfschmerz, erhöht sich auch die Wahrscheinlichkeit, eine relevante Pathologie zu finden (sog. Vortest-Wahrscheinlichkeit) (8). Die Identifizierung der zugrunde liegenden Pathologie ist zudem entscheidend, da auch die erfolgreiche Behandlung der Kopfschmerzen oft erst durch die gezielte Therapie der verursachenden Erkrankung möglich wird.
«Red Flags»
In der Konsultation mit Kopfschmerzpatienten ist es empfehlenswert, von Beginn an auf Warnzeichen, die auf sekundäre Kopfschmerzen hinweisen, sogenannte Red Flags, zu achten. Das Akronym SNNOOP10 aus dem Englischen umfasst 15 wichtige Punkte, die als Gedankenstütze bei der Identifikation von «Red Flags» für sekundäre Kopfschmerzen hilfreich sind (9). In der strukturierten Anamnese gibt die Kopfschmerzdynamik bereits wichtige Hinweise, wie akut der Kopfschmerz auftritt, und hilft, einen vorbestehenden von den aktuellen, neuartigen Kopfschmerzen zu unterscheiden. Begleitphänomene, Medikation und Vorerkrankungen können zudem wichtige Informationen für die Genese der Kopfschmerzen liefern. Im nächsten Schritt kann der Kopfschmerzphänotyp dann genauer analysiert werden.
Kurzkasuistik
Eine 45-jährige Patientin mit einer bekannten Migräne ohne Aura stellt sich notfallmässig mit stärksten Kopfschmerzen vor, welche plötzlich begonnen hätten. Sie kommt gerade aus dem Skiurlaub zurück. Während des Urlaubes sei es ihr sehr gut gegangen. Ein Trauma wird verneint. Der Kopfschmerz habe sich nicht, wie sonst üblich, nach Einnahme eines Triptans gebessert. Da sich die Kopfschmerzen wie die bekannte Migräne präsentieren, wird die Patientin nach unauffälligem CT-Schädel und regredienten Schmerzen unter Analgesie wieder nach Hause entlassen. Wenige Tage später stellt sie sich erneut mit einem Donnerschlagkopfschmerz vor. Nun zeigen sich bildgebend nicht nur eine Subarachnoidalblutung in der Konvexität, sondern auch Gefässspasmen. Klinisch finden sich eine leichte linksseitige Armschwäche, Wortfindungsstörungen und eine Abduzensparese. Es wird die Diagnose eines reversiblen zerebralen Vasokonstriktionssyndroms (RCVS), eines sekundären Kopfschmerzes, gestellt. Während der intensivmedizinischen Behandlung kommt es rezidivierend zu Kopfschmerzexazerbationen. Die fokal neurologischen Defizite sind im Verlauf vollständig regredient.
Diese Kasuistik zeigt, dass es schwierig sein kann, anhand des Phänotyps einen primären und vorbestehenden Kopfschmerz von einem sekundären, potenziell bedrohlichen Kopfschmerz zu unterscheiden (10). Bei dieser Patientin äusserte sich der sekundäre Kopfschmerz im Rahmen eines reversiblen zerebralen Vasokonstriktionssyndroms (RCVS) ähnlich wie eine schwere Migräneattacke. Auffallend waren der schnelle Beginn – bei der Migräne gibt es in der Regel eine Vorphase –, die hohe Intensität (Donnerschlagkopfschmerz) und das fehlende Ansprechen auf die gewohnte Akutmedikation. Die Kopfschmerzdynamik, Intensität und Medikation lieferten hier genauere Informationen als die Analyse des Phänotyps. Es ist nicht ungewöhnlich, dass sekundäre Kopfschmerzen Merkmale eines Migräne- oder Spannungskopfschmerzes aufweisen. Dieser Fall zeigt auch, dass die meist auf dem Notfall durchgeführte Bildgebung eines CT die Pathologie nicht immer aufzeigt.
Ausschlaggebend für die Differenzierung von primären und sekundären Kopfschmerzen ist das Gesamtbild, das sich aus gezielter Anamnese und klinischer Untersuchung ergibt.
Anamnese
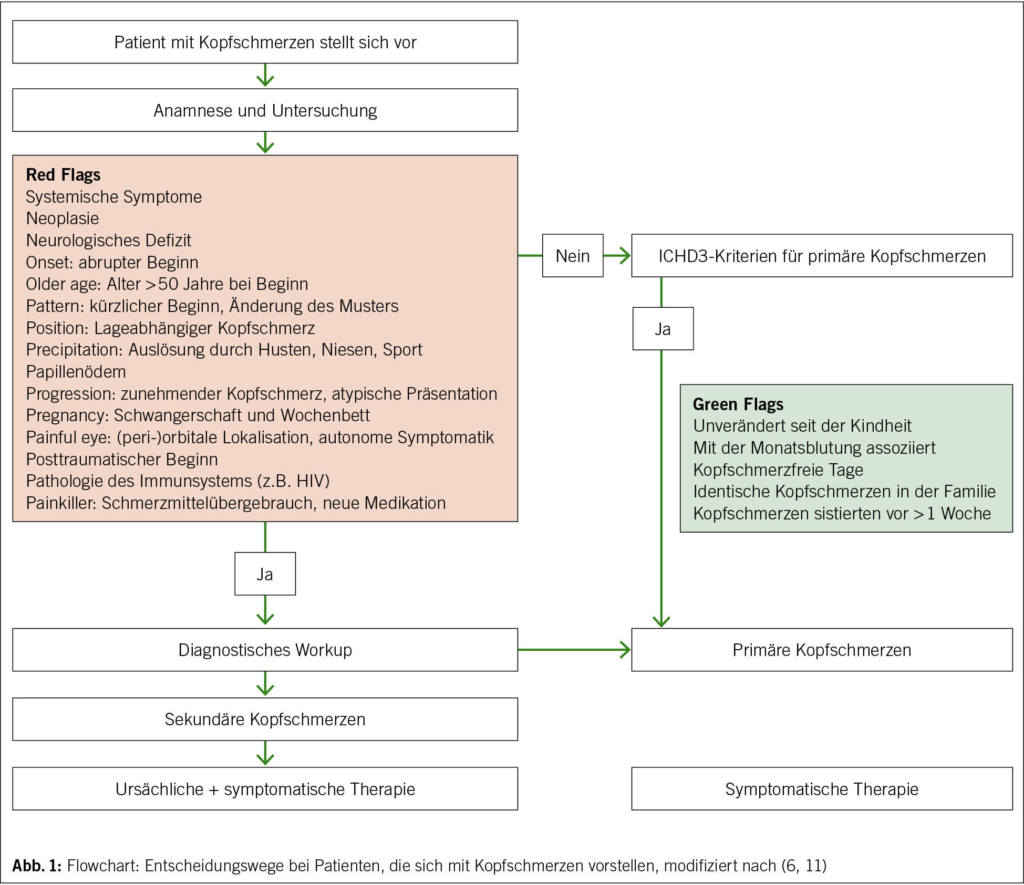
Im Folgenden sind die wichtigsten Punkte für eine strukturierte Anamnese von Kopfschmerzpatienten aufgelistet (Abb. 1) (11,12). Die Punkte sind aktiv zu erfragen (Holprinzip). Jeder Punkt, der nicht vorbestehend ist, sollte zunächst als «Red Flag» gewertet werden.
Kopfschmerzspezifische Anamnese
• Dynamik
– Seit wann besteht der aktuelle Kopfschmerz?
– Wie hat er beim ersten Mal begonnen?
– Wie häufig trat der Kopfschmerz zu Beginn auf?
– Wie hat sich die Kopfschmerzfrequenz im Verlauf
verändert?
– Wie häufig tritt der Kopfschmerz aktuell auf?
• Phänotyp
– Lokalisation, Intensität, Qualität und Dauer der einzelnen Attacken
– Begleitbeschwerden wie Photophobie, Phonophobie, Osmophobie, Übelkeit und Erbrechen
– Zunahme bei körperlicher Anstrengung, Ruhebedürfnis, psychomotorische Unruhe
– Kranioautonome Symptome, z. B. Augentränen,
Nasenlaufen, verstopfte Nase, gerötetes Auge, Lidödem, verstopftes Ohr, Schwitzen auf der Stirn, einseitige Ptose
– Aura (visuell, sensibel, motorisch), Dauer und Zeitpunkt des Auftretens
– Nicht-Kopfschmerz-Symptome, z. B. Konzentrationsstörungen, Reizbarkeit, Müdigkeit oder Hungergefühl
– Vorboten, z. B. Müdigkeit, häufiges Gähnen, Gereiztheit, Euphorie
– Triggerfaktoren, z. B. Lageabhängigkeit, Husten, Niesen, Pressen, Trauma
Allgemeine Anamnese
• Aktuelle Medikation
– Akut- und Basistherapie (Dosis, Dauer, Effekt, Nebenwirkungen)
– Weitere Medikation
• Frühere Kopfschmerzmedikation (getrennt nach Akut- und Basistherapie)
– Dosis, Dauer, Effekt, Nebenwirkungen
• Vorerkrankungen, z. B. Tumor, Immundefizite
• Systemanamnese inkl. Schlaf, Stimmung, B-Symptomatik etc.
• Familienanamnese
• Sozialanamnese inkl. Auswirkungen der Kopfschmerzen
• Bisher erfolgte Untersuchungen
Untersuchung
Bei jeder Erstvorstellung sowie bei neuen anamnestischen Aspekten sollte eine umfassende körperliche Untersuchung mit besonderem Fokus auf neurologische Defizite, Meningismus, Schmerzlokalisation und systemische Zeichen, die auf einen sekundären Kopfschmerz hinweisen können, erfolgen.
Die körperliche Untersuchung sollte folgende Aspekte umfassen:
• Erhebung der Vitalparameter
• Vollständige neurologische Untersuchung mit Beurteilung der Hirnnerven, fokal neurologischer Defizite, Meningismus
• Untersuchung der Austrittspunkte des Nervus trigeminus
• Prüfung auf bulbären Druck- oder Bewegungsschmerz
• Inspektion der Schleimhäute und des Zahnstatus
• Beurteilung der Beweglichkeit der Halswirbelsäule
• Erfassung einer möglichen Druckschmerzhaftigkeit der perikranialen Muskulatur
• Untersuchung auf Schmerzen bei Kieferöffnung oder -okklusion
• Palpation der Arteria temporalis superficialis
• Systemische Auffälligkeiten wie Hautveränderungen
Diagnostisches Work-up
Auf Basis der erhobenen Anamnese und klinischen Untersuchung kann eine erste Arbeitshypothese zur Kopfschmerzursache erstellt werden. Wenn «Red Flags» vorliegen, sollte abhängig von der Verdachtsdiagnose ein gezieltes diagnostisches Work-up durchgeführt werden. Dabei unterscheidet sich die Abklärung eines akuten, neu aufgetretenen Kopfschmerzes wesentlich von einem seit Monaten bestehenden chronischen Kopfschmerz. Während bei Ersterem eine sofortige Bildgebung und ggf. Lumbalpunktion erforderlich sein könnte, ist zur weiteren Abklärung systemischer Ursachen beispielsweise eine Blutuntersuchung zunächst ausreichend. So kann Kopfschmerz z. B. auch als Symptom von Elektrolytstörungen, beispielsweise im Rahmen einer Dialyse, auftreten. Darüber hinaus können Kopfschmerzen bei rheumatologischen Erkrankungen, endokrinologischen Störungen oder autoimmunen Enzephalitiden auftreten (13). Je nach klinischer Symptomatik sind daher spezifische Laboruntersuchungen indiziert, um mögliche systemische Ursachen zu identifizieren. Die Diagnostik und Therapie komplexer Kopfschmerzerkrankungen erfolgen häufig in interdisziplinärer Zusammenarbeit mit verschiedenen Fachrichtungen, u.a. der Radiologie, Kardiologie, Ophthalmologie, HNO, Schlafmedizin, Psychosomatik, Infektiologie, Endokrinologie und Zahnmedizin.
«Smarter Medicine»
Im klinischen Alltag ist es teilweise schwierig zu entscheiden, bei welchen Patienten eine ausführliche Diagnostik erfolgen sollte und bei welchen beispielsweise auf eine wiederholte Bildgebung verzichtet werden sollte. Im Rahmen des Expertenkonsens «Smarter Medicine» wurden Situationen definiert, in denen auf weiterführende Diagnostik verzichtet werden kann (14).
Diese 5 Empfehlungen sind im Folgenden aufgelistet:
• Keine Wiederholung der zerebralen Bildgebung bei unverändertem Kopfschmerzphänotyp
• Keine Computertomographie des Schädels zur Diagnostik nicht akuter Kopfschmerzen
• Keine Zahnextraktion zur Behandlung eines anhaltenden idiopathischen Gesichtsschmerzes
• Keine Migränechirurgie
• Keine Entfernung von Amalgamfüllungen zur Kopfschmerzbehandlung
«Green Flags»
Um mit hoher Sicherheit einen primären Kopfschmerz diagnostizieren zu können, ist das Konzept «Green Flags» entwickelt worden. «Green Flags» sind Symptome und Befunde, die nach Ausschluss von «Red Flags» mit hoher Wahrscheinlichkeit auf einen primären Kopfschmerz hindeuten (15). Dieses Konzept beruht auf einem Expertenkonsens. Eine Validierung der «Red Flags» nach der SNNOOP10-Liste und der «Green Flags» steht noch aus (6). Zusätzlich wird in der Forschung weiter nach Biomarkern für primäre Kopfschmerzerkrankungen, wie z. B. der Migräne, die im klinischen Alltag eingesetzt werden können, gesucht.
Entscheidungswege bei Kopfschmerzpatienten
Das Vorgehen im klinischen Alltag zeigt Abb. 1. Stellen sich Patienten mit Kopfschmerzen vor, wird in Anamnese und klinischer Untersuchung auf «Red Flags» und «Green Flags» geachtet. Bei fehlenden «Red Flags» sollte geprüft werden, ob der berichtete Kopfschmerz mit den ICHD3-Diagnosekriterien für primäre Kopfschmerzen übereinstimmt. Ist dies nicht der Fall, sind die «Green Flags» Hinweise auf das wahrscheinliche Vorliegen eines primären Kopfschmerzes. Beim Vorliegen von «Red Flags» wird weitere Diagnostik veranlasst. Zeigen sich hier unauffällige Befunde, ist ebenfalls mit einer hohen Wahrscheinlichkeit von dem Vorliegen eines primären Kopfschmerzes auszugehen.
Therapie sekundärer Kopfschmerzen
Bei sekundären Kopfschmerzen sollte primär die zugrunde liegende Ursache therapiert werden. Die Schmerzbehandlung erfolgt dabei durchaus nach WHO-Stufenschema, wobei Opiate in der Kopfschmerztherapie aufgrund des Gewöhnungseffektes und des Risikos der Entwicklung eines Medikamentenübergebrauchskopfschmerzes zurückhaltend eingesetzt werden sollten. Aus praktischer Sicht empfiehlt sich vielmehr die Wahl der Akut- und Basistherapie anhand des Kopfschmerzphänotyps. Für die primären Kopfschmerzerkrankungen gibt es Therapieempfehlungen der Schweizerischen Kopfwehgesellschaft (www.headache.ch).
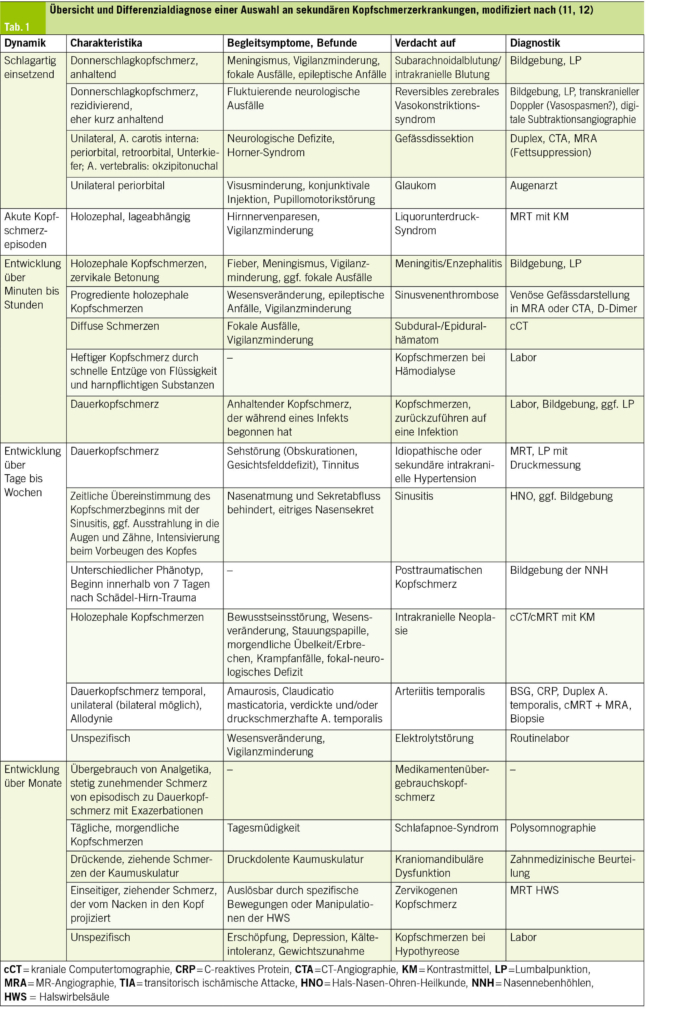
Differenzialdiagnosen sekundärer Kopfschmerzen
Mögliche Ursachen sekundärer Kopfschmerzen sind in der Tab. 1 aufgeführt.
Chronische sekundäre Kopfschmerzen
Zu den chronischen sekundären Kopfschmerzformen, die im klinischen Alltag zwar selten sind, aber leicht mit primären Kopfschmerzen verwechselt werden können und eine spezifische Diagnostik benötigen, zählen die idiopathische intrakranielle Hypertension (IIH) und die spontane intrakranielle Hypotension (SIH). An beide sollte bei Patienten mit unklaren chronischen Kopfschmerzen gedacht werden, da eine effektive Therapie zwingend die Ursache behandelt.
Die idiopathische intrakranielle Hypertension weist eine erhöhte Komorbidität mit Migräne auf, stellt aber gleichzeitig auch eine Differenzialdiagnose zur chronischen Migräne dar. Zu den «Red Flags», die für IIH sprechen, gehören u. a. lageabhängige Kopfschmerzen, die im Liegen zunehmen. Das Auftreten von Sehstörungen, welche sich in Form von kurz anhaltendem, wolkenartigem Verschwommensehen (visuellen Obskurationen), Photopsien oder Diplopie äussern und für ein Papillenödem sprechen, werden von etwa zwei Dritteln der Patienten berichtet. Seltener treten auch Gesichtsfelddefekte oder Abduzensparesen auf. Etwa die Hälfte der Patienten leidet an einem pulsatilen Tinnitus, der sich typischerweise im Liegen verstärkt. Auch Schwindel ist ein häufiges Symptom. IIH betrifft überwiegend Frauen im gebärfähigen Alter und ist mit Adipositas assoziiert. Eine Gewichtsreduktion kann zu einer Besserung der Symptomatik führen. Bei Verdacht auf IIH sollte eine Bildgebung vor Lumbalpunktion mit Liquordruckmessung durchgeführt werden. Die MRT spielt eine entscheidende Rolle bei der Diagnosestellung der IIH. Typische bildgebende Indikatoren für IIH sind eine Empty Sella, gewundene Sehnerven, eine Erweiterung der Sehnervenscheide, eine Abflachung des hinteren Augapfels, eine Vorwölbung des Sehnervenkopfes sowie eine Stenose des transversalen Sinus. Zur medikamentösen Behandlung gibt es nur Off-label-Optionen. Es werden Acetazolamid und Topiramat eingesetzt, insbesondere bei milden Verlaufsformen. Auch für die Therapie mit GLP-1-Agonisten zeigten sich in Bezug auf Kopfschmerzen und Gewichtsabnahme gute Ergebnisse (16). Bei schweren Verlaufsformen, die auf die medikamentöse Therapie nicht ausreichend ansprechen, oder bei Patienten mit Papillenödem wird neben der Optikusscheidenfenestrierung und der Anlage eines ventrikuloperitonealen Shunts auch eine Stentimplantation evaluiert, wenn eine Stenose des Sinus transversus vorliegt (17, 18). Wenn die Kopfschmerzen persistieren, nachdem sich der Liquordruck normalisiert hat, kommen CGRP-Antikörper ins Spiel (19).
Das Leitsymptom der spontanen intrakraniellen Hypotension (SIH) ist ein orthostatischer Kopfschmerz, der im Stehen stärker ausgeprägt ist und im Tagesverlauf zunimmt. Charakteristisch ist ein plötzlicher Beginn, wobei viele Betroffene den genauen Tag des Auftretens der Beschwerden benennen können. Die Diagnose wird meist anhand der Anamnese und der bildgebenden Befunde gestellt. Dabei können unspezifische Beschwerden auftreten. Typisch für SIH sind neben lageabhängigen Kopfschmerzen Nackenschmerzen, Tinnitus, Übelkeit und Sehstörungen. Der neurologische Status ist in der Regel unauffällig. Gelegentlich treten jedoch Doppelbilder infolge von Hirnnervenparesen auf.
Da der Liquordruck bei etwa zwei Drittel der Patienten mit SIH normal ist und eine Lumbalpunktion das Krankheitsbild durch ein zusätzliches postpunktionelles Syndrom verschlechtern kann, ist die Lumbalpunktion primär nicht indiziert. Zur Sicherung der Diagnose kommt die zerebrale und spinale Magnetresonanztomographie zum Einsatz. Mithilfe eines Scores kann die Wahrscheinlichkeit für das Vorliegen eines Liquorlecks errechnet werden. Folgende typische MRT-Befunde werden hierbei berücksichtigt: subdurale Flüssigkeitsansammlung, pachymeningeales Enhancement, Vergrösserung der Sinus durae matris, Distanz der suprasellären Zisterne, pontomamilläre Distanz und präpontine Zisterne (20). Die häufigste Ursache für SIH sind ventrale Duralecks, die vorwiegend im thorakalen Bereich auftreten und durch Mikrosporne oder Verkalkungen verursacht werden. Weniger häufig sind meningeale Divertikel, Ektasien, Schwachstellen der Dura an den spinalen Nervenwurzeln oder direkte Fisteln zwischen dem Liquorraum und den epiduralen Venen als Auslöser anzutreffen (21). Symptomatische Therapien mit Koffein, Theophyllin, Gabapentin und Hydrokortison können versucht werden. Bei fehlendem Effekt sollte rasch eskaliert werden. Neben dem epiduralen Blutpatch, der ggf. auch wiederholt werden muss, muss das Liquorleck oftmals mikrochirurgisch verschlossen oder endovaskulär, transvenös embolisiert werden. Zu beachten ist, dass der SIH-Kopfschmerz sich oft über Jahre bessern kann und seine Lageabhängigkeit verliert. Da das Leck aber oft doch nicht verschlossen ist, kann es zu schwerwiegenden Komplikationen wie zerebraler Siderose und bibrachialer Atrophie kommen.
Wann überweise ich Patienten zu Kopfschmerzspezialisten?
Eine Überweisung zu Neurologen oder Kopfschmerzspezialisten ist zu jedem Zeitpunkt richtig. Insbesondere in folgenden Situationen ist eine Mitbeurteilung indiziert:
• Neuartige Kopfschmerzen und «Red Flags». Ausnahme ist der Verdacht auf einen dringend zu behandelnden sekundären Kopfschmerz, bei dem eine unmittelbare Zuweisung auf einen Notfall notwendig ist.
• Unklare Kopfschmerzen
• Beginnende Chronifizierung mit Zunahme der Kopfschmerzfrequenz oder -intensität
• Chronische Kopfschmerzen
• Fehlendes Ansprechen auf Basistherapien wie Betablocker oder Amitriptylin
• Komorbiditäten
Fazit
Bei der Vorstellung von Patienten mit Kopfschmerzen gelingt die Unterscheidung zwischen primären und sekundären Kopfschmerzen durch eine strukturierte und kopfschmerzspezifische Anamnese und neurologische Untersuchung. Hilfreiche Instrumente in der Differenzialdiagnostik sind «Red Flags» und «Green Flags». Je nach Verdachtsdiagnose kann dann entschieden werden, welche Diagnostik und Therapie für den individuellen Kopfschmerzpatienten gewählt werden sollten.
Copyright
Aerzteverlag medinfo AG
Zweitabdruck aus Therapeutische Umschau 03-25
Universitätsklinik für Neurologie
Inselspital
Rosenbühlgasse 25
3010 Bern
– Universitätsklinik für Neurologie
Inselspital
Rosenbühlgasse 25
3010 Bern
– Zentrum für Migräne und Kopfschmerzen
Bellevue Medical Group
Theaterstrasse 22
8001 Zürich
christoph.schankin@bmg-swiss.ch
Die Autorenschaft hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Hoglinger G, Trenkwalder C. Parkinson-Krankheit, S2k-Leitlinie, 2023. Deutsche Gesellschaft für Neurologie (Hrsg), Leitlinien für Diagnostik und Therapie in der Neurologie. 2023.
2. Schapira AHV, Chaudhuri KR, Jenner P. Non-motor features of Parkinson disease. Nat Rev Neurosci. 2017 Aug;18(8):509.
3. Fereshtehnejad SM, Zeighami Y, Dagher A, Postuma RB. Clinical criteria for subtyping Parkinson’ s disease: biomarkers and longitudinal progression. Brain. 2017 Jul 1;140(7):1959-76.
4. Mylius V, Perez Lloret S, Cury RG, Teixeira MJ, Barbosa VR, Barbosa ER, et al. The Parkinson disease pain classification system: results from an international mechanism-based classification approach. Pain. 2021 Apr 1;162(4):1201-10.
5. Zaja-Milatovic S, Milatovic D, Schantz AM, Zhang J, Montine KS, Samii A, et al. Dendritic degeneration in neostriatal medium spiny neurons in Parkinson disease. Neurology. 2005 Feb 8;64(3):545-7.
6. Storch A, Schneider CB, Wolz M, Sturwald Y, Nebe A, Odin P, et al. Nonmotor fluctuations in Parkinson disease: severity and correlation with motor complications. Neurology. 2013 Feb 26;80(9):800-9.
7. Lee MA, Walker RW, Hildreth TJ, Prentice WM. A survey of pain in idiopathic Parkinson’ s disease. J Pain Symptom Manage. 2006 Nov;32(5):462-9.
8. Mylius V, Moller JC, Bohlhalter S, Ciampi de Andrade D, Perez Lloret S. Diagnosis and Management of Pain in Parkinson’ s Disease: A New Approach. Drugs Aging. 2021 Jul;38(7):559-77.
9. Mylius V, Perez Lloret S, Brook CS, Kruger MT, Hagele-Link S, Gonzenbach R, et al. The new Parkinson’ s disease pain classification system (PD-PCS). Nervenarzt. 2022 Oct;93(10):1019-27.
10. Mylius V, Moisset X, Rukavina K, Rosner J, Korwisi B, Marques A, et al. New ICD-11 diagnostic criteria for chronic secondary musculoskeletal pain associated with Parkinson disease. Pain. 2024 Jan 11.
11. Cohen SP, Vase L, Hooten WM. Chronic pain: an update on burden, best practices, and new advances. Lancet. 2021 May 29;397(10289):2082-97.
12. Finnerup NB, Haroutounian S, Kamerman P, Baron R, Bennett DL, Bouhassira D, et al. Neuropathic pain: an updated grading system for research and clinical practice. Pain. 2016 Aug;157(8):1599-606.
13. Bouhassira D, Attal N, Alchaar H, Boureau F, Brochet B, Bruxelle J, et al. Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain. 2005 Mar;114(1-2):29-36.
14. Chaudhuri KR, Rizos A, Trenkwalder C, Rascol O, Pal S, Martino D, et al. King’ s Parkinson’ s disease pain scale, the first scale for pain in PD: An international validation. Mov Disord. 2015 Oct;30(12):1623-31.
15. Brefel-Courbon C, Payoux P, Thalamas C, Ory F, Quelven I, Chollet F, et al. Effect of levodopa on pain threshold in Parkinson’ s disease: a clinical and positron emission tomography study. Mov Disord. 2005 Dec;20(12):1557-63.
16. Boura E, Stamelou M, Vadasz D, Ries V, Unger MM, Kagi G, et al. Is increased spinal nociception another hallmark for Parkinson’ s disease? J Neurol. 2017 Mar;264(3):570-5.
17. Mylius V, Brebbermann J, Dohmann H, Engau I, Oertel WH, Moller JC. Pain sensitivity and clinical progression in Parkinson’ s disease. Mov Disord. 2011 Oct;26(12):2220-5.
18. Mylius V, Engau I, Teepker M, Stiasny-Kolster K, Schepelmann K, Oertel WH, et al. Pain sensitivity and descending inhibition of pain in Parkinson’ s disease. J Neurol Neurosurg Psychiatry. 2009 Jan;80(1):24-8.
19. Gerdelat-Mas A, Simonetta-Moreau M, Thalamas C, Ory-Magne F, Slaoui T, Rascol O, et al. Levodopa raises objective pain threshold in Parkinson’ s disease: a RIII reflex study. J Neurol Neurosurg Psychiatry. 2007 Oct;78(10):1140-2.
20. Mylius V, Baars JH, Witt K, Benninger D, de Andrade DC, Kagi G, et al. Deep Brain Stimulation Improves Parkinson’ s Disease-Associated Pain by Decreasing Spinal Nociception. Mov Disord. 2024 Feb;39(2):447-9.
21. Stocchi F, Rascol O, Kieburtz K, Poewe W, Jankovic J, Tolosa E, et al. Initiating levodopa/carbidopa therapy with and without entacapone in early Parkinson disease: the STRIDE-PD study. Ann Neurol. 2010 Jul;68(1):18-27.
22. Kassubek J, Chaudhuri KR, Zesiewicz T, Surmann E, Boroojerdi B, Moran K, et al. Rotigotine transdermal system and evaluation of pain in patients with Parkinson’ s disease: a post hoc analysis of the RECOVER study. BMC Neurol. 2014 Mar 6;14:42.
23. Rascol O, Zesiewicz T, Chaudhuri KR, Asgharnejad M, Surmann E, Dohin E, et al. A Randomized Controlled Exploratory Pilot Study to Evaluate the Effect of Rotigotine Transdermal Patch on Parkinson’ s Disease-Associated Chronic Pain. J Clin Pharmacol. 2016 Jul;56(7):852-61.
24. Borgohain R, Szasz J, Stanzione P, Meshram C, Bhatt MH, Chirilineau D, et al. Two-year, randomized, controlled study of safinamide as add-on to levodopa in mid to late Parkinson’ s disease. Mov Disord. 2014 Sep;29(10):1273-80.
25. Nebe A, Ebersbach G. Pain intensity on and off levodopa in patients with Parkinson’ s disease. Mov Disord. 2009 Jun 15;24(8):1233-7.
26. Li J, Zhu BF, Gu ZQ, Zhang H, Mei SS, Ji SZ, et al. Musculoskeletal Pain in Parkinson’ s Disease. Front Neurol. 2021;12:756538.
27. Buhmann C, Wrobel N, Grashorn W, Fruendt O, Wesemann K, Diedrich S, et al. Pain in Parkinson disease: a cross-sectional survey of its prevalence, specifics, and therapy. J Neurol. 2017 Apr;264(4):758-69.
28. Trenkwalder C, Chaudhuri KR, Martinez-Martin P, Rascol O, Ehret R, Valis M, et al. Prolonged-release oxycodone-naloxone for treatment of severe pain in patients with Parkinson’ s disease (PANDA): a double-blind, randomised, placebo-controlled trial. Lancet Neurol. 2015 Dec;14(12):1161-70.
29. Chagas MH, Zuardi AW, Tumas V, Pena-Pereira MA, Sobreira ET, Bergamaschi MM, et al. Effects of cannabidiol in the treatment of patients with Parkinson’ s disease: an exploratory double-blind trial. J Psychopharmacol. 2014 Nov;28(11):1088-98.
30. Freo U, Furnari M, Ori C. Effects of tapentadol on pain, motor symptoms and cognitive functions in Parkinson’ s disease. J Pain Res. 2018;11:1849-56.
31. Rieu I, Degos B, Castelnovo G, Vial C, Durand E, Pereira B, et al. Incobotulinum toxin A in Parkinson’ s disease with foot dystonia: A double blind randomized trial. Parkinsonism Relat Disord. 2018 Jan;46:9-15.
32. Djaldetti R, Yust-Katz S, Kolianov V, Melamed E, Dabby R. The effect of duloxetine on primary pain symptoms in Parkinson disease. Clin Neuropharmacol. 2007 Jul-Aug;30(4):201-5.
33. Iwaki H, Ando R, Tada S, Nishikawa N, Tsujii T, Yamanishi Y, et al. A double-blind, randomized controlled trial of duloxetine for pain in Parkinson’ s disease. J Neurol Sci. 2020 Jul 15;414:116833.
34. Brefel-Courbon C, Harroch E, Marques A, Devos D, Thalamas C, Rousseau V, et al. Oxycodone or Higher Dose of Levodopa for the Treatment of Parkinsonian Central Pain: OXYDOPA Trial. Mov Disord. 2024 Jun 8.
35. Reuter I, Mehnert S, Leone P, Kaps M, Oechsner M, Engelhardt M. Effects of a flexibility and relaxation programme, walking, and nordic walking on Parkinson’ s disease. J Aging Res. 2011;2011:232473.
36. Huissoud M, Boussac M, Joineau K, Harroch E, Brefel-Courbon C, Descamps E. The effectiveness and safety of non-pharmacological intervention for pain management in Parkinson’ s disease: A systematic review. Rev Neurol (Paris). 2023 Oct 11.
37. Cury RG, Galhardoni R, Fonoff ET, Dos Santos Ghilardi MG, Fonoff F, Arnaut D, et al. Effects of deep brain stimulation on pain and other nonmotor symptoms in Parkinson disease. Neurology. 2014 Oct 14;83(16):1403-9.
der informierte @rzt
- Vol. 16
- Ausgabe 1
- Januar 2026