- Welche Impfungen werden für Personen ab 65 Jahren empfohlen?
Angesichts der alternden Bevölkerung wird jeder Arzt ältere Patienten behandeln müssen, bei denen ein erhöhtes Risiko besteht, schwere Infektionsformen zu entwickeln und Begleiterkrankungen wie Herzinsuffizienz oder chronische Lungenerkrankungen zu dekompensieren. Präventionsmassnahmen sind daher unerlässlich. Impfungen sind eine der wirksamsten Strategien. Ab einem Alter von 65 Jahren werden mehrere Impfungen empfohlen. Zwischen Grippe, COVID-19, Gürtelrose, Pneumokokken, Tetanus und dem Respiratorischen Synzytial-Virus ist es nicht immer einfach, den Überblick zu behalten. Dieser Artikel bietet Klinikern praktische Hilfsmittel und Empfehlungen, um die Durchimpfungsrate ihrer Patienten ab 65 Jahren zu verbessern.
With the aging of the population, every healthcare worker will take care of older patients, who are at higher risk of developing severe infections and decompensation of their comorbidities. Preventive measures are therefore essential, and vaccination is one of the most effective strategies. From the age of 65, several vaccines are recommended. With influenza, COVID-19, shingles, pneumococcus, tetanus, and respiratory syncytial virus, it can be confusing. This article provides clinicians with practical tools and recommendations to help improve vaccine coverage among patients aged 65 and older.
Keywords: Vaccine-preventable diseases, Vaccination recommendations, prevention, gerontology, Vaccine hesitancy
Einleitung
Der Anteil der Bevölkerung ab 65 Jahren steigt (1). Laut Angaben der Weltgesundheitsorganisation (WHO) basiert gesundes Altern auf der Erhaltung «der funktionellen Fähigkeiten, die das Wohlbefinden im fortgeschrittenen Alter ermöglichen» (2). Impfungen sind eine sichere und wirksame Präventionsmassnahme, die zu diesem Ziel beiträgt. Menschen ≥ 65 Jahre haben ein erhöhtes Risiko für schwere Infektionen mit kardiorespiratorischen und neurologischen Komplikationen sowie einem Verlust der Selbstständigkeit (3). Das Bundesamt für Gesundheit (BAG) aktualisiert jedes Jahr den Impfplan, der teilweise speziell auf diese Bevölkerungsgruppe zugeschnitten ist (4). Dennoch ist die Durchimpfungsrate nach wie vor gering, obwohl sie für die Vorbeugung schwerer Erkrankungen in dieser gefährdeten Bevölkerungsgruppe von entscheidender Bedeutung ist. Dieser Artikel bietet Ärzten praktische Hilfsmittel für die Impfung von Personen ≥ 65 Jahren und aktualisiert die Daten zu konjugierten Pneumokokken-Impfstoffen (PCV) und Impfstoffen gegen das Respiratorische Synzytial-Virus (RSV).
Impfempfehlungen für Personen ab 65 Jahren
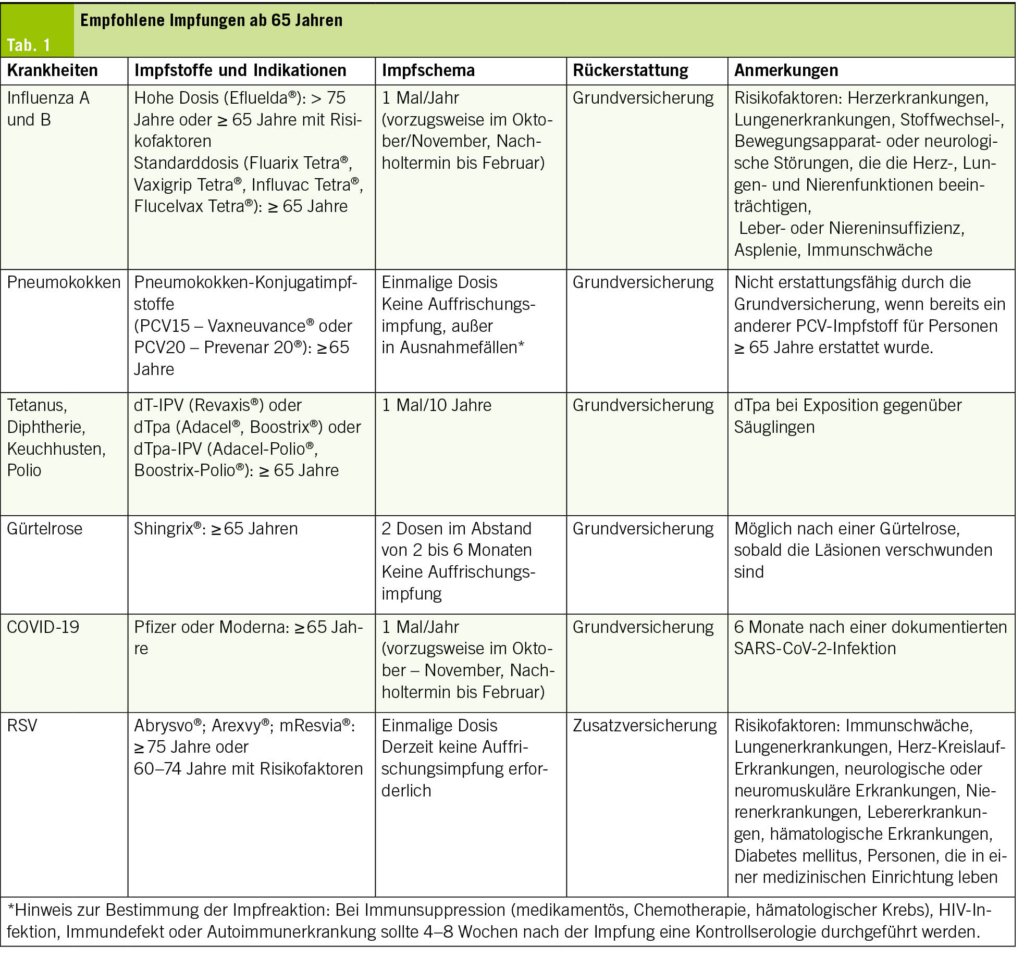
Das Immunsystem verändert sich im Laufe des Lebens. Ein Merkmal der Immunoseneszenz sind altersbedingte Veränderungen in Anzahl und Qualität der angeborenen und adaptiven Immunzellen. Beispiele hierfür sind eine Abnahme der Anzahl naiver B- und T-Zellen, eine Abnahme der Antikörperproduktion sowie eine Zunahme der Produktion proinflammatorischer Zytokine. Dadurch kann es zu einer chronischen, leichtgradigen Entzündung kommen, die als „Inflammaging” bezeichnet wird. Diese Veränderungen des Immunsystems erhöhen das Risiko von Komplikationen im Falle einer Infektion und verringern die Impfantwort (5, 6). Auch wenn die Wirksamkeit der Impfstoffe in dieser Bevölkerungsgruppe möglicherweise geringer ist, können sie dennoch die Schwere der Erkrankung verringern sowie Krankenhausaufenthalte, Komplikationen und Mortalität begrenzen (7). Die gemäß dem Impfplan 2025 ab 65 Jahren empfohlenen Impfstoffe sind in Tab. 1 zusammengefasst (4).
Impfstoffe gegen die saisonale Grippe
Personen ab 65 Jahren, die mit dem Grippevirus infiziert sind, haben ein erhöhtes Risiko, pulmonale, aber auch extrapulmonale Komplikationen zu entwickeln. Der Impfstoff wird jedes Jahr entsprechend den zirkulierenden Virusstämmen aktualisiert. Seine Wirksamkeit hängt vom Alter, von Begleiterkrankungen, aber auch von der Übereinstimmung zwischen den ausgewählten Impfvirenstämmen und den zirkulierenden Virenstämmen ab (8). Um die Immunantwort bei älteren Menschen zu verbessern, ist ein hochdosierter Impfstoff (HD) erhältlich, der viermal mehr Hämagglutinin-Antigen enthält als ein Standardimpfstoff. Er verstärkt die Immunogenität und senkt das Risiko einer grippebedingten Krankenhausbehandlung bei Personen ≥ 65 Jahren im Vergleich zum Standardimpfstoff um etwa 15 % (9, 10). Der Grippeimpfstoff soll schwere Formen der Infektion, Krankenhausaufenthalte und Komplikationen verhindern, aber auch Herz-Kreislauf-Erkrankungen und die Sterblichkeit begrenzen (3). In der Schweiz wird der HD-Impfstoff für Personen ≥ 75 Jahre und Personen ≥ 65 Jahre mit Risikofaktoren erstattet (Tab. 1). Grippeimpfstoffe sind sicher und gut verträglich. Im Durchschnitt zeigt 1 von 2 Personen lokale Reaktionen (Schmerzen an der Injektionsstelle, lokale Rötung, Schwellung oder Verhärtung) und 1 von 3 Personen allgemeine Symptome (Muskelschmerzen, Fieber usw.).
Impfung gegen COVID-19
SARS-CoV-2 ist weiterhin im Umlauf. In der Schweiz wird Personen ab 65 Jahren eine jährliche Impfung gegen COVID-19 im Herbst empfohlen (4). Die Impfung verringert das Risiko schwerer Verläufe, Krankenhausaufenthalte, Komplikationen und Todesfälle. Der Schutz vor Infektion und Übertragung ist jedoch nach wie vor sehr gering. Laut einer Fall-Kontroll-Studie in England ist die Wirksamkeit gegen Krankenhausaufenthalte im ersten Monat mit ca. 50 % am höchsten und nimmt dann allmählich auf ca. 13 % ab (11). Dies unterstreicht die Bedeutung einer jährlichen Wiederholungsimpfung bei älteren Menschen. Die Impfstoffe werden von dieser Bevölkerungsgruppe gut vertragen.
Die Nebenwirkungen ähneln denen des Grippeimpfstoffs, sind in der Regel mild und vorübergehend. Die Verabreichung mehrerer Dosen scheint das Risiko einer langen COVID-Erkrankung zu verringern (12).
Impfstoff gegen Gürtelrose
Gürtelrose steht im Zusammenhang mit der Reaktivierung des Varizella-Zoster-Virus (VZV) und äussert sich in der Regel durch einen bläschenartigen Hautausschlag. Das Risiko einer Reaktivierung des VZV steigt mit zunehmendem Alter: Jeder Dritte erkrankt im Laufe seines Lebens an Gürtelrose, jeder Zweite nach dem 85. Lebensjahr (13). Die häufigste Komplikation ist die postherpetische Neuralgie, die zu einer Mehrfachmedikation, Depressionen und einem Verlust der Selbstständigkeit führen kann. Es können auch ophthalmologische und neurologische Komplikationen auftreten (14). Der rekombinante Herpes-Zoster-Impfstoff (RZV), der aus dem Glykoprotein E des VZV (gE) und dem Adjuvans AS01B besteht, wird in zwei Dosen im Abstand von 2 bis 6 Monaten verabreicht. Er reduziert das Risiko einer Post-Zoster-Neuralgie um 87 % und das Risiko einer ophthalmischen Herpes-Zoster-Infektion um 78 % (15). Die Wirksamkeit ist nach einer einzigen Dosis deutlich geringer (15, 16), weshalb es wichtig ist, die Patienten über die Notwendigkeit beider Dosen aufzuklären. RZV kann nach einer Gürtelrose-Episode verabreicht werden, sobald die Hautläsionen verheilt sind. Seine Wirksamkeit zur Vorbeugung einer Gürtelrose-Episode bleibt über einen längeren Zeitraum bestehen (70–84 %) ohne signifikante Unterschiede je nach Alter (17, 18). Nebenwirkungen wie Schmerzen an der Injektionsstelle, Muskelschmerzen und Müdigkeit treten häufig auf, sind in der Regel leicht bis mässig stark und vorübergehend (19). Es ist wichtig, die Patienten über diese Nebenwirkungen zu informieren und sie zu beruhigen: Eine Reaktion nach der ersten Injektion bedeutet nicht, dass sie auch nach der zweiten eine Reaktion haben werden, und umgekehrt.
Impfstoffe gegen Tetanus, Diphtherie (+/– Keuchhusten, +/– Poliomyelitis)
In der Schweiz sind nur Impfstoffe gegen Tetanus-Diphtherie in Kombination mit Keuchhusten und/oder Poliomyelitis zugelassen. Ab einem Alter von 65 Jahren wird alle 10 Jahre eine Auffrischungsimpfung gegen Tetanus empfohlen. Bei Kontakt mit Säuglingen wird ein Impfstoff empfohlen, der Keuchhusten einschliesst. Bei Reisen in ein Risikoland ist eine Impfung gegen Poliomyelitis angezeigt.
Neuheiten
Konjugierte Pneumokokken-Impfstoffe
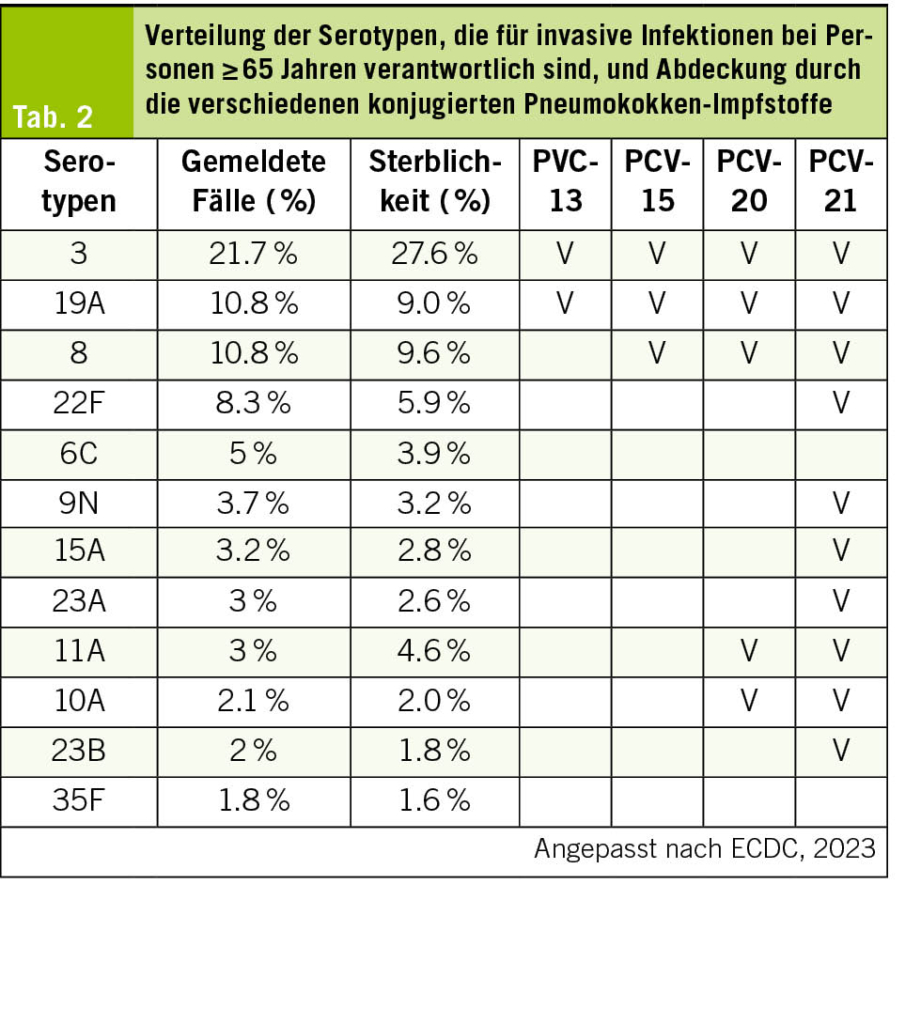
Es wurden über 100 Serotypen von Streptococcus pneumoniae identifiziert, von denen einige mit invasiven Erkrankungen wie Bakteriämien oder Meningitiden in Verbindung gebracht werden. Die Inzidenz und Mortalität invasiver Infektionen mit S. pneumoniae betrifft vor allem Kinder unter 5 Jahren und Erwachsene über 65 Jahren (20). Bei letzteren kann eine Pneumokokkeninfektion zu kardiovaskulären und pulmonalen Komplikationen sowie zu einem Verlust der Selbstständigkeit führen. Pneumokokken-Konjugatimpfstoffe (PCV) wurden entwickelt, um die Immunogenität zu verbessern und die Schutzdauer zu verlängern (21). Im Gegensatz zu Polysaccharid-Impfstoffen verbinden PCV die Polysaccharide mit einem Trägerprotein, wodurch eine Gedächtnisimmunität und Antikörper mit hoher Affinität ermöglicht werden (22). Aufgrund der begrenzten Serotypabdeckung der ersten PCV haben einige Länder weiterhin den 23-valenten Polysaccharid-Impfstoff verwendet, manchmal nach Verabreichung einer Dosis PCV-13. Mit der Einführung von PCV mit höherer Valenz (PCV-15, PCV-20) stehen nun mehr Optionen zur Verfügung. Tab. 2 zeigt die zehn Pneumokokken-Serotypen, die am häufigsten für invasive Infektionen (IIP) bei Personen ≥ 65 Jahren in Europa verantwortlich sind, sowie deren Abdeckung durch PCV gemäss den Daten des Europäischen Zentrums für die Prävention und die Kontrolle von Krankheiten (ECDC).
In Europa beträgt die Abdeckung der für IIP verantwortlichen Serotypen bei Personen ≥ 65 Jahren etwa 33 % für PCV13, 43 % für PCV15 und 56,7 % für PCV-20 (23). Ein PCV-21, das entwickelt wurde, um die für invasive Erkrankungen bei älteren Menschen verantwortlichen Serotypen besser abzudecken, wurde bereits von der FDA und der EMA zugelassen. Es wird derzeit von Swissmedic geprüft. Diese neuen Impfstoffe bieten einen besseren Schutz als PPSV-23.
In der Schweiz wird empfohlen, Personen ab 65 Jahren mit PCV-15 oder PCV-20 zu impfen. Bei einer früheren Impfung mit dem Polysaccharid-Impfstoff oder PCV-13 kann eine Impfung ein Jahr nach der Auffrischungsimpfung durchgeführt werden. Cave: Wenn eine PCV-13-Impfung im Alter von 65 Jahren oder älter durchgeführt und von der Grundversicherung übernommen wurde, erstattet diese die neue PCV-Impfung nicht. Die Konjugatimpfstoffe sind sicher und gut verträglich. Bei Personen über 65 Jahren ist die häufigste Nebenwirkung eine Rötung an der Injektionsstelle (30 %), gefolgt von einer lokalen Schwellung (18 %), Schmerzen an der Injektionsstelle und Müdigkeit.
Impfstoffe gegen das Respiratorische Synzytial-Virus
RSV verursacht Atemwegsinfektionen, die von einfachen Infektionen der oberen Atemwege bis hin zu schweren, potenziell tödlichen Infektionen der unteren Atemwege reichen. Es kann auch zu kardiovaskulären Komplikationen führen oder bestimmte Begleiterkrankungen verschlimmern. Die klinischen Symptome des RSV ähneln denen anderer Atemwegsviren. Krankenhausaufenthalte betreffen hauptsächlich Erwachsene mit Grunderkrankungen wie Asthma, chronisch obstruktiver Lungenerkrankung (COPD) oder Herzinsuffizienz (24).
In der Schweiz sind drei Impfstoffe gegen RSV zugelassen und erhältlich: Abrysvo®, ein nicht adjuvierter Impfstoff, der das Präfusions-Oberflächenprotein RSVPreF beider RSV-Subtypen (A und B) enthält; Arexvy®, ein adjuvierter Impfstoff, der das Präfusions-Oberflächenprotein RSVpreF3 des RSV-Subtyps A2 und das Adjuvans AS01E enthält. Es handelt sich um dasselbe Adjuvans wie in Shingrix®, jedoch in halber Dosierung; und mRESVIA®, ein mRNA-Impfstoff, der für das Präfusions-Oberflächenprotein RSVpreF des Subtyps A kodiert und in Nanopartikeln eingekapselt ist. In den Phase-3-Studien wurden nicht dieselben Bewertungskriterien verwendet, sodass ein Vergleich nicht möglich ist. Ihre Wirksamkeit gegen Infektionen der unteren Atemwege scheint jedoch ähnlich zu sein, mit einem akzeptablen Verträglichkeitsprofil (25–27). Eine Studie in den Vereinigten Staaten bei Personen ≥ 60 Jahren zeigte eine Impfwirksamkeit von 80 % (95 % KI: 71–85) gegen RS-Virus-assoziierte Krankenhausaufenthalte (28).
In der Schweiz werden diese drei Impfstoffe für Personen ab 75 Jahren und für Personen zwischen 60 und 74 Jahren mit Risikofaktoren empfohlen (Tab. 1). Sie werden für diese Bevölkerungsgruppe noch nicht von der Grundversicherung erstattet. Aktuelle Daten zeigen eine Wirksamkeit von mindestens zwei Saisons nach der Impfung mit diesen Impfstoffen (29–31). Derzeit wird keine zusätzliche Dosis empfohlen.
Fragen und Antworten zur Impfpraxis
Wann und wie impfen?
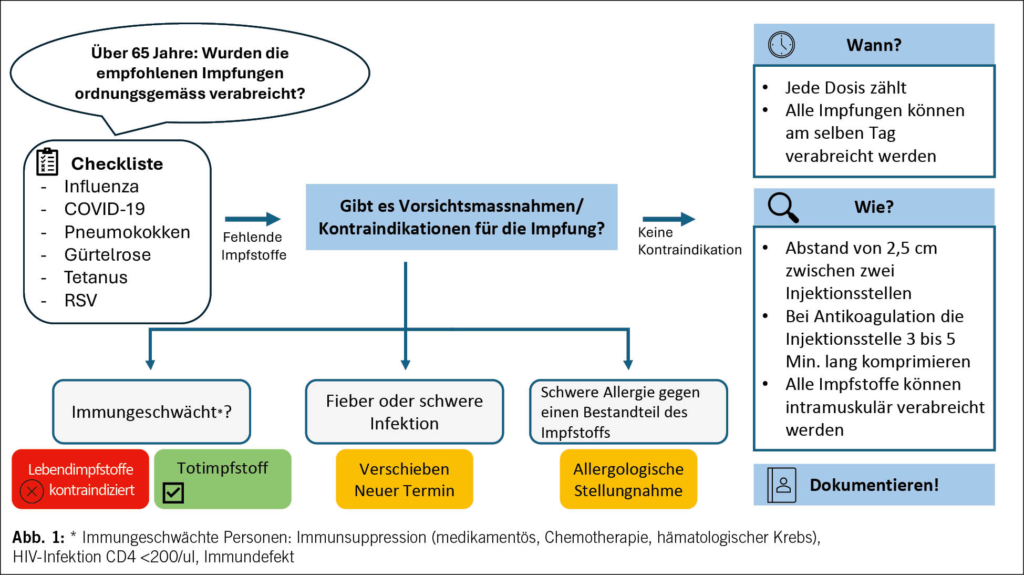
Abb. 1 fasst die praktischen Aspekte der Impfung in Bezug auf die Art der Injektion, den zeitlichen Abstand zwischen den einzelnen Impfungen und Vorsichtsmassnahmen/Kontraindikationen zusammen. Die gleichzeitige Verabreichung ist sicher und wirksam (32). Sie führt nicht zu mehr Nebenwirkungen. Eine Auffrischungsimpfung kann am selben Tag oder nach Belieben des Patienten und des Arztes über einen längeren Zeitraum verteilt erfolgen. Es ist nie zu spät, die Impfungen für seine Patienten auf den neuesten Stand zu bringen.
Patienten, die aufgrund ihrer Grunderkrankung oder aufgrund immunsuppressiver Behandlungen immunsupprimiert sind, haben ein höheres Risiko, Infektionen zu entwickeln, und sprechen schlechter auf Impfstoffe an (33). Die Überwachung der Immunantwort auf Impfstoffe wie Pneumokokken und Tetanus kann als Orientierung für spätere Impfungen dienen (Auffrischungsdosen, Verwendung hoher Dosen). Die Analyse kann im Impfstofflabor der Kantonsspitäler durchgeführt werden. Lebendimpfstoffe sind aufgrund des Risikos einer Impfkrankheit bei Immunsuppression kontraindiziert.
Wie behält man Impfungen im Blick?
Mangelnde Kenntnisse, Zeitmangel des Gesundheitspersonals für Präventionsmassnahmen, fehlende Dokumentation der Impfgeschichte, Impfskepsis von Patienten und Pflegekräften, Verbreitung falscher Informationen, Kosten und Zugang zu bestimmten Impfstoffen sind Beispiele für Hindernisse für die Impfung.
Die vom BAG unterstützte Plattform Infovac (www.infovac.ch) besteht aus einem Netzwerk von Impfexperten, das regelmässig aktualisierte Informationen zu impfpräventablen Erkrankungen bereitstellt und den Abonnentinnen und Abonnenten einen Dienst zur Beantwortung von Fragen zur Impfung anbietet.
Die Aufforderung an Patienten, ihren Impfpass zu vervollständigen, ist eine Möglichkeit, die Dokumentation zu verbessern. Einige personalisierte elektronische Patientenakten verfügen über einen speziellen Bereich für die Erfassung von Impfungen. Die systematische Identifizierung von Patienten mit veralteten Impfungen und die Einführung von Impfprotokollen erleichtern die Aktualisierung des Impfstatus (34). Alle Angehörigen der Gesundheitsberufe, auch im Krankenhausbereich, spielen eine Rolle bei der Bekämpfung von Fehlinformationen und der Förderung von Impfungen. Impfungen im Krankenhaus verlängern nicht die Dauer des Krankenhausaufenthalts. Sie ist sogar mit einem Rückgang der Wiederaufnahmen verbunden (35).
Die Aufnahme in eine medizinisch-soziale Einrichtung ist ein strategischer Zeitpunkt, um den Impfstatus der Patienten zu bewerten und sie sowie ihre therapeutischen Vertreter über die durchzuführenden Impfungen zu informieren. Jedes Jahr sollte eine Informationskampagne gegen Grippe und COVID-19 dazu beitragen, diese Impfungen auf den neuesten Stand zu bringen.
Was soll ich meinem Patienten vor der Impfung sagen?
Es scheint von entscheidender Bedeutung zu sein, dass der Patient versteht, welche Krankheiten durch die Impfung verhindert werden und welche Auswirkungen diese Krankheiten haben können, damit er die Impfvorschläge akzeptiert. Die Aufklärung des Patienten über mögliche Nebenwirkungen der Impfstoffe trägt ebenfalls zu einer besseren Akzeptanz künftiger Impfungen bei.
Wie geht man mit einem impfkritischen Patienten um?
Im Gegensatz zu einem faktenbasierten Ansatz ermöglicht ein motivierender Ansatz, impfkritische Patienten und/oder ihre therapeutischen Vertreter bei kognitiven Störungen zu einer besseren Akzeptanz von Impfungen zu begleiten. Ein motivierendes Gespräch verläuft in der Regel in mehreren Schritten: 1. Aufbau einer Vertrauensbeziehung durch einfühlsames Zuhören ohne Wertung. 2. Erforschung und Verständnis der persönlichen Gründe für die Impfskepsis der Person, um herauszufinden, welche Art von Informationen ihre Meinung ändern könnten. 3. Nach der Zustimmung des Patienten werden klare und relevante Informationen bereitgestellt, die eine fundierte und autonome Entscheidungsfindung unterstützen. 4. Respektierung ihrer Autonomie, während das Gespräch in Richtung einer positiveren Sichtweise auf die Impfung gelenkt wird (36).
Fazit
Infektionskrankheiten gehören zu den Haupttodesursachen bei Menschen über 65 Jahren. Impfungen sind eine sichere und wirksame Präventionsmassnahme; sie schützen nicht nur vor Infektionen, sondern auch vor Krankenhausaufenthalten, Komplikationen durch Begleiterkrankungen und dem Verlust der Selbstständigkeit. Dennoch ist die Durchimpfungsrate in dieser Risikogruppe nach wie vor gering.
Die Einführung von Impfprogrammen, die auf die Bedürfnisse älterer Menschen zugeschnitten sind, sowie eine verstärkte Informations- und Kommunikationsarbeit können dazu beitragen, die Impfskepsis zu verringern und Menschen ab 65 Jahren besser zu schützen.
Copyright
Aerzteverlag medinfo AG
Übersetzung aus la gazette médicale 06/25
Service de médecine interne de l’ âgé
Département de Réadaptation et Gériatrie
Hôpitaux Universitaires de Genève
– Service de médecine interne de l’ âgé
Département de Réadaptation et Gériatrie
Hôpitaux Universitaires de Genève
– Service de maladies infectieuses
Département de Médecine
Hôpitaux Universitaires de Genève
Centre de vaccinologie
Hôpitaux Universitaires de Genèv
Es liegen keine Interessenkonflikte im Zusammenhang mit diesem Artikel vor.
- Personen ≥ 65 Jahren haben ein erhöhtes Risiko, schwere Infektionen zu entwickeln und nach einer Infektion insbesondere kardiorespiratorische und neurologische Komplikationen zu erleiden.
- Die Impfung ist eine sichere und wirksame Präventionsmassnahme, mit der sich durch Impfungen vermeidbare Infektionen, deren Schweregrad und Komplikationen begrenzen lassen.
- Die Impfung hat auch eine indirekte kardioprotektive Wirkung und wirkt sich auf die Gesamtmortalität aus.
- An die Impfung zu denken, die Patienten und sogar ihre Familien zu informieren, ihre Fragen zu beantworten, die Impfungen gemäss den Empfehlungen zu dokumentieren und zu aktualisieren, sind wichtige Schritte, die in die tägliche Praxis integriert werden müssen, um unsere Patienten zu schützen und ihre Selbstständigkeit zu erhalten.
1. Ageing and health [Internet]. [cité 18 juill 2024]. Disponible sur: www.who.int/news-room/fact-sheets/detail/ageing-and-health
2. WHO’ s work on the UN Decade of Healthy Ageing (2021-2030) [Internet]. [cité 5 août 2024]. Disponible sur: https://www.who.int/initiatives/decade-of-healthy-ageing
3. Addario A, Célarier T, Bongue B, Barth N, Gavazzi G, Botelho-Nevers E. Impact of influenza, herpes zoster, and pneumococcal vaccinations on the incidence of cardiovascular events in subjects aged over 65 years: a systematic review. GeroScience. déc 2023;45(6):3419‑47.
4. Plan de vaccination suisse [Internet]. [cité 1 juill 2025]. Disponible sur: https://www.bag.admin.ch/fr/plan-de-vaccination-suisse
5. Chambers ES, Akbar AN. Can blocking inflammation enhance immunity during aging? J Allergy Clin Immunol. mai 2020;145(5):1323‑31.
6. Ecarnot F, Maggi S. Vaccination against Respiratory Infections in the Immunosenescent Older Adult Population: Challenges and Opportunities. Semin Respir Crit Care Med. févr 2025;46(1):53‑62.
7. Ciarambino T, Crispino P, Buono P, Giordano V, Trama U, Iodice V, et al. Efficacy and Safety of Vaccinations in Geriatric Patients: A Literature Review. Vaccines. 24 août 2023;11(9):1412.
8. Recommended composition of influenza virus vaccines for use in the 2025-2026 northern hemisphere influenza season [Internet]. [cité 25 juin 2025]. Disponible sur: https://www.who.int/publications/m/item/recommended-composition-of-influenza-virus-vaccines-for-use-in-the-2025-2026-nh-influenza-season
9. DiazGranados CA, Dunning AJ, Kimmel M, Kirby D, Treanor J, Collins A, et al. Efficacy of high-dose versus standard-dose influenza vaccine in older adults. N Engl J Med. 14 août 2014;371(7):635‑45.
10. Lee JKH, Lam GKL, Shin T, Samson SI, Greenberg DP, Chit A. Efficacy and effectiveness of high-dose influenza vaccine in older adults by circulating strain and antigenic match: An updated systematic review and meta-analysis. Vaccine. 15 mars 2021;39 Suppl 1:A24‑35.
11. Kirsebom FCM, Stowe J, Bernal JL, Allen A, Andrews N. Effectiveness of autumn 2023 COVID-19 vaccination and residual protection of prior doses against hospitalisation in England, estimated using a test-negative case-control study. J Infect [Internet]. 1 juill 2024 [cité 25 juin 2025];89(1). Disponible sur: https://www.journalofinfection.com/article/S0163-4453(24)00111-7/fulltext
12. Byambasuren O, Stehlik P, Clark J, Alcorn K, Glasziou P. Effect of covid-19 vaccination on long covid: systematic review. BMJ Med. 2023;2(1):e000385.
13. Forbes HJ, Thomas SL, Langan SM. The Epidemiology and Prevention of Herpes Zoster. Curr Dermatol Rep. 1 mars 2012;1(1):39‑47.
14. Kennedy PGE. The Spectrum of Neurological Manifestations of Varicella-Zoster Virus Reactivation. Viruses. 30 juill 2023;15(8):1663.
15. Zerbo O, Bartlett J, Fireman B, Goddard K, Duffy J, Glanz J, et al. Recombinant Zoster Vaccination and Risk of Postherpetic Neuralgia or Zoster Ophthalmicus. JAMA Netw Open. 10 juin 2025;8(6):e2514615.
16. Zerbo O, Bartlett J, Fireman B, Lewis N, Goddard K, Dooling K, et al. Effectiveness of Recombinant Zoster Vaccine Against Herpes Zoster in a Real-World Setting. Ann Intern Med. févr 2024;177(2):189‑95.
17. Izurieta HS, Wu X, Forshee R, Lu Y, Sung HM, Agger PE, et al. Recombinant Zoster Vaccine (Shingrix): Real-World Effectiveness in the First 2 Years Post-Licensure. Clin Infect Dis Off Publ Infect Dis Soc Am. 15 sept 2021;73(6):941‑8.
18. Boutry C, Hastie A, Diez-Domingo J, Tinoco JC, Yu CJ, Andrews C, et al. The Adjuvanted Recombinant Zoster Vaccine Confers Long-Term Protection Against Herpes Zoster: Interim Results of an Extension Study of the Pivotal Phase 3 Clinical Trials ZOE-50 and ZOE-70. Clin Infect Dis Off Publ Infect Dis Soc Am. 28 avr 2022;74(8):1459‑67.
19. Parikh R, Singer D, Chmielewski-Yee E, Dessart C. Effectiveness and safety of recombinant zoster vaccine: A review of real-world evidence. Hum Vaccines Immunother. 15 déc 2023;19(3):2263979.
20. Humphreys H, Corcoran M, Mereckiene J, Cunney R, Cotter S. Invasive pneumococcal surveillance to assess the potential benefits of extended spectrum conjugate vaccines (PCV15/PCV20) in older adults. Epidemiol Infect. 26 janv 2023;151:e27.
21. Vadlamudi NK, Parhar K, Altre Malana KL, Kang A, Marra F. Immunogenicity and safety of the 13-valent pneumococcal conjugate vaccine compared to 23-valent pneumococcal polysaccharide in immunocompetent adults: A systematic review and meta-analysis. Vaccine. 14 févr 2019;37(8):1021‑9.
22. Pollard AJ, Perrett KP, Beverley PC. Maintaining protection against invasive bacteria with protein-polysaccharide conjugate vaccines. Nat Rev Immunol. mars 2009;9(3):213‑20.
23. Surveillance Atlas of Infectious Diseases [Internet]. [cité 15 juill 2025]. Disponible sur: https://atlas.ecdc.europa.eu/public/index.aspx?Dataset=27&HealthTopic=40
24. Landi SN, Garofalo DC, Reimbaeva M, Scott AM, Jiang L, Cappell K, et al. Hospitalization Following Outpatient Diagnosis of Respiratory Syncytial Virus in Adults. JAMA Netw Open. 19 nov 2024;7(11):e2446010.
25. Walsh EE, Pérez Marc G, Zareba AM, Falsey AR, Jiang Q, Patton M, et al. Efficacy and Safety of a Bivalent RSV Prefusion F Vaccine in Older Adults. N Engl J Med. 20 avr 2023;388(16):1465‑77.
26. Papi A, Ison MG, Langley JM, Lee DG, Leroux-Roels I, Martinon-Torres F, et al. Respiratory Syncytial Virus Prefusion F Protein Vaccine in Older Adults. N Engl J Med. 16 févr 2023;388(7):595‑608.
27. Wilson E, Goswami J, Baqui AH, Doreski PA, Perez-Marc G, Zaman K, et al. Efficacy and Safety of an mRNA-Based RSV PreF Vaccine in Older Adults. N Engl J Med. 14 déc 2023;389(24):2233‑44.
28. Payne AB, Watts JA, Mitchell PK, Dascomb K, Irving SA, Klein NP, et al. Respiratory syncytial virus (RSV) vaccine effectiveness against RSV-associated hospitalisations and emergency department encounters among adults aged 60 years and older in the USA, October, 2023, to March, 2024: a test-negative design analysis. The Lancet. 19 oct 2024;404(10462):1547‑59.
29. Walsh EE, Eiras D, Woodside J, Jiang Q, Patton M, Marc GP, et al. Efficacy, Immunogenicity, and Safety of the Bivalent Respiratory Syncytial Virus (RSV) Prefusion F Vaccine in Older Adults Over 2 RSV Seasons. Clin Infect Dis. 10 févr 2025;ciaf061.
30. Ison MG, Papi A, Athan E, Feldman RG, Langley JM, Lee DG, et al. Efficacy, safety, and immunogenicity of the AS01E-adjuvanted respiratory syncytial virus prefusion F protein vaccine (RSVPreF3 OA) in older adults over three respiratory syncytial virus seasons (AReSVi-006): a multicentre, randomised, observer-blinded, placebo-controlled, phase 3 trial. Lancet Respir Med. juin 2025;13(6):517‑29.
31. Priddy F. – Safety & Immunogenicity in 18-59 Year Olds at increased Risk for RSV Disease* – Revaccination of Adults at 12 or 24 Months. 2025;
32. Chang YC, Chou YJ, Liu JY, Yeh TF, Huang N. Additive benefits of pneumococcal and influenza vaccines among elderly persons aged 75 years or older in Taiwan–a representative population-based comparative study. J Infect. sept 2012;65(3):231‑8.
33. Eperon G, Bühler S, Enriquez N, Vaudaux B. [The immunosuppressed traveler : vaccination guidelines]. Rev Med Suisse. 2 mai 2018;14(605):922‑33.
34. Frangos E, Barratt J, Michel JP, Ecarnot F. Vaccines in Long-Term Care Settings: A Narrative Review. Gerontology. 2024;70(3):241‑7.
35. Tartof SY, Qian L, Liu ILA, Tseng HF, Sy LS, Hechter RC, et al. Safety of Influenza Vaccination Administered During Hospitalization. Mayo Clin Proc. mars 2019;94(3):397‑407.
36. Verger P, Cogordan C, Fressard L, Gosselin V, Donato X, Biferi M, et al. A postpartum intervention for vaccination promotion by midwives using motivational interviews reduces mothers’ vaccine hesitancy, south-eastern France, 2021 to 2022: a randomised controlled trial. Euro Surveill Bull Eur Sur Mal Transm Eur Commun Dis Bull. sept 2023;28(38):2200819.
der informierte @rzt
- Vol. 16
- Ausgabe 2
- Februar 2026