- Orale GnRH-Antagonisten
Relugolix plus Add-back (Ryeqo®) kombiniert einen oralen GnRH-Antagonisten mit Estradiol und Norethisteronacetat zur Behandlung von Myom-assoziierter Hypermenorrhoe und Endometriose-assoziierten Schmerzen. Phase-3-Studien (LIBERTY, SPIRIT) zeigten signifikante Reduktionen von Menstruationsblutungen, Myomvolumen (> 50 %) und Endometriose-bedingten Schmerzen bei stabiler Knochendichte. Häufige Nebenwirkungen waren Kopfschmerzen, Hitzewallungen und Zwischenblutungen; nach Therapieende traten teilweise Rezidive auf. Relugolix plus Add-back eignet sich für präoperative oder konservative Anwendungen sowie bei Endometriose als Alternative zu einer Gestagentherapie bei ungenügender Wirkung oder nicht akzeptablen Nebenwirkungen. Daten zur Langzeitanwendung (über 2 Jahre) fehlen.
Relugolix plus add-back (Ryeqo®) combines an oral GnRH antagonist with estradiol and norethisterone acetate for the treatment of myoma-associated hypermenorrhea and endometriosis-associated pain. Phase 3 studies (LIBERTY, SPIRIT) showed significant reductions in menstrual bleeding, fibroid volume (>50%) and endometriosis-related pain with stable bone density. Common side effects included headaches, hot flashes, and breakthrough bleeding; some patients experienced recurrence after the end of therapy. Relugolix plus add-back is suitable for preoperative or conservative applications as well as for endometriosis as an alternative to progestin therapy in cases of insufficient effect or unacceptable side effects. Data on long-term use (over 2 years) are lacking.
Keywords: orale GnRH-Antagonisten mit add back, Myome, Hypermenorrhoe, Endometriose
Myome und Endometriose zählen zu den häufigsten gynäkologischen Erkrankungen im reproduktiven Alter und sind mit erheblicher Morbidität verbunden (1). Die hormonabhängige Pathogenese beider Erkrankungen bildet die Grundlage für medikamentöse Therapiestrategien, die eine Suppression der Östrogenproduktion anstreben. Relugolix plus add back (Estradiol 1 mg und Norethisteronacetat 0.5 mg), unter dem Handelsnamen Ryeqo®, ist ein Medikament zur Behandlung Endometriose-assoziierter Schmerzen sowie für die Behandlung von Myom-assoziierter Hypermenorrhoe.
Wirkungsweise
Ryeqo® beinhaltet eine Kombination aus Relugolix 40 mg sowie einer integrierten add-back-Therapie mit Estradiol 1 mg und Norethisteronacetat 0.5 mg. Relugolix ist ein nicht-peptidischer GnRH-Rezeptorantagonist, welcher kompetitiv an die GnRH-Rezeptoren im Hypophysenvorderlappen bindet und zu einer Suppression des luteinisierenden Hormons (LH) sowie des follikelstimulierenden Hormons (FSH) führt. Diese Suppression resultiert in einer ausgeprägten Reduktion der ovariellen Östrogen- und Progesteronproduktion.
Endometriosegewebe ist sensibel auf Östrogene und wird für die Proliferation und Inflammation des endometrialen Gewebes benötigt (2, 3). Auch Myomgewebe weist Rezeptoren für Östrogene und Progesteron auf. Sexualsteroide zählen zu den wichtigsten Faktoren für die Pathogenese von Uterusmyomen (4).
Relugolix als Monotherapie kann die Östradiolspiegel bis unter 60 pmol/l senken (5). Dadurch können Beschwerden wie myombedingte Hypermenorrhoe sowie mittelschwere bis starke Schmerzen im Zusammenhang mit Endometriose, einschliesslich Dysmenorrhoe, nichtmenstruellen Beckenschmerzen und Dyspareunie gelindert werden. Als Monotherapie ist die Anwendung von Relugolix jedoch mit Anzeichen und Symptomen eines hypoöstrogenen Zustands, wie Knochendichteverlust oder vasomotorischen Symptome, verbunden (6). Durch das add back von Estradiol 1 mg und Norethisteronacetat 0.5 mg wird die Östradiolblutkonzentration angehoben auf 90–150 pmol/l. Somit ist Östradiol in einem Bereich ohne Symptome eines hypoöstrogen Zustands, aber weiterhin in einem Bereich unter der Schwelle für die Stimulation von Myomwachstum und endometrialer Proliferation und somit von myom- und endometriosebedingten Symptomen und Schmerzen (7).
Ergebnisse der LIBERTY- und SPIRIT-Studien
LIBERTY 1 und 2-Studie
Die LIBERTY-Studien 1-und 2 sind multizentrische, randomisierte, doppelt-blinde, placebo-kontrollierte Phase-3-Studien (n=388 in LIBERTY-1 und n=382 in LIBERTY-2, 24 Wochen), welche die Wirksamkeit und Sicherheit von Relugolix mit add back bei der Behandlung von schweren Menstruationsblutungen aufgrund von Uterusmyomen prüfen.
Es wurde in drei Gruppen randomisiert: Frauen mit Relugolix und add back vs. Frauen mit 12 Wochen Relugolix-Monotherapie und dann 12 Wochen Relugolix mit add back vs. Placebo. Unter der Therapie mit Relugolix und add back konnte für signifikant mehr Patientinnen eine Reduktion des menstruellen Blutverlusts auf kleiner als 80 ml sowie um mehr als die Hälfte im Vergleich zum Ausgangswert in Woche 24 (LIBERTY-1 73 % vs. 19 %; LIBERTY-2 71 % vs. 15 %; p < 0.001 für beide Vergleiche) gezeigt werden. Zusätzlich kam es zu einer signifikanten Verbesserung myombedingter Schmerzen und Anämie, zu einer höheren Amenorrhoerate sowie zu einer signifikanten Verringerung des Gebärmuttervolumens (8).
LIBERTY long-term extension study
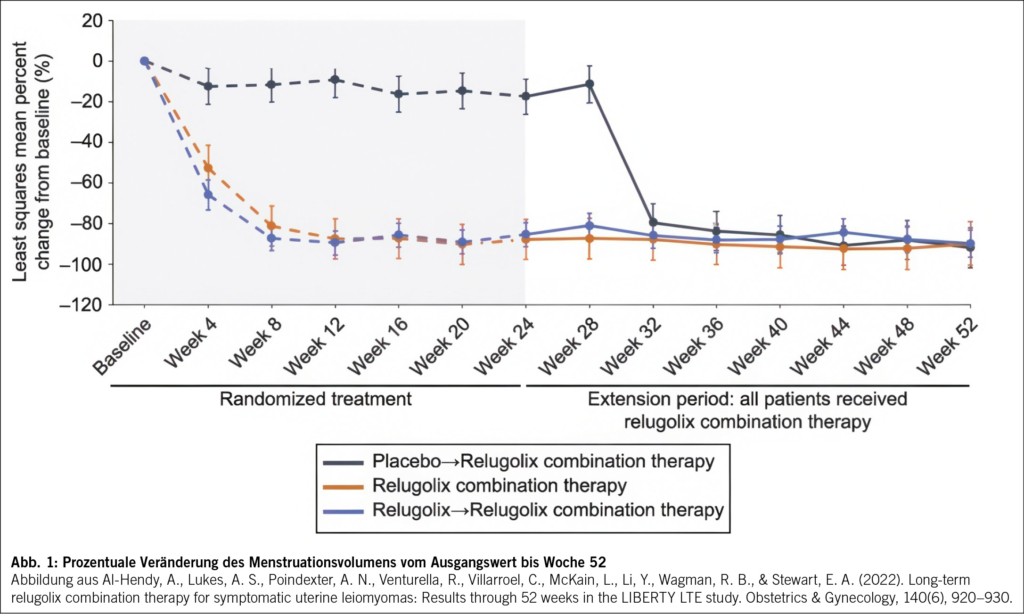
Die anschliessenden LIBERTY Long-Term Extension Study (n = 477, 52 Wochen) war eine offene, einarmige Langzeit-Extension mit der täglichen Gabe der Relugolix mit add-back-Therapie. Relugolix mit add back zeigte eine anhaltende Wirksamkeit bei Blutungskontrolle (Abb. 1), Verbesserung von Anämie und Symptomen, mit stabiler Knochendichte und guter Verträglichkeit. Des Weiteren konnte eine Reduktion der Myomgrösse von >50 % bei 36.6 % der Patientinnen in Woche 52 dokumentiert werden (9).
LIBERTY Randomized Withdrawal Study
In der anschliessenden LIBERTY Randomized Withdrawal Study (n=229, 104 Wochen) wurden Frauen nach Relugolix mit add back, welche die 24-wöchige LIBERTY1/2-Studien + 28-wöchige Extension abgeschlossen hatten, randomisiert für Relugolix mit add back vs. Placebo. Patientinnen, welche erneute Menstruationsblutungen mit > 80 ml nach Absetzen der Therapie zeigten, wurde eine Rescue-Therapie mit Relugolix und add back angeboten (10).
Die Ergebnisse zeigten in Woche 104 eine signifikante Wirkung von Relugolix mit add back auf die Blutungsstärke (69.8 % Relugolix vs. 11.8 % Placebo (Δ 58.0 %; p<0.0001). Die Rückfallrate lag beim Placebo bei 88.3 % bis Woche 104 (Median Zeit bis Rückfall: 5.9 Wochen). Eine Rescue-Therapie benötigten 97.8 % der Placebo-Patientinnen (10).
Zudem wurde 2025 eine post-hoc-Analyse der LIBERTY 1- und 2-Studien durchgeführt sowie eine Subgruppenanalyse der 111 Frauen mit Adenomyose, welche ebenfalls eine signifikante Verbesserung der Symptomatik zeigten (11).
SPIRIT 1 und 2, SPIRIT-Verlängerungsstudie
Die SPIRIT 1 und SPIRIT 2-Studien waren doppelblind-randomisierte Phase-3-Studien zur Überprüfung von Wirksamkeit und Sicherheit von Relugolix mit add back bei Endometriose-bedingten Schmerzen im Vergleich zu Placebo. Insgesamt wurden 638 (SPIRIT 1) bzw. 623 Frauen (SPIRIT 2) über 24 Wochen behandelt. Die Therapie mit Relugolix und add back zeigte hohe Ansprechraten und signifikante Reduktionen von Dysmenorrhoe (75 %), nicht-menstruellen Unterbauchschmerzen (59 % in SPIRIT 1, 66 % in SPIRIT 2) und Dyspareunie (12).
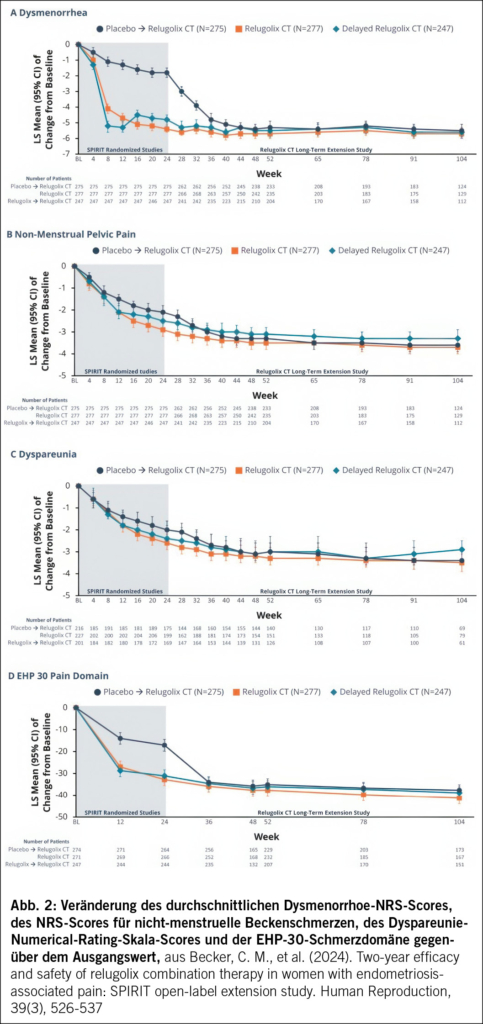
Die SPIRIT-Verlängerungsstudie (einarmig, 104 Wochen) bestätigte eine anhaltende Verbesserung von Dysmenorrhoe und Unterbauchschmerzen sowie eine Verringerung des Einsatzes von Analgetika (13) (Abb. 2).
Indikation
Seit Februar 2023 ist Relugolix plus add back in der Schweiz zugelassen für die Therapie einer Myom-assoziierten Hypermenorrhoe bei prämenopausalen Frauen sowie seit 2025 zur Behandlung mässiger bis starker Endometriose-assoziierter Schmerzen, welche auf eine Gestagentherapie unzureichend angesprochen haben oder wenn eine Gestagentherapie nicht möglich ist (14).
Anwendung
Eine Tablette Relugolix plus add back wird täglich etwa zur selben Tageszeit und ohne Unterbrechung eingenommen (15). Begonnen werden soll mit Relugolix plus add back in den ersten 5 Zyklustagen, sonst werden vermehrt unregelmässige Blutungen erwartet (15).
Vor Beginn mit Relugolix plus add back muss bei der Krankenkasse eine Kostengutsprache eingeholt werden. Meist werden die Kosten von einer Zusatzversicherung, aktuell jedoch (noch) nicht von der Grundversicherung übernommen. Dies zu erwähnen ist wichtig bei der Besprechung einer Ryeqo®-Therapie mit der Patientin. Relugolix plus add back ist für eine Therapiedauer von bis zu 24 Monaten zugelassen (14).
Häufige Nebenwirkungen umfassten Kopfschmerzen (13 %), Hitzewallungen (8.1 %), Hypertonie (5 %), Zwischenblutungen, Übelkeit und leichte gastrointestinale Beschwerden (8, 16).
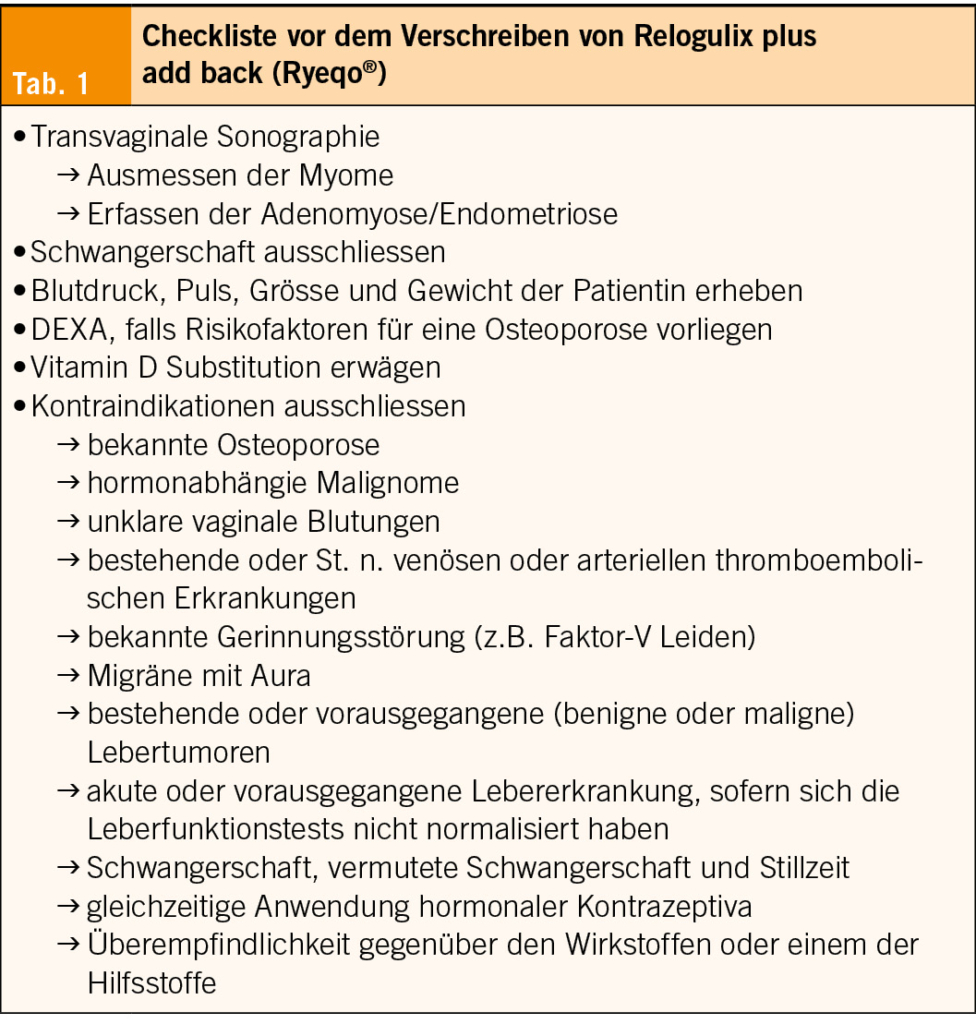
Vor dem Therapiestart sollten Kontraindikationen wie zum Beispiel thromboembolische Erkrankungen und Risiken ausgeschlossen, im transvaginalen Ultraschall Myome oder die Endometriose/Adenomyose erfasst und der Blutdruck der Patientin gemessen werden. (Siehe Checkliste vor dem Verschreiben von Relugolix plus add back in Tab. 1).
Eine Kontrolle der Verträglichkeit mit Blutdruckmessung wird drei Monate nach Beginn mit Relugolix plus add back empfohlen.
Knochendichte
Dank der add-back-Therapie mit Östradiol ist das Risiko einer Abnahme der Knochendichte im Vergleich zur alleinigen Anwendung eines GnRH-Antagonisten deutlich reduziert. In der SPIRIT 1 und 2 Studie konnte gezeigt werden, dass nach einer anfänglichen, klinisch meist nicht relevanten, Abnahme der Knochendichte nach ca. 24 Wochen (Durchschnittliche Abnahme um 0.69 %) ein Plateau erreicht wurde. Danach blieb die Knochendichte bis zu 2 Jahre stabil (12, 17). Über den Verlauf der Knochendichte über mehr als 2 Jahre liegen keine Daten vor.
Eine Dual Energy X-Ray Absorptiomerie (DEXA) wird nach einem Anwendungsjahr empfohlen und danach im zweijährigen Intervall, sofern die Knochendichte unauffällig war (15).
Über die Anwendung von Relugolix plus add back vor dem Erreichen der endgültigen Skelettreife (Peak-Bone-Mass) mit ca. 25 Jahren ist die Datenlage begrenzt und erfordert daher bei diesen Patientinnen eine strenge Risiko-Nutzen-Analyse. Bei Patientinnen unter 18 Jahren sollte Ryeqo® nicht angewendet werden.
Schwangerschaft und Fertilität
Zur möglichen Auswirkung auf die Fertilität liegen keine Daten vor. Eine regelmässige Ovulation und Menstruation treten nach Absetzen von Relugolix plus add back rasch wieder auf, sofern vor der Einnahme keine ovulatorische Störung bestand (10).
Diskussion
Relugolix plus add back reduziert die Hypermenorrhoe bei Frauen mit Uterus myomatosus, und das Volumen der Myome (um bis zu 50 %) sowie Adenomyose- und Endometriose-assoziierte Schmerzen. Dank dem integrierten Östradiol können vasomotorische Symptome grossteils verhindert werden und der Effekt auf die Knochendichte ist minimal und meist klinisch nicht relevant (8, 9, 12).
Was bedeutet nun eine Reduktion des Myomvolumens um 50 % für den Durchmesser im Ultraschall? Bei einem Myomdurchmesser von 50 mm bedeutet eine 50 % Reduktion des Volumens, dass sich der Durchmesser hier auf 40 mm verkleinert, was klinisch zwar relevant ist.
Nach dem Absetzen von Relugolix plus add back erlebten die meisten Frauen ein Wiederauftreten von starkem Menstruationsblutverlust, typischerweise innerhalb von etwa 6 Wochen (10).
Es gibt keine Daten zur Langzeitanwendung von Relugolix plus add back. Die Liberty- und die Spirit-Studien zeigen uns Daten über die Anwendung des Medikamentes über zwei Jahre. Aus diesem Grund ist Relugolix plus add back (zum aktuellen Zeitpunkt) eher für die kurzzeitige Anwendung in Betracht zu ziehen und nicht als Langzeittherapie (17). Somit eignet sich Relugolix plus add back gut präoperativ zum Anheben des Hämoglobins vor hysteroskopischer oder laparoskopischer Myomenukletaion, zum konservativen Management bei perimenopausalen Patientinnen mit Wunsch nach Uteruserhalt ohne chirurgischen Eingriff bis zum Erreichen der Menopause oder als Second-line-Alternative zu Dienogest für Patientinnen mit Endometriose/Adenomyse.
Ebenso sind die Langzeitdaten zur Fertilität und Schwangerschaft nach Beendigung der Therapie bislang limitiert, jedoch sprechen bisherige Studien für eine reversible Wirkung und rasche Wiederherstellung der ovulatorischen Funktion (10), wenn vor der Therapie keine ovulatorische Störung vorlag. Interessant wären auch Untersuchungen zu Relugolix plus add back im «adjuvanten» Bereich nach Myomenukleation vor Kinderwunschtherapie.
Mit Relugolix plus add back haben wir eine Alternative für die kurzzeitige Anwendung für Patientinnen mit Myom-assoziierter Hypermenorrhoe und Endometriose-assoziierten Schmerzen, welche unzureichend auf eine Dienogesttherapie angesprochen haben, oder bei Patientinnen, welche Dienogest nicht vertragen. Die Frage nach der Langzeittherapie bleibt zum aktuellen Zeitpunkt offen.
Copyright
Aerzteverlag medinfo AG
Oberärztin Frauenklinik
Kantonsspital Winterthur
Brauerstrasse 15
8401 Winterthur
Leitende Ärztin Frauenklinik
Kantonsspital Winterthur
Brauerstrasse 15
8401 Winterthur
Die Autorinnen haben keine Interessenskonflikte in Zusammenhang mit diesem Artikel deklariert.
- Relugolix plus add back reduziert die Hypermenorrhö bei Frauen mit Uterus myomatosus, das Volumen der Myome (um bis zu 50%) und adenomyose- und endometriose-assoziierte Schmerzen
- In der Schweiz ist Relugolix plus add back bei Frauen mit myom-assoziierter Hypermenorrhö und bei Endmetriose/Adenomyoseassoziierten Schmerzen (als second line) zugelassen.
- Dank dem integrierten Östradiol sind vasomotorische Symptome selten und der Effekt auf die Knochendichte ist minimal und meist klinisch nicht relevant.
- Die Frage zur Langzeittherapie bleibt offen und Reugolix mit add back wird daher aktuell eher kurzzeitig angewandt.
1. Flake GP, Andersen J, Dixon D. Etiology and pathogenesis of uterine leiomyomas: a review. Environ Health Perspect. 2003;111(8):1037–1054.
2. Chantalat E, Valera MC, Vaysse C, et al. Estrogen receptors and endometriosis. Int J Mol Sci. 2020;21(8):2815
3. Zondervan KT, Becker CM, Missmer SA. Endometriosis. N Engl J Med. 2020;382(13):1244–1256.
4. Buttram VC, Reiter RC(1981)Uterine leiomyomata: etiology, symptomatology and management.Fertil Steril36:433–445
5. Osuga Y, Enya K, Kudou K, Tanimoto M, Hoshiai H (2019) Oral gonadotropin-releasing hormone antagonist relugolix compared with leuprorelin injections for uterine leiomyomas: a randomized controlled trial. Obstet Gynecol 133(3):423–433.
6. Juan C. Arjona Ferreira, M.D. and Elizabeth Migoya, Pharm.D. Development of relugolix combination therapy as a medical treatment option for women with uterine fibroids or endometriosis, June 2023, Fertil Steril Rep doi:10.1093/humrep/deaa305
7. Friedman, A. J., Lobel, S. M., Rein, M., & Barbieri, R. L. (1990). Efficacy and safety considerations in women with uterine leiomyomas treated with gonadotropin-releasing hormone agonists: The estrogen threshold hypothesis. American Journal of Obstetrics and Gynecology, 163(3), 1114–1119.
8. Al-Hendy, A., Venturella, R., Arjona, J. C., et al. (2021). Efficacy and safety of relugolix combination therapy for heavy menstrual bleeding associated with uterine fibroids: Results from the LIBERTY study. The Lancet, 398(10304), 2211-2221
9. Al-Hendy, A., Lukes, A. S., Poindexter, A. N., Venturella, R., Villarroel, C., McKain, L., Li, Y., Wagman, R. B., & Stewart, E. A. (2022). Long-term relugolix combination therapy for symptomatic uterine leiomyomas: Results through 52 weeks in the LIBERTY LTE study. Obstetrics & Gynecology, 140(6), 920–930.
10. Al-Hendy, A., Lukes, A. S., Bradley, L., Simon, J. A., Venturella, R., Donnez, J., … Schlaff, W. D. (2023). LIBERTY randomized withdrawal study: Relugolix combination therapy for heavy menstrual bleeding associated with uterine fibroids. American Journal of Obstetrics and Gynecology, 229(6), 662.e1–662.e25.
11. Catherino, W. H., Al-Hendy, A., Zaim, S., Bouzegaou, N., Venturella, R., Stewart, E. A., Wu, R., Vannuccini, S., Perry, J. S., Rakov, V. G., & Munro, M. G. (2025). Efficacy and safety of relugolix combination therapy in women with uterine fibroids and adenomyosis: Subgroup analysis of LIBERTY 1 and LIBERTY 2. American Journal of Obstetrics and Gynecology, 232(4), 449.e1–449.e12.
12. Giudice, L. C., As-Sanie, S., Ferreira, J. C., Brown, E., Dynowski, K., Wilk, K., Li, Y., Mathur, V., Warsi, Q. A., Wagman, R. B., & Johnson, N. P. (2022). Once daily oral relugolix combination therapy versus placebo in patients with endometriosis-associated pain: two replicate phase 3, randomised, double-blind studies (SPIRIT 1 and 2). The Lancet, 399(10343), 2267-2279
13. Becker, C. M., et al. (2024). Two-year efficacy and safety of relugolix combination therapy in women with endometriosis-associated pain: SPIRIT open-label extension study. Human Reproduction, 39(3), 526-537.
14. Swissmedic: https://www.swissmedic.ch/swissmedic/de/home/ueber-uns/publikationen/public-summary-swiss-par/public-summary-swiss-par-ryeqo.html (stand 17.09.2025
15. Schweizerisches Arzeimittelcompendium: https://compendium.ch/product/1541674-ryeqo-filmtabl-40-mg-1-mg-0-5-mg/mpro
16. Taylor HS, Giudice LC, Lessey BA, et al. Treatment of endometriosis-associated pain with relugolix combination therapy: a randomized controlled trial. Obstet Gynecol. 2021;138(5):553-563.
17. Donnez J, Taylor HS, Taylor RN, et al. Effects of relugolix combination therapy on bone mineral density and vasomotor symptoms: a phase 3 trial analysis. Fertil Steril. 2021;116(6):1503-1511
info@gynäkologie
- Vol. 15
- Ausgabe 5
- Oktober 2025