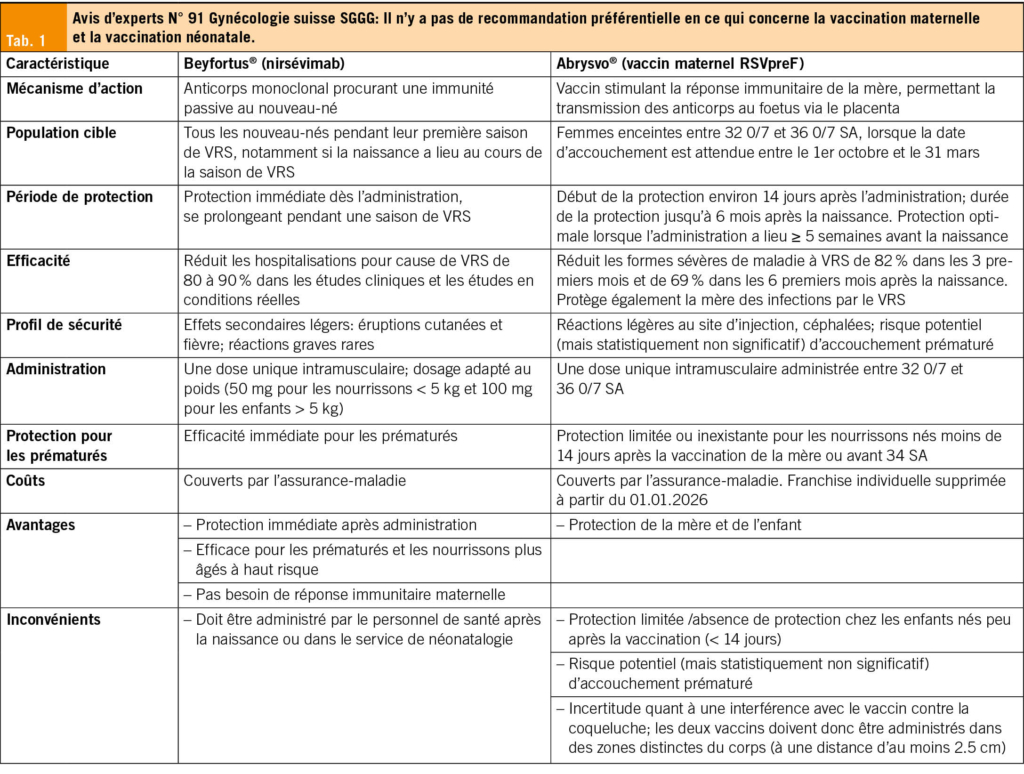
- Prévention du virus respiratoire syncytial (RSV) chez le nouveau-né
Le virus respiratoire syncytial (RSV) représente la principale cause d’infection respiratoire basse sévère et d’hospitalisation chez le nourrisson durant les premiers mois de vie. Depuis 2023, deux stratégies préventives efficaces sont disponibles en Suisse: la vaccination maternelle par vaccin bivalent RSVpreF administrée au troisième trimestre de grossesse et l’immunisation néonatale par anticorps monoclonal à longue durée d’action (nirsevimab). La recommandation suisse actualisée (Recommandation de pratique clinique n°91, AFMM/SGGG 2025) précise qu’il n’existe pas de préférence entre ces deux approches, toutes deux étant couvertes maintenant par l’assurance maladie de base. Toutefois, la mise en œuvre soulève des questions pratiques et scientifiques, notamment concernant le signal de prématurité observé dans certains essais de vaccination maternelle. Cet article propose une synthèse des données actuelles et des implications pour la pratique gynécologique en Suisse.
Respiratory syncytial virus (RSV) is the leading cause of severe lower respiratory tract infection and hospitalisation in infants during the first months of life. Since 2023, two effective preventive strategies have been available in Switzerland: maternal vaccination with the bivalent RSVpreF vaccine administered in the third trimester of pregnancy and neonatal immunisation with long-acting monoclonal antibodies (nirsevimab). The updated Swiss recommendation (Clinical Practice Guideline No. 91, AFMM/SGGG 2025) specifies that there is no preference between these two approaches, both of which are now covered by basic health insurance. However, implementation raises practical and scientific questions, particularly regarding the signal of prematurity observed in some maternal vaccination trials. This article provides a summary of the current data and implications for gynaecological practice in Switzerland.
Keywords: Respiratory syncytial virus (RSV), pregnancy, infants, vaccination, prevention
Une question nouvelle pour les gynécologues
«Anticorps ou vaccin?» La question, qui aurait semblé purement pédiatrique il y a encore trois ans, concerne désormais directement les gynécologues suisses. Le virus respiratoire syncytial (VRS) est la première cause d’infection respiratoire basse sévère et d’hospitalisation chez le nourrisson. Depuis 2023–2025, deux stratégies préventives efficaces sont disponibles: l’immunisation passive du nourrisson par anticorps monoclonal à longue durée d’action (nirsevimab) et la vaccination maternelle par vaccin bivalent RSVpreF (Abrysvo®).
En Suisse, ces deux stratégies sont désormais recommandées et intégrées dans les cadres réglementaires et de remboursement. L’enjeu n’est plus scientifique mais organisationnel et stratégique: comment protéger au mieux les nouveau-nés suisses dès leur première saison VRS?
Impact du VRS chez les nouveau-nés: données Suisses
L’impact du VRS en Suisse est loin d’être marginal. On estime à environ 6000 hospitalisations hivernales par an le nombre d’enfants hospitalisés pour VRS en Suisse, toutes classes d’âge pédiatriques confondues. Chez les enfants de moins d’un an, le pic d’incidence se concentre durant les trois premiers mois de vie.
Les données issues de la cohorte suisse (Stucki 2024, 348002 naissances) montrent que la proportion d’hospitalisations VRS est fortement dépendante du mois de naissance, avec un risque maximal chez les nourrissons nés juste avant ou au début de la saison hivernale. En période épidémique, environ 500 cas de VRS par semaine sont rapportés chez les enfants de moins de deux ans en Suisse. Même si la mortalité reste faible en valeur absolue dans un pays à haut niveau de soins, elle n’est pas négligeable.
Il est important de rappeler que la majorité des nourrissons hospitalisés sont nés à terme et ne présentent pas de comorbidité majeure. Les prématurés et enfants porteurs de pathologies cardiorespiratoires sont à risque accru, mais ils ne représentent qu’une minorité des hospitalisations totales.
Impact sociétal: Au-delà de l’hospitalisation
Le VRS ne se limite pas à un problème hospitalier. L’impact social est considérable. Aux États-Unis, on estime à environ 700 000 le nombre de jours de travail perdus chaque hiver par les parents en raison d’une infection VRS chez leur enfant. Si l’on extrapole proportionnellement à la population suisse, cela représenterait plusieurs dizaines de milliers de journées de travail perdues chaque saison.
Chaque hospitalisation implique en moyenne plusieurs jours d’absence parentale, une désorganisation familiale importante, et parfois une hospitalisation en soins intensifs. En France, les données hospitalières montrent que 27 % des nourrissons hospitalisés pour VRS nécessitent un passage en soins intensifs. Le coût moyen par hospitalisation dépasse 3000 euros, et le coût annuel national excède 130 millions d’euros. Transposé au système suisse, le poids économique direct et indirect est important.
La surcharge hospitalière hivernale est également documentée. Durant les pics épidémiques, les unités de pédiatrie et de soins intensifs pédiatriques fonctionnent à capacité maximale, avec un effet domino sur l’ensemble du système hospitalier.
eux stratégies de prévention: un changement de paradigme
Les stratégies actuelles reposent sur deux approches immunologiques distinctes.
L’immunisation passive consiste à administrer directement au nouveau-né un anticorps monoclonal ciblant la protéine F du VRS. La protection est immédiate et ne dépend pas de la réponse immunitaire du nourrisson. L’avantage principal réside dans la rapidité d’action et l’indépendance vis-à-vis du statut immunitaire maternel.
La vaccination maternelle repose sur un mécanisme différent. L’administration du vaccin RSVpreF entre 32 et 36 semaines d’aménorrhée induit une production d’anticorps neutralisants chez la mère, transférés activement au fœtus par voie transplacentaire. L’avantage réside dans l’absence d’injection à l’enfant à la naissance et dans la protection concomitante de la mère.
Nirsevimab (Beyfortus®): Données cliniques
Les essais cliniques randomisés ont inclus plus de 10 000 nourrissons, montrant une réduction des hospitalisations de plus de 80 %. Les données de vie réelle confirment une réduction d’environ 80 % des hospitalisations liées au VRS, avec une efficacité contre les admissions en soins intensifs également significative.
En Suisse, la recommandation prévoit une administration intramusculaire unique, idéalement en maternité pour les nouveau-nés nés entre octobre et mars.
Les nourrissons nés hors saison reçoivent une dose en début de saison suivante. Les enfants atteints de maladies chroniques peuvent bénéficier d’une dose supplémentaire lors de leur deuxième saison.
Vaccination maternelle (Abrysvo®)
Les essais cliniques de phase 3 (MATISSE) ont inclus plus de 7300 femmes enceintes. L’efficacité contre les hospitalisations sévères liées au VRS chez les nourrissons est d’environ 70–80 % durant les six premiers mois de vie. Les données en vie réelle en Argentine confirment une efficacité de 78.6 % contre les hospitalisations jusqu’à trois mois et de 71.3 % jusqu’à six mois. Le vaccin RSVpreF est disponible depuis 2024 en Suisse et pleinement remboursé depuis janvier 2026.
La question de la prématurité: Analyse critique
Un point central du débat concerne le risque d’accouchement prématuré. Dans les données présentées, la prématurité était observée chez 5.7 % des femmes vaccinées versus 4.2 % dans le groupe placebo, différence non statistiquement significative. L’analyse détaillée de l’étude MATISSE publiée dans Obstetrics & Gynecology 2025 confirme l’absence d’augmentation significative des naissances prématurées lorsque le vaccin est administré entre 32 et 36 SA. Les méta-analyses récentes et une synthèse NEJM 2025 concluent également à l’absence d’association significative dans la fenêtre recommandée. Plusieurs registres nationaux de suivi de patientes vaccinées n’ont pas retrouvé d’augmentation des naissances prématurées.
Il est fondamental de rappeler que la restriction à 32–36 SA vise précisément à minimiser tout risque théorique, tout en optimisant le transfert d’anticorps.
Hospitalisations évitées: Projections
Les modélisations britanniques suggèrent une réduction potentielle de plus 15 000 hospitalisations par saison en cas de couverture élevée. Rapporté à la Suisse, une réduction proportionnelle pourrait éviter plusieurs milliers d’hospitalisations annuelles, dont une part significative en soins intensifs.
Conclusion: Quel choix pour la Suisse?
Le VRS représente chaque hiver un fardeau significatif pour les nouveau-nés suisses, les familles et le système hospitalier. Les deux stratégies disponibles offrent une réduction de 70 à 80 % des hospitalisations, sans signal de sécurité démontré à ce jour.
L’immunisation passive offre une protection immédiate indépendante du statut maternel. La vaccination maternelle offre une protection transplacentaire et s’intègre naturellement dans le suivi du troisième trimestre.
Pour les gynécologues suisses, la vaccination maternelle contre le VRS s’inscrit désormais dans la continuité des stratégies de prévention périnatale. Cependant, les deux options doivent être discutées par le gynécologue. La décision entre anticorps et vaccin n’est pas exclusive, mais stratégique et organisationnelle. L’objectif reste unique: qu’aucun nourrisson suisse n’entre dans sa première saison VRS sans protection.
Copyright
Aerzteverlag medinfo AG
CHUV, Department Woman-Mother-Child
Materno-Fetal Medicine (MFM) specialist
Bureau Maternité CI/04-209
Avenue Pierre-Decker 2
CH-1011 Lausanne
L’auteur n’a déclaré aucun conflit d’intérêts en rapport avec cet article.