- Schwangerschaftsverlust im 1. Trimenon
Als früher Schwangerschaftsverlust wird eine nicht lebensfähige Schwangerschaft mit einem leeren Fruchtsack oder einem Fruchtsack mit Embryo ohne Herzaktion in den ersten 12 Schwangerschaftswochen mit Lokalisation innerhalb oder ausserhalb des Uterus definiert. Dazu gehört auch die Extrauteringravidität. Die Inzidenz eines Abortes liegt bei 10–15% aller klinisch erkannten Schwangerschaften (1–4). Mit unserem Artikel wollen wir die wichtigsten Aspekte der aktuellen diagnostischen und therapeutischen Vorgehensweise sowie die psychischen Folgen gemäss der neuen S2k-Leitlinie zum Schwangerschaftsverlust im 1. Trimenon beleuchten (1–4).
Early pregnancy loss is defined as a non-viable pregnancy with an empty gestational sac or a gestational sac containing an embryo without cardiac activity in the first 12 weeks of pregnancy, located inside or outside the uterus. This also includes ectopic pregnancy. The incidence is 10–15% of all clinically diagnosed pregnancies (1–4). With our article, we aim to highlight the most important aspects of current diagnostic and therapeutic procedures, as well as the psychological consequences, according to the new S2k guideline on pregnancy loss in the first trimester (1–4).
Keywords: Früher Schwangerschaftsverlust, Abort, gestörte Frühgravidität, EUG
Einleitung
Ein Schwangerschaftsverlust ist häufig. Ungefähr 80% aller Aborte treten im ersten Trimenon auf. Der Abort tritt zumeist unerwartet auf und kann psychisch sehr belastend sein (1–4).
Abortformen und Epidemiologie
Es werden verschiedene Abortformen unterschieden (Frühstabort, Abortus imminens, Abortus incipiens, Abortus incompletus, septischer Abort, missed abortion), wobei auch die ektope Schwangerschaft zu den gestörten Frühschwangerschaften zählt. Risikofaktoren für Aborte sind mütterliches Alter sowie die Anzahl vorausgegangener Fehlgeburten (5). Zu den häufigsten Ursachen gehören Chromosomenanomalien, Uterusanomalien, ein tiefer Progesteronspiegel, mütterliche Erkrankungen sowie Infektionen oder Umwelt- und Lebensstilfaktoren (6, 7). Sexuell übertragbare Erkrankungen, die Anwendung assistierter Reproduktionstechnologien und das Rauchen werden mit einem erhöhten Risiko für eine Eileiterschwangerschaft gesehen (8, 9).
Diagnostik
Bei V.a. einer gestörten Frühschwangerschaft (Unterbauchschmerzen, vaginalen Blutungen) gilt es die Allgemein-Anamnese mit speziellem Augenmerk auf Zyklusunregelmässigkeiten, STD und Voroperationen zu erheben. Neben der gynäkologischen Spekulumuntersuchung kommt der Transvaginalsonographie eine überragende Bedeutung bei der Diagnostik und Therapiekontrolle zu. Eine intrauterine Schwangerschaft sollte ab einem b-HCG Wert von 1500 IU/l darstellbar sein. Eine Blutgruppenbestimmung, ein Hämatogramm und das Infektlabor sind bei starken Blutungen oder Infektzeichen indiziert. Bei unklarer Schwangerschaftslokalisation (Pregnancy of unknown location – PUL) ist eine serielle, quantitative ß-hCG-Kontrolle hilfreich. Ein Anstieg der ß-hCG-Konzentration um mindestens 53 % nach zwei Tagen wurde bei 99 % der Frauen festgestellt, die im Verlauf eine lebensfähige, intrauterine Schwangerschaft hatten (10). 21 % der ektopen Schwangerschaften wiesen ebenfalls einen adäquaten ß-hCG-Anstieg auf (11).
Zur Vorhersage des Schwangerschaftsverlaufs wurden verschiedene Modelle entwickelt, basierend auf der hCG-Ratio (M1), den mittleren (0/48h) Serum–Progesteronwerten (logProg) (M2) bzw. hCG-Ratio, logProg und Alter zusammen (M3). Den besten Vorhersagewert birgt das M6-Modell, entwickelt durch das Imperial College London und KU Leuven, das anhand von Progesteron- und b-hCG-Werten in ein bis zwei Schritten die Schwangerschaft in risikoarm und risikoreich einteilt (12, 13). Details zum Modell findet man unter: https://tinyurl.com/mw2awm43
Ebenfalls hilfreich sind die Entscheidungskriterien gemäss der ACOG (2, 14). Eine Scheitel-Steiss-Länge von ≥ 7 mm ohne Herzaktion oder ein Gestationssack von ≥ 25 mm ohne Embryo sind ebenfalls beweisend für eine gestörte Frühschwangerschaft (z.B. Windmole).
Therapieoptionen und Beratung
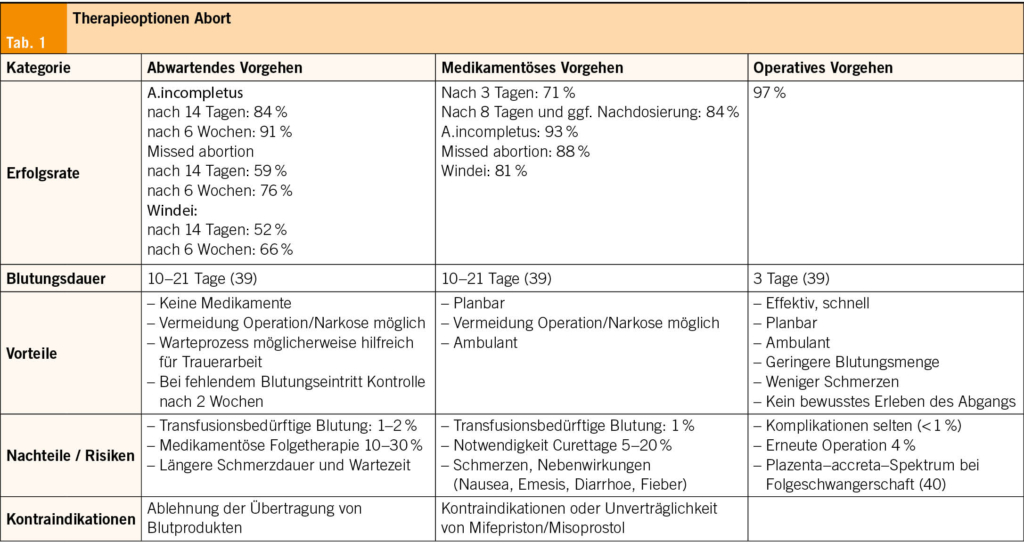
Nach der Diagnosestellung einer gestörten Frühgravidität werden die Therapieoptionen (abwartendes, medikamentöses und operatives Vorgehen), deren Vor- und Nachteile sowie die Risiken und Komplikationen im Sinne eines Shared decision making mit der Patientin besprochen (Tab. 1).
Abwartendes versus medikamentöses Vorgehen zeigen in randomisierten Studien vergleichbare Erfolge bis zu 80 % (15, 16). Das operative Vorgehen führt am schnellsten zur Uterusentleerung, bei 11 % der konservativ behandelten Frauen kann dies bis zu 6 Wochen dauern (1, 2).
Beim medikamentösen Vorgehen steigert die Kombination aus Mifepriston (200 mg) und Misoprostol (800 µg vaginal) die Erfolgsrate auf 83,8 % gegenüber 67,1 % mit Misoprostol allein. Zudem wird eine niedrigere Rate operativer Eingriffe benötigt (17). Dabei ist die vaginale Applikation wegen geringerer Nebenwirkungen zu bevorzugen (18). Eine sonographische Kontrolle nach 7–14 Tagen wird empfohlen. Liegt das Endometrium > 30 mm, kann Misoprostol erneut verabreicht werden; die Erfolgsrate liegt dann bei über 98 % (19).
Eine primär operative Therapie wird empfohlen bei Wunsch der Patientin, kreislaufrelevanter oder anämisierender Blutung, Gerinnungsstörungen, Kontraindikation gegenüber Mifepriston/Misoprostol, septischem Abort, Trophoblasterkrankung oder heterotoper Schwangerschaft. Nur 4 % benötigen einen Wiederholungseingriff (20). Die Saugcurettage ist dabei schonender als die Kürettage und reduziert das Perforationsrisiko (21, 22). Ein vorgängiges Zervixpriming mit Misoprostol reduziert Zervixverletzungen (23). Eine Antibiotikagabe ist nur bei septischem Abort indiziert und ist möglichst 12–24 Stunden präoperativ zu starten (24).
Komplikationen (uterine Perforation, intrauterine Adhäsionen, Verletzungen des Gebärmutterhalses, Infektionen, Asherman-Fritsch-Syndrom) oder anästhesiologische Risiken sind sehr selten (25, 26). Nachteile des exspektativen Vorgehens sind ein erhöhtes Blutungsrisiko (27, 28). Das Risiko für eine Infektion ist für alle Vorgehen vergleichbar, zwischen 1–3 % (27). Die Abort- und Frühgeburtsrate zukünftiger Schwangerschaften scheint unabhängig vom Therapieverfahren erhöht zu sein (29).
Für eine Ursachenklärung wird die histopathologische Untersuchung des Abortmaterials empfohlen. Dies kann für die Beratung bei offenem Kinderwunsch und zur psychologischen Aufarbeitung des Verlustes hilfreich sein.
Anti-D-Prophylaxe
Das Risiko einer Rhesus-Sensibilisierung vor der 10. Schwangerschaftswoche ist höchstwahrscheinlich äusserst gering, die Folgen für die Folgeschwangerschaft können jedoch erheblich sein (30). Gemäss den NICE-Richtlinien soll eine Anti-D-Prophylaxe nur im Falle eines Aborts nach der 9+0. Schwangerschaftswoche verabreicht werden (31). Unabhängig vom Schwangerschaftsalter sollen im Falle eines abwartenden Vorgehens, einer Abortcurettage oder einer ektopen Schwangerschaft eine Anti-D-Prophylaxe erfolgen.
Verhaltensempfehlungen für die Patientin
Patientinnen sollen über den variablen Verlauf von Blutungen und Schmerzen sowie über die Möglichkeit einer analgetischen und antiemetischen Therapie aufgeklärt werden. Eine Wiedervorstellung bei übelriechendem Ausfluss, Unterbauchschmerzen, Fieber > 38°C oder allgemeinem Krankheitsgefühl ist indiziert.
Hygieneartikel wie Binden, Menstruationstassen, Tampons u.a. können verwendet werden. Entgegen früheren Empfehlungen muss aufgrund fehlender Evidenz auf Geschlechtsverkehr, körperliche Anstrengung oder Sport nicht verzichtet werden.
Die Ovulation tritt in Einzelfällen schon 8 bis 10 Tage und bei 90 % der Frauen innerhalb eines Monats nach dem Abortgeschehen ein (32). Patientinnen ohne Kinderwunsch können nach dem bestätigten Abgang der Frühschwangerschaft mit der medikamentösen Antikonzeption beginnen. Entgegen früheren Empfehlungen kann die Patientin eine weitere Schwangerschaft unmittelbar anstreben (33, 34).
Psychische Aspekte
Ein früher Schwangerschaftsverlust kann für viele Patientinnen und deren Partner eine Belastung darstellen. Es besteht ein Zusammenhang zwischen Fehlgeburten und psychischen Symptomen wie Trauer, depressiven Symptomen, Angst und posttraumatischen Belastungsreaktionen (35, 36). Mit zunehmendem zeitlichem Abstand nehmen die Symptome in der Regel ab (35). Zusätzliche Risikofaktoren für schwere psychische Belastung sind rezidivierende Aborte, junges Alter, psychiatrische Vorerkrankungen, Beziehungsprobleme, belastende soziale Umstände oder niedriger sozioökonomischer Status (36–38).
Die Mitteilung der Diagnose kann als traumatisch erlebt werden. Das medizinische Personal sollte eine empathische, sensible und situationsangepasste Kommunikation wählen und die Partnerperson miteinbeziehen.
Auf die psychische Befindlichkeit sollte in jeder Kontrolle eingegangen werden und entsprechend auf die Möglichkeit einer psychologischen Unterstützung hingewiesen werden.
Copyright
Aerzteverlag medinfo AG
Oberärztin
Luzerner Kantonsspital Frauenklinik
Kantonsspital 37
6004 Luzern
Oberärztin mbF
Zuger Kantonsspital
Landhausstrasse 1
6340 Baar
Die Autorinnen haben keine Interessenskonflikte in Zusammenhang mit diesem Artikel deklariert.
- Frühe Schwangerschaftsverluste sind häufig. Die Inzidenz liegt bei 10–15%
- Das M6-Modell zeigt die beste Vorhersage des Schwangerschaftsverlaufs bei PUL, Windei, Blasenmole, Termindiskrepanz und EUG.
- Therapeutisch stehen konservative, medikamentöse und chirurgische Verfahren zur Verfügung.
- Eine Rhesusprophylaxe wird ab der 10. Schwangerschaftswoche sowie im Falle eines abwartenden Vorgehens, einer Abortcurettage oder einer ektopen Schwangerschaft empfohlen.
- Eine Folgeschwangerschaft kann nach einem Abort sogleich geplant werden und erhöht das Risiko von perinatalen Komplikationen nicht.
1. Early pregnancy loss in the 1st trimester. Guideline oft he DGGG, OEGGG and SGGG (S2k-Level, AWFM Registry No.015/075, August 2024).
2. American College of Obstetricians and Gynecologists. ACOG Practice Bulletin No. 200: Early Pregnancy Loss. Obstet Gynecol 2018; 132(5):e197-e207.
3. Musik T, Grimm J, Juhasz-Böss I, Bäz E. Treatment Options After a Diagnosis of Early Miscarriage : Expectant, Medical, and Surgical. Dtsch Arztebl Int 2021 ; 118(46) :789-94.
4. Quenby S, et al. Miscarriage matters : the epidemiological, physical, psychological, and economic costs of early pregnancy loss. Lancet 2021 ; 397(10285) :1658-67.
5. Magnus MC, et al. Role of maternal age and pregnancy history in risk of miscarriage : pospective register based study. BMJ 2019 ; 364 :1869.
6. Zhao Y, et al. Progestogens in women with threatened miscarriage: an updated meta-analysis of randomised trials. Arch Gynecol Obstet 2021; 303(1):27-36.
7. Alijotas-Reig J, et al. Current concepts and new trends in the diagnosis and management of recurrent miscarriage. Obstet Gynecol Surv 2013 ; 68(6) :445-66.
8. Condous G. Ectopic prenancy – risk factors and diagnosis. Aust Fam Physician 2006 ; 35(11) :854-7.
9. Marion LL, et al. Ectopic pregnancy: History, incidence, epidemiology, and risk factors. Clin Obstet Gynecol 55(2): 376-386.
10. Barnhart KT, et al. Symptomatic patients with an early viable intrauterine pregnancy : HCG curves redefined. Obstet Gynecol 2004 ; 104(1) :50-5.
11. Barnhart KT, et al. Clinical practice. Ectopic pregnancy. N Engl J Med 2009 ;361(4) :379-87.
12. Van Calster B, et al. Managing pregnancy of unknown location based on initial serum progesterone and serial serum hCG levels : development and validation of a two-step triage protocol. Ultrasound Obstet Gynecol 2016 ; 48(5) :642-9.
13. Bobdiwala S, et al. Triaging women with pregnancy of unknown location using two-step protocol including M6 model : clinical implementation study. Ultrasound Obstet Gynecol 2020 ; 55(1) :105-14.
14. Doubilet PM, et al. Diagnosis criteria for nonviable pregnancy early in the first trimester. Society of Radiologists in Ultrasound Multispecialty Panel of Early First Trimester Diagnosis of Miscarriage and Exclusion of Viable Intrauterine Pregnancy. N Engl J Med 2013;369:1443-51.
15. Nielson S, et al. Randomised trial comparing expectant with medical management for first trimester miscarriage. Br J Obstet Gynaecol 1999 ; 106(8) :804-7.
16. Shelley JM, et al. A randomised trial of surgical, medical and expectant management of first trimester spontaneous miscarriage. Aust N Z J Obstet Gynecol 2005; 45(2) :122-7.
17. Schreiber CA, et al. Mifepristone Pretreatment for the Medical Management of Early Pregnancy Loss. N Engl J Med 2018; 378(23):2161-70.
18. Pang MW, et al. Incomplete miscarriage: a randomized controlled trial comparing oral with vaginal misoprostol for medical evacuation. Hum Reprod 2001; 16(11):2283-7.
19. Zhang J, et al. Medical methods for first trimester abortion. Cochrane database Syst Rev 2022 ; 5(5) :CD002855.
20. Nanda K, et al. Expectant care versus surgical treatment for miscarriage. Cochrane Database Syst Rev 2012 ; 2012(3) :CD003518.
21. Tuncalp O, et al. Surgical procedures for evacuating incomplete miscarriage. Cochrane Database Syst Rev 2010; 2010(9):CD001993.
22. Yonke N, et al. First-trimster surgical abortion technique. Obstet Gynecol Clin North Am 2013; 40(4):647-70.
23. Kapp N, et al. Cervical preparation for first trimester surgical abortion. Cochrane Database Syst Rev 2010 ; (2) :CD007207.
24. Sajadi-Ernazarova KR, et al. Statpearls: Abortion Complications. Treasure Island (FL), 2024.
25. Kim C, et al. Medical treatments for incomplete miscarriage. Cochrane Database Syst Rev 2017; 1(1):CD007223.
26. Gilman Barber AR, et al. Curettage and Asherman’s syndrome-lessons to (re-) learn? J Obstet Gyaecol Can 2014; 36(11):997-1001.
27. Luise C, et al. Outcome of expectant management of spontaneous first trimester miscarriage : observational study. BMJ 2002 ; 324(7342) :873-5.
28. Erez O, et al. Disseminated intravascular coagulation in pregnancy: insights in pathophysiology, diagnosis and management. Am J Obstet Gynecol 2015 ; 213(4) :452-63.
29. Brittain JJ, et al. Spontaneous or induced abortion is a risk factor for cervical dysfunction in pregnant women : a Systematic Review and Meta-analysis. Reprod Sci 2023 ; 30(7) :2025-39.
30. Chan MC, et al. Rhesus isoimmunisation in unsensitised RhD –negative individuals seeking abortion at less than 12 weeks‘ gestation: a systematic review. BMJ Sex Reprod Health 2022; 48(3):163–8. doi: 10.1136/bmjsrh-2021-201225.
31. Visser GHA, et al. FIGO/ICM guidelines for preventing Rhesus disease: A call to action. Int J Gynaecol Obstet 2021; 152(2):144–7. doi: 10.1002/ ijgo.13459
32. Kaunitz AM, et al. Abortions that fail. Obstet Gynecol 1985; 66(4):533–7.
33. Tessema GA, et al. Interpregnancy interval and adverse pregnancy outcomes among pregnancies following miscarriages or induced abortions in Norway (2008 -2016): A cohort study. PLoS Med 2022; 19(11):e1004129. doi: 10.1371/journal.pmed.1004129.
34. Schliep KC, et al. Trying to Conceive After an Early Pregnancy Loss: An Assessment on How Long Couples Should Wait. Obstet Gynecol 2016; 127(2):204–12. doi:10.1097/AOG.0000000000001159.
35. Quenby S, et al. Miscarriage matters: the epidemiological, physical, psychological, and economic costs of early pregnancy loss. Lancet 2021; 397(10285):1658–67. doi:10.1016/S0140-6736(21)00682-6.
36. Farren J, et al. The psychological impact of early pregnancy loss. Hum Reprod Update 2018; 24(6):731–49. doi: 10.1093/humupd/dmy025
37. Nynas J, et al. Depression and Anxiety Following Early Pregnancy Loss: Recommendations for Primary Care Providers. Prim Care Companion CNS Disord 2015; 17(1). doi: 10.4088/PCC.14r01721
38. Farren J, et al. Posttraumatic stress, anxiety and depression following miscarriage or ectopic pregnancy: a prospective cohort study. BMJ Open 2016; 6(11 ):e011864. doi:10.1136/bmjopen-2016-011864.
39. Victoria Timlin, et al. Miscarriage- Management of Miscarriage and Threatened Miscarriage: Trust ref: C30/2013; (4).
40. Gan C, Zou Y, et al. The influence of medical abortion compared with surgical abortion on subsequent pregnancy outcome. Int J Gynaecol Obstet 2008; 101(3):231–8.
info@gynäkologie
- Vol. 16
- Ausgabe 1
- Februar 2026