- Hochsensitives kardiales Troponin
Kardiales Troponin ist ein strukturelles Protein des kontraktilen Apparats der Herzmuskelzelle und der spezifischste Biomarker zur Detektion eines Myokardschadens. Mit der Einführung hochsensitiver kardialer Troponin-Assays hat sich die Diagnostik des akuten Myokardinfarkts (AMI) grundlegend verändert. Diese ermöglichen den Nachweis minimaler Troponinfreisetzungen bereits kurze Zeit nach Symptombeginn und haben die bisherige Diagnostik revolutioniert. Insbesondere die in den aktuellen Leitlinien der europäischen Gesellschaft für Kardiologie verankerten 0/1-h- und 0/2-h-Algorithmen erlauben einen raschen Ein- und Ausschluss des AMI bei Patientinnen und Patienten, die sich mit akuten Brustschmerzen auf der Notfallstation vorstellen. Hierdurch wird der klinische Workflow in der Notfallstation erheblich beschleunigt. Dennoch erfordert die Interpretation von kardialen Troponin-Erhöhungen stets die Berücksichtigung klinischer und kontextueller Faktoren, da zahlreiche andere Krankheitsbilder ebenfalls mit erhöhten Troponinwerten einhergehen können. Neben den laborbasierten Verfahren gewinnen zunehmend auch Point-of-Care-Tests an Bedeutung.
Cardiac troponin (cTn) is a structural protein of the contractile apparatus of cardiomyocytes and the most specific biomarkers for the detection of myocardial injury. The introduction of high-sensitivity cardiac troponin assays has fundamentally transformed the diagnosis of acute myocardial infarction (AMI). These assays enable the detection of minimal troponin release within a short time after symptom onset and have revolutionized the diagnostic approach. In particular, the 0/1-h and 0/2-h algorithms endorsed by the European Society of Cardiology guidelines allow for rapid and reliable rule-in and rule-out decisions in patients presenting with suspected AMI, thereby substantially accelerating emergency department workflows. Nevertheless, interpretation of hs-cTn elevations always requires careful consideration of clinical and contextual factors, as numerous other conditions may also lead to elevated troponin levels. In addition to laboratory-based measurements, point-of-care tests are gaining increasing importance.
Keywords: high-sensitivity cardiac troponin; acute myocardial infarction; 0/1-hour algorithm; biomarker; point-of-care testing
Warum hochsensitives Troponin der kardiale Biomarker Nr. 1 ist
Das kardiale Troponin (cTn) ist ein strukturelles Protein des kontraktilen Apparats der Herzmuskelzelle und spielt eine zentrale Rolle in der Regulation der Myofilamentkontraktion (1, 2). Im Gegensatz zu Troponin C, das auch in der Skelettmuskulatur vorkommt, sind cTn T und I nahezu ausschliesslich im Myokard exprimiert und gelten daher als herzmuskelspezifische Marker (1–3). Die Freisetzung von Troponin in den Blutkreislauf ist ein direktes Zeichen für eine strukturelle Schädigung von Kardiomyozyten, unabhängig von deren Ursache (1–3). Damit ist Troponin der kardiale Biomarker zur Erfassung eines akuten oder chronischen Myokardschadens und essenzieller Bestandteil der Definition des akuten Myokardinfarkts (AMI) (4, 5). Vor der Einführung der hochsensitiven Assays konnten konventionelle Troponin-Tests nur deutlich erhöhte Konzentrationen nachweisen, sodass zur Diagnosestellung häufig serielle Messungen über 6–12 Stunden notwendig waren. Die Einführung der hochsensitiven Troponin-Assays (hs-cTn T und I) ab etwa 2010 markierte einen Paradigmenwechsel: Diese Methoden detektieren Troponinkonzentrationen, die bei bis zu 50–90 % gesunder Individuen messbar sind, und unterscheiden sich in zwei wesentlichen Punkten von konventionellen Troponin-Assays (1, 6–8). Erstens ermöglichen sie den Nachweis von Troponin bei einem erheblichen Anteil gesunder Personen und zweitens erlauben sie eine präzisere Definition des Normalbereichs (entsprechend der 99. Perzentile), wobei die analytische Präzision der Assays durch den Variationskoeffizienten beschrieben wird, der idealerweise <10 % betragen sollte (1). So wird eine präzise Quantifizierung minimaler Freisetzungen bereits kurz nach Symptombeginn ermöglicht. In der aktuellen ESC-Leitlinie 2023 werden hs-cTn T und I als Biomarker der Wahl für die Diagnose des AMI empfohlen (5). Zusammen mit Anamnese, klinischer Untersuchung und 12-Kanal-EKG bilden sie die diagnostische Trias (5). Dank der hohen analytischen Sensitivität und Reproduzierbarkeit lassen sich dynamische Veränderungen (Anstieg/Abfall) bereits innerhalb von 1–2 Stunden erfassen, was die Grundlage der modernen 0/1-h- und 0/2-h-Algorithmen bildet (6, 7, 9–12). Durch diese Innovation konnten die Infarktdiagnostik entscheidend beschleunigt und die Patientensicherheit verbessert werden (10). Frühe Rule-out-Entlassungen, rasche Identifikation von Hochrisikopatienten und eine zeitkritische Therapieeinleitung sind möglich.
Analytik
Hochsensitive Troponin-Assays zeichnen sich durch eine Messpräzision mit einem Variationskoeffizienten ≤ 10 % im Bereich der 99. Perzentile des oberen Referenzwerts sowie durch eine Nachweisrate ≥ 50 % bei gesunden Personen aus (1). Die Grosszahl der kommerziell erhältlichen hs-cTn T- und auch hs-cTn I-Assays erfüllt diese Kriterien. Wichtig ist zu beachten, dass die 99. Perzentile für jeden hs-cTn Assay in unterschiedlichen gesunden Populationen deriviert wird. Somit sind die Referenzwerte eines hs-cTn Assays nicht auf einen anderen übertragbar. Für eine valide Interpretation sind zudem präanalytische Faktoren wie korrekte Probenentnahme, zeitgerechte Zentrifugation und Vermeidung von Hämolyse entscheidend, welche einen Einfluss haben können (3, 13, 14). Auch wenn die analytischen Details komplex sind, ist die klinisch entscheidende Botschaft klar: Hochsensitive Troponin-Assays vereinen Genauigkeit mit hervorragender Reproduzierbarkeit und bilden damit die Grundlage für eine verlässliche und differenzierte Diagnostik des AMI.
Myokardschaden und Freisetzungskinetik
Die kardialen Troponine sind intrazelluläre Proteine, die im Zytosol und an den kontraktilen Myofibrillen der Herzmuskelzellen gebunden vorliegen (15). Kommt es zum Beispiel infolge einer ischämischen Schädigung zu einer gestörten Zellmembranintegrität, werden zytosolische wie auch gebundene Troponinanteile freigesetzt (15). Die Halbwertszeit von cTn T im Blut beträgt etwa 120 Minuten, wobei das verlängerte Nachweisfenster darauf zurückzuführen ist, dass während der zellulären Nekrose fortlaufend Troponin T aus dem myofibrillären Pool freigesetzt wird, während sich der kontraktile Apparat der Kardiomyozyten schrittweise abbaut (15). Die Freisetzung erklärt die Kinetik des hs-cTn-Anstiegs beim AMI: Der Troponinwert beginnt meist innerhalb von 1–3 Stunden nach Symptombeginn zu steigen, erreicht nach etwa 12–24 Stunden seinen Gipfel und fällt anschliessend über mehrere Tage wieder ab. Neben der Ischämie-induzierten Nekrose können auch andere Mechanismen, etwa Apoptose, Dehnung, Entzündung oder toxische Schädigung, zur Freisetzung von Troponin führen, wobei die Dynamik des Anstiegs meist geringer ausfällt. Die hochsensitiven Assays ermöglichen es, diese feinen Konzentrationsänderungen zu erkennen und damit zwischen akuter und chronischer Myokardschädigung zu unterscheiden, ein entscheidender Fortschritt für die differenzierte Interpretation erhöhter Troponinwerte.
Revolutionierte Infarktdiagnostik – Rolle des Troponins und der ESC-Algorithmen
Mit Einführung der hochsensitiven Troponin-Assays wurde die Diagnostik des AMI grundlegend verändert. Während frühere Testverfahren erst nach mehreren Stunden pathologische Werte zeigten, erlauben die hochsensitiven Assays den Nachweis minimaler Myokardschädigungen bereits kurz nach Symptombeginn (16–22). Damit wurde die Zeit bis zur gesicherten Diagnose deutlich verkürzt, was einen entscheidenden Vorteil mit sich bringt, denn weiterhin gilt: «Time is muscle».
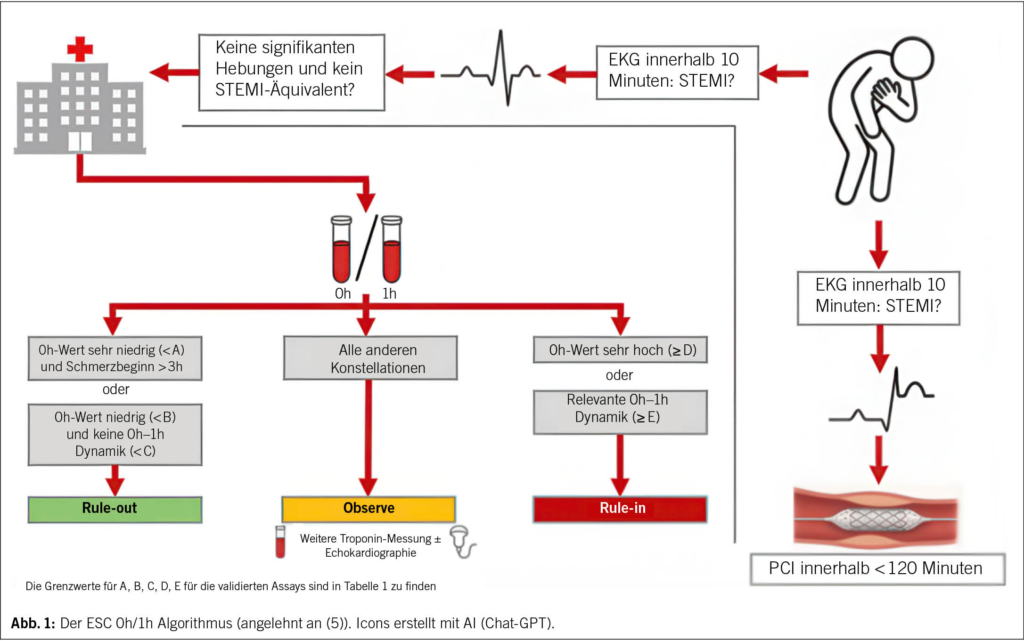
Die aktuellen ESC-Leitlinien von 2023 empfehlen den 0/1-h-Algorithmus als bevorzugte Strategie zum schnellen und sicheren Ein- oder Ausschluss des AMI (Abb. 1) (5).
Dieser Algorithmus basiert auf zwei Troponinmessungen: einer initialen Bestimmung zum Zeitpunkt 0 (Stunden) und einer zweiten Messung 1 Stunde später (5). Alternativ kann, etwa bei organisatorischen Einschränkungen oder verzögerter Blutabnahme, der 0/2-h-Algorithmus angewendet werden (5). Beide Verfahren sind für verschiedene Assays validiert und liefern eine ausgezeichnete diagnostische Sicherheit, wobei der 0/1-h-Algorithmus aufgrund seiner frühzeitigeren Entscheidungsmöglichkeit bevorzugt wird. Das Konzept beruht auf zwei zentralen Prinzipien: Erstens ist das Troponin eine kontinuierliche Variable, deren absolute Konzentration eng mit der Wahrscheinlichkeit eines Myokardinfarkts korreliert (23). Zweitens liefern frühe absolute Änderungen («Deltas») der Troponinwerte zwischen der Erst- und der Folgemessung entscheidende Informationen zur Dynamik des Myokardschadens (24, 25). Während relative Veränderungen (z. B. + 20 %) in der Vergangenheit häufig verwendet wurden, empfehlen die Leitlinien heute die Verwendung Assay-spezifischer absoluter Deltas, da diese weniger durch Messvariabilität beeinflusst sind und eine höhere diagnostische Genauigkeit bieten (5).
Ein Rule-out ist möglich, wenn der Troponinwert entweder bereits bei der ersten Messung sehr niedrig ist oder wenn der Ausgangswert niedrig bleibt und sich innerhalb von 1 Stunde keine relevante Dynamik zeigt (5, 26). In mehreren grossen Validierungsstudien lag der negative Vorhersagewert (NPV) dieser Strategien bei über 99 %, was eine sichere Entlassung vieler Patienten bereits nach kurzer Zeit ermöglicht (22, 27, 28). Ein Rule-in erfolgt, wenn der Troponinwert bereits bei Aufnahme deutlich erhöht ist, oder wenn innerhalb von 1 bzw. 2 Stunden ein klarer absoluter Anstieg beobachtet wird (5). Der positive Vorhersagewert (PPV) liegt zwischen 70 und 75 %. Patienten, die weder die Rule-out- noch die Rule-in-Kriterien erfüllen, fallen in die sogenannte «Observe-Zone» und benötigen eine dritte Troponin-Messung nach 3 Stunden und weitere Abklärung, wie zum Beispiel eine ergänzende bildgebende kardiale Diagnostik (5, 29).
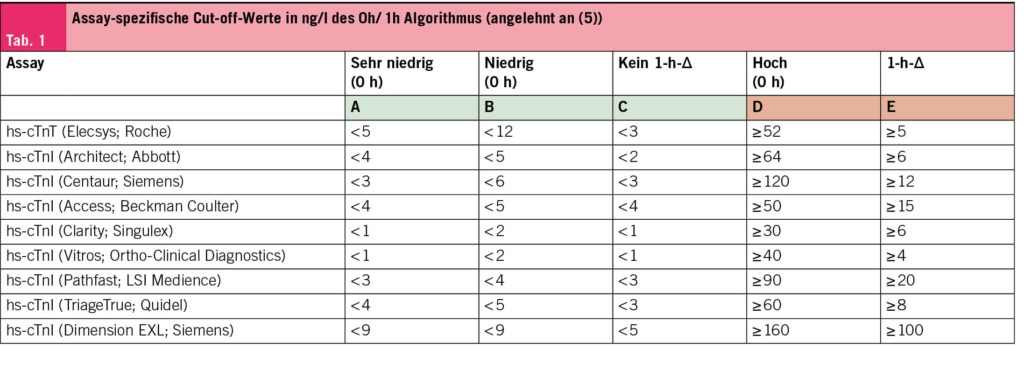
Wie bereits erwähnt sind die Grenzwerte Assay-spezifisch und dürfen nicht zwischen verschiedenen Assays übertragen werden (Tab. 1).
Für den weit verbreiteten Roche Elecsys hs-cTnT-Assay gelten nach ESC-Empfehlung folgende Schwellen: Ein Wert < 5 ng/L (bei Symptombeginn > 3 h) oder ein Ausgangswert < 12 ng/L ohne einen Anstieg von ≥ 3 ng/L nach 1 Stunde schliesst einen AMI aus (5). Ein Wert ≥ 52 ng/L oder ein Anstieg von ≥ 5 ng/L innerhalb 1 Stunde gilt als klarer Hinweis auf einen akuten Infarkt (5). Für den Abbott Architect hs-cTnI-Assay werden etwas andere Grenzwerte verwendet: Ein Wert < 4 ng/L (bei Schmerzbeginn vor > 3h) oder < 5 ng/L ohne Δ ≥ 2 ng/L nach 1 Stunde spricht für Rule-out, während Werte ≥ 64 ng/L oder ein 1-h-Δ ≥ 6 ng/L ein Rule-in definieren (5).
Bei Anwendung des 0/2-h-Algorithmus bleiben die Entscheidungsgrenzen ähnlich, die zulässigen Deltas sind jedoch etwas grösser, da die Zeit zwischen den Messungen länger ist und das Troponin kontinuierlich über die Zeit ansteigt (5). Auch hier liegt die diagnostische Sicherheit für den Ausschluss eines AMI bei über 99 %. In der Praxis wird der 0/2-h-Algorithmus insbesondere eingesetzt, wenn die 1-h-Blutabnahme organisatorisch nicht zuverlässig möglich ist.
Mehrere grosse prospektive Studien, darunter randomisierte Implementierungsstudien, haben gezeigt, dass der 0/1-h-Algorithmus im Vergleich zu älteren Strategien sowohl die Zeit bis zur Diagnose als auch die Aufenthaltsdauer in der Notaufnahme signifikant verkürzt, ohne die Sicherheit zu beeinträchtigen (22, 27, 28). Entsprechend wurde der frühere Algorithmus in den ESC-Leitlinien 2023 hinsichtlich des Empfehlungsgrades abgestuft, während der 0/1-h-Algorithmus eine Klasse-I-Empfehlung besitzt (5). Damit haben die hochsensitiven Troponin-Assays die Diagnostik des akuten Myokardinfarkts revolutioniert: Sie ermöglichen eine frühe, hochpräzise Abgrenzung zwischen akuter und chronischer Myokardschädigung, reduzieren unnötige Hospitalisierungen und verbessern die Risikostratifizierung. In Kombination mit klinischer Beurteilung und einem 12-Kanal-EKG bilden sie heute das zentrale Fundament der modernen Infarktdiagnostik.
Altersabhängige Effekte und Einfluss der Nierenfunktion
Die 99. Perzentile der oberen Referenzgrenze (upper reference limit, URL) bildet die zentrale diagnostische Schwelle für die Definition eines Myokardschadens und eines AMI. Troponin-Konzentrationen oberhalb dieses Wertes gelten als erhöht (4). Diese Schwelle ist Assay-spezifisch und beruht auf Messungen in grosse Kollektiven gesunder Personen. Dabei zeigte sich, dass biologische Unterschiede, insbesondere Alter und Nierenfunktion, einen relevanten Einfluss auf die Troponin-Konzentration haben können.
Mit zunehmendem Alter steigt die Prävalenz leicht erhöhter Troponinspiegel auch in Abwesenheit einer akuten Ischämie (31). Dieser Anstieg reflektiert meist subklinische strukturelle Myokardschäden, Fibrose, hypertensive oder diastolische Belastung. Dennoch wird derzeit kein altersadjustierter Grenzwert in den Leitlinien empfohlen, da die Sicherheit weiterhin gegeben ist und die Verwendung altersspezifischer Grenzwerte zu Herausforderungen in der klinischen Praxis führen könnte (32, 33).
Die chronische Niereninsuffizienz stellt einen weiteren häufigen und klinisch relevanten Confounder der Troponindiagnostik dar (34). Bei eingeschränkter glomerulärer Filtrationsrate finden sich häufig persistierend erhöhte hs-cTn-Konzentrationen, vermutlich bedingt durch eine Kombination aus verminderter renaler Clearance und chronischem Myokardschaden infolge Druck- und Volumenbelastung. Somit empfiehlt es sich, bei Patienten mit eingeschränkter Nierenfunktion (ebenso bei Patienten im fortgeschrittenen Alter) nicht den absoluten Ausgangswert, sondern vor allem die Dynamik (Anstieg oder Abfall) zwischen den Messungen zu bewerten (5). Ein signifikanter Anstieg über die Assay-spezifische Δ-Schwelle hinaus gilt auch in dieser Population als starkes Indiz für eine akute Myokard schädigung z. B. im Rahmen eines ischämischen Prozesses. Folglich sollte die Diagnose eines AMI in diesem Kontext nur bei nachweisbarer Dynamik in Verbindung mit Symptomen und/oder EKG-Veränderungen gestellt werden. Ein persistierend stabil erhöhter Troponinwert ohne Klinik hingegen spricht eher für eine chronische kardiale Schädigung und ist prognostisch bedeutsam, ohne zwingend auf ein akutes Koronarsyndrom hinzuweisen.
Klinische Szenarien und Pitfalls
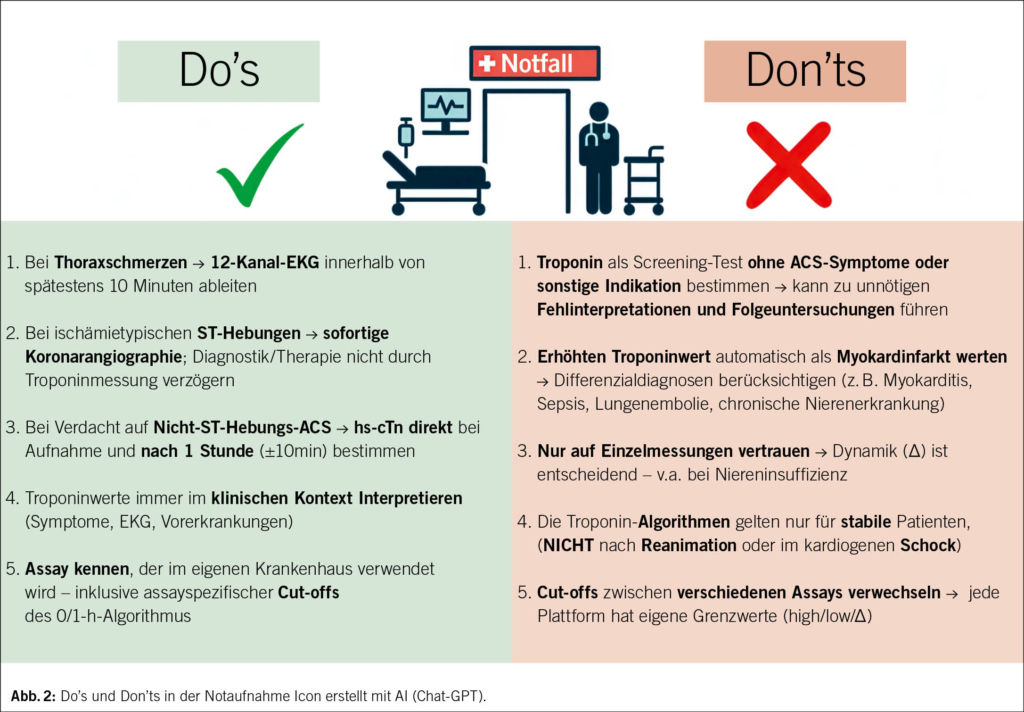
Die Interpretation erhöhter hochsensitiver Troponinwerte erfordert stets eine enge Verknüpfung mit Anamnese, klinischem Kontext und EKG-Befunden (Abb. 2). Eine Troponinerhöhung weist grundsätzlich auf einen Myokardschaden, aber nicht zwingend auf einen AMI hin. Erst das Zusammenspiel aus klinischer Präsentation mit Symptomen, ischämietypischer Dynamik und ggf. korrespondierenden EKG-Veränderungen erlaubt die sichere Diagnose eines AMI (4, 5). Der Typ-1-Myokardinfarkt entsteht infolge eines (plaqueassoziierten) koronaren (teilweise)-Verschlusses mit Thrombusbildung und akuter Myokardischämie. Der Typ-2-Myokardinfarkt hingegen beruht auf einer Ungleichgewichts-Ischämie zwischen myokardialem Sauerstoffbedarf und -angebot ohne akute Plaqueruptur (35). Er tritt sekundär im Rahmen anderer Erkrankungen auf, die zu einem verminderten Sauerstoffangebot (z. B. bei Hypoxie) oder einem erhöhten Sauerstoffbedarf (z. B. Tachykardie) führen (35). Aggraviert kann dies werden durch bestehende, unter «normalen Umständen» nicht-signifikanten Stenosen. Typische klinische Konstellationen sind die Anämie (reduziertes Sauerstoffangebot bei stabiler KHK oder auch blanden Koronarien), das tachykarde Vorhofflimmern oder andere tachykarde Herzrhythmusstörungen (erhöhter Sauerstoffverbrauch und diastolische Minderversorgung) und die Lungenembolie (akute Druckbelastung und Dilatation des rechten Ventrikels mit subendokardialer Ischämie) (35). In all diesen Fällen kann das hs-cTn deutlich erhöht sein, ohne dass eine akute Koronarobstruktion vorliegt. Entscheidend ist die Gesamtinterpretation der klinischen Situation: Ein Typ-2-Infarkt ist kein primär koronar-interventionelles Krankheitsbild, sondern Ausdruck eines sekundären myokardialen Schadens, der eine kausale Behandlung der Grunderkrankung erfordert (35).
Neben ischämischen Mechanismen existieren zahlreiche nicht-ischämische Ursachen für erhöhte hs-cTn-Werte, die eine differenzierte Beurteilung erfordern. Ein möglicher Befund in der klinischen Praxis ist die Troponinerhöhung nach Liegetrauma oder bei ausgeprägter Skelettmuskelschädigung, etwa bei einer Rhabdomyolyse oder rheumatischen Erkrankung (36, 37). Dabei kann das Troponin T erhöht sein, das Troponin I bleibt in der Regel normal (36). Auch die Myokarditis präsentiert sich mit Troponinerhöhung und Brustschmerz und kann somit ein akutes Koronarsyndrom imitieren (38). Charakteristisch ist häufig eine moderate, teilweise länger anhaltende Troponinfreisetzung ohne koronares Korrelat (38). Die Differenzierung gelingt insbesondere durch die kardiale MRT, welche ein myokardiales Ödem und Spätkontrastmittelaufnahme (late gadolinium enhancement, vorwiegend subepikardial oder mittmyokardial in einem nicht-ischämischen Verteilungsmuster) nachweist (39). Nach perkutaner Koronarintervention (PCI) oder koronarer Bypass-Operation (CABG) treten Troponinerhöhungen häufig auf (40). Diese spiegeln in der Mehrzahl der Fälle prozedurale Myokardschäden wider, die definitionsgemäss erst ab Überschreiten des fünffachen 99. Perzentils (PCI) bzw. des zehnfachen (CABG) als prozedurbezogener Myokardinfarkt (Typ 4a/5 MI) gewertet werden (in Kombination mit neuen EKG-Veränderungen/ neuen Veränderungen in der Bildgebung, zum Beispiel Wandbewegungsstörungen im Echo) (4). Eine isolierte moderate Troponinerhöhung ohne klinische oder elektrokardiographische Hinweise auf Ischämie sollte hier nicht als Infarkt fehlinterpretiert werden (4). Ein weiterer häufiger Sonderfall betrifft intensiven Sport, bei dem transiente, meist moderate Anstiege des hs-cTn beobachtet werden können (41). Die zugrunde liegende Mechanik ist multifaktoriell und umfasst myozytäre Membranpermeabilität, Dehnung, zellulären Stress und Skelettmuskelschäden, ohne dass strukturelle Nekrose vorliegen muss (41). Zusammenfassend gilt: Nicht jede Troponinerhöhung ist Ausdruck eines AMI. Die differenzierte Betrachtung von Ursache, Dynamik, Begleitsymptomen und EKG-Verlauf ist entscheidend, um Überdiagnosen zu vermeiden und eine gezielte Therapie einzuleiten.
Point-of-Care-Assays
Neben den laborbasierten Hochdurchsatzsystemen gewinnen in den letzten Jahren Point-of-Care-(POC)-Assays zunehmend an Bedeutung (42, 43). Sie ermöglichen eine schnelle Messung von Troponin ohne zeitliche Verzögerung durch den Probentransport und Laborprozess. Ziel ist es, den diagnostischen Ablauf weiter zu beschleunigen und insbesondere in präklinischen oder ressourcenlimitierten Settings, wie im Rettungsdienst, peripheren Spitälern, ambulanten Praxen oder ländliche Regionen eine zeitnahe Entscheidungsfindung zu ermöglichen.
Moderne POC-Systeme verwenden Technologien, die in ihrer analytischen Leistungsfähigkeit den Labor-Assays zunehmend nahekommen (42, 43). Einige der neueren Geräte, etwa der Siemens Atellica VTLi, der Abbott i-STAT Alinity oder der Roche LumiraDx hs-cTnI-Assay, erfüllen bereits viele Kriterien für «high-sensitivity». Damit können sie, im Gegensatz zu älteren POC-Tests, in standardisierte 0/1-h- oder 0/2-h-Algorithmen integriert werden, jedoch sind auch hier die Assay-spezifischen Grenzwerte zu beachten (42, 43). Der Hauptvorteil dieser Systeme liegt in der Zeitersparnis. Es konnte gezeigt werden, dass sich mit POC-Assays die «door-to-troponin result time» um bis zu 54 Minuten verkürzen lässt, bei neueren POC-Systemen ohne relevante Einbussen in diagnostischer Sicherheit (42–44). Dadurch können Rule-out-Entscheidungen bereits innerhalb einer Stunde getroffen werden (bei Schmerzbeginn vor > 3h), ein Vorteil insbesondere in überlasteten Notaufnahmen oder präklinischen Situationen (42, 43). Insgesamt stellen POC-Assays eine vielversprechende Ergänzung der etablierten Laboranalytik dar. Sie können die Versorgung von Patienten mit Verdacht auf akutes Koronarsyndrom deutlich beschleunigen und sind insbesondere für den Einsatz in präklinischen und dezentralen Strukturen geeignet. Mit der fortschreitenden Miniaturisierung und Standardisierung dieser Technologien ist absehbar, dass hochpräzise POC-Systeme künftig einen festen Platz in der AMI-Diagnostik einnehmen und die zeitkritischen ESC-Algorithmen auch ausserhalb des Krankenhauses ermöglichen werden.
Ausblick: KI-gestützte Pfade und transdermale Messung von Troponin I
Mit der Einführung hochsensitiver Troponin-Assays wurde die Diagnostik des akuten Myokardinfarkts bereits erheblich beschleunigt und standardisiert. Dennoch beruhen die aktuell empfohlenen ESC-Algorithmen auf festen Schwellenwerten und Zeitpunkten, die individuelle Unterschiede, etwa Alter, Nierenfunktion, EKG-Veränderungen (ausser ST-Hebungen), Komorbiditäten oder Zeitpunkt des Symptombeginns, nicht berücksichtigen (5). Hier setzt der Einsatz von künstlicher Intelligenz (KI) an: Machine-Learning-Modelle ermöglichen eine individualisierte Interpretation von Labor- und EKG-Daten und könnten die bisher starren Entscheidungsgrenzen ablösen.
Hierzu wurde der CoDE-ACS-Algorithmus (Collaboration for the Diagnosis and Evaluation of Acute Coronary Syndrome) entwickelt und in internationalen Kohorten validiert (45, 46). Dieses System kombiniert Troponinkonzentrationen, sowohl bei Aufnahme als auch in seriellen Messungen, mit klinischen Variablen wie Alter, Geschlecht, Blutdruck, Herzfrequenz, Nierenfunktion, Hämoglobin, Symptombeginn und EKG-Befunden (45, 46). Aus diesen Informationen berechnet das Modell eine individuelle Wahrscheinlichkeit für das Vorliegen eines Myokardinfarkts (0–100 Punkte). In einer prospektiven Analyse zeigte CoDE-ACS eine ausgezeichnete Diskriminationsleistung (AUC ≈ 0.95) und identifizierte deutlich mehr Patienten mit niedriger Infarkt-Wahrscheinlichkeit (61 vs. 27 %) bei gleichem negativem prädiktivem Wert (45). Die Folgestudie bestätigte diese Ergebnisse in über 4000 Patienten und zeigte, dass CoDE-ACS unabhängig vom Zeitpunkt der Messung (0, 1 oder 2 h) stabil performt und mehr Patienten sicher als «low probability» klassifizieren kann als die ESC-0/1- oder 0/2-h-Algorithmen (46). KI-gestützte Entscheidungssysteme wie CoDE-ACS könnten künftig Labor-, EKG- und klinische Daten in Echtzeit integrieren und die Wahrscheinlichkeit eines AMI patientenspezifisch quantifizieren. Damit eröffnen sie den Weg zu dynamischen, adaptiven Diagnosepfaden, die sich an individuellen Risikoprofilen orientieren und Über- wie Unterdiagnosen reduzieren. Ob dieser Ansatz im klinischen Alltag zu einer verbesserten Versorgung und Ressourcennutzung führt, bleibt abzuwarten.
Eine vielversprechende Weiterentwicklung stellt die transdermale Messung von kardialem Troponin mittels optischer IR-Sensoren dar (47). Das neu entwickelte, nichtinvasive Wearable-Device («Infrasensor») ermöglicht eine Troponin I-Bestimmung innerhalb von nur 3 Minuten und zeigte in einer multizentrischen Pilotstudie eine gute Sensitivität (90 %) und eine C-Statistik-AUC von 0.90 zur Identifikation erhöhter cTnI-Spiegel (47). Künftige Studien müssen klären, ob diese Technologie in der Notaufnahme oder sogar präklinisch eingesetzt werden kann, um den diagnostischen Prozess beim akuten Koronarsyndrom weiter zu beschleunigen.
Copyright
Aerzteverlag medinfo AG
Zweitabdruck aus «der informierte arzt» 12/2025
Klinik für Kardiologie und
Cardiovascular Research Institute Basel (CRIB)
Universitätsspital Basel
Petersgraben 4
4031 Basel
Klinik für Kardiologie und
Cardiovascular Research Institute Basel (CRIB)
Universitätsspital Basel
Petersgraben 4
4031 Basel
Klinik für Kardiologie und
Cardiovascular Research Institute Basel (CRIB)
Universitätsspital Basel
Petersgraben 4
4031 Basel
jasper.boeddinghaus@usb.ch
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Hochsensitive Troponin-Assays (hs-cTnT und hs-cTnI) sind heute der zentrale Biomarker in der Diagnostik des AMI und ermöglichen den Nachweis minimaler Myokardschädigungen bereits kurz nach Symptombeginn.
- Die ESC-0/1-h- und 0/2-h-Algorithmen haben die AMI-Diagnostik revolutioniert, indem sie eine schnelle und sichere Rule-out/Rule-in-Entscheidung mit hoher Sensitivität und Spezifität erlauben.
- Die Interpretation der hs-cTn-Werte muss immer im klinischen Kontext erfolgen. Besonders Alter, Nierenfunktion und Begleiterkrankungen beeinflussen die Troponinkonzentration und erfordern eine individuelle Bewertung des Absolutwertes und auch der Dynamik.
- Nicht jede Troponinerhöhung bedeutet einen AMI. Differenzialdiagnosen wie Myokarditis, Tachyarrhythmien, Lungenembolie oder Niereninsuffizienz sind häufige Fallstricke in der Interpretation.
- KI-basierte Systeme wie CoDE-ACS kombinieren Labor-, EKG- und klinische Daten zu einem patientenspezifischen Risikoscore und könnten künftig die diagnostische Präzision und Effizienz weiter verbessern.
1. Mueller C. Biomarkers and acute coronary syndromes: an update. European Heart Journal [Internet]. 1. März 2014 [zitiert 22. Oktober 2025];35(9):552–6. Verfügbar unter: https://academic.oup.com/eurheartj/article-lookup/doi/10.1093/eurheartj/eht530
2. Thygesen K, Mair J, Katus H, Plebani M, Venge P, Collinson P, u. a. Recommendations for the use of cardiac troponin measurement in acute cardiac care. European Heart Journal [Internet]. 2. September 2010 [zitiert 22. Oktober 2025];31(18):2197–204. Verfügbar unter: https://academic.oup.com/eurheartj/article-lookup/doi/10.1093/eurheartj/ehq251
3. Giannitsis E, Kurz K, Hallermayer K, Jarausch J, Jaffe AS, Katus HA. Analytical Validation of a High-Sensitivity Cardiac Troponin T Assay. Clinical Chemistry [Internet]. 1. Februar 2010 [zitiert 22. Oktober 2025];56(2):254–61. Verfügbar unter: https://academic.oup.com/
clinchem/article/56/2/254/5622529
4. Thygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ, Morrow DA, u. a. Fourth Universal Definition of Myocardial Infarction (2018). Journal of the American College of Cardiology [Internet]. Oktober 2018 [zitiert 27. Oktober 2025];72(18):2231–64. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0735109718369419
5. Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, u. a. 2023 ESC Guidelines for the management of acute coronary syndromes. European Heart Journal [Internet]. 25. August 2023;1–107. Verfügbar unter: https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehad191/7243210
6. Reichlin T, Schindler C, Drexler B, Twerenbold R, Reiter M, Zellweger C, u. a. One-Hour Rule-out and Rule-in of Acute Myocardial Infarction Using High-Sensitivity Cardiac Troponin T. Arch Intern Med [Internet]. 10. September 2012 [zitiert 22. Oktober 2025];172(16):1211. Verfügbar unter: http://archinte.jamanetwork.com/article.aspx?doi=10.1001/
archinternmed.2012.3698
7. Thygesen K, Mair J, Giannitsis E, Mueller C, Lindahl B, Blankenberg S, u. a. How to use high-sensitivity cardiac troponins in acute cardiac care. European Heart Journal [Internet]. 2. September 2012 [zitiert 22. Oktober 2025];33(18):2252–7. Verfügbar unter: https://academic.oup.com/eurheartj/article-lookup/doi/10.1093/eurheartj/ehs154
8. Than M, Cullen L, Reid CM, Lim SH, Aldous S, Ardagh MW, u. a. A 2-h diagnostic protocol to assess patients with chest pain symptoms in the Asia-Pacific region (ASPECT): a prospective observational validation study. The Lancet [Internet]. März 2011 [zitiert 22. Oktober 2025];377(9771):1077–84. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0140673611603103
9. Reichlin T, Twerenbold R, Reiter M et al. Introduction of High-sensitivity Troponin Assays: Impact on Myocardial Infarction Incidence and Prognosis. The American Journal of Medicine [Internet]. Dezember 2012 [zitiert 22. Oktober 2025];125(12):1205-1213.e1. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S000293431200647X
10. Reichlin T, Hochholzer W, Bassetti S, Steuer S, Stelzig C, Hartwiger S, u. a. Early Diagnosis of Myocardial Infarction with Sensitive Cardiac Troponin Assays. N Engl J Med [Internet]. 27. August 2009 [zitiert 22. Oktober 2025];361(9):858–67. Verfügbar unter: http://www.nejm.org/doi/abs/10.1056/NEJMoa0900428
11. Keller T, Zeller T, Peetz D, Tzikas S, Roth A, Czyz E, u. a. Sensitive Troponin I Assay in Early Diagnosis of Acute Myocardial Infarction. N Engl J Med [Internet]. 27. August 2009 [zitiert 22. Oktober 2025];361(9):868–77. Verfügbar unter: http://www.nejm.org/doi/abs/10.1056/NEJMoa0903515
12. Giannitsis E, Becker M, Kurz K et al. High-Sensitivity Cardiac Troponin T for Early Prediction of Evolving Non–ST-Segment Elevation Myocardial Infarction in Patients with Suspected Acute Coronary Syndrome and Negative Troponin Results on Admission. Clinical Chemistry [Internet]. 1. April 2010 [zitiert 22. Oktober 2025];56(4):642–50. Verfügbar unter: https://academic.oup.com/clinchem/article/56/4/642/5622453
13. Hawkins RC. Hemolysis Interference in the Ortho-Clinical Diagnostics Vitros ECi cTnI Assay. Clinical Chemistry [Internet]. 1. Juli 2003 [zitiert 22. Oktober 2025];49(7):1226–7. Verfügbar unter: https://academic.oup.com/clinchem/article/49/7/1226/5642043
14. Dasgupta A, Wells A, Biddle DA. Negative interference of bilirubin and hemoglobin in the MEIA troponin I assay but not in the MEIA CK‐MB assay. Clinical Laboratory Analysis [Internet]. März 2001 [zitiert 22. Oktober 2025];15(2):76–80. Verfügbar unter: https://onlinelibrary.wiley.com/doi/10.1002/jcla.5
15. Apple FS, Collinson PO, for the IFCC Task Force on Clinical Applications of Cardiac Biomarkers. Analytical Characteristics of High-Sensitivity Cardiac Troponin Assays. Clinical Chemistry [Internet]. 1. Januar 2012 [zitiert 22. Oktober 2025];58(1):54–61. Verfügbar unter: https://academic.oup.com/clinchem/article/58/1/54/5620628
16. Boeddinghaus J, Nestelberger T, Twerenbold R, Wildi K, Badertscher P, Cupa J, u. a. Direct Comparison of 4 Very Early Rule-Out Strategies for Acute Myocardial Infarction Using High-Sensitivity Cardiac Troponin I. Circulation [Internet]. 25. April 2017 [zitiert 26. Oktober 2025];135(17):1597–611. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.116.025661
17. Wildi K, Boeddinghaus J, Nestelberger T, Twerenbold R, Badertscher P, Wussler D, u. a. Comparison of fourteen rule-out strategies for acute myocardial infarction. International Journal of Cardiology [Internet]. Mai 2019 [zitiert 26. Oktober 2025];283:41–7. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0167527318347843
18. Rubini Gimenez M, Twerenbold R, Jaeger C, Schindler C, Puelacher C, Wildi K, u. a. One-hour Rule-in and Rule-out of Acute Myocardial Infarction Using High-sensitivity Cardiac Troponin I. The American Journal of Medicine [Internet]. August 2015 [zitiert 26. Oktober 2025];128(8):861-870.e4. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0002934315002569
19. Badertscher P, Boeddinghaus J, Twerenbold R, Nestelberger T, Wildi K, Wussler D, u. a. Direct Comparison of the 0/1h and 0/3h Algorithms for Early Rule-Out of Acute Myocardial Infarction. Circulation [Internet]. 5. Juni 2018 [zitiert 26. Oktober 2025];137(23):2536–8. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.118.034260
20. Chapman AR, Anand A, Boeddinghaus J, Ferry AV, Sandeman D, Adamson PD, u. a. Comparison of the Efficacy and Safety of Early Rule-Out Pathways for Acute Myocardial Infarction. Circulation [Internet]. 25. April 2017 [zitiert 26. Oktober 2025];135(17):1586–96. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.116.025021
21. Chapman AR, Fujisawa T, Lee KK, Andrews JP, Anand A, Sandeman D, u. a. Novel high-sensitivity cardiac troponin I assay in patients with suspected acute coronary syndrome. Heart [Internet]. 15. November 2018 [zitiert 26. Oktober 2025];heartjnl-2018-314093. Verfügbar unter: https://heart.bmj.com/lookup/doi/10.1136/heartjnl-2018-314093
22. Chew DP, Lambrakis K, Blyth A, Seshadri A, Edmonds MJR, Briffa T, u. a. A Randomized Trial of a 1-Hour Troponin T Protocol in Suspected Acute Coronary Syndromes: The Rapid Assessment of Possible Acute Coronary Syndrome in the Emergency Department With High-Sensitivity Troponin T Study (RAPID-TnT). Circulation [Internet]. 5. November 2019 [zitiert 26. Oktober 2025];140(19):1543–56. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.119.042891
23. Neumann JT, Twerenbold R, Ojeda F, Sörensen NA, Chapman AR, Shah ASV, u. a. Application of High-Sensitivity Troponin in Suspected Myocardial Infarction. N Engl J Med [Internet]. 27. Juni 2019 [zitiert 26. Oktober 2025];380(26):2529–40. Verfügbar unter: http://www.nejm.org/doi/10.1056/NEJMoa1803377
24. Reichlin T, Irfan A, Twerenbold R, Reiter M, Hochholzer W, Burkhalter H, u. a. Utility of Absolute and Relative Changes in Cardiac Troponin Concentrations in the Early Diagnosis of Acute Myocardial Infarction. Circulation [Internet]. 12. Juli 2011 [zitiert 26. Oktober 2025];124(2):136–45. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.111.023937
25. Reichlin T, Twerenbold R, Wildi K, Gimenez MR, Bergsma N, Haaf P, u. a. Prospective validation of a 1-hour algorithm to rule-out and rule-in acute myocardial infarction using a high-sensitivity cardiac troponin T assay. CMAJ [Internet]. 19. Mai 2015 [zitiert 26. Oktober 2025];187(8):E243–52. Verfügbar unter: http://www.cmaj.ca/lookup/doi/10.1503/cmaj.141349
26. Rubini Giménez M, Hoeller R, Reichlin T, Zellweger C, Twerenbold R, Reiter M, u. a. Rapid rule out of acute myocardial infarction using undetectable levels of high-sensitivity cardiac troponin. International Journal of Cardiology [Internet]. Oktober 2013 [zitiert 26. Oktober 2025];168(4):3896–901. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0167527313011030
27. Stoyanov KM, Hund H, Biener M, Gandowitz J, Riedle C, Löhr J, u. a. RAPID-CPU: a prospective study on implementation of the ESC 0/1-hour algorithm and safety of discharge after rule-out of myocardial infarction. European Heart Journal: Acute Cardiovascular Care [Internet]. Februar 2020 [zitiert 26. Oktober 2025];9(1):39–51. Verfügbar unter: https://academic.oup.com/ehjacc/article/9/1/39-51/5933825
28. Twerenbold R, Costabel JP, Nestelberger T, Campos R, Wussler D, Arbucci R, u. a. Outcome of Applying the ESC 0/1-hour Algorithm in Patients With Suspected Myocardial Infarction. Journal of the American College of Cardiology [Internet]. Juli 2019 [zitiert 26. Oktober 2025];74(4):483–94. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0735109719353811
29. Lopez-Ayala P, Nestelberger T, Boeddinghaus J, Koechlin L, Ratmann PD, Strebel I, u. a. Novel Criteria for the Observe-Zone of the ESC 0/1h-hs-cTnT Algorithm. Circulation [Internet]. 7. September 2021 [zitiert 26. Oktober 2025];144(10):773–87. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.120.052982
30. Reiter M, Twerenbold R, Reichlin T, Haaf P, Peter F, Meissner J, u. a. Early diagnosis of acute myocardial infarction in the elderly using more sensitive cardiac troponin assays. European Heart Journal [Internet]. Juni 2011 [zitiert 27. Oktober 2025];32(11):1379–89. Verfügbar unter: https://academic.oup.com/eurheartj/article-lookup/doi/10.1093/eurheartj/ehr033
31. Gore MO, Seliger SL, deFilippi CR, Nambi V, Christenson RH, Hashim IA, u. a. Age- and Sex-Dependent Upper Reference Limits for the High-Sensitivity Cardiac Troponin T Assay. Journal of the American College of Cardiology [Internet]. April 2014 [zitiert 27. Oktober 2025];63(14):1441–8. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0735109714003386
32. Boeddinghaus J, Nestelberger T, Twerenbold R, Neumann JT, Lindahl B, Giannitsis E, u. a. Impact of age on the performance of the ESC 0/1h-algorithms for early diagnosis of myocardial infarction. European Heart Journal [Internet]. 7. November 2018 [zitiert 27. Oktober 2025];39(42):3780–94. Verfügbar unter: https://academic.oup.com/eurheartj/article/39/42/3780/5086724
33. Twerenbold R, Badertscher P, Boeddinghaus J, Nestelberger T, Wildi K, Puelacher C, u. a. 0/1-Hour Triage Algorithm for Myocardial Infarction in Patients With Renal Dysfunction. Circulation [Internet]. 30. Januar 2018 [zitiert 26. Oktober 2025];137(5):436–51. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.117.028901
34. Chapman AR, Taggart C, Boeddinghaus J, Mills NL, Fox KAA. Type 2 myocardial infarction: challenges in diagnosis and treatment. European Heart Journal [Internet]. 7. Februar 2025 [zitiert 28. Oktober 2025];46(6):504–17. Verfügbar unter: https://academic.oup.com/eurheartj/article/46/6/504/7920120
35. Du Fay De Lavallaz J, Prepoudis A, Wendebourg MJ, Kesenheimer E, Kyburz D, Daikeler T, u. a. Skeletal Muscle Disorders: A Noncardiac Source of Cardiac Troponin T. Circulation [Internet]. 14. Juni 2022 [zitiert 26. Oktober 2025];145(24):1764–79. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.121.058489
36. Giger RD, Du Fay De Lavallaz J, Prepoudis A, Stoll T, Lopez-Ayala P, Glarner N, u. a. Rhabdomyolysis. Journal of the American College of Cardiology [Internet]. Dezember 2020 [zitiert 26. Oktober 2025];76(22):2685–7. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0735109720374167
37. Prepoudis A, Koechlin L, Nestelberger T, Boeddinghaus J, Lopez-Ayala P, Wussler D, u. a. Incidence, clinical presentation, management, and outcome of acute pericarditis and myopericarditis. European Heart Journal Acute Cardiovascular Care [Internet]. 8. Februar 2022 [zitiert 28. Oktober 2025];11(2):137–47. Verfügbar unter: https://academic.oup.com/ehjacc/article/11/2/137/6445206
38. Schulz-Menger J, Collini V, Gröschel J, Adler Y, Brucato A, Christian V, u. a. 2025 ESC Guidelines for the management of myocarditis and pericarditis. European Heart Journal [Internet]. 22. Oktober 2025 [zitiert 28. Oktober 2025];46(40):3952–4041. Verfügbar unter: https://academic.oup.com/eurheartj/article/46/40/3952/8234483
39. Koechlin L, Boeddinghaus J, Nestelberger T, Lopez-Ayala P, Shrestha S, Wussler D, u. a. Lower diagnostic accuracy of hs-cTnI in patients with prior coronary artery bypass grafting. International Journal of Cardiology [Internet]. Mai 2022 [zitiert 26. Oktober 2025];354:1–6. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0167527322002601
40. Gresslien T, Agewall S. Troponin and exercise. International Journal of Cardiology [Internet]. Oktober 2016 [zitiert 28. Oktober 2025];221:609–21. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0167527316312505
41. Koechlin L, Boeddinghaus J, Lopez-Ayala P, Reber C, Nestelberger T, Wildi K, u. a. Clinical and Analytical Performance of a Novel Point-of-Care High-Sensitivity Cardiac Troponin I Assay. Journal of the American College of Cardiology [Internet]. August 2024 [zitiert 26. Oktober 2025];84(8):726–40. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0735109724076307
42. Boeddinghaus J, Nestelberger T, Koechlin L, Wussler D, Lopez-Ayala P, Walter JE, u. a. Early Diagnosis of Myocardial Infarction With Point-of-Care High-Sensitivity Cardiac Troponin I. Journal of the American College of Cardiology [Internet]. März 2020 [zitiert 26. Oktober 2025];75(10):1111–24. Verfügbar unter: https://linkinghub.elsevier.com/retrieve/pii/S0735109720302527
43. Koehler J, Flarity K, Hertner G, Aker J, Stout JP, Gifford M, u. a. Effect of Troponin I Point-of-Care Testing on Emergency Department Throughput Measures and Staff Satisfaction. Advanced Emergency Nursing Journal [Internet]. Juli 2013 [zitiert 28. Oktober 2025];35(3):270–7. Verfügbar unter: https://journals.lww.com/01261775-201307000-00010
44. Doudesis D, Lee KK, Boeddinghaus J, Bularga A, Ferry AV, Tuck C, u. a. Machine learning for diagnosis of myocardial infarction using cardiac troponin concentrations. Nat Med [Internet]. Mai 2023 [zitiert 28. Oktober 2025];29(5):1201–10. Verfügbar unter: https://www.nature.com/articles/s41591-023-02325-4
45. Boeddinghaus J, Doudesis D, Lopez-Ayala P, Lee KK, Koechlin L, Wildi K, u. a. Machine Learning for Myocardial Infarction Compared With Guideline-Recommended Diagnostic Pathways. Circulation [Internet]. 2. April 2024 [zitiert 28. Oktober 2025];149(14):1090–101. Verfügbar unter: https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.123.066917
46. Peacock WF, Soto-Ruiz KM, Jaffe AS, Tiffany BR, Mahler SA, Patterson BW, u. a. A rapid noninvasive wearable device for assessing cardiac troponin I level. Clin Exp Emerg Med [Internet]. 6. September 2024 [zitiert 28. Oktober 2025];12(3):251–8. Verfügbar unter: http://ceemjournal.org/journal/view.php?doi=10.15441/ceem.24.294
info@herz+gefäss
- Vol. 16
- Ausgabe 1
- März 2026