- Katheterbasierte Behandlungen der akuten Lungenembolie – der Beginn einer neuen Ära
Die antithrombotische Therapie mit Antikoagulanzien und der systemischen Thrombolyse stellt einen zentralen Bestandteil der Behandlung der akuten Lungenembolie dar. Das Feld der interventionellen, katheterbasierten Therapien hat sich rasant entwickelt und ist deshalb in den verfügbaren Leitlinien nicht ausreichend abgebildet. Im Folgenden möchten wir einen konzisen Überblick über die konservative und interventionelle Behandlung von Lungenembolien im intermediären bis hohen Risikospektrum bieten, unter Berücksichtigung der aktuellen Evidenz.
Antithrombotic therapy with anticoagulants and systemic fibrinolysis represents an integral part of the treatment of acute pulmonary embolisms. The field of interventional catheter-based therapies is evolving rapidly and is therefore not adequately reflected in available guidelines. We aim to provide a concise overview of conservative and interventional therapies of intermediate- as well as high-risk pulmonary embolisms, taking the latest evidence into account.
Keywords: Lungenembolie, antithrombotische Therapie, katheterbasierte Therapien
Einleitung
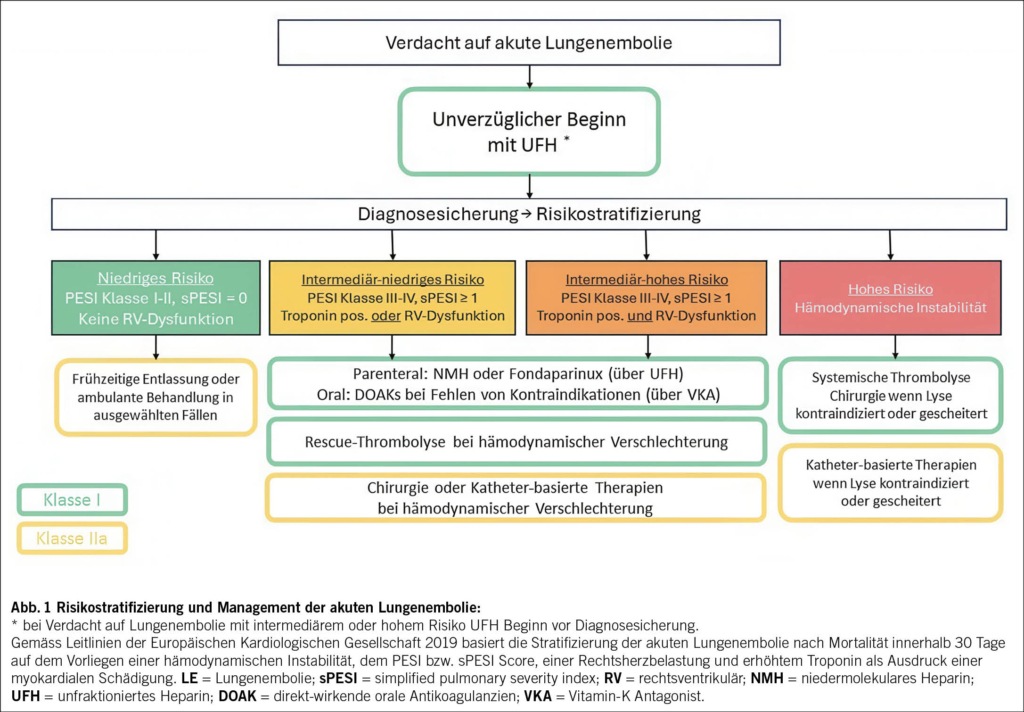
Die antithrombotische Therapie, sei es durch Antikoagulanzien oder durch systemische Thrombolyse, stellt einen zentralen Bestandteil der Behandlung der akuten Lungenembolie dar. Die Wahl der Behandlungsmodalität hängt in erster Linie vom Risikoprofil der Patienten bei Erstvorstellung ab (Abb. 1). Die aktuellen Richtlinien der Europäischen Gesellschaft für Kardiologie (ESC) aus dem Jahr 2019 empfehlen eine systemische Thrombolyse für Patientinnen und Patienten mit hohem Sterblichkeitsrisiko, insbesondere bei hämodynamischer Instabilität oder obstruktivem Schock. Für alle anderen Patienten ohne Kontraindikationen wird eine parenterale oder orale Antikoagulation mittels direkt wirkender oraler Antikoagulanzien (DOAKs) empfohlen. Kontraindikationen für DOAKs wären eine schwere Niereninsuffizienz, Schwangerschaft oder das Antiphospholipidsyndrom (1).
Gemäss Leitlinien sollte bei Patientinnen und Patienten im intermediären Risikospektrum eine «Rescue Lyse», chirurgische Embolektomie oder katheterbasierte Therapien in Erwägung gezogen werden, wenn es unter der oralen Antikoagulation zu einer hämodynamischen Verschlechterung kommt (Klasse IIa, Evidenzlevel C). Bei Hochrisiko-Patientinnen und -Patienten, bei denen eine systemische Thrombolyse entweder erfolglos war oder kontraindiziert ist, wurde ebenfalls eine Empfehlung für katheterbasierte Therapien ausgesprochen (Klasse IIa, Evidenzlevel C) (1).
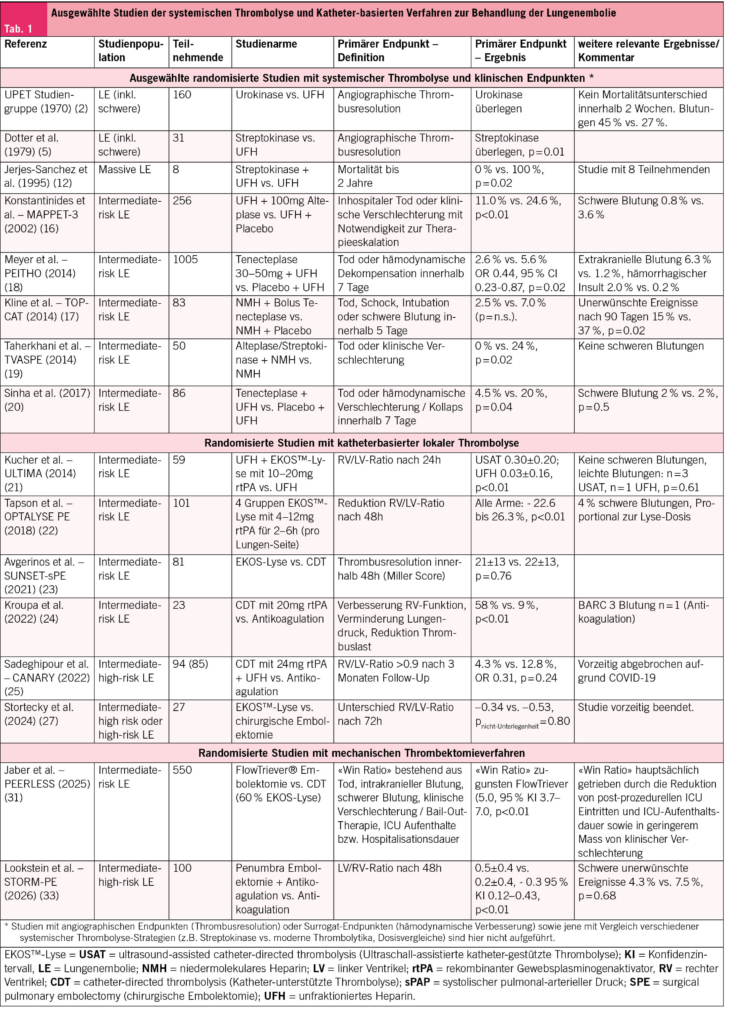
Das Evidenzlevel C (Expertenmeinung, nicht-randomisierte Studien) für katheterbasierte Therapien spiegelt die im Jahr 2019 noch begrenzte Datenlage für interventionelle Therapiealternativen wider. Seitdem hat sich dieses Feld jedoch rasant weiterentwickelt. Eine Zusammenfassung der randomisierten Studienevidenz, insbesondere der neuesten Erkenntnisse zu katheterbasierten Therapien, ist in Tab. 1 zu finden. Im Folgenden möchten wir einen konzisen Überblick über die konservative und interventionelle Behandlung von Lungenembolien im intermediären bis hohen Risikospektrum bieten.
Die systemische Thrombolyse
Die Evidenz zur systemischen Lyse stammt überwiegend aus Studien der 1970er bis 1990er Jahre (2–14). Studien, die zu einer Klasse-I-Empfehlung für die systemische Thrombolyse führen, umfassen insgesamt bis dato etwa 219 Patientinnen und Patienten und zeigten eine Mortalitätsreduktion auf Kosten eines Anstiegs schwerer und intrazerebraler Blutungen (2, 5, 12, 15). Die Inzidenz schwerer Blutungen unter systemischer Thrombolyse liegt in der Grössenordnung von etwa 10 %, jene von intrazerebralen Blutungen bei rund 2 % (15).
Seit den 2000er Jahren liegt zunehmend auch Evidenz für das intermediäre Risikospektrum vor. In diesem Bereich scheint die systemische Thrombolyse jedoch nicht mit einem Überlebensvorteil verbunden zu sein (15–20). Die qualitativ hochwertigste Studie – PEITHO – randomisierte 1005 Teilnehmende mit intermediär-hohem Sterblichkeitsrisiko zu einer Behandlung mit Körpergewichts-adaptiertem Tenecteplase (30–50mg) oder Placebo. Der primäre Endpunkt, bestehend aus Tod oder hämodynamischer Dekompensation innerhalb von 7 Tagen, trat in 2.6 % der Probanden der Thrombolysegruppe und in 5.6 % der Placebogruppe auf (OR 0.4; 95 % KI 0.2–0.9; p = 0.02). Dies war hauptsächlich auf eine Reduktion des Risikos für eine hämodynamische Verschlechterung (1.6 % vs. 5.0 %) zurückzuführen, während es keinen Unterschied in der Mortalität gab. Demgegenüber stand ein Anstieg schwerer Blutungen gemäss der Definition der International Society on Thrombosis and Haemostasis (ISTH) mit 11.5 % vs. 2.4 % (OR 5.6; 95 % KI 2.3–13.4, p < 0.01). Die Inzidenz von hämorrhagischen Insulten lag bei 2.0 % vs. 0.2 % (18). Die systemische Thrombolyse ist daher bei initial intermediärem Risiko nur im Falle einer hämodynamischen Verschlechterung, also einer Transition zu hohem Sterblichkeitsrisiko, empfohlen (1).
Katheterbasierte Behandlungen
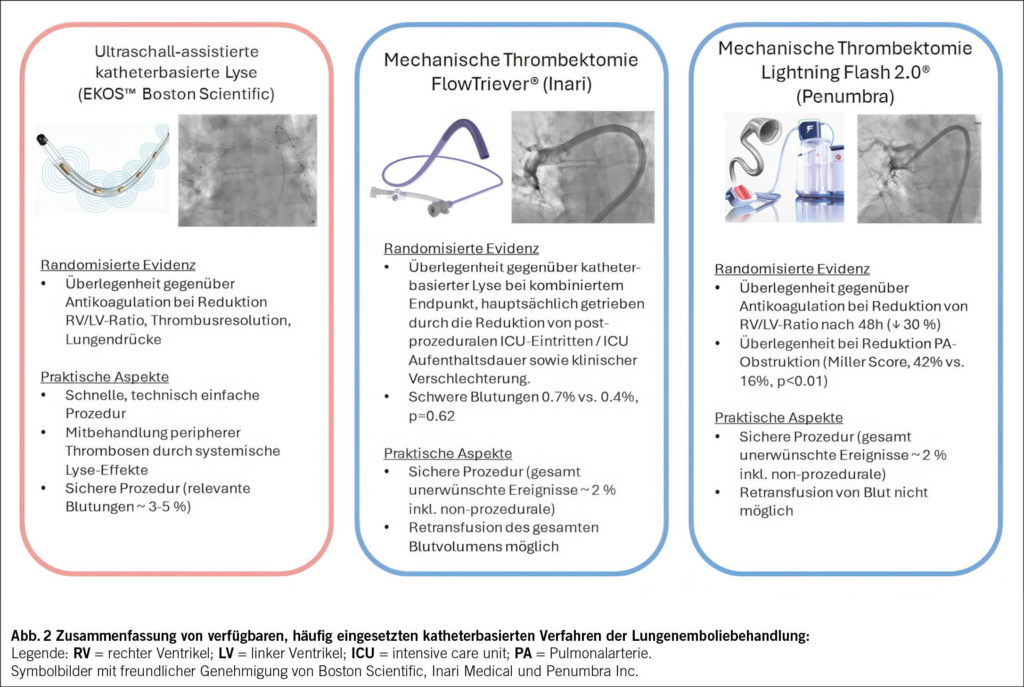
Ergebnisse ausgewählter randomisierter Studien sind in Tab. 1 zusammengefasst. Nachfolgend möchten wir die in der Schweiz hauptsächlich verfügbaren Verfahren zusammenfassen (Abb. 2).
Lokale katheterbasierte Thrombolyse
Der Grossteil der randomisierten Evidenz zur lokalen Thrombolyse (entweder durch die lokale Applikation von Fibrinolytika über einen Standardkatheter in der Pulmonalarterie oder durch ultraschall-assistierte lokale Thrombolyse, USAT, auch als «EKOS™-Lyse» bekannt) wurde bei Patienten im intermediären Risikospektrum erhoben. Die primären Endpunkte dieser Studien waren jeweils Surrogatmarker der Thrombusauflösung (z. B. Miller Score im CT) sowie die Verbesserung der rechtsventrikulären Funktion (z. B. RV/LV – Verhältnis oder Lungendrücke) (21–25).
Das Ziel der lokalen Thrombolyse im Vergleich zur reinen Antikoagulation ist, eine schnellere Reduktion der Rechtsherzbelastung und damit eine potenzielle Minderung des «post pulmonary embolism impairment» zu bewirken, eine schnellere Genesung zu fördern und letztlich zu kürzeren Hospitalisationsdauern zu führen, ohne das erhöhte Blutungsrisiko einer hochdosierten systemischen Thrombolyse in Kauf nehmen zu müssen. So werden Fibrinolytika (rtPA, rekombinant tissue plasminogen activator) über 6–24 Stunden in Gesamtdosen verabreicht, die meist weniger als einem Fünftel der systemischen Dosis betragen (21, 22, 26, 27).
Im Berner ERASE-PE Register wurden 315 Patientinnen und Patienten, welche eine USAT erhalten haben (darunter 18 % Hochrisiko-Patienten), systematisch nachverfolgt. Die Gesamtdosis der Alteplase betrug im Mittel 20 ± 7 mg, die durchschnittliche Verabreichungsdauer lag bei 14 ± 2 Stunden. Bis zum Spitalsaustritt, der im Durchschnitt nur 3 Tage nach dem Eingriff erfolgte, konnte die RV/LV-Ratio um fast 30 % reduziert und der mittlere Pulmonalisdruck von 31 auf 23 mmHg gesenkt werden. Schwere Blutungen gemäss Bleeding Academic Research Consortium (BARC 3) wurden in 5 % beobachtet, tödliche Blutungen traten jedoch nicht auf. Drei Patienten ( < 1 %) erlitten eine intrazerebrale Blutung – etwa halb so viele, wie bei einer systemischen Thrombolyse zu erwarten wären (28).
Katheterbasierte mechanische Thrombektomieverfahren
Thrombolysefreie katheterbasierte Techniken ermöglichen eine unmittelbare Wiederherstellung der pulmonalen Perfusion, ohne Patientinnen und Patienten dem Blutungsrisiko einer systemischen Thrombolyse auszusetzen, oder einen grossen herzchirurgischen Eingriff mit Sternotomie und Herz-Lungen-Maschine zu erfordern. Die katheterbasierte Embolektomie ist insbesondere attraktiv bei Lyse-Kontraindikationen (z. B. post-operative Lungenembolien), bei hohem Blutungsrisiko oder bei Sorge vor intrazerebralen Blutungen, etwa nach Synkope mit Kopfanprall.
In der Schweiz kommen bei der akuten Lungenembolie hauptsächlich zwei Systeme zum Einsatz: Die grosslumige mechanische Embolektomie mittels FlowTriever® (Stryker vormals Inari Medical, «large-bore mechanical thrombectomy», LBMT) sowie die Thrombektomie mit dem Penumbra System (Penumbra Inc., «computer-assisted vacuum thrombectomy», CAVT). FlowTriever® erfordert einen 24-French (0.8 cm) grossen venösen Gefässzugang; mit einer 60 ml Spritze wird manuell ein Vakuum erzeugt, um den Embolus zu aspirieren. Ein wesentlicher Vorteil dieses Verfahrens ist die Möglichkeit der Retransfusion des aspirierten Blutvolumens über ein dediziertes Filtersystem (FlowSaver®). Das Penumbra System ist etwas kleinlumiger (frühere Generation 12 French = 0.4 cm, aktuelle Iteration 16 French = 0.5 cm). Mithilfe eines Computeralgorithmus wird zwischen Thrombus und Blut unterschieden, um den Blutverlust zu minimieren, da hier keine Retransfusion möglich ist. Neben Registerdaten liefern die kürzlich publizierten randomisierten Studien PEERLESS und STORM-PE wichtige Erkenntnisse zur Effektivität und Sicherheit dieser Systeme (29–33).
In PEERLESS wurde die FlowTriever®-Embolektomie mit einer katheterbasierten Thrombolyse (davon 60 % USAT) bei 550 Lungenemboliepatienten mit intermediärem Risiko verglichen. Der kombinierte sequentielle «win ratio» Endpunkt, bestehend aus Tod, intrakranieller Blutung, schwerer Blutung, klinische Verschlechterung oder Bail-Out-Therapie sowie ICU-Aufenthalt und Hospitalisationsdauer, fiel zugunsten der FlowTriever® Embolektomie aus (win ratio 5.0, 95 % KI 3.7–7.0, p < 0.01). Der Vorteil war vor allem durch eine geringere Inzidenz klinischer Verschlechterungen oder Bail-Out-Therapien (1.8 % vs. 5.4 %), seltenere ICU-Aufnahmen (42 % vs. 65 %), sowie durch eine kürzere postprozedurale ICU-Verweildauer (14h vs. 39h) bedingt. Die Mortalität war zwischen den Gruppen vergleichbar (0.4 % vs. 0.8 %), ebenso die Häufigkeit Device- oder medikamentenassoziierter Nebenwirkungen (13 % vs. 12 %) (31).
In der STORM-PE Studie wurde die CAVT (Penumbra System) mit einer alleinigen Antikoagulation (unfraktioniertes oder niedermolekulares Heparin) verglichen. Die Studie ist besonders relevant, da im Kontrollarm der aktuell leitlinienempfohlene Therapiestandard für Lungenemboliepatienten mit intermediär-hohem Risiko, nämlich die reine Antikoagulation, angewandt wurde. Insgesamt wurden 100 Patienten randomisiert; primärer Endpunkt war die RV/LV-Ratio nach 48 Stunden. Die vor Therapiebeginn gemessene mittlere RV/LV-Ratio von 1.6 konnte im CAVT-Arm um 0.5 und im Antikoagulationsarm um 0.2 reduziert werden (mittlerer Unterschied zwischen den Gruppen 0.27, 95 % KI 0.12–0.43, p < 0.01). Der mittlere Pulmonalisdruck sank nach CAVT von durchschnittlich 31 mmHg auf 23 mmHg. Der mittlere Blutverlust betrug 300 ml. Schwere unerwünschte Ereignisse, einschliesslich klinischer Verschlechterung, LE-assoziierte Mortalität, rezidivierende LE und schwerer Blutung, traten mit 4.3 % versus 7.5 % in beiden Gruppen statistisch vergleichbar auf (p = 0.68) (33).
Zusammenfassung und Ausblick
Die hochqualitative, kürzlich veröffentlichte Evidenz, die in den 2019 verabschiedeten ESC-Leitlinien noch nicht abgebildet werden konnte, verleiht uns zunehmend Sicherheit in der Anwendung katheterbasierter Techniken und zeigt klinisch relevante Vorteile. Da das Sterblichkeitsrisiko bei Patientinnen und Patienten im intermediären Risikospektrum niedrig ist (ERASE-PE Register 1.6 % nach 30 Tagen, PEERLESS 0.5 %, STORM-PE 2 %), liegt das Hauptziel dieser Therapien in einer schnelleren Rekonvaleszenz und der Vermeidung einer hämodynamischen Verschlechterung. Der Nettobenefit dieser Eingriffe erscheint durch die niedrigen Komplikationsraten gerechtfertigt.
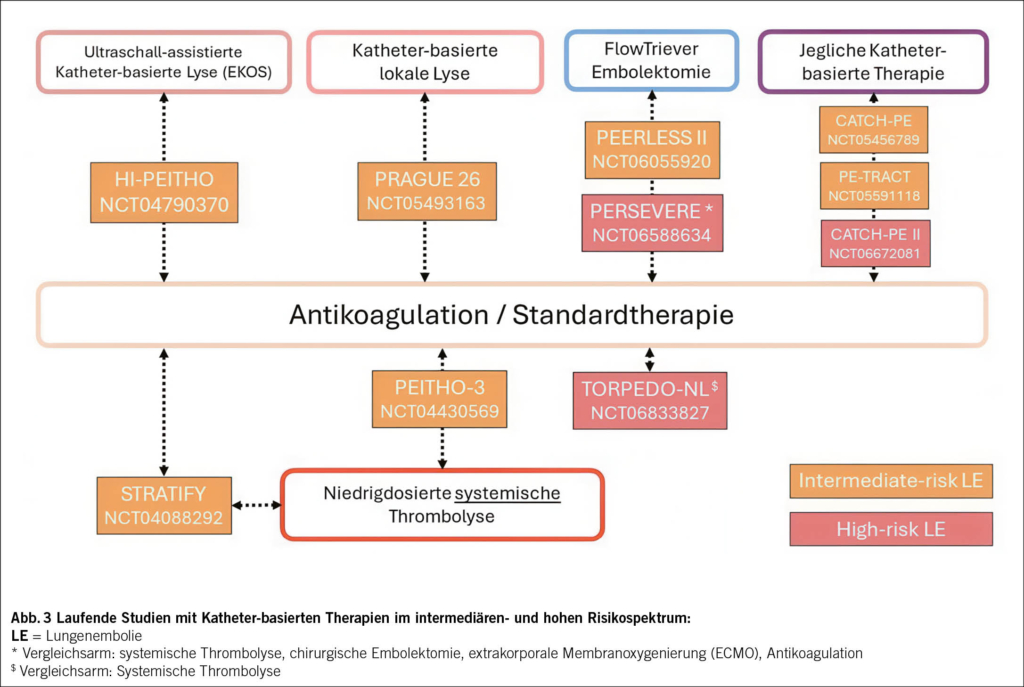
Die geplanten und laufenden gross angelegten randomisierten Studien zu katheterbasierten Therapien sowie zur niedrig-dosierten systemischen Lyse, die in Abb. 3 zusammengefasst sind, werden wesentliche Erkenntnisse liefern. Diese Studien werden insbesondere im Vergleich zu den derzeit in den Leitlinien empfohlenen Erstlinientherapien (Antikoagulation und systemische Thrombolyse) eine entscheidende Rolle spielen.
Copyright
Aerzteverlag medinfo AG
Inselspital, Universitätsspital Bern
Universitätsklinik für Kardiologie
Herz Gefäss Zentrum
Freiburgstrasse 20
3010 Bern
miklos.rohla@insel.ch
Universitätsklinik für Kardiologie
Inselspital
Freiburgstrasse 20
3010 Bern
Abteilung für Kardiologie, Bürgerspital Solothurn
Schöngrünstrasse 42
4500 Solothurn
stefan.stortecky@insel.ch
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Das Feld der katheterbasierten Therapien hat sich rasant entwickelt.
- Rezente Evidenz zur katheterbasierten lokalen Thrombolyse und perkutanen Embolektomie im intermediären Risikospektrum zeigt klinisch relevante Vorteile mit schnellerer Rekonvaleszenz gegenüber der Antikoagulation und geringen Komplikationsrisiken.
- Laufende grossangelegte Studien bei Patientinnen und Patienten mit hohem Sterblichkeitsrisiko werden Alternativen zur systemischen Thrombolyse aufzeigen.
1. Konstantinides SV, Meyer G, Becattini C, Bueno H, Geersing GJ, Harjola VP, et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020;41(4):543-603.
2. Urokinase pulmonary embolism trial. Phase 1 results: a cooperative study. JAMA. 1970;214(12):2163-72.
3. Tibbutt DA, Davies JA, Anderson JA, Fletcher EW, Hamill J, Holt JM, et al. Comparison by controlled clinical trial of streptokinase and heparin in treatment of life-threatening pulmonary embolism. Br Med J. 1974;1(5904):343-7.
4. Ly B, Arnesen H, Eie H, Hol R. A controlled clinical trial of streptokinase and heparin in the treatment of major pulmonary embolism. Acta Med Scand. 1978;203(6):465-70.
5. Dotter CT, Seaman AJ, Rösch J, Porter JM. Streptokinase and Heparin in the Treatment of Pulmonary Embolism: A Randomized Comparison. Vascular Surgery. 1979;13(1):42-52.
6. Tissue plasminogen activator for the treatment of acute pulmonary embolism. A collaborative study by the PIOPED Investigators. Chest. 1990;97(3):528-33.
7. Levine M, Hirsh J, Weitz J, Cruickshank M, Neemeh J, Turpie AG, et al. A randomized trial of a single bolus dosage regimen of recombinant tissue plasminogen activator in patients with acute pulmonary embolism. Chest. 1990;98(6):1473-9.
8. Dalla-Volta S, Palla A, Santolicandro A, Giuntini C, Pengo V, Visioli O, et al. PAIMS 2: alteplase combined with heparin versus heparin in the treatment of acute pulmonary embolism. Plasminogen activator Italian multicenter study 2. J Am Coll Cardiol. 1992;20(3):520-6.
9. Goldhaber SZ, Kessler CM, Heit JA, Elliott CG, Friedenberg WR, Heiselman DE, et al. Recombinant tissue-type plasminogen activator versus a novel dosing regimen of urokinase in acute pulmonary embolism: a randomized controlled multicenter trial. J Am Coll Cardiol. 1992;20(1):24-30.
10. Goldhaber SZ, Haire WD, Feldstein ML, Miller M, Toltzis R, Smith JL, et al. Alteplase versus heparin in acute pulmonary embolism: randomised trial assessing right-ventricular function and pulmonary perfusion. Lancet. 1993;341(8844):507-11.
11. Goldhaber SZ, Agnelli G, Levine MN. Reduced dose bolus alteplase vs conventional alteplase infusion for pulmonary embolism thrombolysis. An international multicenter randomized trial. The Bolus Alteplase Pulmonary Embolism Group. Chest. 1994;106(3):718-24.
12. Jerjes-Sanchez C, Ramirez-Rivera A, de Lourdes Garcia M, Arriaga-Nava R, Valencia S, Rosado-Buzzo A, et al. Streptokinase and Heparin versus Heparin Alone in Massive Pulmonary Embolism: A Randomized Controlled Trial. J Thromb Thrombolysis. 1995;2(3):227-9.
13. Meneveau N, Schiele F, Vuillemenot A, Valette B, Grollier G, Bernard Y, et al. Streptokinase vs alteplase in massive pulmonary embolism. A randomized trial assessing right heart haemodynamics and pulmonary vascular obstruction. Eur Heart J. 1997;18(7):1141-8.
14. Meneveau N, Schiele F, Metz D, Valette B, Attali P, Vuillemenot A, et al. Comparative efficacy of a two-hour regimen of streptokinase versus alteplase in acute massive pulmonary embolism: immediate clinical and hemodynamic outcome and one-year follow-up. J Am Coll Cardiol. 1998;31(5):1057-63.
15. Marti C, John G, Konstantinides S, Combescure C, Sanchez O, Lankeit M, et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J. 2015;36(10):605-14.
16. Konstantinides S, Geibel A, Heusel G, Heinrich F, Kasper W, Management S, et al. Heparin plus alteplase compared with heparin alone in patients with submassive pulmonary embolism. N Engl J Med. 2002;347(15):1143-50.
17. Kline JA, Nordenholz KE, Courtney DM, Kabrhel C, Jones AE, Rondina MT, et al. Treatment of submassive pulmonary embolism with tenecteplase or placebo: cardiopulmonary outcomes at 3 months: multicenter double-blind, placebo-controlled randomized trial. J Thromb Haemost. 2014;12(4):459-68.
18. Meyer G, Vicaut E, Danays T, Agnelli G, Becattini C, Beyer-Westendorf J, et al. Fibrinolysis for patients with intermediate-risk pulmonary embolism. N Engl J Med. 2014;370(15):1402-11.
19. Taherkhani M, Taherkhani A, Hashemi SR, Faghihi Langroodi T, Sadeghi R, Beyranvand M. Thrombolytic-plus-Anticoagulant Therapy versus Anticoagulant-Alone Therapy in Submassive Pulmonary Thromboembolism (TVASPE Study): A Randomized Clinical Trial. J Tehran Heart Cent. 2014;9(3):104-8.
20. Sinha SK, Sachan M, Goel A, Singh K, Mishra V, Jha MJ, et al. Efficacy and Safety of Thrombolytic Therapy in Acute Submassive Pulmonary Embolism: Follow-Up Study. J Clin Med Res. 2017;9(2):163-9.
21. Kucher N, Boekstegers P, Muller OJ, Kupatt C, Beyer-Westendorf J, Heitzer T, et al. Randomized, controlled trial of ultrasound-assisted catheter-directed thrombolysis for acute intermediate-risk pulmonary embolism. Circulation. 2014;129(4):479-86.
22. Tapson VF, Sterling K, Jones N, Elder M, Tripathy U, Brower J, et al. A Randomized Trial of the Optimum Duration of Acoustic Pulse Thrombolysis Procedure in Acute Intermediate-Risk Pulmonary Embolism: The OPTALYSE PE Trial. JACC Cardiovasc Interv. 2018;11(14):1401-10.
23. Avgerinos ED, Jaber W, Lacomis J, Markel K, McDaniel M, Rivera-Lebron BN, et al. Randomized Trial Comparing Standard Versus Ultrasound-Assisted Thrombolysis for Submassive Pulmonary Embolism: The SUNSET sPE Trial. JACC Cardiovasc Interv. 2021;14(12):1364-73.
24. Kroupa J, Buk M, Weichet J, Malikova H, Bartova L, Linkova H, et al. A pilot randomised trial of catheter-directed thrombolysis or standard anticoagulation for patients with intermediate-high risk acute pulmonary embolism. EuroIntervention. 2022;18(8):e639-e46.
25. Sadeghipour P, Jenab Y, Moosavi J, Hosseini K, Mohebbi B, Hosseinsabet A, et al. Catheter-Directed Thrombolysis vs Anticoagulation in Patients With Acute Intermediate-High-risk Pulmonary Embolism: The CANARY Randomized Clinical Trial. JAMA Cardiol. 2022;7(12):1189-97.
26. Valerio L, Mavromanoli AC, Barco S, Abele C, Becker D, Bruch L, et al. Chronic thromboembolic pulmonary hypertension and impairment after pulmonary embolism: the FOCUS study. Eur Heart J. 2022;43(36):3387-98.
27. Stortecky S, Barco S, Windecker S, Heg D, Kadner A, Englberger L, et al. Ultrasound-assisted catheter-directed thrombolysis versus surgical pulmonary embolectomy for intermediate-high or high-risk pulmonary embolism: a randomized phase II non-inferiority trial. Eur J Cardiothorac Surg. 2024;66(1).
28. Draxler DF, Johannes JK, Nakase M, Heg D, Dobner S, Turovskij E, et al. Clinical Outcomes in Patients With Acute Pulmonary Embolism Undergoing Ultrasound-Assisted Catheter-Directed Thrombolysis. J Am Heart Assoc. 2025;14(9):e035916.
29. Silver MJ, Gibson CM, Giri J, Khandhar S, Jaber W, Toma C, et al. Outcomes in High-Risk Pulmonary Embolism Patients Undergoing FlowTriever Mechanical Thrombectomy or Other Contemporary Therapies: Results From the FLAME Study. Circ Cardiovasc Interv. 2023;16(10):e013406.
30. Toma C, Jaber WA, Weinberg MD, Bunte MC, Khandhar S, Stegman B, et al. Acute outcomes for the full US cohort of the FLASH mechanical thrombectomy registry in pulmonary embolism. EuroIntervention. 2023;18(14):1201-12.
31. Jaber WA, Gonsalves CF, Stortecky S, Horr S, Pappas O, Gandhi RT, et al. Large-Bore Mechanical Thrombectomy Versus Catheter-Directed Thrombolysis in the Management of Intermediate-Risk Pulmonary Embolism: Primary Results of the PEERLESS Randomized Controlled Trial. Circulation. 2025;151(5):260-73.
32. Moriarty JM, Schiro BJ, Dohad SY, Tamaddon H, Davis HC, Shavelle DM, et al. Periprocedural Results and Right Ventricular Outcomes of Computer Assisted Vacuum Thrombectomy Treatment of Acute Pulmonary Embolism: Interim Analysis of 300 Patients From the STRIKE-PE Study. J Am Heart Assoc. 2025;14(17):e039975.
33. Lookstein RA, Konstantinides SV, Weinberg I, Dohad SY, Rosol Z, Kopec G, et al. Randomized Controlled Trial of Mechanical Thrombectomy With Anticoagulation Versus Anticoagulation Alone for Acute Intermediate-High Risk Pulmonary Embolism: Primary Outcomes From the STORM-PE Trial. Circulation. 2026;153(1):21-34.
info@herz+gefäss
- Vol. 16
- Ausgabe 2
- Mai 2026