- Ausgewählte Studien aus der Hämato-Onkologie
Universell basenbearbeitete CAR7-T-Zellen für die akute lymphoblastische T-Zell-Leukämie
Die CAR-T-Therapien haben sich etabliert: In Europa wurden bisher über 20 000 Patienten mit B-Zell-Tumoren und einige mit Autoimmunkrankheiten behandelt. Bei T-Zell-Tumoren besteht das Problem des Fratrizids (Brudermord), d. h., wenn sich die CAR-T-Zellen gegenseitig zerstören, nützt das nichts gegen den Tumor. Folgende Lösung wird hier präsentiert.
CD7 ist eine attraktive Zielstruktur, da sie auf allen T-Zell-Tumoren vorhanden ist (ausgenommen sind die kutanen T-Zell-Tumoren). Der grösste Bedarf besteht bei der rezidivierten/refraktären T-akuten lymphoblastären Leukämie. Über erste Patienten wurde mit triple-eliminierten CD7-spezifischen CAR-T-Zellen berichtet, d. h. ohne T-Zell-Rezeptor (um eine allogene Gabe ohne GvHD zu ermöglichen), ohne CD52 (um eine Lymphodepletion mit CAMPATH durchführen zu können) und ohne CD7 (um den Fratrizid zu umgehen).
Dies ist eine Phase-I-Studie, in der BE-CAR7-T-Zellen bei Kindern mit rezidivierter/refraktärer T-ALL nach Fludarabine und Cyclophosphamid sowie CAMPATH angewendet wurden. Erwachsene Patienten konnten auch in einem Erweiterungsprogramm behandelt werden. Im Anschluss an das Erreichen einer Remission war eine allogene Stammzelltransplantation geplant. Diese Therapie wurde bei neun Kindern und zwei Erwachsenen angewendet. Zirkulierende allogene CAR-T-Zellen konnten bei allen nachgewiesen werden. CRS und opportunistische Infektionen wurden beobachtet. Bei allen Patienten konnte eine komplette Remission beobachtet werden. Bei 82 % der Patienten wurde eine tiefe Remission beobachtet. Neun Patienten kamen zur Stammzelltransplantation, sieben Patienten (64 %) sind in anhaltender Remission. Bei zwei Patienten kam es zu einem Leukämie-Rezidiv mit CD7-Verlust.
Quelle
Robert Chiesa, Christos Georgiadis, Hebatalla Rashed,et al. Universal Base-Edited CAR7 T Cells for T-Cell Acute Lymphoblastic Leukemia. For the Base-Edited CAR T Group N Engl J Med 2026;394:152-165
Über den Hag geschaut
17 Patienten wurden mit einem CD7-CAR-T-Produkt behandelt, die mit einem CD7-Protein-Expressionsblocker behandelt waren, um den oben beschriebenen Fratrizid zu verhindern. Der Ursprung der CAR-T-Zellen war autolog und nicht allogen. 16 Patienten erreichten eine MRD-negative komplette Remission nach einem Monat. Nebenwirkungen waren CRS Grad I–II und Neurotoxizität bei einem Patienten. Elf Patienten sind rezidivfrei, neun von ihnen erhielten eine allogene Stammzelltransplantation zur Konsolidierung. Bei einzelnen Patienten konnten zirkulierende CAR-T-Zellen über einen Zeitraum von zwei Jahren nachgewiesen werden.
Quelle
Bernice L Z Oh, Noriko Shimasaki, Elaine Coustan-Smith et al Nat Med . 2024 Dec;30(12):3687-3696. Fratricide-resistant CD7-CAR T cells in T-ALL
Teclistamab plus Daratumumab bei rezidiviertem oder refraktärem multiplem Myelom
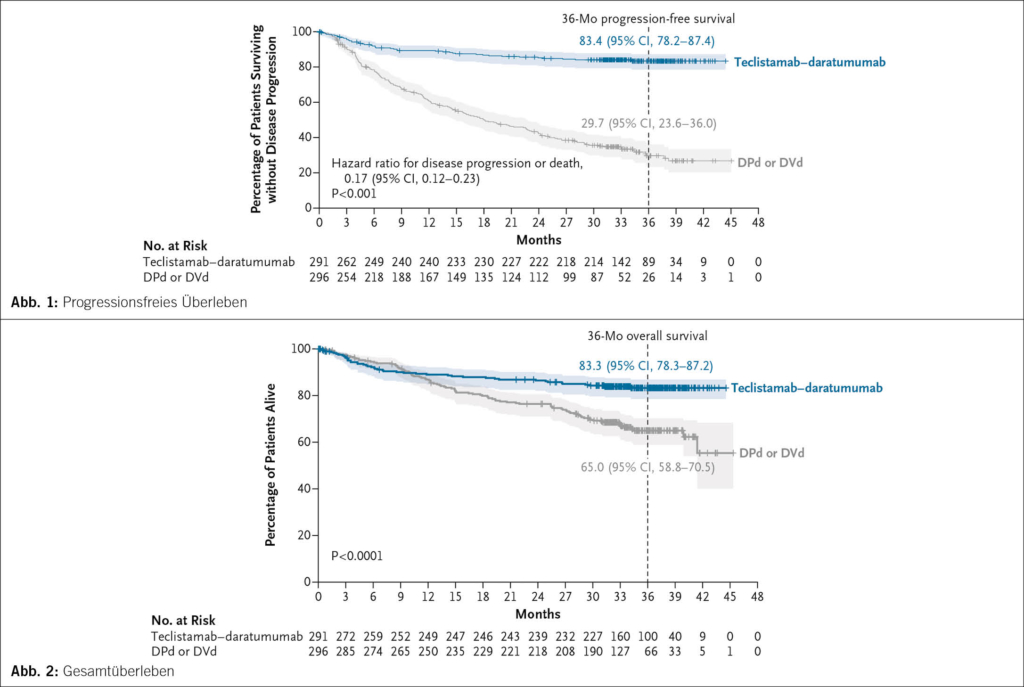
Teclistamab ist ein bispezifischer Antikörper (T-Zell-Stimulator); Daratumumab ein CD38 spezifischer Antikörper. In dieser Studie wurden Patienten mit refraktärem/rezidivierendem Plasmazellmyelom eingeschlossen, die meisten in der zweiten Therapielinie. Sie erhielten die Kombination aus Teclistamab und Daratumumab oder Daratumumab in Kombination mit Pomalidomid und Dexamethason bzw. Bortezomib und Dexamethason, also eine Standard-3er-Kombination. Die Patienten durften nicht Daratumumab-refraktär sein. 587 Patienten wurden randomisiert. 291 bzw. 296 Patienten wurden in die Gruppen Teclistamab-Daratumumab bzw. DPD oder DBD randomisiert. Die Kombination des BCMA-gerichteten bispezifischen Antikörpers war im progressionsfreien Überleben (Abb. 1) hochsignifikant überlegen: Nach 34.5 Monaten betrug die Hazard Ratio 0.17 (95 % CI 0.12–0.23; p < 0.001), das 3-Jahres-PFS betrug 83.4 % gegenüber 29.7 %. Die Rate an kompletter Remission war unter dem experimentellen Arm mit 81.8 % vs. 32.1 % höher und die Rate an MRD-Negativität entsprechend mit 58.4 % vs. 17.1 %. Alle Untergruppen profitierten.
Nebenwirkungen traten bei 70.7 % der Patienten auf, davon tödliche bei 7.1 %, wobei fast alle Todesfälle auf infektiöse Nebenwirkungen zurückzuführen waren. Das Gesamtüberleben war ebenfalls besser unter Teclistamab-Daratumumab (Abb. 2).
Quelle
Costa LJ, Bahlis NJ, Perrot et al. MajesTEC-3 Trial Investigators. N Engl J Med. 2025 Dec 9. doi: 10.1056/NEJMoa2514663. Online ahead of print.PMID: 41363801
Dual-Targeting des extramedullären Myeloms mit Talquetamab und Teclistamab
Unter den Patienten mit Plasmazellmyelom hat die extramedulläre Krankheit eine besonders schlechte Prognose. Diese meist spät im Krankheitsverlauf auftretenden Krankheiten sind besonders häufig therapierefraktär. Verschiedene Organsysteme können betroffen sein, ausserhalb des Skelettes und des Knochenmarks. Bispezifische Antikörper haben bei Patienten mit Plasmazellmyelom neue Therapieoptionen eröffnet und zur Zeit gibt es Teclistamab, einen BCMA (B-cell maturation antigen) spezifischen, sowie Talquetamab, einen GPRC5D (anti-G protein-coupled receptor family C group 5 member D) spezifischen bispezifischen Antikörper.
In dieser Studie wurde Talquetamab mit Teclistamab kombiniert. Besonders hervorzuheben ist die Tatsache, dass es sich um Patienten mit «wahrer» extramedullärer Krankheit handelt, d.h. ein mit dem Knochen per continuitatem gewachsener Herd gilt nicht als extramedullär. Zum Beispiel ist ein aus einer Rippe in die Pleura einwachsender Herd in dieser Definition nicht extramedullär.
In diese Phase-II-Studie wurden Patienten eingeschlossen, die nach einer Vorbehandlung mit CD38-Antikörpern sowie Imiden und Proteasom-Inhibitoren (triple class exposed) eine rezidivierte/refraktäre Krankheit hatten.
Insgesamt wurden 90 Patienten mit beiden bispezifischen Antikörpern behandelt. Das mediane Follow-up betrug 12.6 Monate. Ein Ansprechen wurde bei 79 % (95 % CI, 69–87 %) beobachtet. 64 % (95 % CI, 48–76 %) hatten ein Ansprechen von > 12 Monaten Dauer. Das Gesamtüberleben betrug 74 % (95 % CI, 63–83). Zu den Nebenwirkungen zählten Beschwerden des Mundes mit Geschmacksstörungen und Trockenheit (87 % der Patienten), CRS (Cytokine Release Syndrome) (78 %) und Hautnebenwirkungen (69 %). Grad-3/4-Nebenwirkungen, am häufigsten hämatologisch, wurden bei 76 % der Patienten beobachtet. Von den zehn verstorbenen Patienten war bei fünf eine Infektion die Ursache. Die Autoren schliessen, dass das Ansprechen bei therapierefraktärer extramedullärer Krankheit hoch ist, die Verträglichkeit jedoch problematisch ist. Insbesondere die Infektprophylaxe ist zu verbessern (das Gleiche gilt für die nachfolgend besprochene Studie).
Quelle
Shaji Kumar, María-Victoria Mateos, Jing Christine Ye, et al. Dual Targeting of Extramedullary Myeloma with Talquetamab and Teclistamab. N Engl J Med 2026;394:51-61. DOI: 10.1056/NEJMoa2514752
CD19-CAR-T-Zelltherapie bei autoimmuner hämolytischer Anämie
Die autoimmunhämolytische Anämie (AIHA) ist eine typische, meist gutartig verlaufende Autoimmunerkrankung, welche aber in seltenen Fällen schwer und therapierefraktär verlaufen kann. Patienten mit mehr als drei Therapielinien gelten als multi-refraktär. CD19-spezifische autologe CAR-T-Zellen werden derzeit bei verschiedenen Autoimmunerkrankungen getestet. Darüber wurde in früheren Ausgaben berichtet.
In diese Phase-I-Studie wurden 11 Patienten eingeschlossen (6 in die Phase I, 5 als Compassionate Use). Sie erhielten autologe, CD19-spezifische CAR-T-Zellen. Die lymphodepletierende Therapie erfolgte mit Fludarabine und Cyclophosphamid. Das mediane Follow-up beträgt 12 Monate. Alle Patienten sprachen auf die Therapie an, die Hämolyse sistierte und das Hämoglobin wurde korrigiert. Die mediane behandlungsfreie Remissionsdauer betrug 11.5 Monate. CRS (Cytokine Release Syndrome) Grad I–II wurde bei neun Patienten beobachtet, Neurotoxizität Grad I bei einem Patienten.
Quelle
CD19 CAR T-Cell Therapy for Autoimmune Hemolytic Anemia Ruonan Li, Hong Pan, Lele Zhang et al. N Engl J Med 2026;394:253-267
Klinik für Hämatologie
Hämatologische Diagnostik Labormedizin
Universitätsspital Basel und Blutspendezentrum beider Basel SRK
Petersgraben 4
4031 Basel
jakob.passweg@usb.ch