- Der Spitz-Nävus ist kein Melanom im Kindesalter
Der klassische Spitz-Nävus ist im Kindesalter eine gutartige, biologisch stabile melanozytäre Läsion und weder mit einem Melanom noch mit einer Vorstufe davon gleichzusetzen. Spitzoide Tumoren insgesamt bilden eine heterogene Gruppe melanozytärer Neoplasien mit variabler Biologie, die neben benignen Nävi auch intermediäre Läsionen mit unsicherem biologischem Verhalten sowie seltene maligne Spitz Melanome umfasst. Die differenzierte Einordnung stützt sich auf eine integrative Bewertung klinischer, histologischer und immunhistochemischer Befunde, ergänzt durch molekulargenetische Analysen in ausgewählten Fällen. Die altersabhängige Risikobewertung, das Wachstumsverhalten, die architektonische Symmetrie sowie Reifungs- und Proliferationsmarker sind zentrale Entscheidungsfaktoren. Ziel ist nicht die begriffliche Klassifikation, sondern die möglichst präzise Einschätzung des biologischen Potenzials. Dieses diagnostische Vorgehen ermöglicht es, unnötige Eingriffe bei stabilen Läsionen zu vermeiden und zugleich seltene progressive Verläufe frühzeitig zu erkennen. Eine strukturierte, altersgerechte und interdisziplinär abgestimmte Diagnostik bildet die Grundlage für eine differenzierte, klinisch verantwortungsvolle Entscheidungsfindung.
The classic Spitz nevus is a benign, biologically stable melanocytic lesion in children and should not be equated with melanoma or its precursors. In contrast, Spitz tumors as a group represent a heterogeneous spectrum of melanocytic neoplasms, ranging from benign nevi to intermediate lesions with uncertain biological behavior and, rarely, malignant Spitz melanomas. Accurate classification relies on an integrative assessment of clinical, histological, and immunohistochemical features, complemented by molecular analyses in selected cases. Age-related risk stratification, growth behavior, architectural symmetry, and markers of maturation and proliferation are key determinants. The primary objective is not semantic categorization but rather a precise estimation of biological potential. This diagnostic approach helps to avoid overtreatment of stable lesions while enabling early detection of rare progressive cases. A structured, age-appropriate, and interdisciplinary diagnostic strategy is essential for informed and responsible clinical decision-making.
Keywords: Spitz nevus, spitzoid tumors, melanoma, pediatric skin tumors
Einleitung
Spitz-Tumoren stellen eine eigenständige, heterogene Gruppe melanozytärer Neoplasien dar, die ein breites Spektrum biologischer Verhaltensweisen aufweisen können (1). Innerhalb dieses Spektrums werden drei Hauptgruppen unterschieden: der klassische Spitz-Nävus, der atypische Spitz-Tumor (auch Spitz-Melanozytom genannt) und das Spitz-Melanom (2). Der klassische Spitz- Nävus manifestiert sich überwiegend im Kindes- und Jugendalter und zeigt typischerweise ein rasches, lokalisiertes Wachstum (3). Weniger als 1 % aller im Kindesalter exzidierten melanozytären Läsionen entfallen auf Spitz- Tumoren (4). Die Prädilektionsstellen sind der Kopfbereich sowie die Extremitäten (5). Etwa 70 % aller Spitz-Tumoren werden in den ersten beiden Lebensdekaden diagnostiziert, ein erstmaliges Auftreten im Erwachsenenalter ist jedoch ebenfalls möglich (3). Klinisch präsentiert sich der klassische Spitz-Nävus in der Regel als symmetrische, kuppelförmige oder flache Hautläsion mit klarer Begrenzung, die eine rötliche, rosafarbene oder bräunliche Pigmentierung aufweisen kann (6). In einzelnen Fällen können jedoch auch atypische Merkmale auftreten, etwa asymmetrische Strukturen, inhomogene Pigmentierung oder eine rasche Grössenzunahme, wodurch ein klinisches Bild entstehen kann, das einem kutanen Melanom ähnelt (6). In der überwiegenden Mehrzahl der Fälle erlaubt die histopathologische Analyse jedoch die beruhigende Diagnose eines benignen Spitz-Nävus. Entscheidend bleibt, dass der klassische Spitz-Nävus biologisch stabil bleibt und keinen malignen Verlauf nimmt (7).
Während klassische melanozytäre Läsionen meist klinisch und histopathologisch eindeutig als benigne eingestuft werden können, umfasst das Spektrum der Spitz-Tumoren neben klar benignen Nävi und sehr seltenen malignen Spitz-Melanomen auch intermediäre Formen mit uneindeutigen Eigenschaften, wobei klinisch meist ein gutartiger Verlauf beobachtet wird (6). Atypische Spitz-Tumoren weisen histopathologische Auffälligkeiten wie asymmetrisches Wachstum, Reifungsverlust, ausgeprägte zytologische Atypien und eine erhöhte mitotische Aktivität auf (6). Sie können in lokoregionäre Lymphknoten metastasieren, ohne dass dies die Prognose wesentlich beeinflusst, und eine hämatogene Metastasierung wird bei diesen Tumoren in der Regel nicht beobachtet (8). Eine Sentinel-Lymphknotenbiopsie ergibt daher bei atypischen Spitz-Tumoren keine prognostisch relevante Information (8). Spitz-Melanome hingegen weisen ein deutlich erhöhtes Risiko für extranodale und hämatogene Metastasierung auf und sind mit einem potenziell letalen Verlauf assoziiert (9).
Die historische Grundlage für das Verständnis dieser Tumorgruppe legte Sophie Spitz im Jahr 1948 mit ihrer Publikation «Melanomas of Childhood», in der sie 13 kindliche Hautläsionen beschrieb (10). Obwohl diese Läsionen histologisch Merkmale eines Melanoms aufwiesen, verliefen die meisten klinisch indolent. Nur ein Patient entwickelte eine fernmetastasierende Erkrankung, was zur Hypothese führte, dass altersabhängige Faktoren das biologische Verhalten dieser Tumoren günstig beeinflussen könnten (10). In späteren Jahren wurde erkannt, dass die meisten dieser Läsionen keine klassischen kutanen Melanome darstellen, sondern eine eigenständige Gruppe überwiegend benigner melanozytärer Tumoren (11). Dies führte Ende der 1960er-Jahre zur Einführung des Begriffs Spitz-Nävus, um gutartige Spitz-Läsionen klar von echten Melanomen abzugrenzen (11). Über mehrere Jahrzehnte galt dieser Tumor als vollständig benigne, und vereinzelte Fälle mit metastasierendem Verlauf wurden retrospektiv als fehldiagnostizierte Melanome mit Spitz-ähnlicher Morphologie interpretiert (12). Mit zunehmender Erfahrung zeigte sich jedoch, dass innerhalb dieses Spektrums auch atypische Spitz-Tumoren mit intermediärem Verhalten sowie Spitz-Melanome mit eindeutig malignem Potenzial existieren. Die differenzierte Betrachtung von Spitz-Tumoren ist nicht nur für die histopathologische Klassifikation, sondern auch für die therapeutische Strategie und die Einschätzung der Prognose von wesentlicher Bedeutung, insbesondere da viele betroffene Patientinnen und Patienten sehr jung sind (3). Trotz aller Fortschritte in der histopathologischen, immunhistochemischen und molekulargenetischen Diagnostik existieren bis heute keine verlässlichen Kriterien, die eine sichere Unterscheidung zwischen benignen und malignen Spitz-Tumoren in jedem Einzelfall ermöglichen würden (13, 14). Der einzige definitive Beweis für das Vorliegen eines malignen Spitz- Tumors bleibt das Auftreten von Fernmetastasen oder ein letaler Verlauf (15). Trotz der beschriebenen diagnostischen Herausforderungen ist hervorzuheben, dass sowohl klassische Spitz-Nävi als auch atypische Spitz-Tumoren in der überwiegenden Mehrzahl der Fälle eine exzellente Prognose aufweisen (8, 16). Fernmetastasen oder ein letaler Verlauf stellen eine Seltenheit dar (16). Insgesamt erlaubt das biologische Verhalten dieser Läsionen eine ausgesprochen günstige Einschätzung für die betroffenen Patienten und Patientinnen (17). Eine integrative diagnostische Abklärung ist daher insbesondere bei unklaren Befunden essenziell. Ziel bleibt es, unnötige Übertherapien zu vermeiden und gleichzeitig eine frühzeitige Erkennung seltener, potenziell progressiver Spitz-Tumoren zu ermöglichen.
Spitz-Tumoren: Definition und Abgrenzung gegenüber spitzoiden melanozytären Läsionen
Nicht jede melanozytäre Läsion mit Zügen einer histopathologischen spitzoiden Morphologie gehört zur Gruppe der echten Spitz-Tumoren. Nach der aktuellen WHO-Klassifikation wird ein Spitz-Tumor sowohl durch eine charakteristische spitzoide Histomorphologie als auch durch spezifische genetische Alterationen definiert (2). Histologisch zeichnen sich Spitz-Tumoren durch das Vorherrschen von spindelzelligen und/oder epitheloidzelligen Komponenten aus (1). Auf genetischer Ebene finden sich typischerweise translokationsinduzierte Fusionen, die Gene für Rezeptor-Tyrosinkinasen wie ALK, ROS1, NTRK1–3, RET oder MET betreffen können, oder sehr selten aktivierende Punktmutationen in HRAS (18–21). Diese genetischen Veränderungen stellen die primären Treiber der Tumorentstehung dar und sind somit für das initiale Wachstum und die morphologische Ausprägung der Läsion verantwortlich.
Es existieren jedoch auch konventionelle Nävi oder Melanome, die Züge einer spitzoiden Morphologie aufweisen können, deren genetisches Profil jedoch typische Treibermutationen wie BRAFV600E-, NRAS- oder inaktivierende Punktmutationen in NF1 zeigt (21–23). Solche Läsionen sind formal nicht Teil der Spitz-Tumoren-Familie, obwohl sie histologisch spitzoide Merkmale imitieren können. Dieses Verständnis ist zentral für die korrekte Einordnung spitzoider Läsionen. Da die spitzoide Morphologie allein keine zuverlässige Aussage über die biologische Natur einer melanozytären Läsion erlaubt, ist eine integrative Bewertung von klinischen, dermatoskopischen, histologischen und in ausgewählten Fällen teils molekulargenetischen Befunden essenziell. Nur durch diese gesamtheitliche Betrachtung kann eine präzise diagnostische Einordnung erfolgen, mit unmittelbaren Konsequenzen für Prognose und therapeutisches Vorgehen. Abb. 1 zeigt die molekulare Einteilung melanozytärer Tumoren basierend auf den genetischen Alterationen, die jeweils als Treiber der Tumorentstehung gelten.
Klinische Erscheinungsbilder und diagnostische Herausforderung
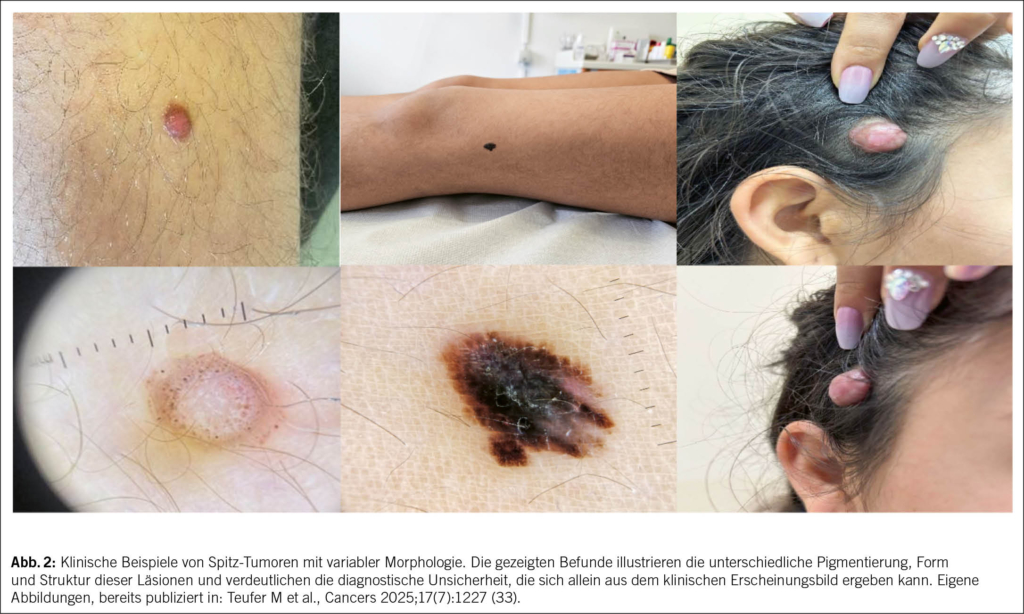
Der klassische Spitz-Nävus kann ein charakteristisches klinisches und dermatoskopisches Erscheinungsbild aufweisen, das die Diagnosestellung in vielen Fällen erleichtert. Typischerweise zeigen diese Läsionen entweder ein sogenanntes Sternmuster (starburst pattern) mit zentraler homogener Pigmentierung und symmetrisch angeordneten, radial ausstrahlenden Pseudopodien, regelmässig verteilte punktförmige Gefässe bei nicht pigmentierten Varianten oder ein globuläres Muster mit begleitender retikulärer Depigmentierung (24). Allen diesen klassischen Mustern ist eine ausgeprägte Symmetrie der Farb- und Strukturverteilung gemeinsam. Diese Symmetrie gilt als diagnostisches Kennzeichen gutartiger Spitz-Nävi und erleichtert die Abgrenzung gegenüber malignen Läsionen (24). Sie allein bietet jedoch keine absolute Sicherheit, da insbesondere das Alter eine entscheidende Rolle für die diagnostische Einordnung spielt (13). Während Spitz-Läsionen mit symmetrischem Erscheinungsbild im Kindes- und Jugendalter überwiegend benigne verlaufen, steigt das Risiko einer malignen Entartung mit zunehmendem Alter deutlich an (25). So liegt bei Patientinnen und Patienten unter 30 Jahren die Wahrscheinlichkeit, dass eine symmetrisch erscheinende Spitz-Läsion ein Melanom darstellt, bei etwa 7 %, während sie bei über 50-Jährigen auf etwa 50 % ansteigt (25). Abb. 2 zeigt drei unterschiedlich erscheinende Spitz-Tumoren aus der klinischen Praxis.
Ein weiteres klinisch relevantes Merkmal ist das Wachstumsverhalten der Läsion. Klassische Spitz-Nävi zeigen typischerweise eine kurze Phase rascher Grössenzunahme, die sich über Wochen bis wenige Monate erstreckt, gefolgt von einer Phase der Stabilität oder sogar partieller Regression (26). Zeichen einer beginnenden Regression wie zentrale Aufhellung oder Depigmentierung können klinisch erkennbar sein. Im Gegensatz dazu wächst ein Spitz-Melanom meist kontinuierlich weiter, ohne Anzeichen einer spontanen Stabilisierung. Diese unterschiedliche Dynamik liefert zusätzliche Hinweise auf das biologische Verhalten und sollte bei der Beurteilung mitberücksichtigt werden (24). Besonders anspruchsvoll gestaltet sich die klinische Einschätzung, wenn das architektonische Muster der Läsion untypisch ist. Spitz-Tumoren können ein breites Spektrum an Erscheinungsformen zeigen, das von symmetrischen, regelmässigen Befunden bis hin zu stark melanomverdächtigen Konstellationen reicht (27). In einzelnen Fällen ist die klinische Präsentation nicht von einem malignen Melanom zu unterscheiden, obwohl es sich histologisch um eine benigne Veränderung handelt. Umgekehrt kann eine unauffällige Läsion in der Histologie Kriterien eines malignen Tumors erfüllen (28). Solche Diskrepanzen unterstreichen die begrenzte Aussagekraft klinischer und dermatoskopischer Merkmale bei atypischer Präsentation. Die histopathologische Untersuchung ist in diesen Fällen zwingend erforderlich, um eine sichere diagnostische Einordnung zu ermöglichen.
Rolle der Histopathologie und Molekularbiologie
Die histopathologische Beurteilung ist der zentrale diagnostische Ansatz zur Einschätzung des biologischen Verhaltens von Spitz-Tumoren. Bei klassischen Spitz-Nävi genügt in der Regel die Beurteilung histologischer und immunhistochemischer Merkmale, um eine gutartige Diagnose zuverlässig zu stellen. Typisch sind eine ausgeprägte Symmetrie, eine gewisse Reifung der Melanozyten und eine geringe mitotische Aktivität (6, 13, 29). Ergänzend liefern immunhistochemische Marker wie p16, Ki-67 und HMB45 Hinweise auf Seneszenz, Proliferation und Differenzierung (30, 31). Auch bei vielen atypischen Läsionen, die histopathologisch vom klassischen Bild eines Spitz-Nävus abweichen, kann ein Melanom ausgeschlossen werden, sofern zentrale Merkmale einer malignen Entartung fehlen. Dazu zählen eine geringe mitotische Aktivität in der Tiefe, eine regelhafte Reifung der Melanozyten und das Fehlen signifikanter zytologischer Atypien (32). In einzelnen Fällen mit auffälliger Zellmorphologie, asymmetrischer Architektur oder tief reichender Proliferation ist ein sicherer Ausschluss jedoch nicht möglich, sodass eine weiterführende diagnostische Abklärung erforderlich werden kann (32). In solchen Fällen kann eine molekulargenetische Analyse mittels Next-Generation-Sequencing zur erweiterten diagnostischen Einschätzung beitragen (17). Ziel ist eine möglichst fundierte Einschätzung, ob zentrale Kontrollmechanismen wie Zellzykluskontrolle, Apoptose oder Seneszenz gestört sind, wie es auch bei Melanomen vorkommt und Rückschlüsse auf die biologische Stabilität und das Progressionsrisiko ermöglicht (33). Spitz-Tumoren mit intermediärem biologischem Potenzial zeigen in der Regel nur einzelne genetische Veränderungen in isolierten Signalwegen (13). Meist handelt es sich um kleine heterozygote Deletionen oder vereinzelte Punktmutationen in Genen, die an der Zellzykluskontrolle, Apoptose oder Seneszenz beteiligt sind (beispielsweise CDKN2A, TERT-p, TP53, PTEN oder ARID2) (33). Solche Veränderungen lassen zwar auf eine gewisse genetische Instabilität schliessen, weisen jedoch in ihrer isolierten Form nicht auf eine umfassende Störung der zellulären Regulation hin (13). Demgegenüber finden sich bei Spitz-Melanomen häufig komplexere molekulare Veränderungen, bei denen mehrere zentrale Kontrollmechanismen gleichzeitig betroffen sind. Diese gehäufte Beeinträchtigung regulatorischer Signalwege deutet auf eine erhöhte biologische Aggressivität hin (9, 13). Ergänzend bietet die Analyse der Tumormutationslast und von Kopienzahlveränderungen zusätzliche Hinweise auf das Ausmass genomischer Veränderungen, wobei höhere Werte typischerweise mit einem gesteigerten Malignitätsrisiko einhergehen (34–36). Insgesamt ergänzt die molekulargenetische Diagnostik die histopathologische und immunhistochemische Beurteilung in ausgewählten Fällen mit intermediärem Profil oder unklarer Biologie. Sie liefert zusätzliche Informationen zur Einschätzung des Progressionspotenzials und unterstützt die therapeutische Entscheidungsfindung.
Diagnostisches Vorgehen und Managementempfehlungen
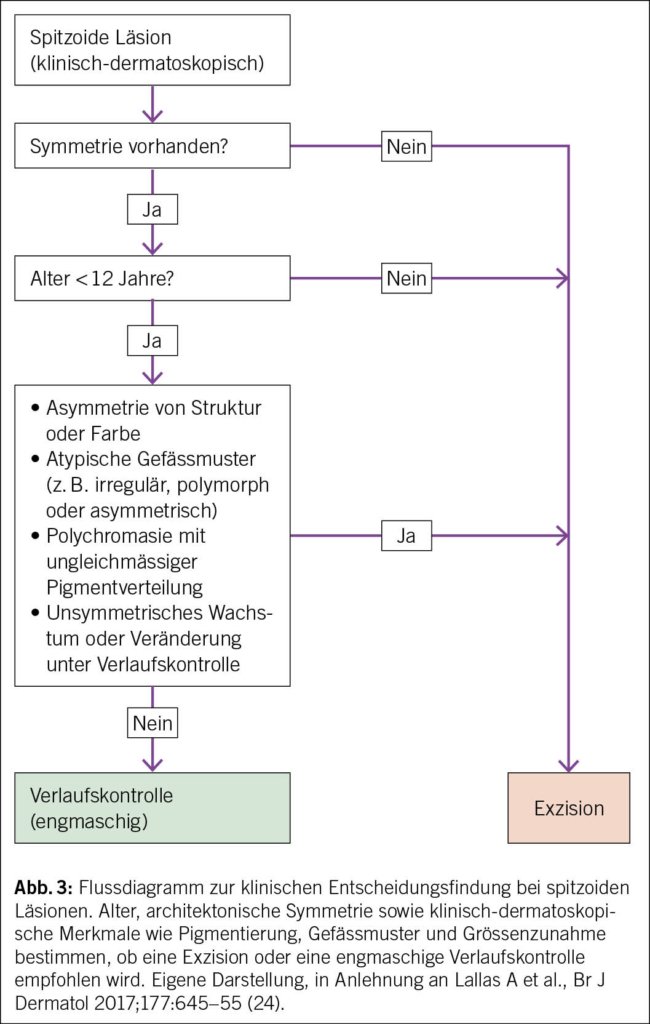
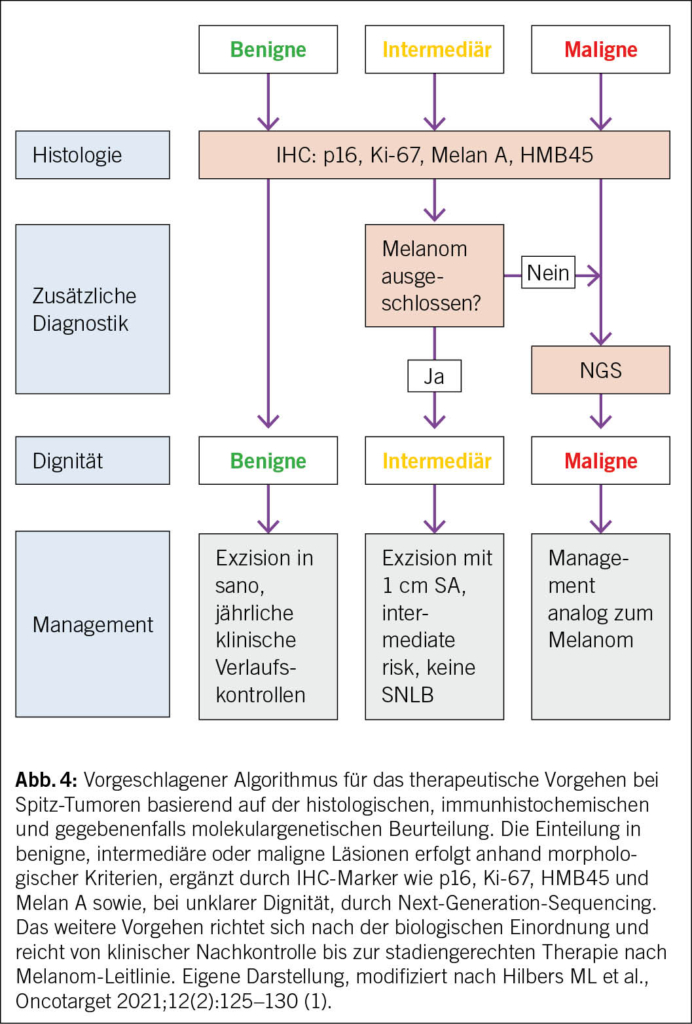
Das diagnostische und therapeutische Vorgehen bei Spitz-Tumoren richtet sich nach dem Alter der Patientin oder des Patienten, der klinischen Präsentation sowie den histologischen, immunhistochemischen und gegebenenfalls molekulargenetischen Befunden. Abb. 3 und Abb. 4 geben einen Überblick über das diagnostische Vorgehen sowie das daraus abgeleitete Management bei Spitz-Tumoren. Zu den zentralen klinischen Kriterien zählen die architektonische Symmetrie, das Alter sowie das Verlaufsmuster der Läsion. Während spitzoide Läsionen im Erwachsenenalter grundsätzlich vollständig entfernt werden sollten, kann bei Kindern unter zwölf Jahren mit kleinen symmetrischen Läsionen und homogener Pigmentierung zunächst eine engmaschige Beobachtung erfolgen (24, 25). Eine rasche Grössenzunahme ist in dieser Altersgruppe häufig und per se nicht verdächtig (3). Entscheidend ist vielmehr der weitere Verlauf: Zeigt sich eine Stabilisierung oder gar Regression, kann unter dokumentierter Kontrolle zugewartet werden. Bei Persistenz, erneutem Wachstum oder dem Auftreten asymmetrischer Strukturen, polychromatischer Pigmentierung oder atypischer Gefässarchitektur ist eine Exzision indiziert (24). Bei Jugendlichen und Erwachsenen empfiehlt sich aufgrund der erhöhten Wahrscheinlichkeit eines malignen Verlaufs grundsätzlich die operative Entfernung (24).
Nach erfolgter Exzision erfolgt die histopathologische Beurteilung, ergänzt durch eine immunhistochemische Untersuchung (p16, Ki-67, HMB45, Melan A). Diese Marker liefern Hinweise zur Reifung, Proliferationsaktivität und Differenzierung und bilden den diagnostischen Mindeststandard (30, 31). In Fällen mit auffälliger Morphologie oder diskrepanten klinisch-histologischen Befunden kann eine molekulargenetische Analyse mittels Next-Generation-Sequencing zusätzliche Hinweise zur biologischen Einschätzung liefern (13). Die Befundinterpretation sollte interdisziplinär und vorzugsweise an einem erfahrenen Zentrum erfolgen, das mit der differenzierten Diagnostik von Spitz-Tumoren vertraut ist. Die Einteilung in benigne, intermediäre oder maligne Spitz-Tumoren bestimmt das weitere therapeutische Vorgehen. Benigne Läsionen erfordern nach vollständiger Entfernung keine weiterführende Therapie, jedoch werden jährliche klinische Nachkontrollen empfohlen. Intermediäre Tumoren sollten nach Nachresektion mit Sicherheitsabstand klinisch engmaschig kontrolliert werden, ergänzt durch eine regelmässige sonographische Kontrolle der lokoregionären Lymphknoten. Eine Sentinel-Lymphknotenbiopsie wird in diesen Fällen aufgrund der fehlenden prognostischen Relevanz einer nodalen Manifestation nicht empfohlen (8). Bei eindeutig malignen Spitz-Melanomen erfolgt die stadiengerechte Behandlung gemäss den aktuellen ESMO-Leitlinien zum kutanen Melanom, inklusive Sentinel-Lymphknotenbiopsie und gegebenenfalls systemischer Therapie (37).
Dieses strukturierte, altersdifferenzierte Vorgehen ermöglicht eine individualisierte Entscheidungsfindung, bei der unnötige Eingriffe bei biologisch stabilen Läsionen vermieden, aber potenziell progressive Verläufe frühzeitig erkannt und adäquat behandelt werden.
Klinischer Ausblick
Spitz-Tumoren stellen insbesondere im Kindes- und Jugendalter häufig eine besondere diagnostische Herausforderung dar. Ihre klinisch auffällige Morphologie steht nicht selten in Kontrast zu ihrem biologischen Verhalten. Ausschlaggebend ist nicht ein einzelnes Merkmal, sondern das Zusammenspiel aller relevanten klinischen und pathologischen Faktoren im jeweiligen Kontext. Der klassische Spitz-Nävus ist in diesem Zusammenhang klar einzuordnen. Er stellt im Kindesalter eine eigenständige, biologisch stabile Entität dar, die weder einem kutanen Melanom noch dessen Vorstufen zuzuordnen ist. Seine gutartige Natur erlaubt ein zurückhaltendes, altersgerechtes Management, sofern die Befundkonstellation eindeutig auf ein biologisch stabiles Verhalten hinweist. Seit der Erstbeschreibung durch Sophie Spitz im Jahr 1948 hat sich das Verständnis von Spitz-Tumoren stetig weiterentwickelt. Die Einführung immunhistochemischer Marker und moderner molekularer Techniken hat die diagnostische Präzision verbessert und liefert insbesondere bei unklaren Befunden zusätzliche Anhaltspunkte. Dennoch bleibt die Abgrenzung im Einzelfall anspruchsvoll und erfordert klinische Erfahrung sowie eine interdisziplinäre Bewertung. Mit dem weiteren Fortschritt der molekularbiologischen Diagnostik ist zu erwarten, dass auch künftig neue Erkenntnisse zur Einordnung spitzoider Tumoren beitragen werden. Entscheidend bleibt, dass solche Entwicklungen mit Augenmass in die klinische Praxis integriert werden. Der Spitz-Nävus im Kindesalter steht exemplarisch für die Bedeutung eines differenzierten, verantwortungsbewussten und patientenzentrierten diagnostischen Vorgehens, das sich am biologischen Verhalten orientiert und nicht allein an morphologischen Auffälligkeiten.
Copyright
Aerzteverlag medinfo AG
Zweitabdruck aus «Therapeutische Umschau» 4/2025
Dermatologische Klinik
Universitätsspital Zürich
The Circle 59
8058 Zürich-Flughafen
mario.teufer@usz.ch
– Senior Consultant
Klinik für Dermatologie
Universitätsspital Zürich
Rämistrasse 100, 8091 Zürich
reinhard.dummer@usz.ch
– Leiter Hautkrebszentrum
Kantonsspital Aarau, Hautkrebszentrum
Bahnhofplatz 3C
5001 Aarau
reinhard.dummer@ksa.ch
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Hilbers ML, Brändli R, Mühleisen B, Freiberger SN, Mangana J, Dummer R. Standardized diagnostic algorithm for spitzoid lesions aids clinical decision-making and management: a case series from a Swiss reference center. Oncotarget. 2021 Jan 19;12(2):125–30.
2. Elder DE, Bastian BC, Cree IA, Massi D, Scolyer RA. The 2018 World Health Organization Classification of Cutaneous, Mucosal, and Uveal Melanoma: Detailed Analysis of 9 Distinct Subtypes Defined by Their Evolutionary Pathway. Archives of Pathology & Laboratory Medicine. 2020 Apr 1;144(4):500–22.
3. Dika E, Ravaioli GM, Fanti PA, Neri I, Patrizi A. Spitz Nevi and Other Spitzoid Neoplasms in Children: Overview of Incidence Data and Diagnostic Criteria. Pediatric Dermatology. 2017 Jan;34(1):25–32.
4. Herzum A, Occella C, Vellone VG, Gariazzo L, Pastorino C, Ferro J, et al. Paediatric Spitzoid Neoplasms: 10-Year Retrospective Study Characterizing Histological, Clinical, Dermoscopic Presentation and FISH Test Results. Diagnostics. 2023 Jul 15;13(14):2380.
5. Lott JP, Wititsuwannakul J, Lee JJ, Ariyan S, Narayan D, Kluger HH, et al. Clinical characteristics associated with Spitz nevi and Spitzoid malignant melanomas: The Yale University Spitzoid Neoplasm Repository experience, 1991 to 2008. Journal of the American Academy of Dermatology. 2014 Dec;71(6):1077–82.
6. Cheng TW, Ahern MC, Giubellino A. The Spectrum of Spitz Melanocytic Lesions: From Morphologic Diagnosis to Molecular Classification. Front Oncol. 2022 Jun 7;12:889223.
7. Bastian BC, LeBoit PE, Pinkel D. Mutations and Copy Number Increase of HRAS in Spitz Nevi with Distinctive Histopathological Features. The American Journal of Pathology. 2000 Sep;157(3):967–72.
8. Lallas A, Kyrgidis A, Ferrara G, Kittler H, Apalla Z, Castagnetti F, et al. Atypical Spitz tumours and sentinel lymph node biopsy: a systematic review. The Lancet Oncology. 2014 Apr;15(4):e178–83.
9. Lee S, Barnhill RL, Dummer R, Dalton J, Wu J, Pappo A, et al. TERT Promoter Mutations Are Predictive of Aggressive Clinical Behavior in Patients with Spitzoid Melanocytic Neoplasms. Sci Rep. 2015 Jun 10;5(1):11200.
10. Spitz S. Melanomas of childhood. Am J Pathol. 1948 May;24(3):591–609.
11. Chatzopoulos K, Syrnioti A, Linos K. Spitz Melanocytic Tumors: A Fascinating 75-Year Journey. Genes. 2024 Jan 31;15(2):195.
12. Kernen JA, Ackerman LV. Spindle cell nevi and epithelioid cell nevi (so-called juvenile melanomas) in children and adults.A clinicopathological study of 27 cases. Cancer. 1960 May;13(3):612–25.
13. Hillen LM, Van Den Oord J, Geybels MS, Becker JC, Zur Hausen A, Winnepenninckx V. Genomic Landscape of Spitzoid Neoplasms Impacting Patient Management. Front Med. 2018 Dec 13;5:344.
14. Gerami P, Busam K, Cochran A, Cook MG, Duncan LM, Elder DE, et al. Histomorphologic Assessment and Interobserver Diagnostic Reproducibility of Atypical Spitzoid Melanocytic Neoplasms With Long-term Follow-up. American Journal of Surgical Pathology. 2014 Jul;38(7):934–40.
15. Sargen MR, Barnhill RL, Elder DE, Swetter SM, Prieto VG, Ko JS, et al. Evaluation and Surgical Management of Pediatric Cutaneous Melanoma and Atypical Spitz and Non-Spitz Melanocytic Tumors (Melanocytomas): A Report From Children’s Oncology Group. JCO. 2024 Oct 4;JCO.24.01154.
16. Sepehr A. Long-term Outcome of Spitz-Type Melanocytic Tumors. Arch Dermatol. 2011 Oct 1;147(10):1173.
17. Gassenmaier M, Soltanpour N, Held L, Metzler G, Yazdi AS, Brecht IB, et al. Diagnostic and prognostic classification of atypical spitzoid tumours based on histology and genomic aberrations: A prospective cohort study with long-term follow-up. European Journal of Cancer. 2022 Mar;163:200–10.
18. Delsupehe L, Steelandt T, Lemahieu J, Volders PJ, Geerdens E, Berden S, et al. Novel gene fusion discovery in Spitz tumours and its relevance in diagnostics. Virchows Arch. 2024 Aug;485(2):269–79.
19. Wiesner T, He J, Yelensky R, Esteve-Puig R, Botton T, Yeh I, et al. Kinase fusions are frequent in Spitz tumours and spitzoid melanomas. Nat Commun. 2014 Jan 20;5(1):3116.
20. Daruish M, Ambrogio F, Colagrande A, Marzullo A, Alaggio R, Trilli I, et al. Kinase Fusions in Spitz Melanocytic Tumors: The Past, the Present, and the Future. Dermatopathology. 2024 Feb 14;11(1):112–23.
21. Van Dijk MCRF, Bernsen MR, Ruiter DJ. Analysis of Mutations in B-RAF, N-RAS, and H-RAS Genes in the Differential Diagnosis of Spitz Nevus and Spitzoid Melanoma. American Journal of Surgical Pathology. 2005 Sep;29(9):1145–51.
22. Raghavan SS, Peternel S, Mully TW, North JP, Pincus LB, LeBoit PE, et al. Spitz melanoma is a distinct subset of spitzoid melanoma. Modern Pathology. 2020 Jun;33(6):1122–34.
23. Quan VL, Zhang B, Zhang Y, Mohan LS, Shi K, Wagner A, et al. Integrating Next-Generation Sequencing with Morphology Improves Prognostic and Biologic Classification of Spitz Neoplasms. Journal of Investigative Dermatology. 2020 Aug;140(8):1599–608.
24. Lallas A, Apalla Z, Ioannides D, Lazaridou E, Kyrgidis A, Broganelli P, et al. Update on dermoscopy of Spitz/Reed naevi and management guidelines by the International Dermoscopy Society. Br J Dermatol. 2017 Sep;177(3):645–55.
25. Lallas A, Moscarella E, Longo C, Kyrgidis A, De Mestier Y, Vale G, et al. Likelihood of finding melanoma when removing a Spitzoid-looking lesion in patients aged 12 years or older. Journal of the American Academy of Dermatology. 2015 Jan;72(1):47–53.
26. Argenziano G, Agozzino M, Bonifazi E, Broganelli P, Brunetti B, Ferrara G, et al. Natural Evolution of Spitz Nevi. Dermatology. 2011;222(3):256–60.
27. Yeh I, Busam KJ. Spitz melanocytic tumours – a review. Histopathology. 2022 Jan;80(1):122–34.
28. Olsen SH, Patel RM, Ma L, Fullen DR. Difficulties in the diagnosis of spitzoid melanocytic lesions. Expert Review of Dermatology. 2010 Oct;5(5):549–60.
29. Menezes FD, Mooi WJ. Spitz Tumors of the Skin. Surgical Pathology Clinics. 2017 Jun;10(2):281–98.
30. Garola R, Singh V. Utility of p16-Ki-67-HMB45 score in sorting benign from malignant Spitz tumors. Pathology – Research and Practice. 2019 Oct;215(10):152550.
31. Uguen A, Talagas M, Costa S, Duigou S, Bouvier S, De Braekeleer M, et al. A p16-Ki-67-HMB45 immunohistochemistry scoring system as an ancillary diagnostic tool in the diagnosis of melanoma. Diagn Pathol. 2015 Dec;10(1):195.
32. Cho-Vega JH. A diagnostic algorithm for atypical spitzoid tumors: guidelines for immunohistochemical and molecular assessment. Modern Pathology. 2016 Jul;29(7):656–70.
33. Teufer M, Theiler M, Lanz J, Weibel L, Wagner U, Levesque MP, et al. A Retrospective Analysis of Ambiguous Spitz Tumors Using Next-Generation Sequencing. Cancers. 2025 Apr 4;17(7):1227.
34. Raskin L, Ludgate M, Iyer RK, Ackley TE, Bradford CR, Johnson TM, et al. Copy Number Variations and Clinical Outcome in Atypical Spitz Tumors. American Journal of Surgical Pathology. 2011 Feb;35(2):243–52.
35. Mones JM, Ackerman AB. “Atypical” Spitz’s Nevus, “Malignant” Spitz’s Nevus,
info@onco-suisse
- Vol. 16
- Ausgabe 1
- März 2026