- Ergebnisse der RATIONALE 306 Studie
Die RATIONALE-306-Studie untersuchte den Nutzen von Tislelizumab, einem PD-1-Inhibitor, in Kombination mit platinhaltiger Chemotherapie. Es zeigte sich dabei ein signifikanter Überlebensvorteil für die Erstlinienbehandlung mit Tislelizumab plus Chemotherapie im Vergleich zu Placebo plus Chemotherapie bei Patienten mit fortgeschrittenem ESCC, sowohl bei der primären Analyse (2) als auch nach einer Mindestnachbeobachtungszeit von drei Jahren (3). Bei der 3-Jahres-Nachbeobachtungszeit zeigten die OS-Ergebnisse eine stratifizierte HR von 0,70 für alle Patienten in der ITT-Population. Bei Patienten mit einem Tumor-PD-L1-TAP-Score von ≥ 10 % bzw. ≥ 5 % betrugen die HRs 0,70 bzw. 0,62 (3).
Anlässlich des ESMO-GI-Kongresses 2025 präsentierten Prof. David Tougeron aus Poitiers, Frankreich, und seine Kollegen von insgesamt 18 internationalen Institutionen nun Daten von RATIONALE-306 in der Untergruppe mit einem Tumor-PD-L1-TAP-Score von ≥ 5 %, wie ihn auch die Europäische Arzneimittelagentur (EMA) für die Zulassung berücksichtigte (4).
RATIONALE-306 (NCT03783442) ist eine randomisierte, doppelblinde Phase-3-Studie mit globaler Beteiligung zur Bewertung der Wirksamkeit und Sicherheit von Tislelizumab plus Chemotherapie im Vergleich zu Placebo plus Chemotherapie als Erstlinienbehandlung von metastasiertem oder inoperablem ESCC. Patienten mit nicht resezierbarem, lokal fortgeschrittenem oder metastasierendem ESCC, die keine systemische Vorbehandlung für fortgeschrittene Krankheit erhalten hatten, mit ECOG-PS 0 oder 1 und messbarer oder auswertbarer Krankheit nach RECIST v1.1 wurden mit Tislelizumab 200 mg i.v. Q3W plus Chemotherapie (Platin + Fluoropyrimidin oder Platin + Paclitaxel im Verhältnis 1:1) versus Placebo i.v. Q3W plus Chemotherapie (Platin + Fluoropyrimidin oder Platin + Paclitaxel) als Erhaltungstherapie bis zu unannehmbarer Toxizität oder Krankheitsprogression behandelt.
Primärer Endpunkt war das Gesamtüberleben (OS) in der ITT-Analysegruppe. Sekundäre Endpunkte waren das OS in der Untergruppe mit PD-L1-TAP-Score ≥ 10 %, progressionsfreies Überleben (PFS), objektive Ansprechrate (ORR), Ansprechdauer (DoR) sowie gesundheitsbezogene Lebensqualität (HRQoL) und Sicherheit.
Die Post-hoc-Analyse umfasste die Subgruppenanalyse von Patienten mit ESCC-Tumor-PD-L1-TAP-Score ≥ 5 %.
Stratifikationsfaktoren waren:
• Die geografische Region (Asien [ohne Japan] vs. Japan vs. Rest der Welt)
• Die vorherige endgültige Therapie (ja vs. nein)
• Die vom Prüfarzt gewählte Chemotherapie (Platin + Fluoropyrimidin).
Die Patienten wurden unabhängig von ihrer PD-L1-Expression beim Screening in die Studie aufgenommen. Die Proben wurden mit dem VENTANA PD-L1 (SP263) Assay (Roche) auf PD-L1 angefärbt und die Expression anhand des TAP-Scores bestimmt. Zu explorativen Zwecken bewerteten Pathologen die gleichen angefärbten Proben nach dem CPS im Zentrallabor.
Patientendisposition und Baseline-Charakteristiken
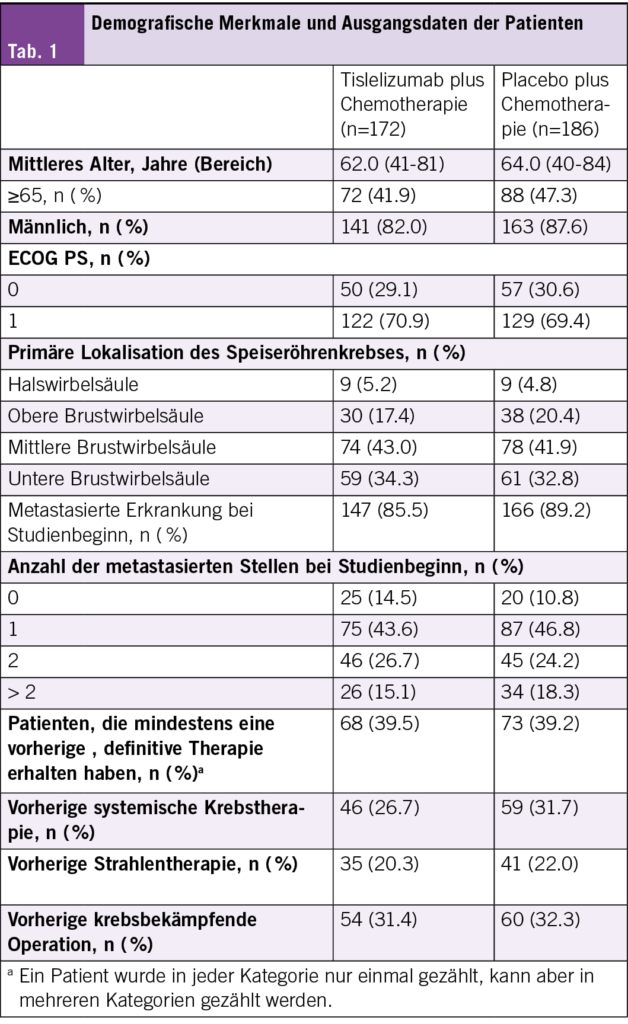
Von 649 randomisierten Patienten (Tislelizumab plus Chemotherapie n = 326; Placebo plus Chemotherapie n = 323) hatten 358 (55,2 %) einen Tumor-PD-L1-TAP-Score ≥ 5 % (Tislelizumab plus Chemotherapie n = 172; Placebo plus Chemotherapie n = 186) (Tab. 1). Die Ausgangscharakteristika der Patienten mit einem Tumor-PD-L1-TAP-Score von ≥ 5 % entsprachen der ITT-Population. Bei Datenschnitt (22. August 2024) betrug die minimale Nachbeobachtungszeit der Studie 45,2 Monate (Bereich: 0,4–63,6). Im Tislelizumab-plus-Chemotherapie-Arm erhielten 106 Patienten (61,6 %) gegenüber 126 (67,7 %) im Placebo-plus-Chemotherapie-Arm eine systemische Therapie nach der Behandlung, von denen 27 (25,5 %) gegenüber 44 (34,9 %) eine systemische Immuntherapie hatten.
Wirksamkeit
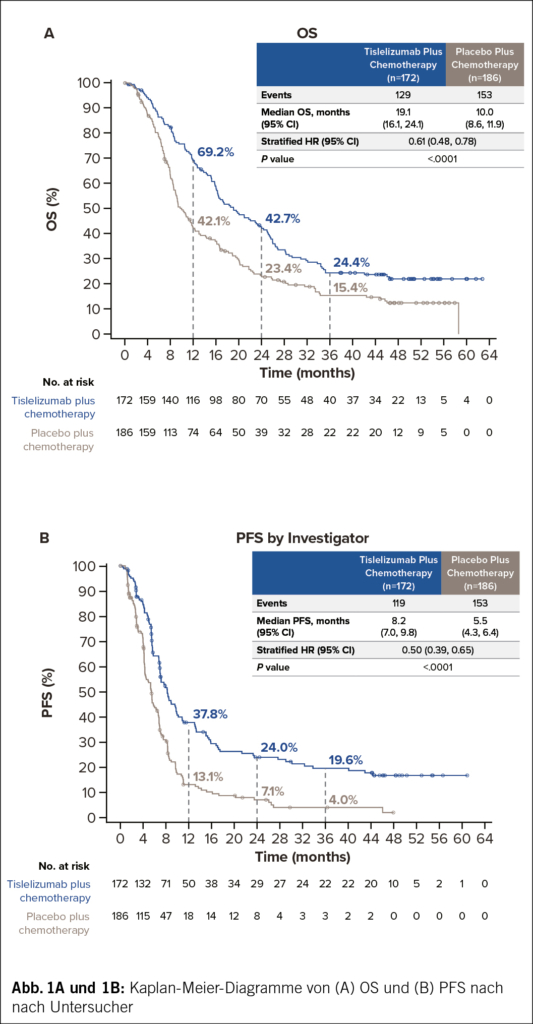
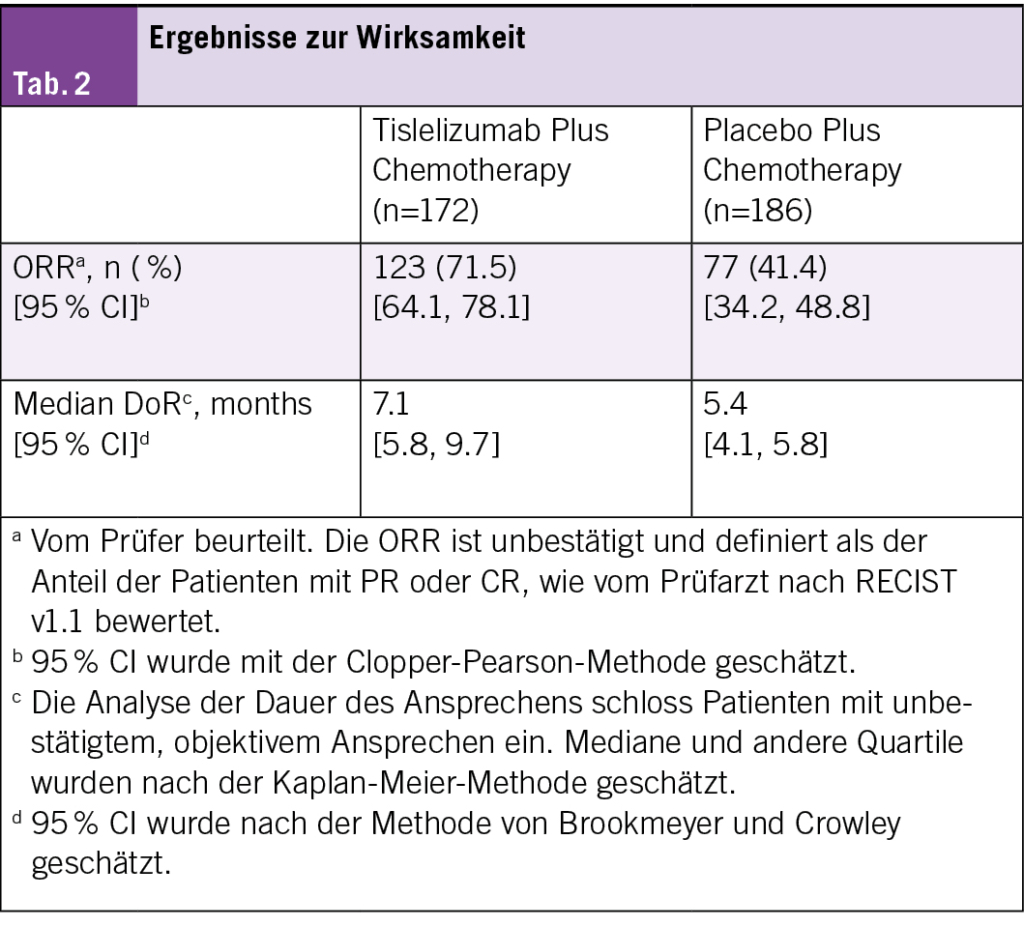
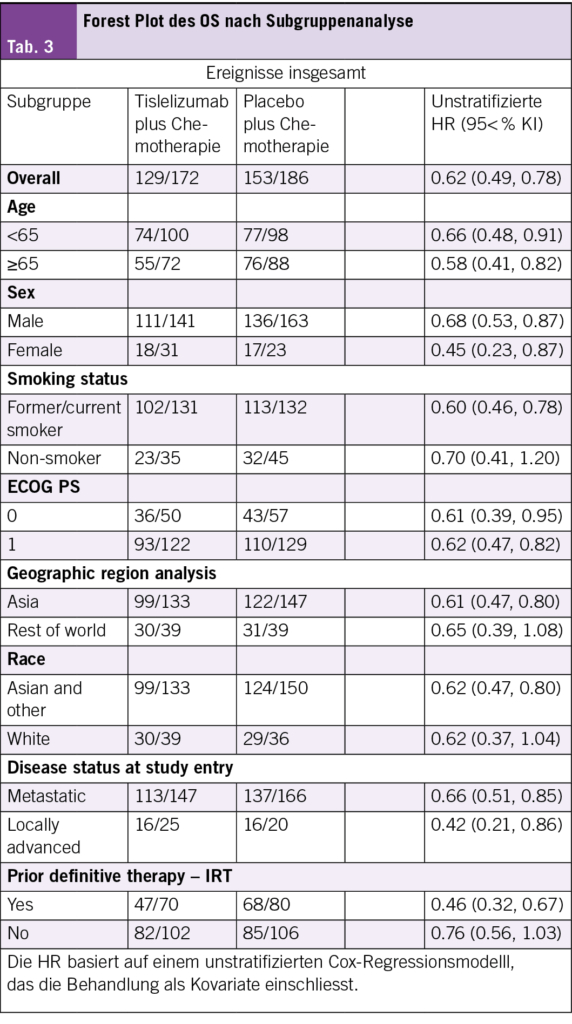
Klinisch bedeutsame Verbesserungen des OS (Abb. 1A) und des vom Prüfer bewerteten PFS (Abb. 1B) wurden mit Tislelizumab plus Chemotherapie im Vergleich zu Placebo plus Chemotherapie beobachtet. Eine höhere ORR und eine verbesserte DoR wurden mit Tislelizumab plus Chemotherapie im Vergleich zu Placebo plus Chemotherapie festgestellt (Tab. 2). Der OS-Vorteil wurde in allen vordefinierten Untergruppen beobachtet (Tab. 3).
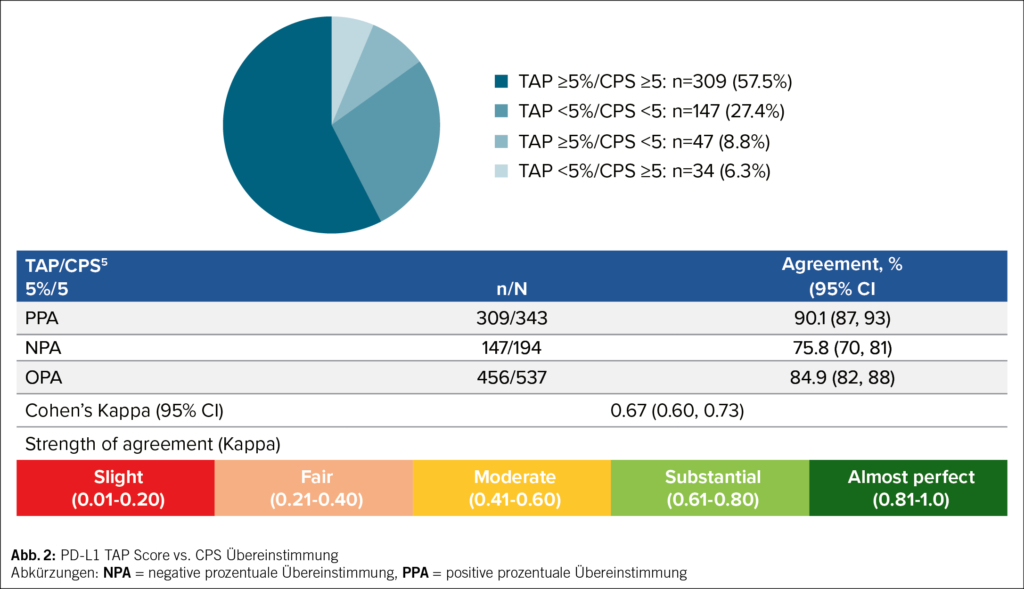
PD-L1 TAP Score vs. CPS Konkordanz
TAP Score 5 % und CPS 5 Cutoffs zeigten 84 % Gesamtübereinstimmung in Prozent, die eine erhebliche Übereinstimmung ergibt. (Abb. 2).
Sicherheit, Verträglichkeitsprofil
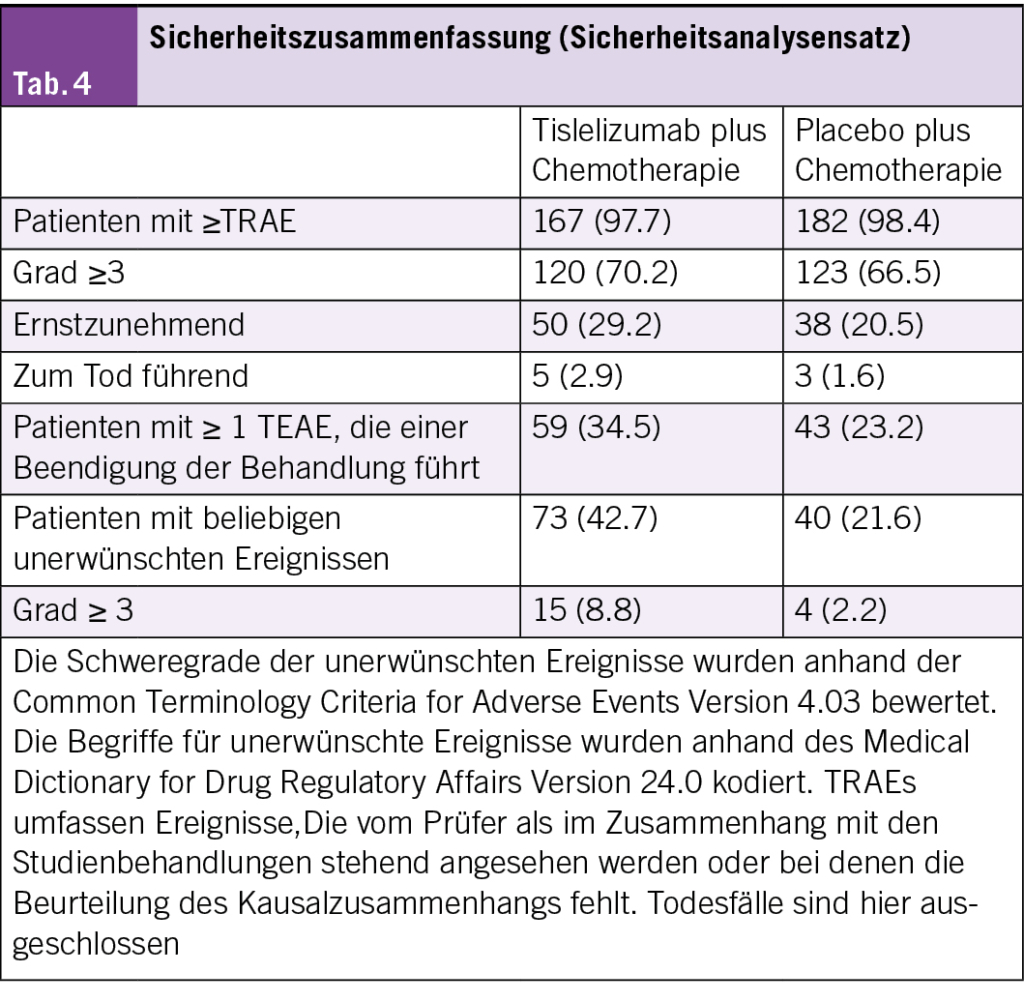
Behandlungsbedingte unerwünschte Ereignisse (TRAEs) wurden bei den meisten Patienten in beiden Kohorten beobachtet, mit ähnlichen Raten für alle Schweregrade. Eine höhere Inzidenz von TRAEs der Schweregrade ≥ 3 und schweren TRAEs wurde für Tislelizumab plus Chemotherapie festgestellt (Tab. 4).
Die TRAEs der Schweregrade ≥ 3, die bei ≥ 10 % der Patienten mit Tislelizumab plus Chemotherapie im Vergleich zu Placebo plus Chemotherapie auftraten, umfassten eine verringerte Neutrophilenzahl (35,1 % vs. 31,9 %), eine verringerte Anzahl weisser Blutkörperchen (12,3 % vs. 17,8 %) und Anämie (13,5 % vs. 11,4 %).
Mehr TRAEs, die zum Tod führten (2,9 % vs. 1,6 %) und behandlungsbedingte unerwünschte Ereignisse (TEAEs), die zu einem Abbruch der Behandlung führten (34,5 % vs. 23,2 %), traten in der Gruppe mit Tislelizumab plus Chemotherapie auf als in der Gruppe mit Placebo plus Chemotherapie.
Immunvermittelte unerwünschte Ereignisse (imAEs) wurden in beiden Gruppen beobachtet. Die Inzidenz von imAEs der Schweregrade ≥ 3 war höher bei Tislelizumab plus Chemotherapie im Vergleich zu Placebo plus Chemotherapie (8,8 % vs. 2,2 %) (Tab. 4).
Schlussfolgerungen
Das mediane Gesamtüberleben (OS) von 19,1 Monaten unter Tislelizumab plus Chemotherapie bei Patienten mit einem Tumor-PD-L1-Status ≥ 5 % setzt eine neue Messlatte für die Wirksamkeit in dieser Gruppe von Patienten mit fortgeschrittenem/metastasiertem Oesophagus-Plattenepithelkarzinom bei akzeptabler Sicherheit. Der Nutzen in Bezug auf die Wirksamkeit und die Sicherheitsergebnisse blieb konsistent mit den Ergebnissen der Primäranalyse und des 3-Jahres-Follow-ups, die eine anhaltende Verbesserung ohne neue Sicherheitssignale zeigten.
Diese Daten sprechen für die Integration dieser Kombinationstherapie in die klinische Entscheidungsfindung, insbesondere auch im Schweizer Versorgungsauftrag.
riesen@medinfo-verlag.ch
1. Kato K, et al. Nivolumab plus chemotherapy or ipilimumab versus chemotherapy in patients with advanced esophageal squamous cell carcinoma (CheckMate 648): 29-month follow-up from a randomized, open-label, phase III tria. l Cancer Med. 2024;13:e7235.
2. Xu J, et al. Tislelizumab plus chemotherapy versus placebo plus chemotherapy as first-line treatment for advanced or metastatic oesophageal squamous cell carcinoma (RATIONALE-306): a global, randomised, placebo-controlled, phase 3 study. Lancet Oncol. 2023;24:483-495.
3. Yoon HH, et al. First-Line Tislelizumab Plus Chemotherapy Shows OS Benefit in PD-L1+ ESCC Subgroups. J Clin Oncol. 2024;42(Suppl 16):4032.
4. European Medicine Agency. Tevimbra 100mg concentrate for solution for infusion. Summary of product characteristics. https//www.ema.europa.eu/en/documents/product .information/Levimbra-epar-product-information_en.pdf. Assessed December 19,2 024.
info@onco-suisse
- Vol. 15
- Ausgabe 5
- Juli 2025