- Perioperative Therapie des muskelinvasiven Urothelkarzinoms
Das muskelinvasive Urothelkarzinom (MIBC) der Harnblase ist eine aggressive Erkrankung mit hohem Rezidivrisiko. Die radikale Zystektomie bleibt der Goldstandard der lokalen Therapie. Der grösste Fortschritt in den letzten Jahren in der Verbesserung des Gesamtüberlebens (OS) wurde jedoch durch die Integration systemischer Therapien in das perioperative Setting erzielt. Die perioperative Chemo- und Immuntherapie ist bei Cisplatin-fitten Patient/-innen die etablierte Standardtherapie vor der Zystektomie. Zudem gibt es die Möglichkeit der adjuvanten Immuncheckpoint-Inhibition (ICI). Neu können nun auch die Cisplatin-unfitten Patient/-innen eine perioperative Therapie mit Enfortumab Vedotin und Pembrolizumab erhalten. Auch die multimodale Therapie mit dem Ziel des Blasenerhalts ist immer besser untersucht und bietet eine alternative Therapieoption.
Muscle-invasive urothelial carcinoma (MIBC) of the urinary bladder is an aggressive disease with a high risk of recurrence. Radical cystectomy remains the gold standard of local therapy. However, the greatest progress in improving overall survival (OS) in recent years has been achieved through the integration of systemic therapies into the perioperative setting. Perioperative chemotherapy and immunotherapy are the established standard therapies prior to cystectomy in cisplatin-eligible patients. In addition, there is the option of adjuvant immune checkpoint inhibition (ICI). Now, cisplatin-unfit patients can also receive perioperative therapy with enfortumab vedotin and pembrolizumab. Multimodal therapy with the goal of bladder preservation is also being increasingly studied and offers an alternative treatment option.
Keywords: Urothelkarzinom, perioperative Systemtherapie, Immuntherapie, radikale Zystektomie
Einleitung
Das Urothelkarzinom gehört zu den häufigen malignen Tumoren mit 1400 Neudiagnosen jährlich. Männer sind dreimal häufiger betroffen als Frauen. Das mittlere Erkrankungsalter liegt bei über 70 Jahren. In der Schweiz führt die Erkrankung zu 600 Todesfällen jährlich (1). Das MIBC (pT2-T4a) macht etwa 25 % aller Urothelkarzinome der Harnblase aus. Während die radikale Zystektomie (RC) die notwendige lokale Kontrolle bietet, sind Fernmetastasen der Hauptgrund für das erhöhte Mortalitätsrisiko. Die perioperative systemische Behandlung zielt darauf ab, allfällig vorhandene Mikrometastasen zu eliminieren und somit das krankheitsfreie Überleben (DFS) und das OS zu verlängern.
Neoadjuvante Chemotherapie (NAC) – der langjährige Goldstandard
Bei Cisplatin-fitten Patient/-innen führt die neoadjuvante oder adjuvante Chemotherapie gemäss diverser Metaanalysen zu einer absoluten Verbesserung des 5-Jahres-OS um ca. 5 % (2, 3). Die beiden am besten untersuchten Chemotherapie-Schemata, 4 Zyklen Cisplatin mit Gemcitabin (CG) à jeweils 3 Wochen und 6 Zyklen dosisdichtes Methotrexat, Vinblastin, Doxorubicin und Cisplatin (ddMVAC) à jeweils 2 Wochen, wurden in der Phase 3 VESPER-Studie gegeneinander verglichen. Das OS nach 5 Jahren war in der ddMVAC-Gruppe mit 66 % im Vergleich zur CG-Gruppe mit 57 % signifikant besser (4).
Adjuvante Immuntherapie
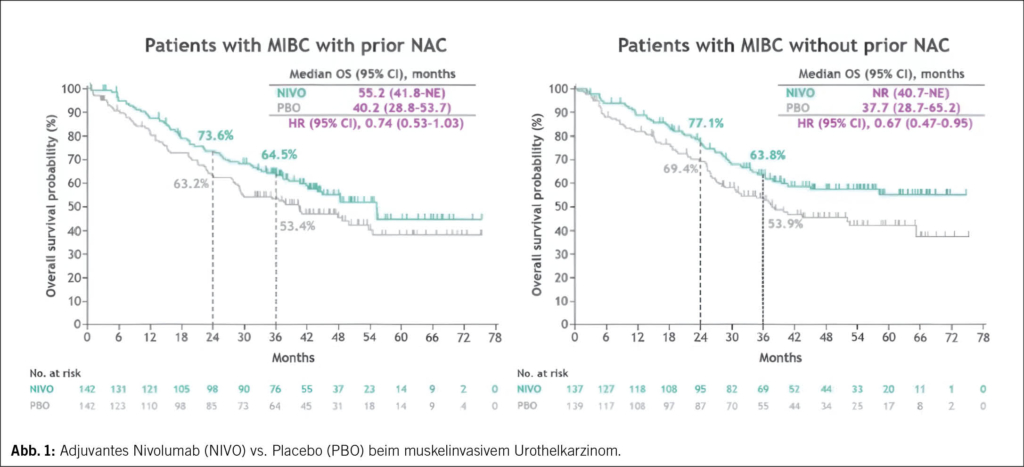
Trotz NAC und RC ist die Rezidivrate bei Patient/-innen mit Resttumoranteilen (ypT2-4 oder ypN+) deutlich erhöht. Aufgrund der Resultate der CheckMate 274-Studie ist Nivolumab bei einer PD-L1-Expression von ≥ 1 % als adjuvante Therapie über ein Jahr zugelassen, entweder nach einer neoadjuvanten Cisplatin-haltigen Chemotherapie in den Stadien ypT2-T4a, bei nachgewiesenen lokoregionären Lymphknotenmetastasen, bei Cisplatin-unfitten Patient/-innen in den Stadien pT3-T4a oder unabhängig vom T-Stadium mit lokoregionären Lymphknotenmetastasen. In der initialen Publikation 2021 zeigte sich bei einer PD-L1-Expression der Karzinomzellen von ≥ 1 % ein medianes DFS von 52.6 Monaten mit Nivolumab versus 8.4 Monaten mit Placebo (5). Beim ASCO GU 2025 wurden die Auswertungen des OS nach 36 Monaten präsentiert, wobei sowohl in der Gruppe der neoadjuvant vorbehandelten Patient/-innen das OS mit adjuvanter Nivolumab-Gabe über ein Jahr verbessert werden konnte (HR 0.74, 95 % CI 0.53–1.03) als auch bei den Cisplatin-unfitten Patient/-innen (HR 0.67, 95 % CI 0.47–0.95) (Abb. 1).
Perioperative Systemtherapie
Den grössten Fortschritt gab es in den letzten Jahren durch die neuen perioperativen Therapiekonzepte, die eine neoadjuvante Systemtherapie mit einer adjuvanten Immuntherapie kombinieren.
Bei den Cisplatin-fitten Patient/-innen kann, seit der Publikation der Phase 3 NIAGARA-Studie, die Immuntherapie Durvalumab neoadjuvant, in Kombination mit 4 Zyklen CG, gefolgt von der RC und anschliessend adjuvant alleinig für 8 weitere Zyklen à jeweils 4 Wochen verabreicht werden (6). Der primäre Endpunkt der Studie war das ereignisfreie Überleben (EFS). Nach einer Beobachtungszeit von 2 Jahren zeigte sich ein signifikant höheres EFS im Interventionsarm mit zusätzlich Durvalumab von 67.8 % (95 % CI 63.6–71.7) verglichen mit 59.8 % (95 % CI 55.4–64.0) in der Gruppe mit der alleinigen Chemotherapie. Beim sekundären Endpunkt OS nach 24 Monaten betrug der Unterschied 7 %, 82.2 % (95 % CI 78.7–85.2) im Durvalumab-Arm versus 75.2 % (95 % CI 71.3–78.8) im Kontrollarm. Cisplatin durfte in der Studie bei Patient/-innen mit einer mittelschwer eingeschränkten Nierenfunktion (errechnete glomeruläre Filtrationsrate (eGFR) von 40–60 ml/min) aufgeteilt auf 2 Dosen à jeweils 35 mg/m2 an Tag 1 und Tag 8 gegeben werden, was die Anzahl der Cisplatin-fitten Patient/-innen erhöht. Ob durch den Einsatz von ddMVAC, anstelle von CG, bessere Ergebnisse erzielt würden, ist derzeit nicht untersucht.
Bei den Cisplatin-unfitten Patient/-innen war bisher die alleinige RC das Standardvorgehen. Analog zur Standard-Erstlinientherapie beim metastasierten Urothelkarzinom bestehend aus Enfortumab Vedotin und Pembrolizumab seit der Publikation der EV-302-Studie (7), wurde kürzlich in der Phase 3 KEYNOTE-905-Studie dasselbe Regime perioperativ getestet. Die Patient/-innen im Interventionsarm erhielten 3 Zyklen Enfortumab Vedotin in Kombination mit Pembrolizumab à jeweils 3 Wochen präoperativ. Postoperativ erfolgten weitere 6 Zyklen Enfortumab Vedotin in Kombination mit Pembrolizumab, wonach noch 8 Zyklen alleinig Pembrolizumab fortgeführt wurde. Im Kontrollarm wurden die Patient/-innen einer RC ohne perioperative Systemtherapie unterzogen.
Am ESMO-Kongress 2025 wurde die erste Auswertung des primären Endpunkts (EFS) präsentiert. Durch die perioperative Therapie konnte eine signifikante Verlängerung des mittleren EFS im Vergleich zur alleinigen RC bewirkt werden. So lag das mittlere EFS bei 15.7 Monaten in der Kontrollgruppe, wohingegen in der Interventionsgruppe mit perioperativer Therapie das mittlere EFS zum Zeitpunkt der Auswertung noch nicht erreicht worden war (HR 0.40, 95 % CI 0.28–0.57; p < 0.0001) (8). Auch einzelne Patient/-innen, die Cisplatin-fit gewesen wären, aber eine Chemotherapie abgelehnt haben, wurden eingeschlossen. Die Anzahl der Patient/-innen war aber zu klein, um eine Aussage bezüglich der Wirksamkeit in dieser Gruppe machen zu können (Abb. 2).
Im Dezember 2025 wurden am Jahreskongress der Society of Urologic Oncology (SUO) die erste Auswertung des OS und des pathologischen Ansprechens präsentiert. Das mittlere OS in der Interventionsgruppe war noch nicht erreicht, verglichen mit 41.7 Monaten in der Kontrollgruppe (HR 0.50; p = 0.0002). Bei 57.1 % der Patient/-innen in der Interventionsgruppe konnte eine komplette pathologische Remission (pCR) festgestellt werden, verglichen mit 8.6 % in der Kontrollgruppe (p < 0.000001) (10). Aufgrund dieser Resultate dürfte die perioperative Therapie mit Enfortumab Vedotin in Kombination mit Pembrolizumab sich zur neuen Standardtherapie für Cisplatin-unfitte Patient/-innen etablieren, wobei die Publikation der Studie noch aussteht. Mit Spannung erwarten wir die Resultate der EV-304/KEYNOTE-B15-Studie (NCT04700124), welche dieses perioperative Therapie-Konzept auch bei den Cisplatin-fitten Patient/-innen untersucht. Laut einer Pressemitteilung der Herstellerfirma dürfen wir hier positive Resultate erwarten.
Multimodale organerhaltende Therapie
Multimodale Therapiekonzepte sind vor allem für Patient/-innen mit einem lokal begrenzten muskelinvasiven Blasenkarzinom (insbesondere cT2 cN0 cM0) geeignet, die nicht für eine Zystektomie qualifizieren oder diese ablehnen. Ungünstige Prognosefaktoren sind multifokale Tumore, eine nicht urotheliale Histologie, eine Hydronephrose und das Vorliegen eines synchronen Carcinoma in situ (9). Vor der definitiven kombinierten Radio- und Chemotherapie muss mittels transurethraler Resektion der Blase (TUR-B) der Primarius möglichst komplett reseziert werden. Gemäss einer Single-Center-Studie mit 348 Patient/-innen wurde bei einem cT2-Stadium eine komplette Remission bei 81 % der Patient/-innen erzielt, im Vergleich zu 64 % bei cT3-4-Stadien (11). In einer retrospektiven Matched Pair-Studie von 722 Patient/-innen mit cT2-T4 cN0 cM0-Stadien war das onkologische Ergebnis zwischen trimodaler Therapie und radikaler Zystektomie, mit neoadjuvanter Systemtherapie, gleichwertig. Eine Salvage-Zystektomie nach trimodaler Therapie war bei 13 % der Patient/-innen erforderlich (12). Gross randomisierte Studien, welche die beiden Konzepte vergleichen, wurden bisher nicht durchgeführt.
Ausblick
Die zukünftigen Studien müssen die optimale Therapiesequenz von Chemotherapie, Immuntherapie und RC klären. Individualisierte, Biomarker-gesteuerte Behandlungsstrategien werden den Weg für verbesserte onkologische Ergebnisse ebnen. Das Ziel muss es sein, die pCR-Raten zu maximieren und dadurch das langfristige Überleben zu optimieren. Dies bei gleichzeitiger Minimierung therapiebedingter Toxizität. Auch Liquid Biopsy-gesteuerte Therapiekonzepte dürften in Zukunft in Studienkonzepte integriert werden.
Copyright
Aerzteverlag medinfo AG
Abteilung für Onkologie und Hämatologie
Kantonsspital Baselland
Rheinstrasse 26
4410 Liestal
angela.kohler@ksbl.ch
Oberarzt meV
Abteilung für Onkologie und Hämatologie
Kantonsspital Baselland
Rheinstrasse 26
4410 Liesta
Die Autorenschaft hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Beim muskelinvasiven Urothelkarzinom ist die perioperative Systemtherapie bei Cisplatin-fitten Patient/-innen die Standardtherapie und hat zu einer Verbesserung der Prognose geführt. Eine weiterhin wichtige Alternative ist ddMVAC, jedoch verbunden mit erhöhter Toxizität.
- Neu können auch Cisplatin-unfitte Patient/-innen mit einer perioperativen Therapie mit Enfortumab Vedotin und Pembrolizumab behandelt werden.
- Multimodale Therapiekonzepte sind beim lokal begrenztem muskelinvasivem Blasenkarzinom (insbesondere im Stadium cT2 cN0 cM0) eine mögliche Alternative zum operativen Vorgehen.
1. Krebsliga: Krebs in der Schweiz, Wichtige Zahlen, Stand Nov 2025; www.krebsliga.ch/ueber-krebs/zahlen-fakten
2. Neoadjuvant chemotherapy in invasive bladder cancer: a systematic review and meta-analysis. Lancet. 2003;361(9373):1927
3. Neoadjuvant chemotherapy in invasive bladder cancer: update of a systematic review and meta-analysis of individual patient data advanced bladder cancer (ABC) meta-analysis collaboration. Eur Urol. 2005;48(2):202. Epub 2005 Apr 21
4. Pfister, C, Gravis G, Flechon A et al. Perioperative dose-dense methotrexate, vinblastine, doxorubicin, and cisplatin in muscle-invasive bladder cancer (VESPER): survival endpoints at 5 years in an open-label, randomised, phase 3 study. Lancet Oncol, 2024. 25(2): p. 255-264
5. Galsky MD, Witjes JA, Gschwend JE et al. Adjuvant Nivolumab in High-Risk Muscle-Invasive Urothelial Carcinoma: Expanded Efficacy From CheckMate 274. J Clin Oncol, 2024: p. Jco2400340.
6. Powles T, Catto JWF, Galsky MD et al. Perioperative Durvalumab with Neoadjuvant Chemotherapy in Operable Bladder Cancer. N Engl J Med, 2024. 391(19): p. 1773-1786.
7. Powles T, Valderrama BP, Gupta S et al. Enfortumab Vedotin and Pembrolizumab in Untreated Advanced Urothelial Cancer. N Engl J Med. 2024;390(10):875
8. Vulsteke C, et al. Perioperative (periop) enfortumab vedotin (EV) plus pembrolizumab (pembro) in participants (pts) with muscle-invasive bladder cancer (MIBC) who are cisplatin-ineligible: The phase 3 KEYNOTE-905 study. ESMO Congress 2025
9. Onkopedia Leitlinien, Urothelkarzinom (Harnblasenkarzinom), Stand November 2024
10. Kaimakliotis HZ, Shore N, Adra N, et al: Primary efficacy and surgical details in KEYNOTE-905: Neoadjuvant and adjuvant enfortumab vedotin plus pembrolizumab in participants with muscle-invasive bladder cancer who are cisplatin ineligible. 2025 SUO Annual Meeting. Presented December 5, 2025.
11. Long-term outcomes of selective bladder preservation by combined-modality therapy for invasive bladder cancer: the MGH experience. Eur Urol. 2012 Apr;61(4):705-11.
12. Zlotta AR, Ballas LK, Niemierko A et al. Radical cystectomy versus trimodality therapy for muscle-invasive bladder cancer: a multi-institutional propensity score matched and weighted analysis. Lancet Oncol, 2023. 24(6): p. 669-681
info@onco-suisse
- Vol. 16
- Ausgabe 1
- März 2026