- Dénutrition et cachexie cardiaque: un défi sous-estimé dans l’insuffisance cardiaque
L’insuffisance cardiaque chronique est l’une des maladies cardiovasculaires les plus fréquentes. Elle est étroitement liée à des syndromes associés à l’alimentation tels que la dénutrition liée à la maladie, la cachexie cardiaque, la sarcopénie ou la fragilité. Malgré des mécanismes physiopathologiques similaires, ces syndromes doivent être clairement distingués et identifiés à temps dans le cadre de la prise en charge. Pour cela, il est toutefois nécessaire de sensibiliser le personnel clinique travaillant dans les soins hospitaliers et ambulatoires et d’établir le bon diagnostic. L’objectif en cardiologie devrait être l’intégration structurée des traitements nutritionnels et la collaboration étroite avec la thérapie nutritionnelle pour les patients souffrant d’insuffisance cardiaque chronique.
Chronic heart failure is one of the most common cardiological diseases and is strongly associated with nutrition-related comorbidities such as disease-related malnutrition, cardiac cachexia, sarcopenia, and frailty. Despite similar pathomechanisms, these syndromes must be distinguished from one another and recognised in good time during treatment. However, this requires raising awareness among clinical staff working in inpatient and outpatient care, as well as accurate diagnosis. The goal should be the structured integration of nutritional treatment procedures in cardiology and close cooperation with nutritional therapy for patients with chronic heart failure.
Keywords: Heart failure, malnutrition, cachexia, sarcopenia, frailty
L’insuffisance cardiaque est un syndrome clinique dû à un dysfonctionnement structurel ou fonctionnel du cœur, qui s’accompagne d’une augmentation de la pression intracardiaque et/ou de symptômes d’insuffisance cardiaque au repos ou à l’effort (1). La prévalence de l’insuffisance cardiaque est d’environ 1 à 3 % de la population et augmente avec l’âge en raison de la fréquence accrue des maladies cardiovasculaires, atteignant jusqu’à 16 % chez les personnes âgées de plus de 80 ans (2). Une perte de poids involontaire et une fonte musculaire, pouvant entraîner des complications telles que la dénutrition, la cachexie, la sarcopénie ou la fragilité (frailty), surviennent notamment aux stades avancés de l’insuffisance cardiaque (3). La détection précoce et le traitement de ces syndromes médicaux (qui sont liés entre eux, mais distincts par définition) se trouvent au premier plan dans les directives actuelles de la Société européenne de cardiologie sur l’insuffisance cardiaque et peuvent avoir une influence significative sur l’évolution de la maladie et la qualité de vie des patients.
Bases physiopathologiques
Une alimentation insuffisante et une perte musculaire croissante chez les patients atteints d’insuffisance cardiaque présentent des caractéristiques physiopathologiques communes (4). Les symptômes typiques de l’insuffisance cardiaque, tels qu’une intolérance accrue à l’effort et un essoufflement, augmentent la consommation d’énergie dans l’organisme, tandis que l’apport nutritionnel est réduit en raison d’une sensation de satiété précoce, de nausées accrues et d’une malabsorption gastro-intestinale due à des œdèmes intestinaux (5). Les restrictions alimentaires souvent recommandées (p. ex. un régime pauvre en sel) et la polypharmacie peuvent accentuer la perte d’appétit. Les adaptations neurohormonales et les réactions inflammatoires systémiques qui surviennent dans le cadre d’une insuffisance cardiaque chronique à un stade avancé de la maladie entraînent également un déséquilibre entre les processus métaboliques anaboliques et cataboliques (6). En particulier chez les patients atteints d’insuffisance cardiaque avancée et de «cachexie cardiaque» en particulier, on observe une augmentation des marqueurs inflammatoires et des modifications hormonales (notamment CRP, TNF-α, IL-6, ghréline, GH/IGF1), qui sont à leur tour associées à des processus métaboliques cataboliques accrus, au stress oxydatif et à une protéolyse accrue (7). Associés à une activité physique réduite et à une résistance à l’insuline, ces processus peuvent également entraîner une «résistance anabolique» dans les muscles, qui inhibe la synthèse des protéines musculaires et augmente la dégradation musculaire (8).
Des maladies chroniques fréquentes (p. ex. le diabète sucré, l’insuffisance rénale ou la BPCO) ainsi que des aspects psychosociaux (p. ex. les déficits cognitifs, la dépression, l’isolement social) sont d’autres facteurs de risque de dénutrition et augmentent la vulnérabilité des patients. La combinaison de ces facteurs fréquents dans le processus pathologique chronique, notamment l’augmentation des besoins énergétiques associée à une réduction de l’apport en nutriments et en protéines, l’augmentation des processus métaboliques cataboliques et l’inactivité physique, entraîne finalement chez les patients atteints d’insuffisance cardiaque un risque accru de développer une dénutrition liée à la maladie, une cachexie d’origine cardiaque, de la sarcopénie et de la fragilité (4).
Dénutrition liée à la maladie
La dénutrition est définie comme un état résultant d’un apport ou d’une absorption insuffisants d’énergie et de nutriments accompagné d’une altération des fonctions physiques et mentales (9). Outre les causes liées à l’âge et au statut socio-économique, la «dénutrition liée à la maladie», avec ou sans inflammation, est prédominante dans notre société. Sa prévalence de la dénutrition liée à la maladie chez les personnes âgées est estimée, selon les outils d’évaluation utilisés, à environ 5 % dans la population générale et entre 20 et 50 % chez les patients hospitalisés (10). Chez des patients souffrant d’insuffisance cardiaque, une dénutrition est également constatée chez plus de 40 % d’entre eux (11). Plusieurs études ont montré qu’un état nutritionnel déficient s’accompagne d’une augmentation significative des taux de morbidité et de mortalité ainsi que d’une diminution de la qualité de vie des patients (12, 13, 14). En revanche, ces dernières années, une évidence croissante tend à prouver que la dénutrition représente un facteur de risque modifiable. L’étude EFFORT publiée en 2019 a confirmé que chez les patients présentant un risque accru de dénutrition, le risque de complications et la mortalité à 30 jours pouvait être considérablement réduit grâce à une thérapie nutritionnelle personnalisée (15). Chez les patients souffrant d’insuffisance cardiaque aiguë, une intervention nutritionnelle pendant et après une hospitalisation a également eu un effet bénéfique sur le pronostic (16). De plus, une prise en charge nutritionnelle chez les patients à risque a permis de réduire la probabilité d’événements cardiaques, la durée des séjours à l’hôpital et le taux de réhospitalisations (17, 18, 19). Ce dernier point peut avoir une influence considérable sur la qualité de vie liée à la santé, en particulier chez les patients souffrant d’insuffisance cardiaque chronique.
Dépistage et diagnostic
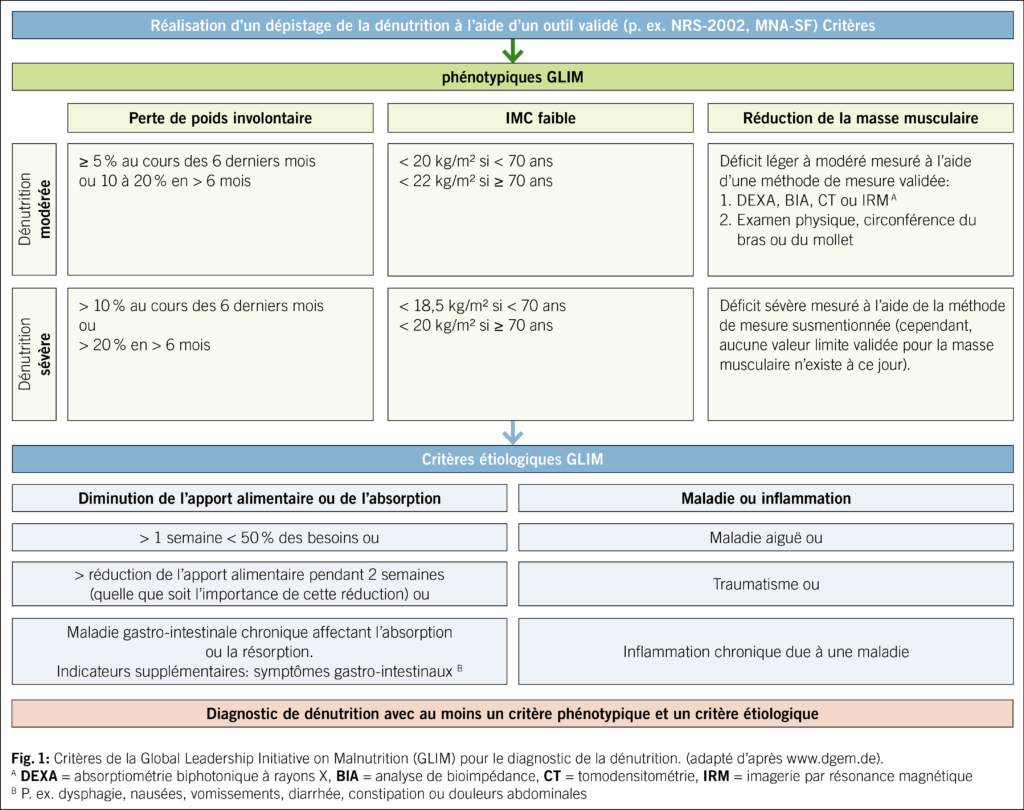
Afin de détecter une éventuelle dénutrition, il est recommandé de procéder dans un premier temps à un dépistage systématique (20). Au cours des dernières décennies, de nombreux outils ont été développés. Outre des paramètres quantifiables (p. ex. le poids, la taille, l’IMC, la perte de poids involontaire), certains d’entre eux évaluent également les risques psychosociaux liés à la dénutrition (p. ex. le stress psychologique, la mobilité au quotidien). Bien que la pertinence et la validité limitées de tous ces instruments doivent être prises en compte, ceux recommandés par l’ESPEN (European Society for Clinical Nutrition and Metabolism), tels que le MUST («Malnutrition Universal Screening Tool», principalement pour les patients non hospitalisés), le MNA ou le MNA-SF («Mini Nutritional Assessment – Short Form», principalement chez les personnes âgées de plus de 65 ans) ou NRS-2002 («Nutrition Risk Screening 2002», principalement chez les patients hospitalisés) permettent d’identifier facilement les personnes présentant un risque accru de dénutrition (21, 22, 23). Chez les patients souffrant d’insuffisance cardiaque, il faut tenir compte des erreurs d’interprétation dues à la rétention d’eau (œdèmes). À ce jour, aucun des instruments utilisés pour détecter le risque ou diagnostiquer la dénutrition n’a été validé chez des patients atteints d’insuffisance cardiaque. Bien que les outils de dépistage mentionnés ci-dessus permettent souvent d’évaluer correctement le risque nutritionnel, même en cas d’insuffisance cardiaque décompensée, l’utilisation d’outils multidimensionnels (p. ex. MNA-SF) avec évaluation d’informations nutritionnelles temporelles et subjectives semble particulièrement importante dans ce groupe de patients (24, 25). En cas de dépistage suspect, il s’agit dans un deuxième temps de vérifier s’il existe effectivement une dénutrition. À cette fin, les critères diagnostiques internationalement standardisés «Global Leadership In Malnutrition» (GLIM) ont été publiés en 2019 (26). Pour diagnostiquer la dénutrition, il faut à la fois un critère phénotypique (perte de poids involontaire, faible IMC, masse musculaire réduite) et un critère étiologique (apport alimentaire réduit ou malassimilation, inflammation ou charge de morbidité élevée). Dans un troisième temps, le degré de gravité de la dénutrition («modérée» ou «sévère») peut être défini (en fonction de l’importance des critères phénotypiques). Il convient toutefois de souligner que les critères GLIM ne remplacent pas une évaluation nutritionnelle professionnelle, car une anamnèse détaillée et une évaluation de l’état nutritionnel sont importantes pour la suite du traitement.
Traitement et suivi
Une fois le diagnostic de dénutrition posé et une évaluation nutritionnelle détaillée réalisée, une intervention nutritionnelle doit être mise en place afin de stabiliser et d’améliorer l’état nutritionnel du patient. Pour ce faire, l’apport alimentaire oral est tout d’abord optimisé moyennant des repas principaux et des collations adaptés individuellement et l’ajout, selon besoin, d’aliments enrichis ou de compléments nutritionnels oraux (CNO) (20). Un suivi et une réévaluation (toutes les 24 à 48 heures) permettent de détecter à un stade précoce les ajustements thérapeutiques éventuellement nécessaires. Les patients qui, après quelques jours, n’atteignent pas au moins 75 % de leurs besoins énergétiques et protéiques déterminés par le biais d’une alimentation orale, doivent recevoir une nutrition entérale supplémentaire et, si leurs besoins ne sont toujours pas couverts, une nutrition parentérale complémentaire (20).
Pour estimer les besoins énergétiques individuels, il est nécessaire de déterminer la dépense énergétique totale (Total Energy Expenditure, TEE), qui se compose du métabolisme basal (Resting Energy Expenditure, REE), de la thermogenèse induite par l’alimentation et des besoins énergétiques liés à l’activité physique. La calorimétrie indirecte étant rarement disponible dans la pratique clinique quotidienne pour mesurer le métabolisme énergétique, on utilise généralement des formules (p. ex. la formule de Harris-Benedict) ou des estimations adaptées au poids (p. ex. 25–30 kcal/kgPC/jour) (20). Ces estimations peuvent constituer une base de départ pour une intervention nutritionnelle, mais doivent être interprétées avec une prudence particulière en raison des écarts fréquents par rapport à la consommation énergétique réelle (27). La quantité de protéines recommandée pour les patients polymorbides est de 1,2 à 1,5 g/kg de poids corporel par jour, à condition qu’il n’y ait pas d’insuffisance rénale grave (DFGe < 30 ml/min/1,73 m²) (20, 28). Dès le début de la prise en charge nutritionnelle, il convient de garantir un apport suffisant en micronutriments pour couvrir les besoins quotidiens et de corriger toute carence documentée par des analyses de laboratoire (20, 29).
Lors du traitement d’une dénutrition, il faut également tenir compte d’un éventuel syndrome de renutrition inappropriée (SRI). Il s’agit d’un trouble potentiellement mortel de l’équilibre électrolytique et hydrique qui survient lorsque la réalimentation (par voie orale, entérale ou parentérale) est trop rapide ou inadéquate (9). Le passage rapide d’un métabolisme catabolique à un métabolisme anabolique peut entraîner, en particulier au cours des 72 premières heures, une hypophosphatémie sévère (réduction > 30 % de la valeur initiale ou < 0,6 mmol/l), à d’autres troubles électrolytiques (notamment une carence en magnésium et en potassium) ou à des déplacements de liquides, qui peuvent à leur tour s’accompagner de troubles fonctionnels cardiorespiratoires, hématologiques et neuromusculaires. En outre, une carence préexistante en thiamine peut se manifester par une acidose lactique, une encéphalopathie de Wernicke ou une insuffisance cardiaque («béribéri humide») (30). Chez les patients à risque (IMC < 18,5 kg/m2, perte de poids > 10 % au cours des 3 à 6 derniers mois, apport alimentaire très faible ou inexistant > 5 jours, abus d’alcool ou de drogues, troubles électrolytiques préexistants), une correction électrolytique et volumique, une supplémentation en thiamine avant le début de la réalimentation ainsi que l’administration d’une préparation multivitaminée et d’oligo-éléments sont importantes. L’apport calorique doit en outre être augmenté progressivement en fonction du risque sur une période de 5 à 10 jours, sous contrôle chimique quotidien initial (30, 31).
Une fois le traitement hospitalier terminé, la poursuite d’un traitement ambulatoire chez les patients présentant un risque nutritionnel ou une dénutrition manifeste constitue un élément essentiel du traitement. L’objectif est de stabiliser le poids corporel et l’état nutritionnel à long terme et d’améliorer ainsi l’état fonctionnel et la qualité de vie (20).
Cachexie cardiaque
La cachexie doit être comprise comme une sous-forme de dénutrition liée à la maladie. Elle décrit un syndrome multifactoriel caractérisé par une perte de poids importante accompagnée d’une diminution de la masse musculaire et du tissu adipeux, ainsi que par une inflammation liée à la maladie (9). Elle survient principalement chez les patients atteints de maladies organiques (p. ex. cancers, BPCO, insuffisance cardiaque chronique ou insuffisance rénale) qui, à un stade avancé, s’accompagnent d’une activité métabolique catabolique. La cachexie cardiaque est définie par une perte de poids supérieure à 5 % du poids corporel en 12 mois (ou un IMC < 20 kg/m2) ainsi que par la présence d’au moins trois autres critères (diminution de la force musculaire, fatigue, anorexie, faible indice de masse maigre ou valeurs de laboratoire anormales avec anémie, marqueurs inflammatoires élevés ou albumine sérique réduite) (32). La prévalence est estimée à environ 5-15 % chez les patients atteints d’insuffisance cardiaque, sans corrélation claire avec la fonction ventriculaire gauche (FEVG) (33, 34, 35). Les patients cachectiques présentent une capacité fonctionnelle réduite, une qualité de vie moindre et une mortalité nettement plus élevée (36, 37). En raison des processus métaboliques inflammatoires et cataboliques chroniques, la cachexie cardiaque ne peut être que partiellement combattue par des interventions nutritionnelles et l’activité physique. Une analyse secondaire de l’étude EFFORT a montré que les patients présentant une inflammation importante (CRP > 100 mg/l) ne bénéficient pas de la même manière d’une thérapie nutritionnelle pendant leur séjour à l’hôpital que les patients présentant des marqueurs inflammatoires plus faibles (38).
Une prise en charge nutritionnelle au moyen d’un régime hypercalorique et riche en protéines associée à un entraînement physique reste néanmoins la mesure thérapeutique la plus importante pour les patients souffrant d’insuffisance cardiaque et présentant une dénutrition ou une cachexie, afin de stabiliser leur poids et d’améliorer leur condition cardiorespiratoire et leur capacité fonctionnelle (39, 40). À l’heure actuelle, il n’existe toutefois aucune recommandation nutritionnelle spécifique pour les patients atteints d’insuffisance cardiaque chronique et de dénutrition ou de cachexie cardiaque. Les sociétés de cardiologie recommandent en cas d’insuffisance cardiaque chronique principalement un régime méditerranéen ou un régime DASH (Dietary Approaches to Stop Hypertension) car ceux-ci présentent les propriétés cardioprotectrices et anti-inflammatoires les plus efficaces (41, 42, 43, 44, 45). Des repas plus fréquents avec des portions plus petites peuvent contribuer à éviter la dyspnée postprandiale et à améliorer l’observance des patients. En cas d’œdèmes, il conviendrait d’envisager une restriction hydrique (1,5 à 2 litres/jour) et une limitation de la consommation de sel (environ 5 g par jour) (1). Toutefois, l’utilité d’une restriction en sel reste controversée en raison de résultats d’études contradictoires et d’effets négatifs éventuels (notamment en raison d’une activation neurohumorale accrue) (46, 47, 48). La supplémentation en acides gras polyinsaturés oméga-3 (AGPI) a également montré des effets positifs sur la fonction ventriculaire gauche, le taux de réhospitalisation et la mortalité dans certaines études, mais ces recommandations ont également été atténuées en raison de données d’études incohérentes et d’un risque potentiellement accru de fibrillation auriculaire (49, 50, 51, 52, 53). En ce qui concerne la substitution en micronutriments, les directives cardiologiques actuelles recommandent l’administration intraveineuse de fer chez les patients atteints d’insuffisance cardiaque avec une fonction ventriculaire gauche réduite (FEVG < 40 %) et une carence en fer (ferritine sérique < 100 ng/ml ou 100-299 ng/ml avec CTS < 20 %) afin d’améliorer leur capacité d’effort et leur qualité de vie (54, 55). Malgré certaines études prometteuses sur d’autres micronutriments ou compléments alimentaires (p. ex. la thiamine, la coenzyme Q10), aucune recommandation claire ne peut être donnée à ce jour concernant la supplémentation en micronutriments chez les patients atteints d’insuffisance cardiaque en raison de l’hétérogénéité des données issues des études (56, 57, 58, 59, 60). En revanche, un traitement médicamenteux à base de bêtabloquants, d’inhibiteurs de l’ECA et d’antagonistes des récepteurs de l’angiotensine II a permis de retarder la perte de poids et le développement d’une cachexie cardiaque, indépendamment de l’amélioration de la fonction ventriculaire gauche (61, 62). D’autres options thérapeutiques possibles, telles que les immunomodulateurs (inhibiteurs du TNF-α), les hormones anabolisantes (ghréline, testostérone) ou les substances stimulant l’appétit, ne sont pas encore utilisées dans la pratique clinique quotidienne pour traiter la cachexie, malgré des résultats positifs isolés dans des études à petite échelle (63).
Sarcopénie et fragilité (frailty)
Les patients atteints d’insuffisance cardiaque chronique souffrent souvent, outre de dénutrition et de cachexie cardiaque, de sarcopénie et d’une fragilité accrue (frailty). La sarcopénie est un syndrome à part entière qui se caractérise par une perte progressive et généralisée de la force et de la masse musculaires (indépendamment de la masse grasse) et qui s’accompagne de conséquences négatives telles qu’une tendance aux chutes et des limitations fonctionnelles (64). Cette perte survient dans le cadre du processus naturel de vieillissement, mais elle est aggravée par des processus inflammatoires et hormonaux liés à la maladie, une activité physique réduite et une dénutrition (en particulier due à un apport insuffisant en protéines) (65, 66). La prévalence chez les patients atteints d’insuffisance cardiaque est estimée entre 10 % et 69 % selon les critères d’inclusion (67). En l’absence de signes cliniques typique faisant suspecter une sarcopénie, le dépistage en 5 points (SARC-F) est recommandé, dont la sensibilité peut être améliorée par la mesure du tour du mollet (68, 69). Une mesure de la force de préhension à l’aide d’un dynamomètre ou, à défaut, la mesure de la force musculaire des jambes à l’aide du «Chair-Stand-Test» peut confirmer un diagnostic présumé (force de préhension < 16 kg pour les femmes et < 27 kg pour les hommes, Chair-Stand-Test < 15 secondes) (64). Pour établir le diagnostic définitif, on procède ensuite à la mesure de la masse musculaire (masse maigre appendiculaire, ALM), pour laquelle on peut utiliser l’analyse d’impédance bioélectrique (BIA), l’absorptiométrie biphotonique à rayons X (DEXA) ou des techniques d’imagerie (IRM, CT). En cas d’indice relatif de masse musculaire squelettique (SMI) < 5,5 kg/m2 chez les femmes ou < 7 kg/m2 chez les hommes, la sarcopénie est confirmée (64). La classification du degré de gravité peut être effectuée à l’aide d’examens fonctionnels supplémentaires (vitesse de marche, test Timed-up-and-go, SPPB ou test de marche de 400 m) (64). Le simple constat d’une force musculaire réduite devrait déjà inciter à rechercher les causes et à commencer un traitement. À cet égard, plusieurs études ont montré que la combinaison d’un entraînement en force (musculation) et d’un apport accru en protéines peut avoir des effets positifs sur la prévention et le traitement de la sarcopénie (70, 71, 72, 73, 74). La substitution de protéines à forte teneur en leucine (p. ex. les protéines de lactosérum) serait associée à d’autres effets positifs sur la synthèse des protéines musculaires (75, 76).
La fragilité (frailty) est souvent considérée comme un syndrome biologique ou gériatrique caractérisé par une perte des fonctions physiques et des capacités cognitives. Son diagnostic repose principalement sur les critères phénotypiques définis par Fried (3 critères sur 5: perte de poids involontaire > 5 kg/an, diminution de la force musculaire ou manuelle, lenteur de la marche, réduction de l’activité physique, sensation subjective d’épuisement) et sur le modèle déficitaire de Rockwood (détermination d’un indice de fragilité à partir des limitations fonctionnelles, cognitives et sociales) (77, 78). Il convient toutefois de souligner que la fragilité ne doit pas être considérée uniquement comme un processus physiologique lié à l’âge. Les patients souffrant d’insuffisance cardiaque en particulier, présentent très souvent un état indépendant de l’âge, qui comprend des domaines cliniques, fonctionnels, cognitifs, psychologiques et sociaux, entraînant une vulnérabilité accrue aux facteurs de stress endogènes ou exogènes (p. ex. inflammations légères, interventions mineures, ajustements médicamenteux) (79). La présence d’une fragilité est donc un facteur supplémentaire qui influence négativement le pronostic des patients atteints d’insuffisance cardiaque en raison de taux de morbidité et de mortalité plus élevés (80, 81, 82).
Dans le cadre du traitement, il est donc judicieux d’identifier précocement ce groupe de patients vulnérables à l’aide d’outils d’évaluation multidimensionnels (p. ex. Clinical Frailty Scale, Essential Frailty Toolset) afin de traiter de manière adéquate les facteurs potentiellement réversibles tels que la dénutrition ou la sarcopénie par des interventions nutritionnelles individuelles et un entraînement physique, idéalement dans le cadre d’une réadaptation cardiaque (83, 84, 85).
Conclusion
En résumé, dans le traitement des patients atteints d’insuffisance cardiaque chronique, il est essentiel que la thérapie ne se limite pas à des mesures interventionnelles ou médicamenteuses. La détection précoce de la dénutrition liée à la maladie et des syndromes associés fréquents tels que la cachexie cardiaque, la sarcopénie ou la fragilité (frailty) est d’une importance capitale pour l’évolution de la maladie et du traitement. C’est pourquoi la mise en place de protocoles thérapeutiques structurés intégrant des interventions nutritionnelles, la sensibilisation et la formation systématique du personnel clinique ainsi qu’une collaboration étroite avec les spécialistes en thérapie nutritionnelle devraient faire partie intégrante du traitement de l’insuffisance cardiaque chronique.
Copyright
Aerzteverlag medinfo AG
Cet article est une traduction de «der informierte arzt – die informierte ärztin» 02_2026
Spécialiste en cardiologie et
médecine interne générale,
Responsable de la réadaptation
cardiovasculaire stationnaire
Inselspital, Centre de réadaptation et de médecine sportive
Freiburgstrasse 18, 3010 Berne
L’auteur n’a pas déclaré de conflit d’intérêts en rapport avec cet article.
La dénutrition, la cachexie, la sarcopénie et la fragilité sont des syndromes concomitants fréquents, souvent négligés, de l’insuffisance cardiaque chronique et sont directement liés à une morbidité et une mortalité accrues ainsi qu’à une qualité de vie réduite.
Le diagnostic de la dénutrition doit suivre une approche en trois étapes: dépistage (p. ex. MNA-SF, NRS-2002), confirmation du diagnostic selon les critères GLIM, puis évaluation nutritionnelle complète pour planifier le traitement.
La combinaison d’une thérapie nutritionnelle personnalisée, d’un entraînement physique et d’une prise en charge multiprofessionnelle, idéalement dans le cadre d’un programme de réadaptation structuré, est essentielle pour améliorer durablement la qualité de vie et le pronostic des patients atteints d’insuffisance cardiaque.
1. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021 Sep 21;42(36):3599-3726.
2. Savarese G, Becher PM, Lund LH, Seferovic P, Rosano GMC, Coats AJS. Global burden of heart failure: a comprehensive and updated review of epidemiology. Cardiovasc Res. 2023 Jan 18;118(17):3272-3287.
3. Saitoh M, Ishida J, Doehner W, von Haehling S, Anker MS, Coats AJS, Anker SD, Springer J. Sarcopenia, cachexia, and muscle performance in heart failure: Review update 2016. Int J Cardiol. 2017 Jul 1;238:5-11.
4. Fernández-Pombo A, Rodríguez-Carnero G, Castro AI, et al. Relevance of nutritional assessment and treatment to counteract cardiac cachexia and sarcopenia in chronic heart failure. Clin Nutr. 2021 Sep;40(9):5141-5155.
5. Sandek A, Bauditz J, Swidsinski A, et al. Altered intestinal function in patients with chronic heart failure. J Am Coll Cardiol. 2007 Oct 16;50(16):1561-9.
6. Rahman A, Jafry S, Jeejeebhoy K, Nagpal AD, Pisani B, Agarwala R. Malnutrition and Cachexia in Heart Failure. JPEN J Parenter Enteral Nutr. 2016 May;40(4):475-86.
7. Martins T, Vitorino R, Amado F, Duarte JA, Ferreira R. Biomarkers for cardiac cachexia: reality or utopia. Clin Chim Acta. 2014 Sep 25;436:323-8.
8. Morton RW, Traylor DA, Weijs PJM, Phillips SM. Defining anabolic resistance: implications for delivery of clinical care nutrition. Curr Opin Crit Care. 2018 Apr;24(2):124-130.
9. Cederholm T, Barazzoni R, Austin P, et al. ESPEN guidelines on definitions and terminology of clinical nutrition. Clin Nutr. 2017 Feb;36(1):49-64.
10. Kaiser MJ, Bauer JM, Rämsch C, et al. Mini Nutritional Assessment International Group. Frequency of malnutrition in older adults: a multinational perspective using the mini nutritional assessment. J Am Geriatr Soc. 2010 Sep;58(9):1734-8.
la gazette médicale
- Vol. 15
- Ausgabe 3
- Mai 2026