- Psychostimulants et vieillissement – repenser le traitement du TDAH tardif
Le trouble du déficit de l’attention avec ou sans hyperactivité (TDAH) est un trouble neurodéveloppemental fréquent pouvant persister jusqu’à un âge avancé. Sa prise en charge chez la population gériatrique demeure peu documentée et codifiée. En pratique clinique, le traitement pharmacologique du TDAH tend, pour des raisons essentiellement assécurologiques, à s’interrompre avant 60 ans, alors même que les symptômes persistent dans la majorité des cas. L’utilisation de psychostimulants chez le sujet âgé soulève des questions de pertinence et de risque cardiovasculaire. Cet article propose une approche clinique de l’utilisation de psychostimulants chez le sujet âgé.
Attention-deficit/hyperactivity disorder (ADHD) is a common neurodevelopmental disorder that may persist into older age. However, its management in the geriatric population remains poorly documented and insufficiently standardized. In clinical practice, pharmacological treatment of ADHD often tends to be discontinued before the age of 60, mainly for insurance-related reasons, even though symptoms persist in most cases. The use of psychostimulants in older adults raises questions regarding their clinical relevance and potential cardiovascular risks. This article proposes a clinical approach to the use of psychostimulants in older adults.
Keywords: TDAH, Méthylphénidate, Risque cardiovasculaire, Psychiatrie gériatrique, Bonne pratique
Introduction
Le trouble du déficit de l’attention avec ou sans hyperactivité (TDAH) est caractérisé par une triade associant inattention persistante, hyperactivité et impulsivité (1). Le TDAH débute durant l’enfance et peut persister à l’âge adulte, avec parfois une diminution progressive de l’intensité symptomatique au fil du temps (2). Chez certains patients, des symptômes cliniquement significatifs peuvent être observés à un âge avancé, bien que les données spécifiques au-delà de 65 ans restent limitées.
Chez l’adulte, l’intensité des symptômes n’est pas homogène au cours de la vie. Elle peut être modulée par des facteurs environnementaux. En particulier, l’activité professionnelle, lorsqu’elle s’exerce dans des environnements structurés et hautement stimulants, peut constituer un facteur de compensation partielle du TDAH pendant de nombreuses années. À l’inverse, l’arrêt de cette stimulation structurante à l’âge de la retraite peut révéler ou majorer des symptômes jusque-là contenus. Cette observation clinique est cohérente avec les modèles d’autorégulation du TDAH, qui soulignent l’importance des contraintes environnementales et des renforcements externes dans la modulation symptomatique (3). Avec l’avancée en âge, les structures de soutien qui ont permis à certains adultes atteints de TDAH de s’adapter peuvent progressivement s’effriter, voire disparaître, notamment en cas de perte ou de maladie du conjoint, de départ des enfants jouant un rôle de soutien, ou de réduction des capacités à maintenir une activité physique régulière. Ces changements peuvent contribuer à une décompensation tardive des symptômes. Par ailleurs, le vieillissement s’accompagne d’une diminution progressive de la flexibilité et des réserves cognitives, ce qui peut réduire les capacités de compensation face aux exigences attentionnelles et exécutives (4). Chez les personnes présentant un TDAH sous-jacent, cette réduction des ressources cognitives peut ainsi favoriser l’émergence ou l’aggravation progressive des symptômes.
Chez les femmes, certaines périodes de transition hormonale, comme la préménopause et la ménopause, pourraient également influencer l’expression des symptômes. Les œstrogènes modulent en effet les processus cognitifs dépendants de la dopamine, notamment les fonctions exécutives et l’attention, suggérant que leur diminution pourrait contribuer à une majoration des symptômes du TDAH (5).
Sur le plan épidémiologique, la prévalence du TDAH est estimée en Europe entre 2 et 4 % chez l’adulte (6). En revanche, les données concernant les sujets âgés demeurent limitées. Cette lacune s’explique en grande partie par un sous-diagnostic historique du TDAH dans cette population. Celui-ci est lié à une reconnaissance tardive du trouble et à des biais de cohorte, les générations plus âgées n’ayant pas bénéficié des critères diagnostiques actuels (1).
La prise en charge du TDAH repose sur une approche multimodale, au sein de laquelle le traitement pharmacologique occupe une place centrale. Les recommandations cliniques européennes soulignent la place centrale du traitement pharmacologique dans la prise en charge du TDAH chez l’adulte. Les psychostimulants constituent les traitements de première intention, le méthylphénidate étant recommandé comme molécule de premier choix en Suisse en raison de son efficacité démontrée et de son profil de tolérance globalement favorable (7). En Suisse, la lisdexamfétamine est l’autre psychostimulant disponible pour traiter le TDAH chez l’adulte, généralement utilisé lorsque le méthylphénidate n’est pas suffisamment efficace ou mal toléré. Le problème qui se pose est que ces données reposent majoritairement sur des populations jeunes ou d’âge moyen. Leur extrapolation aux patients âgés demeure donc incertaine pour les cliniciens. Ce constat soulève la question de la place et de la sécurité d’utilisation du méthylphénidate et de la lisdexamphétamine chez les sujets âgés. Dans ce contexte, cet article se focalise sur l’utilisation de formulations à base de méthylphénidate chez les patients de plus de 65 ans, en mettant l’accent sur les données disponibles concernant leur tolérance et leur sécurité d’emploi. Le terme méthylphénidate sera utilisé dans le reste de l’article.
TDAH et vieillissement: une réalité clinique sous-estimée
En pratique clinique, les psychiatres prenant en charge des patients âgés de plus de 65 ans présentant un TDAH se heurtent à deux obstacles majeurs lorsqu’un traitement par méthylphénidate est envisagé. Le premier concerne les limitations de remboursement en Suisse pour cette tranche d’âge. En effet, certaines formulations à courte durée d’action ne sont remboursées que chez l’enfant et l’adolescent (par exemple la Ritaline ou le Medikinet), tandis que plusieurs formulations à libération prolongée (telles que la Concerta ou la Focaline) ne sont remboursées que jusqu’à l’âge de 65 ans. Ces restrictions limitent l’accès au traitement chez les patients plus âgés. Le second relève des préoccupations relatives à la sécurité cardiovasculaire, notamment le risque d’infarctus du myocarde, d’accident vasculaire cérébral ou d’arythmie chez des patients perçus comme fragilisés par l’âge.
Si l’argument de la productivité et de l’apprentissage est fréquemment avancé dans la prise en charge du TDAH chez l’enfant et l’adulte jeune, les enjeux chez le sujet âgé ne se limitent pas à la performance cognitive. Le TDAH s’accompagne fréquemment d’impulsivité persistante et d’une labilité émotionnelle marquée, avec des répercussions significatives sur les relations interpersonnelles (3). Ne pas traiter efficacement un patient âgé atteint de TDAH peut contribuer à un isolement social, favoriser la survenue de comorbidités psychiatriques telles que les épisodes dépressifs caractérisés ou les troubles anxieux, et altérer l’hygiène de vie (8). Certaines données suggèrent par ailleurs une association entre TDAH tardif et maladies physiques chroniques ainsi qu’une perception subjective de santé plus défavorable (8).
La question du traitement du TDAH chez le sujet âgé ne se résume pas à une simple évaluation du risque médicamenteux, mais doit intégrer les conséquences fonctionnelles, psychologiques et sociales d’une absence de prise en charge.
Le risque cardiovasculaire: une crainte légitime mais parfois disproportionnée
L’évaluation du risque cardiovasculaire constitue l’un des principaux freins à l’utilisation des psychostimulants chez le sujet âgé. Cette prudence est légitime dans une population dont le risque cardiovasculaire de base augmente avec l’âge (9).
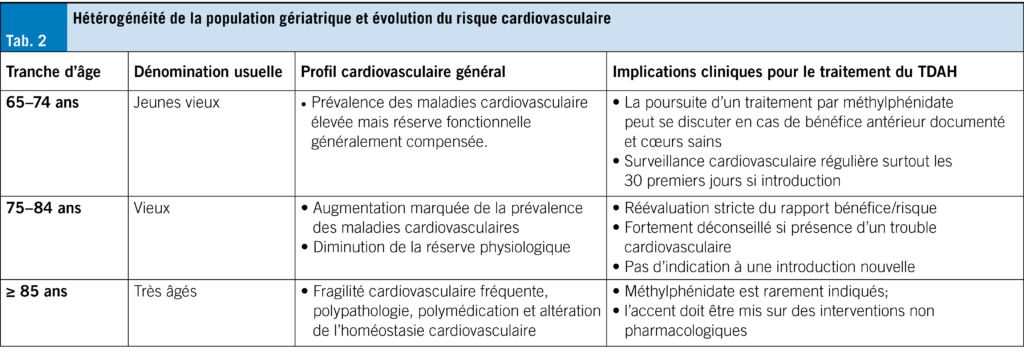
Avant tout, il convient de ne pas considérer les patients gériatriques comme un ensemble homogène. La littérature distingue classiquement les 65–74 ans («jeunes vieux»), les 75–84 ans et les sujets de 85 ans et plus (9).
À mesure que l’âge avance, la réserve physiologique diminue et la prévalence des comorbidités cardiovasculaires augmente, ce qui peut réduire la tolérance aux substances susceptibles d’augmenter la fréquence cardiaque et la pression artérielle.
De grandes cohortes longitudinales ont montré une augmentation marquée de l’incidence de la fibrillation auriculaire, des accidents vasculaires cérébraux et de l’insuffisance cardiaque avec l’avancée en âge, en particulier après 75 ans (10). Une revue synthétique souligne également l’augmentation de la charge cardiovasculaire après 75 ans, en lien avec la rigidification artérielle et l’altération de la fonction diastolique, éléments clés de la vulnérabilité cardiovasculaire du sujet âgé (10).
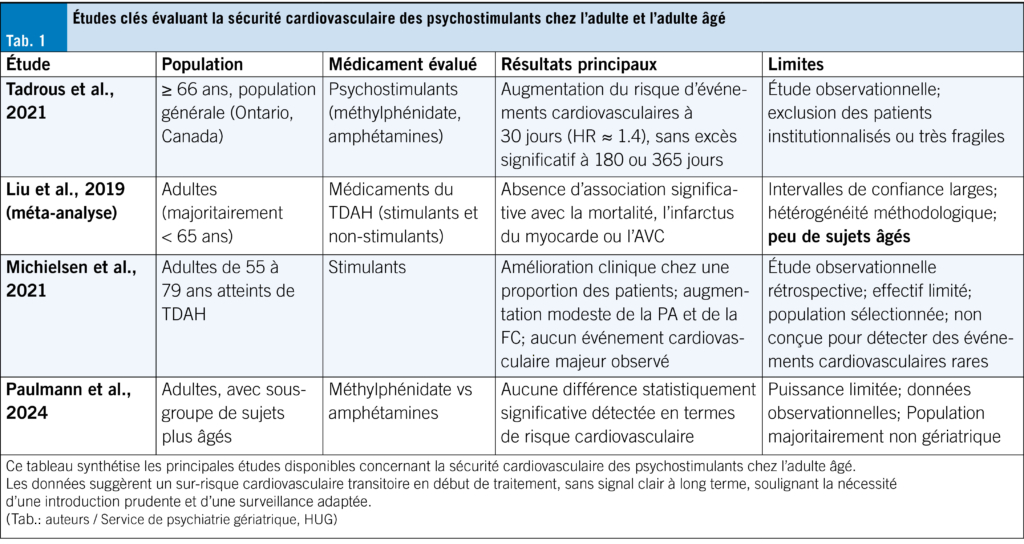
Néanmoins, plusieurs autres études menées chez les personnes âgées rapportent des résultats nuancés et hétérogènes concernant le risque cardiovasculaire associé à la prise de psychostimulants. L’étude de Tadrous et al., menée sur une large cohorte de sujets âgés de 66 ans et plus, montre que l’initiation d’un traitement stimulant est associée à une augmentation modérée du risque cardiovasculaire au cours des 30 premiers jours (HR ≈ 1,4), sans excès de risque significatif à 6 ou 12 mois. Le surrisque apparaît donc précoce et transitoire. Il est important de rappeler que les patients inclus présentaient fréquemment une hypertension artérielle, un diabète ou des antécédents cardiovasculaires, tandis que les sujets les plus fragiles étaient exclus (11). D’autres méta-analyses invitent à une vigilance clinique, sans mettre en évidence d’augmentation claire du risque de mort subite, d’arythmie, d’accident vasculaire cérébral, d’infarctus du myocarde ou de mortalité globale sous traitement du TDAH. Un léger surrisque, en particulier pour les troubles du rythme, ne peut être totalement exclu (12). Des signaux similaires ont également été rapportés dans des populations plus jeunes traitées par psychostimulants, notamment dans une cohorte d’adultes exposés au méthylphénidate (13), suggérant que ce phénomène ne semble pas spécifique au sujet âgé.
En conclusion, chez les adultes plus âgés, les psychostimulants semblent globalement bien tolérés lorsqu’ils sont prescrits avec prudence, même si des essais contrôlés restent nécessaires pour confirmer ces observations (14). Les différentes études disponibles plaident en faveur d’une vigilance, reposant sur une évaluation cardiovasculaire initiale et un suivi régulier de la fréquence cardiaque et de la pression artérielle (Tab. 1).
Approche clinique décisionnelle chez le sujet âgé
La question de l’efficacité du méthylphénidate chez le sujet âgé se pose légitimement. Les recommandations européennes chez l’adulte ne rapportent pas de diminution de l’efficacité des psychostimulants avec l’âge, malgré le manque de données spécifiques chez les personnes âgées (7). Au vu des données disponibles dans la littérature et de notre expérience clinique, l’exclusion systématique du méthylphénidate chez le sujet âgé ne paraît pas justifiée sur le seul critère de l’âge chronologique. Il convient de distinguer au moins deux profils cliniques.
Le premier concerne les patients diagnostiqués avant 65 ans, ayant bénéficié d’un traitement psychostimulant avec une bonne tolérance et un bénéfice fonctionnel clair. Chez ces patients, la question porte principalement sur la poursuite du traitement après 60–65 ans, dans une logique de réévaluation régulière du rapport bénéfice/risque et de surveillance cardiovasculaire adaptée.
Le second profil correspond aux patients jamais diagnostiqués auparavant et sollicitant un bilan tardif. Si le diagnostic est confirmé, l’introduction d’un traitement psychostimulant ne nous paraît généralement pas indiquée en première intention. Le fait qu’un patient ait pu maintenir un fonctionnement personnel et socioprofessionnel stable jusqu’à un âge avancé suggère souvent une sévérité modérée du trouble ou la mise en place de stratégies compensatoires efficaces. Dans ce contexte, l’exposition à un traitement stimulant, au regard du risque cardiovasculaire croissant avec l’âge, doit être discutée avec prudence et réservée aux situations de retentissement fonctionnel marqué ou de trajectoire de vie chaotique.
D’un autre côté, il est vrai que l’âge ne peut être totalement ignoré dans la prise de décision. Nous avons déjà affirmé plus haut qu’un patient de 65 ans ne présente pas le même profil de risque cardiovasculaire qu’un patient de 85 ans. L’indication d’un traitement psychostimulant ainsi que l’intensité de la surveillance doivent donc être adaptées à l’âge et aux comorbidités du patient, en particulier aux âges très avancés (Tab. 2).
La surveillance cardiovasculaire fait déjà partie des recommandations internationales standards lors de l’initiation d’un traitement stimulant, indépendamment de l’âge (15).
En cas de profil cardiovasculaire, l’introduction d’un psychostimulant doit être évitée ou discutée de manière collégiale. Une concertation interdisciplinaire permet de sécuriser la décision thérapeutique et d’adapter la prise en charge aux spécificités du patient âgé. Les facteurs liés au mode de vie: tabagisme actif, obésité, sédentarité doivent également être intégrés dans la balance bénéfice/risque.
Modalités pratiques et précautions de prescription
Chez le sujet âgé, les formes à libération prolongée (LP) sont à privilégier afin de limiter les fluctuations plasmatiques, réduire les pics tensionnels et éviter un rebond symptomatique vespéral. Le traitement débute à faible dose, à 5–10 mg/j de méthylphénidate, selon le principe «start low, go slow». Les données observationnelles suggérant un surrisque cardiovasculaire précoce après l’initiation des psychostimulants chez les sujets âgés (11) plaident en faveur d’une titration lente, avec une réévaluation clinique attentive au cours du premier mois. Une période d’observation prolongée, de l’ordre de minimum quatre semaines, permet d’évaluer la tolérance et le bénéfice clinique avant toute adaptation posologique. Une augmentation progressive peut être envisagée en cas de réponse insuffisante, en tenant compte du profil individuel du patient.
Les modifications pharmacocinétiques et pharmacodynamiques liées au vieillissement peuvent contribuer à une réponse clinique obtenue à des posologies plus faibles que chez l’adulte plus jeune, justifiant une titration prudente et individualisée.
Un ECG de base est recommandé avant l’instauration du traitement, avec exclusion préalable d’un glaucome ou d’une hyperthyroïdie. Une surveillance régulière de la pression artérielle et de la fréquence cardiaque est indiquée, en particulier durant les premières semaines de traitement.
Les effets indésirables sont le plus souvent légers et transitoires, dominés par une diminution de l’appétit et des troubles du sommeil. Une surveillance pondérale est recommandée. En cas d’insomnie, la mélatonine peut être proposée, tandis que les benzodiazépines sont à éviter en raison du risque de chute et de confusion.
Repenser un traitement passe par un bon diagnostic
Chez le sujet âgé, le diagnostic de trouble du déficit de l’attention avec ou sans hyperactivité (TDAH) doit être posé avec une prudence particulière. À cet âge, le diagnostic différentiel avec un trouble neurocognitif, en particulier d’origine neurodégénérative, s’impose de manière immédiate (1).
De façon classique, la maladie d’Alzheimer, qui constitue le trouble neurodégénératif le plus fréquent, affecte en premier lieu la mémoire épisodique plutôt que l’attention dans ses phases initiales (16). Les plaintes attentionnelles chez le sujet âgé peuvent également relever d’un épisode dépressif, d’un trouble anxieux ou encore du vieillissement cognitif normal.
Dans ce contexte, poser un diagnostic de TDAH après 65 ans constitue un véritable défi clinique et exige une démarche diagnostique rigoureuse. Le caractère neurodéveloppemental du TDAH impose de rechercher la présence de symptômes dès l’enfance ou l’adolescence, leur persistance au cours de la vie ainsi que leurs expressions dans plusieurs contextes de vie.
Il convient de préciser qu’un trouble neurocognitif n’exclut pas la présence d’un TDAH, les deux entités pouvant coexister chez un même patient (8).
Enfin, le traitement du TDAH ne saurait être exclusivement pharmacologique. Il implique également des interventions environnementales et comportementales, parmi lesquelles le maintien d’une activité physique régulière, reconnue pour ses effets bénéfiques sur les systèmes dopaminergiques (17), une psychoéducation sur le TDAH ainsi qu’une psychothérapie cognitivo-comportementale.
Copyright
Aerzteverlag medinfo AG
Médecin chef de clinique
Hôpitaux universitaires de Genève (HUG)
Département de psychiatrie – Service de psychiatrie gériatrique – Centre
ambulatoire de psychiatrie et de psychothérapie de l’âgé
Faculté de médecine – Université de Genève
Rue des Épinettes 10, 1227 Carouge, Suisse
Chef de service
Hôpitaux universitaires de Genève (HUG)
Département de psychiatrie – Service des mesures institutionnelles
Faculté de médecine – Université de Genève
Rue Gabrielle-Perret-Gentil 4, 1205 Geneva
Chef de service
Hôpitaux universitaires de Genève (HUG)
Département de psychiatrie – Service de psychiatrie gériatrique
Faculté de médecine – Université de Genève
Chemin du Petit-Bel-Air 2, 1226 Thônex, Suisse
Oussama Latroche n’a aucun conflit d’intérêt à déclarer.
Nader Perroud a reçu des honoraires pour des conférences soutenues par Takeda, Salmon-Pharma/Medice.
Paul Unschuld n’a aucun conflit d’intérêt à déclarer.
Le TDAH peut persister après 65 ans et avoir un retentissement fonctionnel significatif.
La poursuite du méthylphénidate peut être envisagée entre 65 et 74 ans chez des patients ayant un diagnostic établi, un bénéfice fonctionnel antérieur documenté et une bonne tolérance, sous réserve d’une titration lente et surveillance cardiovasculaire.
L’initiation tardive d’un psychostimulant doit rester exceptionnelle et limitée aux situations de retentissement fonctionnel majeur.
1. DSM-5. Diagnostic and statistical manual of mental disorders. 5th ed. Washington (DC): American Psychiatric Association; 2013.
2. Faraone SV, Biederman J, Mick E. The age-dependent decline of attention deficit hyperactivity disorder: a meta-analysis of follow-up studies. Psychol Med. 2006;36(2):159–165. doi:10.1017/S003329170500471X.
3. Servera-Barceló M. Barkley’s model of self-regulation applied to attention deficit hyperactivity disorder: a review [Article in Spanish]. Rev Neurol. 2005 Mar;40(6):358–368. PMID:15795873.
4. Stern Y. Cognitive reserve. Neuropsychologia. 2009;47(10):2015-2028. doi:10.1016/j.neuropsychologia.2009.03.004
5. Jacobs E, D’Esposito M. Estrogen shapes dopamine-dependent cognitive processes: implications for women’s health. J Neurosci. 2011;31(14):5286–5293. doi:10.1523/JNEUROSCI.6394-10.2011.
6. Fayyad J, Sampson NA, Hwang I, et al. The descriptive epidemiology of DSM-IV adult ADHD in the World Health Organization World Mental Health Surveys. Biol Psychiatry. 2017;82(6):444–453. doi:10.1016/j.biopsych.2016.08.026
7. Banaschewski T, et al. European consensus statement on diagnosis and treatment of adult ADHD. Eur Psychiatry. 2017;44:103–115. doi:10.1016/j.eurpsy.2017.03.007
8. Semeijn EJ, Korten NC, Comijs HC, et al. ADHD in older adults: a hidden diagnosis. Eur Psychiatry. 2015;30(6):736–742. doi:10.1016/j.eurpsy.2015.05.007.
9. Baltes PB, Smith J. New frontiers in the future of aging: from successful aging to the young-old and the oldest-old. Gerontology. 2003;49(2):123–135.
10. Yazdanyar A, Newman AB. The burden of cardiovascular disease in the elderly. Clin Geriatr Med. 2009;25(4):563–577. doi:10.1016/j.cger.2009.07.007.
11. Tadrous M, Shakeri A, Chu C, et al. Assessment of Stimulant Use and Cardiovascular Event Risks Among Older Adults. JAMA Netw Open. 2021;4(10):e2130795.
12. Liu H, Feng W, Zhang D. Association of ADHD medications with the risk of cardiovascular diseases: a meta-analysis. Eur Child Adolesc Psychiatry. 2019;28(10):1283-1293. doi:10.1007/s00787-018-1217-x
13. Schelleman H, Bilker WB, Kimmel SE, Daniel GW, Newcomb C, Guevara JP, et al. Methylphenidate and risk of serious cardiovascular events in adults. Am J Psychiatry. 2012;169(2):178-85. doi:10.1176/appi.ajp.2011.11010125.
14. Michielsen M, Kleef D, Bijlenga D, Zwennes C, Dijkhuizen K, Smulders J, Hazewinkel A, Beekman ATF, Kooij JJS. Response and side effects using stimulant medication in older adults with ADHD: an observational archive study. J Atten Disord. 2021 Oct;25(12):1712–1719. doi:10.1177/1087054720925884
15. National Institute for Health and Care Excellence (NICE). Attention deficit hyperactivity disorder: diagnosis and management (NG87). London: NICE; 2018 (updated 2019).
16. Dubois B, Feldman HH, Jacova C, DeKosky ST, Barberger-Gateau P, Cummings J, et al. Advancing research diagnostic criteria for Alzheimer’s disease: the IWG-2 criteria. Lancet Neurol. 2014;13(6):614–629. doi:10.1016/S1474-4422(14)70090-0.
17. Semeijn EJ, Kooij JJS, Michielsen M, Bijlenga D, Deeg DJH, Beekman ATF. Attention-deficit/hyperactivity disorder, physical health, and lifestyle in older adults. J Atten Disord. 2013;17(7):559–567. doi:10.1177/1087054712439562.
la gazette médicale
- Vol. 15
- Ausgabe 3
- Mai 2026