- Polypharmazie
1. Einführung
Die Guideline (GL) «Polypharmazie» des Departements für Innere Medizin (DIM) des Universitätsspitals Zürich (USZ) soll Hilfestellung geben, um die Behandlung von älteren und multimorbiden Patienten zu verbessern. Die GL möchte praktische Anleitungen für den optimierten Umgang mit Polypharmazie in dieser vulnerablen Patientenpopulation bereitstellen. Das Vorgehen kann in einen logischen Ablauf von fünf Schritten ( Kap. 2.1. bis 2.5.) gebracht werden.
Für die kritische Evaluation jedes einzelnen Medikamentes mit der Frage, ob es nicht besser abgesetzt oder reduziert werden soll, stellt diese GL einen einfachen Algorithmus vor ( Kap. 3) sowie Vorschläge für die Gesprächsführung rund um «Deprescribing» inklusive der Entscheidungsfindung.
In der GL wurde die aktuelle Evidenzlage bei Definition, Epidemiologie, Folgen/Risiken und beim Umgang mit Polypharmazie/Deprescribing berücksichtigt. Zusammenfassend zeigen die Studien, dass durch kritisches Überprüfen von Medikationslisten die Anzahl Medikamente leicht reduziert werden kann. Allerdings ist der Evidenzgrad der Studien weiterhin gering. Der Nutzen solcher Interventionen auf klinisch relevante Endpunkte kann weiterhin nicht zuverlässig nachgewiesen werden. Dies soll aber nicht dazu verleiten, dem individuellen Patienten eine kritische Medikamentenüberprüfung vorzuenthalten.
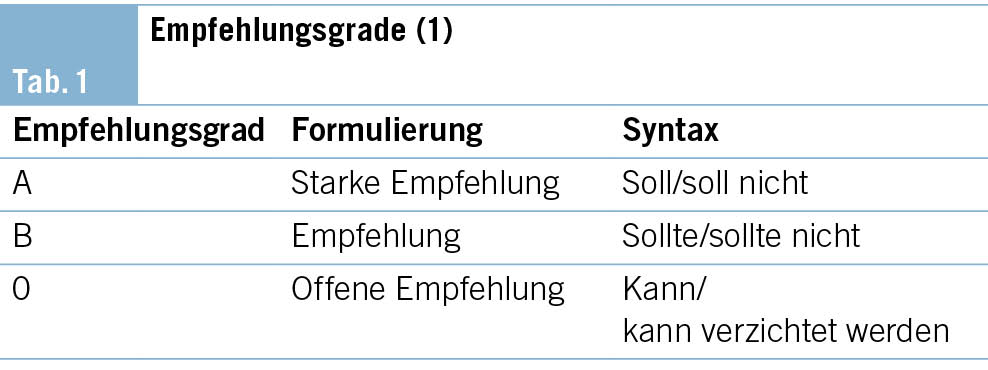
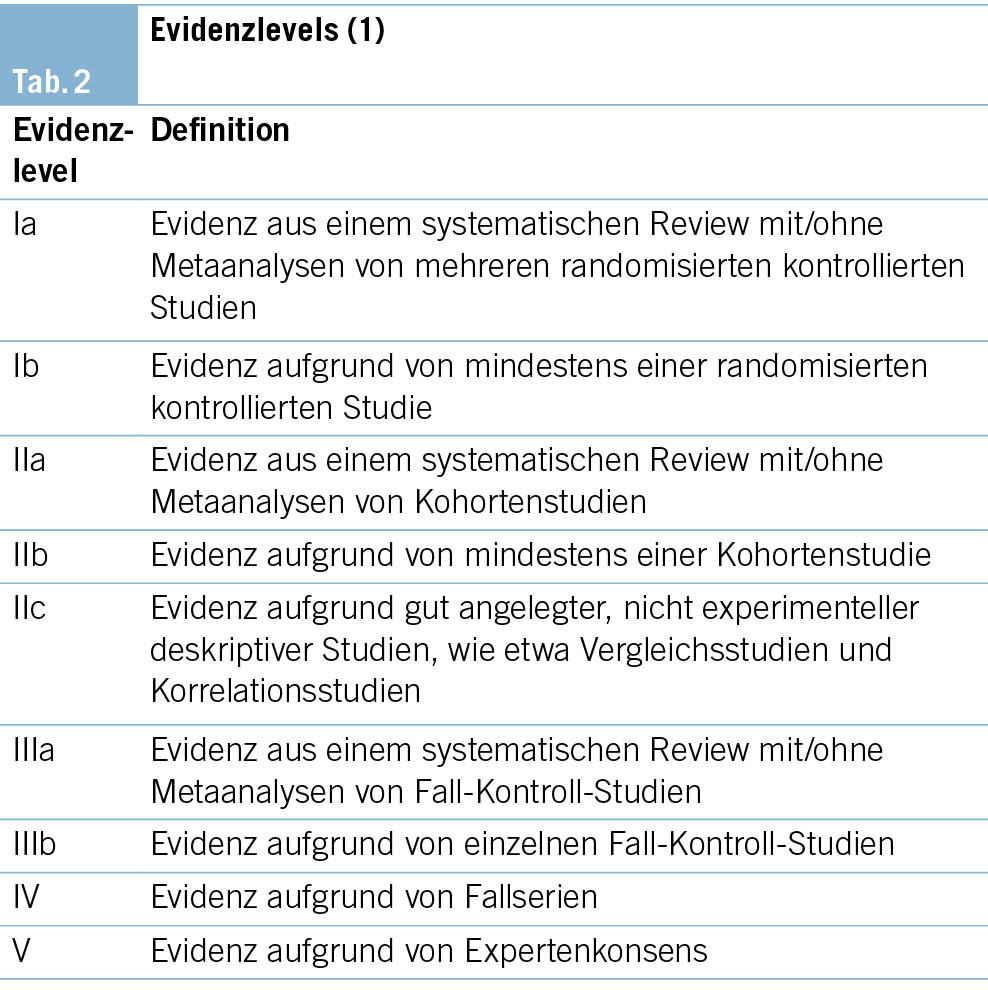
Die vorliegende DIM-GL verwendet die S3-Leitlinie «Multimedikation» der Deutschen Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM) (1) als Quell-Leitlinie und weist für ihre Vorgehensweisen bei Polypharmazie die Empfehlungsstärke (Tab. 1) und Evidenzlevels (Qualität der wissenschaftlichen Grundlage, Tab. 2) analog deren Klassifizierungssystem aus (zum Beispiel: [A/IIIa] ). Zur Definition, für welche Patientenpopulation die Empfehlungsgrade und Evidenzlevels gelten, siehe ( Kap. 2.1.).
Weitere Informationen zur Methodik der Guideline-Erstellung des DIM finden sich auf der Homepage www.guidelines-schweiz.ch.
Ausgangslage
• Mit steigendem Alter steigt die Anzahl chronischer Krankheiten, und es resultiert Multimorbidität.
• Wenn multimorbide Patienten unkritisch nach krankheitsspezifischen Guidelines behandelt werden, resultiert daraus eine Polypharmazie (2).
• Im Sinne von evidence-based medicine soll für die Behandlung älterer und multimorbider Menschen nicht nur die krankheitsspezifische Evidenz, sondern auch die klinische Erfahrung und die individuellen Bedürfnisse der Patienten wegweisend sein (3).
• Um eine bestmögliche Lebensqualität der multimorbiden Patienten zu erreichen, ist eine Nutzen-Risiko-Bewertung der Behandlung erforderlich, inklusive Priorisierung von Zielen und Massnahmen.
Polypharmazie
Definition
Es gibt keine international anerkannte Definition. Zumeist wird als Polypharmazie die gleichzeitige Einnahme von ≥ 4 oder 5 Medikamenten bezeichnet, wenn sie längerfristig eingenommen werden. Neuere Arbeiten ergänzen die numerische Definition mit dem Begriff «problematische Polypharmazie», die sich an der Unangemessenheit und dem Schadenspotenzial orientiert (2).
Epidemiologie
Angesichts der Unschärfe bei der Definition erstaunt es nicht, dass auch die Zahlen zur Häufigkeit (Prävalenzen) stark variieren. Weltweit gehen die Schätzungen von einem Polypharmazie-Anteil zwischen rund 20 % und 65 % für ältere Menschen ab 65 aus (4).
Folgen/Risiken/Möglichkeiten
• Ein Fünftel bis zwei Drittel polypharmazierter, gebrechlicher älterer Menschen zwischen 65 und 90 erleiden einen Schaden durch die Medikation, der in rund der Hälfte der Fälle vermeidbar gewesen wäre (5).
• Polypharmazie führt zu Nebenwirkungen, die wiederum weitere Medikamente nach sich ziehen (Verordnungskaskaden).
• Polypharmazie verursacht häufig unspezifische Beschwerden, z. B. Müdigkeit, Appetitlosigkeit, Schwindel, Verwirrtheitszustände, Tremor.
• Mit der Anzahl der Medikamente und der Komplexität der Einnahmevorschriften sinkt die Patientenadhärenz (6).
• Polypharmazie verursacht vermehrt Spitaleinweisungen wegen unerwünschter Arzneimittelwirkungen (UAW, engl. adverse drug reaction, ADR) von > 10 % der Einweisungen (7).
• Über 50 % der Hospitalisationen von Polypharmazierten wegen UAW sind auf orale Antikoagulantien (OAK)/Thrombozytenaggregationshemmer und Antidiabetika zurückzuführen (8). Allerdings haben diese Substanzen auch ein hohes Nutzenpotenzial. Es geht also darum, bei der Medikationsbewertung das Nutzen-Schaden-Potenzial sorgfältig abzuwägen ( Kap. 2.3.).
2. Umgang mit Polypharmazie
Eine Vielzahl von randomisiert-klinischen Trials, Reviews und Metaanalysen (9–19) zeigt, dass mittels kritischen Überprüfens von Medikationslisten aufgrund definierter Kriterien und patientenzentrierter Kommunikation, sei es durch eine Ärztin/einen Arzt oder durch eine Apothekerin/einen Apotheker ausgeführt, die Anzahl Medikamente leicht reduziert werden kann. Die Sicherheit solcher Interventionen (kein vermehrtes Auftreten adverser Ereignisse) scheint gegeben. Der Evidenzgrad (certainty) ist allerdings gering, und ein Nutzen solcher Interventionen auf klinische Endpunkte wie Hospitalisationen, Stürze oder die Mortalität konnte bisher nicht zuverlässig nachgewiesen werden.
Dasselbe Bild ergibt sich auch für einzelne Substanzgruppen wie Protonenpumpenblocker (PPI), Benzodiazepine, nicht steroidale Antirheumatika, Opioide, Antidepressiva, Neuroleptika und kardiovaskuläre Medikamente, insbesondere Antihypertensiva. Eine Reduktion oder ein Absetzen scheint sicher, allerdings ist der Nutzen davon schwierig nachzuweisen. Laufende randomisiert-klinische Studien zu «Deprescribing» ( Kap. 3) von PPI und Statinen mit Schweizer Patienten sollten hinsichtlich Sicherheit und Nutzen mehr Klarheit bringen (20, 21).
Aktuelle Expertengruppen, zum Beispiel die «Special Interest Group» zu Polypharmazie der Europäischen Gesellschaft für Geriatrische Medizin, empfehlen für den Umgang mit Polypharmazie die Kombination aus den folgenden Elementen (22):
• Regelmässiges Überprüfen der Medikationslisten, besonders bei gebrechlichen Patienten
• Einsatz validierter Vorgehensweisen und Instrumente
• Einbezug der Lebenssituation der Patienten, ihrer Präferenzen, Ziele und Erfahrungen bzw. ihrer Haltung zum «Deprescribing»
• Interprofessionelles Zusammenarbeiten, besonders zwischen Ärztinnen/Ärzten und Apotheken
In den folgenden Abschnitten stellen wir solche Vorgehensweisen und Instrumente vor.
2.1. Definition der Zielpopulation für die nachfolgenden Interventionen
Grundsätzlich sind die nachfolgenden Empfehlungen für alle Patienten mit Polypharmazie sinnvoll. Am meisten lohnen sich die nachfolgenden Interventionen bei Patienten mit hohem Risiko für medikamentenassoziierte Nebenwirkungen, namentlich:
• höheres Lebensalter
• besonders hohe Anzahl von Medikamenten (sowie Medikamente mit enger therapeutischer Breite und/oder hohem Interaktionspotenzial)
• Übergangssituationen wie kürzliche Hospitalisation
• Gebrechlichkeit bezüglich körperlicher Funktionen, kognitiver Kapazität oder sozialer Situation (Einsamkeit)
Die verschiedenen Leitlinien positionieren sich dazu unterschiedlich (23). Unsere Quell-Leitlinie der DEGAM (1) bezieht ihre Empfehlungen auf Patienten mit Polypharmazie (fünf oder mehr Medikamente dauerhaft) und gleichzeitig drei oder mehr chronischen Erkrankungen und bildet damit diese Risikozielpopulation ab. Dementsprechend gelten die in dieser GL aufgeführten Empfehlungsgrade und Evidenzlevels für diese Patientenpopulation. Es gibt auch andere Definitionen von Multimorbidität, die akute Erkrankungen miteinbeziehen, die wir hier nicht adressieren.
2.2. Bestandsaufnahme und Medikationsabgleich (Medication Reconciliation)
Erfassung der Medikamente
• Notwendige Voraussetzung für eine Analyse und Optimierung der Arzneitherapie sind die Erfassung/der Abgleich aller eingenommenen Medikamente bei Patienten mit Multimedikation. Die Erfassung soll systematisch mindestens 1 × pro Jahr [B/V] oder bei Auftreten von Problemen oder nach Hospitalisation stattfinden, letztere ist eine kritische Schnittstelle für Medikationsfehler (23).
Vorgehen: Der Patient (ggf. eine Bezugsperson) bringt alle Arzneimittel (inkl. Selbstmedikation) und Packungsbeilagen von zu Hause mit (Brown-Bag-Methode) [B/V]. Erfassung in der Patientenakte, anschliessend Medikationsplan (s. u.) aktualisieren. Hinweis: Kann auch durch MPA gemacht werden, je nach Praxisorganisation.
• Die Patienten sollen ihren Hausarzt unverzüglich informieren, wenn andere medizinische Institutionen (Spital, Spezialisten, Notfallarzt) diesen Medikationsplan abgeändert haben (z. B. zusätzliche Medikamente oder Medikamentenstreichungen).
2.3. Medikamentenbewertung (Medication Review)
Instrumente
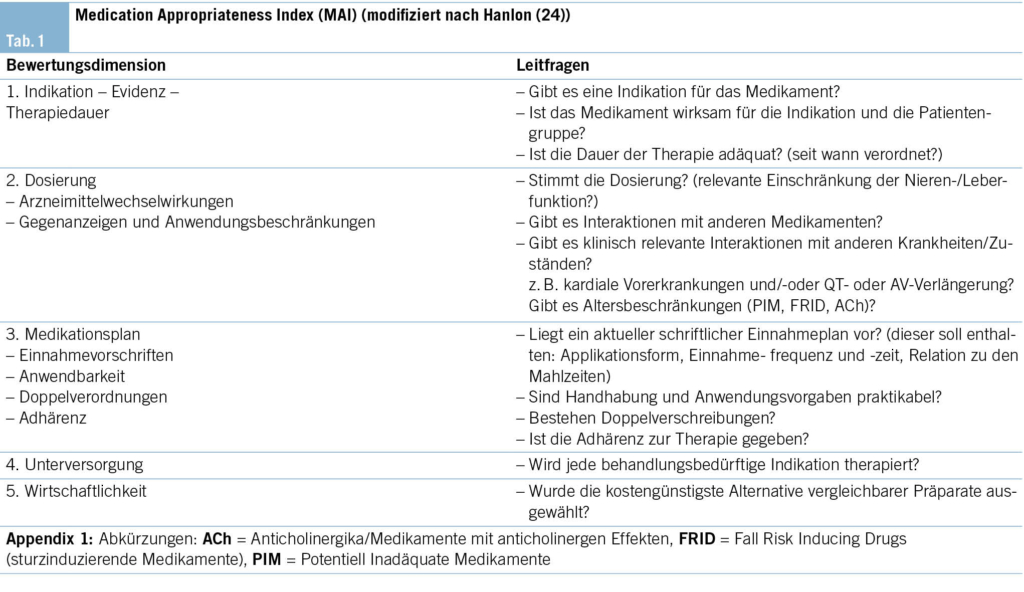
Nach der Erfassung aller Medikamente kann gemäss DEGAM-Leitlinie «Multimedikation» (1) der für die praktische Anwendung modifizierte Medication Appropriateness Index (MAI) (24) als Instrument zur Bewertung deren Angemessenheit eingesetzt werden ( Appendix 1). Die MAI-Leitfragen sind auch relevant für den Prozess des Deprescribing ( Kap. 3).
Es gibt eine Vielzahl von Listen potenziell inadäquater Medikamente (PIM) für ältere Menschen, welche als Instrumente im Rahmen der kritischen Medikamentenbewertung berücksichtigt werden sollten [A/V]. Die PIM-Listen unterscheiden sich deutlich, z. B. in der Anzahl Medikamentenklassen, welche als PIM klassifiziert werden, oder bei der Berücksichtigung von weiteren Kriterien wie Dosis, Dauer der Einnahme, Nierenfunktion und Medikamenteninteraktionen (25). In einer hausärztlichen Patientenpopulation im Alter 65+ waren folgende 5 Medikamentenklassen für die Mehrheit (63.5 %) aller PIM-Verschreibungen verantwortlich (25): Analgetika (26.9 %), PPI (12.1 %), Benzodiazepine- und Z-Substanzen (11.2 %), Antidepressiva (7 %) und Neuroleptika (6.3 %). Für den praktischen Gebrauch im deutschen Sprachraum empfehlen wir die PRISCUS-Liste (https://www.priscus2-0.de/priscus-2.html), die dadurch besticht, dass sie nicht nur von bestimmten PIM abrät, sondern auch Alternativen vorschlägt.
Interaktionen und Risiko der QT-Zeit-Verlängerung
Eine Leitlinie zu Polypharmazie hat nicht den Anspruch, alle Situationen der Medikationssicherheit abzudecken. Dazu gehören beispielsweise klinisch relevante Interaktionen oder spezifische Risiken wie die QT-Zeit-Verlängerung.
Eine Software zur Überprüfung des Interaktionspotenzials von Medikamenten ist sinnvoll, wenn darin auch Aussagen zur klinischen Relevanz und Empfehlungen zum Management gemacht werden. Die meisten Praxissoftwareanbieter stellen eine Interaktionssoftware zur Verfügung. Wir empfehlen die Aktivierung dieser Software. Alternativ stellt Medscape Reference einen kostenlosen «Interaction Checker» online zur Verfügung (https://reference.medscape.com/drug-interactionchecker).
Für die Einschätzung des Risikos einer QT-Zeit-Verlängerung kann das Suchtool «Crediblemeds» der US-Website For Healthcare Providers nützlich sein (https://crediblemeds.org/healthcare-providers); einmalige Registrierung nötig; kostenfrei).
Medikationssicherheit ist auch ein Bestandteil der Qualitätssicherung und findet sich dementsprechend in einem Modul der Stiftung EQUAM (Stiftung für Qualität und Patientensicherheit) wieder: Mit einer Zertifizierung in diesem Modul können die Praxen ein systematisches Vorgehen bei potenziell gefährlicher Medikation nachweisen (https://www.equam.ch/medikationssicherheit/).
Unterbehandlung
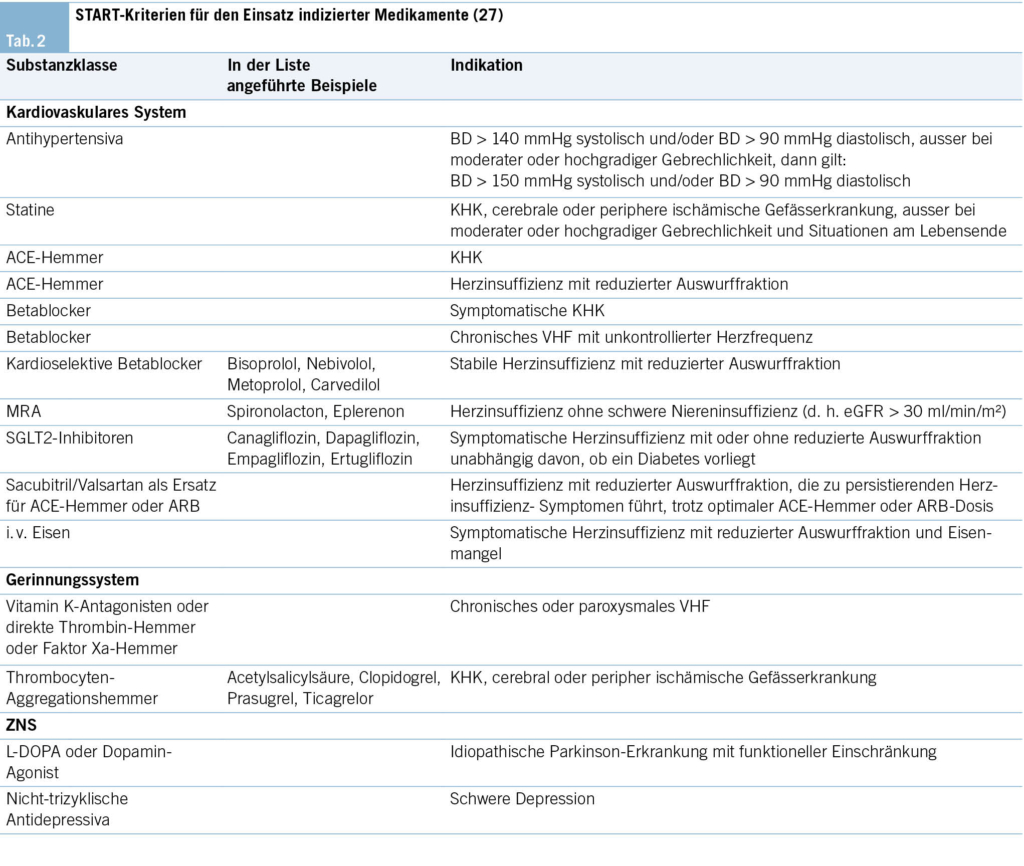
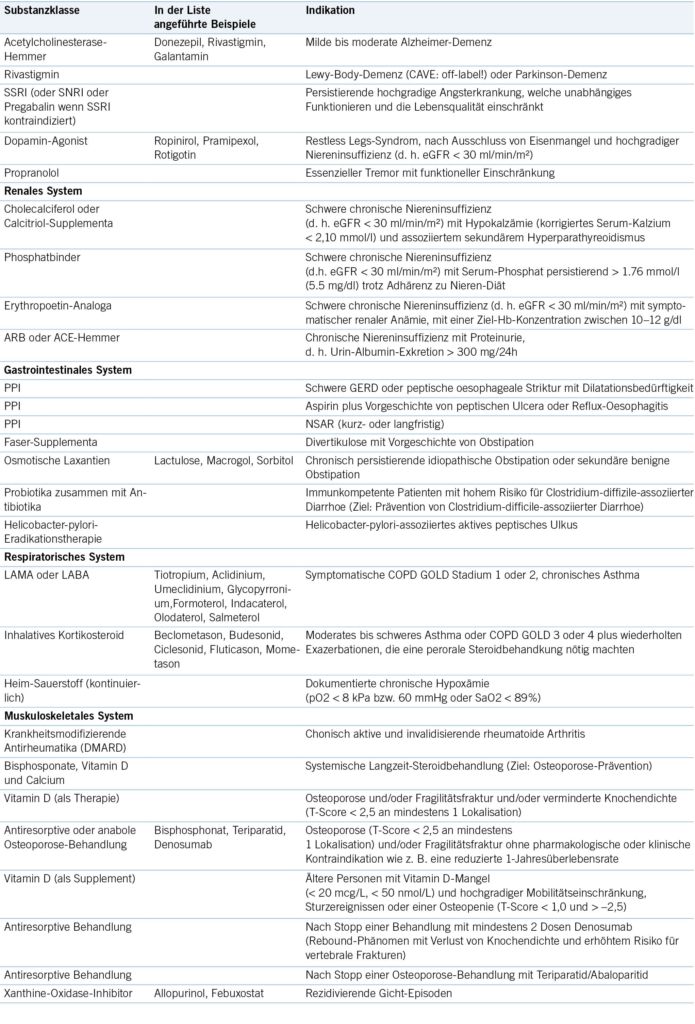
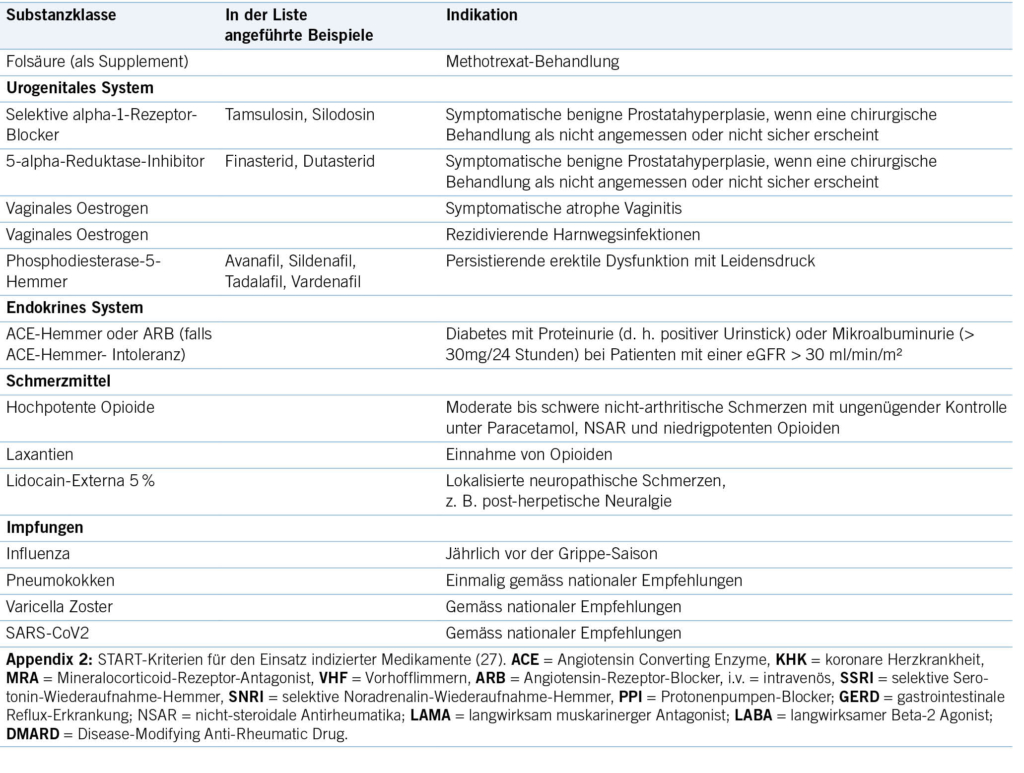
Polypharmazie birgt – paradoxerweise – auch die Gefahr der Unterbehandlung (26). Um dieses Problem bei der Medikamentenbewertung adäquat zu berücksichtigen, wurde in Irland die sogenannte STOPP/START-Liste entwickelt (27). Die START-Liste weist dabei auf Medikamente hin, die bei vorhandener Indikation eingesetzt werden sollten, sofern keine Kontraindikation besteht. Eine Übersicht dazu findet sich im ( Appendix 2).
2.4. Entscheidungsfindung
Priorisierung [A/IIIa]
• Was ist für den Patienten zurzeit das Wichtigste?
• Welche Beschwerden schränken den Patienten zurzeit im Alltag besonders ein?
• «Was wäre Ihr grösster Wunsch, wenn Sie frei wünschen könnten?»
• «Was ist Ihr konkretes Ziel für die Behandlung?»
• Lebenserwartung und Gebrechlichkeit sollen berücksichtigt werden. Letztere lässt sich auf einfache Weise nach dem Schema der «Clinical Frailty Scale»
(https://www.dggeriatrie.de/images/Bilder/PosterDownload/200331_DGG_Plakat_A4_Clinical_Frailty_Scale_CFS.pdf) (28) einschätzen, welche «Frailty» auf einer Skala von 0 (sehr fit) bis 9 (terminal erkrankt) in 9 Kategorien einteilt. Die Einschätzung der «Frailty» spielt eine wesentliche Rolle beim Festlegen von Zielwerten, zum Beispiel bei der Blutdruck- oder Blutzuckereinstellung. Um weniger streng gesetzte Zielwerte zu erreichen, braucht es oft weniger, niedriger dosierte oder gar keine Medikamente.
Kommunikation (Shared Decision Making)
• Behandlung ausführlich erklären (nicht nur auf Nachfragen reagieren) und sich vergewissern, dass der Patient es verstanden hat [A/V]
• Erklären, welcher Nutzen zu erwarten ist, welche Risiken bestehen. Welche Probleme/Nebenwirkungen können auftreten, und was ist dann zu tun?
• Gemeinsam Nutzen und Risiken einer Behandlung entlang der Präferenzen und Werte des Patienten abwägen
• Gemeinsam eine Entscheidung treffen
• Gemeinsam einen konkreten Plan zur Umsetzung entwickeln
• Medikationsplan aktualisieren und ausdrucken [A/V]
• Kontrolltermin vereinbaren, mit der Zusicherung, abgesetzte/reduzierte Medikamente wieder starten zu können, falls nötig (vermittelt Sicherheit) [B/V]
• Hinweise geben, welche Medikamente nicht eigenständig abgesetzt, pausiert oder in der Dosierung verändert werden sollen
Ein «Shared Decision Making»(SDM)-Gespräch lässt sich zwanglos in nachfolgende drei Phasen strukturieren (29). Eingangs sollte jedoch geklärt werden, ob seitens des Patienten überhaupt der Wunsch nach SDM besteht. SDM ist kein «Allheilmittel» für alle Patienten.
1. Schritt «team talk»: Der Arzt ermutigt den Patienten, zusammenzuarbeiten und gemeinsam eine Entscheidung zu finden, die auf die individuellen Bedürfnisse und Ziele zugeschnitten ist. Dies gilt in den Fällen, in denen grundsätzlich mehrere Therapieoptionen bestehen.
2. Schritt «option talk»: Die verschiedenen Optionen werden mit ihren jeweiligen Vor- und Nachteilen vorgestellt und erörtert.
3. Schritt «decision talk»: Entscheidungsgespräch, bei dem Patientenpräferenzen erhoben und verwendet werden, um die bevorzugte Option auszuwählen.
In der Krankenakte sollte dokumentiert werden, wenn sich Arzt und Patient im gemeinsamen Entscheidungsprozess bewusst gegen eine nach Leitlinien für den Patienten empfohlene Massnahme entschieden haben (z. B. im Hinblick auf die Multimedikation, Verträglichkeit oder individuelle Präferenz).
2.5. Erstellen eines Medikationsplanes
Medikationsliste
Die Medikamentenliste soll mindestens enthalten
• Name und Alter
• Medikament (Handelsname) und Dosierung
• Einnahme (Mo–Mi–Ab–Na)
• Zu jedem Arzneimittel sollte ein Hinweis in verständlicher Sprache stehen, für welche Erkrankung es eingesetzt wird [A/V]
• Vermerk: Bitte bei jedem Arztbesuch mitbringen!
Optional sind folgende Informationen
• Allergien/Unverträglichkeiten
• Generikaname
• Identa-Abbildung
• Name und Kontaktdaten des Verschreibers
• Besondere Einnahmemodalitäten (vor/während/nach Mahlzeiten, welche Medikamente nicht gleichzeitig einnehmen etc.)
• Besondere Einnahmedauer (v. a. Datum des geplanten Absetzens)
• QR-Code und digital hinterlegte Informationen
3. Deprescribing
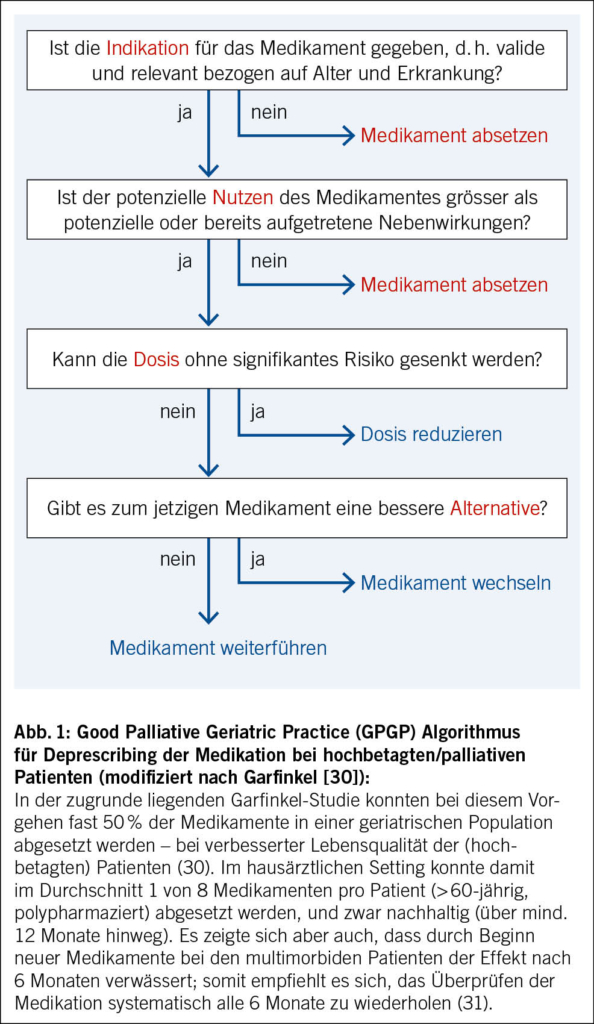
Garfinkel hat einen Abklärungsalgorithmus entwickelt, anhand dessen sich Polypharmazie bei Hochbetagten reduzieren lässt (30). Eine Arbeitsgruppe am Institut für Hausarztmedizin der Universität Zürich hat eine vereinfachte Version für die Anwendung in der Hausarztpraxis entwickelt und getestet (31) (Abb. 1).
Beachte: Ablehnung/Skepsis gegenüber Deprescribing
Nicht alle Patienten sind ohne Weiteres einverstanden mit dem Absetzen oder Reduzieren ihrer «gewohnten» Medikamente: In der oben erwähnten Studie (31) lehnte rund ein Viertel der Patienten den Deprescribing-Vorschlag ihres Arztes ab. Eine Vielzahl von Gründen für diese ablehnende Haltung ist beschrieben, wobei sich die Argumente und Sorgen hausärztlicher Patienten in der Schweiz im Vergleich zum internationalen Kontext nicht wesentlich unterscheiden (32, 33). Die wichtigsten davon sind:
• Eine konservative Grundhaltung mit Angst vor Veränderungen, in diesem Fall vor der Veränderung der Medikation
• Konfirmations-Bias: Das Weiterführen der Medikation bestärkt mich in der Wahrnehmung, dass die Medikation gut ausgewählt wurde und die richtige für mich ist. Eine Veränderung stellt diese bisherige positive Wahrnehmung infrage.
• Angst vor Entwertung: der Eindruck, dass die Reduktion der Medikamente Ausdruck davon ist, dass es sich nicht mehr lohne, für mich Geld auszugeben
• Fragmentierte Betreuung mit verschiedenen Verschreibern und entsprechenden Loyalitätskonflikten: Wenn mir Medikamente von Arzt A verschrieben wurden und jetzt ein anderer Arzt diese infrage stellt, dann wird damit gleichzeitig die Kompetenz von Arzt A angezweifelt. Diesen Zweifeln möchte ich als Patient ausweichen.
• Angst vor Rationierung: die Sorge, dass die Reduktion der Medikamente aus rein finanziellen Gründen motiviert ist und nun ausgerechnet bei mir gespart wird
Ärztliche Kommunikation bei ablehnender Haltung des Patienten
Die Kenntnis solcher Hindernisse ist nützlich, um sie bei zögerlichen Patienten anzusprechen und offen zu diskutieren. Oft helfen dabei folgende organisatorische Elemente und Gesprächsinhalte:
• Die Zusicherung, dass ein abgesetztes Medikament jederzeit wieder eingesetzt werden kann, sollte es ohne dieses Medikament schlechter gehen
• Es vermittelt den Patienten Sicherheit, wenn ein kurzfristiger Kontrolltermin vereinbart wird, bei dem die Situation nach Deprescribing nochmals evaluiert wird.
• Eine Medikation, die bisher richtig war, muss nicht unbedingt in Zukunft auch die richtige sein: Das Alter steigt, und neue/mehrere Krankheiten kommen hinzu. Mit der Veränderung des Menschen macht auch eine Veränderung der Medikation Sinn!
• Die Zusicherung, dass nicht die Kosten, sondern der Schutz vor den gefährlichen Auswirkungen der Überbehandlung/Fehlbehandlung das Ziel der Bemühungen ist
• Die Bereitschaft, mit anderen Verschreibern zu kommunizieren, um einen Konsens zur Behandlung (und speziell zum Absetzen eines Medikamentes) zu finden
Deprescribing-Algorithmen
Für einige Substanzklassen, bei denen der unangemessene Einsatz ein Thema ist, hat eine kanadische Gruppe Deprescribing-Algorithmen entwickelt, beispielsweise zu Protonenpumpenblockern, blutzuckersenkenden Medikamenten, Antipsychotika, Benzodiazepinen oder Antidementiva: (https://deprescribing.org/resources/deprescribing-guidelines-algorithms/)
Stefan Neuner-Jehle 1, Andrea Rosemann 2, Oliver Senn 1
1 Institut für Hausarztmedizin der Universität Zürich, Schweiz
2 Departement für Innere Medizin, Universitätsspital Zürich, Schweiz
Abkürzungen
ACE Angiotensin Converting Enzyme
ADR adverse drug reaction
ARB Angiotensin-Rezeptor-Blocker
CFS Clinical Frailty Scale
DEGAM Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin
DMARD Disease-Modifying Anti-Rheumatic Drug
eGFR geschätzte glomeruläre Filtrationsrate
FRID Fall Risk Inducing Drugs (sturzinduzierende Medikamente)
GERD gastrointestinale Refluxerkrankung i. v. intravenös
KHK koronare Herzkrankheit
LABA langwirksamer Beta-2-Agonist
LAMA langwirksam muskarinerger Antagonist
MRA Mineralocorticoid-Rezeptor-Antagonist
OAK orale Antikoagulantien
PIM potenziell inadäquate Medikamente
PPI Protonenpumpenblocker
NSAR nicht steroidale Antirheumatika
SDM Shared Decision Making
SGLT2-Inhibitoren Sodium glucose linked transporter 2-Hemmer
SNRI selektive Noradrenalin-Wiederaufnahmehemmer
SSRI selektive Serotonin-Wiederaufnahmehemmer
VHF Vorhofflimmern
UAW unerwünschte Arzneimittelwirkungen
Historie
Manuskript eingegangen: 06.11.2025
Angenommen nach Revision: 20.01.2026
Appendix
Stefan Neuner-Jehle (1), Andrea Rosemann (2), Oliver Senn (1)
1 Institut für Hausarztmedizin der Universität Zürich, Schweiz
2 Departement für Innere Medizin, Universitätsspital Zürich, Schweiz
Leiterin Guidelines |
Oberärztin, Fachärztin Kardiologie,
Angiologie, Innere Medizin
Universitätsspital Zürich
Institut für Hausarztmedizin
Pestalozzistrasse 24
8091 Zürich
andrea.rosemann@usz.ch
Institut für Hausarztmedizin
Universität und UniversitätsSpital Zürich
Pestalozzistrasse 24
8091 Zürich
Institut für Hausarztmedizin
Universität und UniversitätsSpital Zürich
Pestalozzistrasse 24
8091 Zürich
oliver.senn@usz.ch
Die Autorenschaft hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. DEGAM. Hausärztliche Leitlinie «Multimedikation». Version 2.0 ed: AWMF; 2021.
2. Tsang JY, Sperrin M, Blakeman T, Payne RA, Ashcroft D. Defining, identifying and addressing problematic polypharmacy within multimorbidity in primary care: a scoping review. BMJ Open. 2024;14(5):e081698.
3. Sackett DL, Rosenberg WM, Gray JA, Haynes RB, Richardson WS. Evidence based medicine: what it is and what it isn’t. BMJ. 1996;312(7023):71-2.
4. Nicholson K, Salerno J, Borhan S, Cossette B, Guenter D, Vanstone M, Queenan J, Greiver M, Howard M, Terry AL, William- son T, Griffith LE, Fortin M, Stranges S, Mangin D. The co-occurrence of multimorbidity and polypharmacy among middle-aged and older adults in Canada: A cross-sectional study using the Canadian Longitudinal Study on Aging (CLSA) and the Canadian Primary Care Sentinel Surveillance Network (CPCSSN). PLoS One. 2025;20(1):e0312873.
5. Lam JYJ, Barras M, Scott IA, Long D, Shafiee Hanjani L, Falconer N. Scoping Review of Studies Evaluating Frailty and Its Asso- ciation with Medication Harm. Drugs Aging. 2022;39(5):333-53.
6. Liu J, Yu Y, Yan S, Zeng Y, Su S, He T, Wang Z, Ding Q, Zhang R, Li W, Wang X, Zhang L, Yue X. Risk factors for self-reported medication adherence in community-dwelling older patients with multimorbidity and polypharmacy: a multicenter cross-sectional study. BMC Geriatrics volume 23, Article number: 75 (2023).
7. Opondo D, Eslami S, Visscher S, de Rooij SE, Verheij R, Korevaar JC, Abu-Hanna A. Inappropriateness of medication prescrip- tions to elderly patients in the primary care setting: a systematic review. PLoS One. 2012;7(8):e43617.
8. Budnitz DS, Shehab N, Lovegrove MC, Geller AI, Lind JN, Pollock DA. US Emergency Department Visits Attributed to Medica- tion Harms, 2017-2019. JAMA. 2021;326(13):1299-309.
9. Linsky AM, Motala A, Booth M, Lawson E, Shekelle PG. Deprescribing in Community-Dwelling Older Adults: A Systematic Re- view and Meta-Analysis. JAMA Netw Open. 2025;8(5):e259375.
10. Chua S, Todd A, Reeve E, Smith SM, Fox J, Elsisi Z, Hughes S, Husband A, Langford A, Merriman N, Harris JR, Devine B, Gray SL, Expert P. Deprescribing interventions in older adults: An overview of systematic reviews. PLoS One. 2024;19(6):e0305215.
11. McCarthy C, Clyne B, Boland F, Moriarty F, Flood M, Wallace E, Smith SM, team SPS. GP-delivered medication review of poly- pharmacy, deprescribing, and patient priorities in older people with multimorbidity in Irish primary care (SPPiRE Study): A cluster randomised controlled trial. PLoS Med. 2022;19(1):e1003862.
12. Cole JA, Goncalves-Bradley DC, Alqahtani M, Barry HE, Cadogan C, Rankin A, Patterson SM, Kerse N, Cardwell CR, Ryan C, Hughes C. Interventions to improve the appropriate use of polypharmacy for older people. Cochrane Database Syst Rev. 2023;10(10):CD008165.
13. Boyd CM, Shetterly SM, Powers JD, Weffald LA, Green AR, Sheehan OC, Reeve E, Drace ML, Norton JD, Maiyani M, Gleason KS, Sawyer JK, Maciejewski ML, Wolff JL, Kraus C, Bayliss EA. Evaluating the Safety of an Educational Deprescribing Inter- vention: Lessons from the Optimize Trial. Drugs Aging. 2024;41(1):45-54.
14. Etherton-Beer C, Page A, Naganathan V, Potter K, Comans T, Hilmer SN, McLachlan AJ, Lindley RI, Mangin D. Deprescribing to optimise health outcomes for frail older people: a double-blind placebo-controlled randomised controlled trial-outcomes of the Opti-med study. Age Ageing. 2023;52(5).
15. Mortsiefer A, Loscher S, Pashutina Y, Santos S, Altiner A, Drewelow E, Ritzke M, Wollny A, Thurmann P, Bencheva V, Gogo- lin M, Meyer G, Abraham J, Fleischer S, Icks A, Montalbo J, Wiese B, Wilm S, Feldmeier G. Family Conferences to Facilitate Deprescribing in Older Outpatients With Frailty and With Polypharmacy: The COFRAIL Cluster Randomized Trial. JAMA Netw Open. 2023;6(3):e234723.
16. Jungo KT, Ansorg AK, Floriani C, Rozsnyai Z, Schwab N, Meier R, Valeri F, Stalder O, Limacher A, Schneider C, Bagattini M, Trelle S, Spruit M, Schwenkglenks M, Rodondi N, Streit S. Optimising prescribing in older adults with multimorbidity and poly- pharmacy in primary care (OPTICA): cluster randomised clinical trial. BMJ. 2023;381:e074054.
17. Ali MU, Sherifali D, Fitzpatrick-Lewis D, Kenny M, Lamarche L, Raina P, Mangin D. Interventions to address polypharmacy in older adults living with multimorbidity: Review of reviews. Can Fam Physician. 2022;68(7):e215-e26.
18. Rao P, Hung A. Impact of medication therapy management programs on potentially inappropriate medication use in older adults: A systematic review. J Manag Care Spec Pharm. 2024;30(1):3-14.
19. Keller MS, Qureshi N, Mays AM, Sarkisian CA, Pevnick JM. Cumulative Update of a Systematic Overview Evaluating Interventi- ons Addressing Polypharmacy. JAMA Netw Open. 2024;7(1):e2350963.
20. Schulthess-Lisibach AE, Luthold RV, Tombez C, Weir KR, Zangger M, Chan S, Jenal F, Roumet M, Mattmann Y, Bieri C, Aubert CE, Rodondi N, Zambrano Ramos SC, Trelle S, Neuner-Jehle S, Juillerat P, Barbier M, Inauen J, Streit S, Jungo KT, Vallejo-Ya- gue E. DepRescribing inapprOpriate Proton Pump InhibiTors (DROPIT): study protocol of a cluster-randomised controlled trial in Swiss primary care. BMJ Open. 2025;15(1):e094495.
21. Aebi PS, Adam L, Haller M, Bardoczi JB, Gencer B, Bonnet F, Beer JH, Carballo S, Christ-Crain M, Feller M, Gabutti L, Haynes AG, Moutzouri E, Chocano-Bedoya PO, Bassetti S, Escher R, Egger M, Poortvliet RKE, Schuetz P, Trelle S, Wertli MM, Zekry D, Mean M, Aujesky D, Bauer D, Blum MR, Rodondi N. Rationale and design of ‚discontinuing statins in multimorbid older adults without cardiovascular disease (STREAM)‘: study protocol of a randomised non-inferiority clinical trial. BMJ Open. 2025;15(5):e093833.
22. van Poelgeest E, Seppala L, Bahat G, Ilhan B, Mair A, van Marum R, Onder G, Ryg J, Fernandes MA, Cherubini A, Denk- inger M, Eidam A, Egberts A, Gudmundsson A, Kocak FOK, Soulis G, Tournoy J, Masud T, Wehling M, van der Velde N, Eu GMSSIGP. Optimizing pharmacotherapy and deprescribing strategies in older adults living with multimorbidity and polypharma- cy: EuGMS SIG on pharmacology position paper. Eur Geriatr Med. 2023;14(6):1195-209.
23. Engels L, van den Akker M, Denig P, Stoffers H, Gerger H, Bohnen J, Jansen J. Medication Management in Patients With Poly- pharmacy in Primary Care: A Scoping Review of Clinical Practice Guidelines. J Evid Based Med. 2025;18(1):e70015.
24. Hanlon JT, Schmader KE, Samsa GP, et al. A method for assessing drug therapy appropriateness. J Clin Epidemiol 1992;45(10):1045-51.
25. Schietzel S, Zechmann S, Rachamin Y, Neuner-Jehle S, Senn O, Grischott T. Potentially Inappropriate Medication Use in Prima- ry Care in Switzerland. JAMA Netw Open. 2024;7(6):e2417988.
26. Kuijpers MA, van Marum RJ, Egberts AC, Jansen PA, Group OS. Relationship between polypharmacy and underprescribing. Br J Clin Pharmacol. 2008;65(1):130-3.
27. O’Mahony D, Cherubini A, Guiteras AR, Denkinger M, Beuscart JB, Onder G, Gudmundsson A, Cruz-Jentoft AJ, Knol W, Bahat G, van der Velde N, Petrovic M, Curtin D. STOPP/START criteria for potentially inappropriate prescribing in older people: ver- sion 3. Eur Geriatr Med. 2023;14(4):625-32.
28. https://www.dggeriatrie.de/images/Bilder/PosterDownload/200331_DGG_Plakat_A4_Clinical_Frailty_Scale_CFS.pdf
29. Elwyn G, Durand MA, Song J, Aarts J, Barr PJ, Berger Z, Cochran N, Frosch D, Galasinski D, Gulbrandsen P, Han PKJ, Harter M, Kinnersley P, Lloyd A, Mishra M, Perestelo-Perez L, Scholl I, Tomori K, Trevena L, Witteman HO, Van der Weijden T. A three- talk model for shared decision making: multistage consultation process. BMJ. 2017;359:j4891.
30. Garfinkel D, Mangin D. Feasibility study of a systematic approach for discontinuation of multiple medications in older adults: addressing polypharmacy. Arch Intern Med. 2010;170(18):1648-54.
31. Zechmann S, Senn O, Valeri F, Essig S, Merlo C, Rosemann T, Neuner-Jehle S. Effect of a patient-centred deprescribing proce- dure in older multimorbid patients in Swiss primary care – A cluster-randomised clinical trial. BMC Geriatr. 2020;20(1):471.
32. Zechmann S, Trueb C, Valeri F, Streit S, Senn O, Neuner-Jehle S. Barriers and enablers for deprescribing among older, multi- morbid patients with polypharmacy: an explorative study from Switzerland. BMC Fam Pract. 2019;20(1):64.
33. Reeve E, To J, Hendrix I, Shakib S, Roberts MS, Wiese MD. Patient barriers to and enablers of deprescribing: a systematic review. Drugs Aging. 2013;30(10):793-807.
PRAXIS
- Vol. 115
- Ausgabe 2
- Februar 2026