Der ESC-Kongress ist eine grossartige Gelegenheit, die Magie der Kardiologie gemeinsam zu erleben, sagte ESC-Präsident Prof. Stephan Achenbach, Erlangen.
 Hier finden Sie das PDF der ESC-Kongresszeitung
Hier finden Sie das PDF der ESC-Kongresszeitung
EDITORIAL Die Magie der Kardiologie
Blutdruckmedikamente morgens oder abends einnehmen?
TIME Studie bringt Klarheit
Vor zwei Jahren hat die spanische HYGIA-Chronotherapie Studie für Aufsehen gesorgt mit ihren Resultaten, welche einen unerwartet hohen Vorteil einer abendlichen versus einer morgendlichen Einnahme der anti-hypertensiven Medikamente zeigte. Am ESC hat Prof. Thomas MacDonald nun die Resultate der grösseren TIME Studie vorgestellt, welche genau diese Fragestellung ebenfalls untersuchte. In der TIME Studie wurden hypertensive Patient:innen, welche im Schnitt unter drei anti-hypertensiven Medikamenten gut therapiert waren, zur Einnahme der Medikamente am Abend (20:00-24:00 Uhr) oder am Morgen (06:00-10:00 Uhr) randomisiert. Insgesamt wurden 21’104 Patient:innen (43% Frauen, mittleres Alter 65 Jahre) eingeschlossen. Die Nachbeobachtung betrug 5 Jahre. Die sorgfältige wiederholte Blutdruckmessung zeigte, dass eine morgendliche Einnahme der Medikamente zu einem etwas tieferen systolischen Blutdruck (-2 mmHg) am Abend, verglichen mit der abendlichen Einnahme führte. Umgekehrt führte eine abendliche Einnahme zu einem etwas tieferen Blutdruckwert (-2 mmHg) am Morgen. Der kombinierte primäre Endpunkt (Hospitalisation wegen Myokardinfarkt, Schlaganfall oder kardiovaskulärer Tod) trat in beiden Behandlungsarmen gleich oft auf (Abend vs. Morgen = 3,4 vs. 3,7%; P=0.53). Die separat betrachtete Anzahl der Schlaganfälle war ebenfalls identisch. Es ergaben sich auch keine Unterschiede in Subgruppen, z.B. in Patient:Innen mit fehlendem zirkadianen Blutdruckverhalten, sogenannten nondippers. Bezüglich Sicherheit bestand ebenfalls kein Unterschied. So waren z.B. Stürze gleich häufig (21.1% bei Einnahme am Abend vs. 22.2% bei Einnahme am Morgen).
Fazit: Die TIME Studie zeigt, dass die morgendliche oder abendliche Einnahme der anti-hypertensiven Medikamente gleich effektiv ist. Patient:Innen können ihre Medikamente einnehmen, wenn es für sie am bequemsten ist und am wenigsten unerwünschte Nebenwirkungen verursacht.
Interpretation: Die grosse TIME Studie gibt eine ziemlich abschliessende Antwort zur Chronotherapie. Die Resultate der HYGIA Studie sind wahrscheinlich Ausreisser. Im nächsten Jahr erwarten wir noch die Resultate der BedMed Studie. Bis dann können wir beruhigt die Blutdruckmedikamente entweder am Abend oder am Morgen einnehmen.
Prof. Dr. med. Franz Eberli
PERSPECTIVE-Studie
Neprilysin-Inhibition mit Sacubitril/Valsartan hat keinen Einfluss auf die kognitiven Fähigkeiten bei Patient:innen mit Herzinsuffizienz
Im Herz und in der Niere bewirkt eine Hemmung von Neprilysin (durch Sacubitril) einen verminderten Abbau der natriuretischen Peptide. Im Hirn ist Neprilysin im Abbau des ꞵ-Amyloid Peptids involviert. Eine Hemmung von Neprilysin durch Sacubitril kann potentiell diesen Abbau von ꞵ-Amyloid verhindern und zu einer Akkumulation von Amyloidfibrillen und in der Folge zur Alzheimer Krankheit führen. Daher besteht seit der Einführung von Sacubitril/Valsartan (Entresto®) eine gewisse Unsicherheit, ob dadurch im Langzeitverlauf die kognitiven Fähigkeiten vermindert werden. Diese Fragestellung hat die PERSPECTIVE Studie untersucht, welche von John McMurray vorgestellt wurde. In die Studie wurden 592 ältere herzinsuffiziente Patient:innen (mittl. Alter 72,4 Jahre) eingeschlossen und 1:1 randomisiert zu einer Therapie mit Sacubirtil/Valsarten oder Valsartan. Die Nachbeobachtungszeit betrug 3 Jahre. Die kognitiven Fähigkeiten wurden mittels des CogState global cognition score (GCCS) evaluiert, die ꞵ-Amyloid-Ablagerung im Gehirn mittels Positronen-Emissions-Tomographie (PET). Es ergab sich kein Unterschied im primären Endpunkt der kognitiven Fähigkeiten. Im PET zeigte sich zudem eine Tendenz (P=0.058) zu weniger ꞵ-Amyloid Ablagerung in der Gruppe die Sacubirtil/Valsarten erhielten (!). Wie in früheren Studien war Sacubirtil/Valsarten assoziiert mit tieferer Mortalität bei guter Verträglichkeit.
Fazit: Die Rolle von Neprilysin im Abbau von ꞵ-Amyloid im Gehirn scheint nicht von grosser Bedeutung zu sein. Sacubitril/Valsarten führt im Langzeitverlauf nicht zu einer kognitiven Einschränkung und kann diesbezüglich ohne Bedenken verschrieben werden.
Interpretation: Die PERSPECTIVE Studie ist eine wichtige negative Studie. Sie räumt ein wichtiges Sicherheitsbedenken aus, welches bisher bezüglich dem Einsatz von Sacubitril/Valsarten bestand. Dieses Sicherheitsbedenken ist umso kleiner, weil neueste wissenschaftliche Erkenntnisse die ätiologische Rolle der Ablagerung von ꞵ-Amyloid Fibrillen im Gehirn für die Entwicklung der Alzheimer Krankheit mehr als in Frage gestellt haben.
Prof. Dr. med. Franz Eberli
FOURIER-OLE: Evolocumab-Langzeittherapie senkt CV-Ereignisse weiter
Für die von Dr. Michelle L. O’Donoghue, Boston, in einer Hot Line vorgestellte Open-Label-Extensionsstudie FOURIER-OLE wurden 6.635 Patienten der FOURIER-Outcome Studie eingeschlossen und mit dem PCSK9-Inhibitor Evolocumab (Repatha®) behandelt, jedoch für die Analyse nach dem originalen Studienarm Evolocumab versus Placebo stratifi ziert. Dabei zeigte sich, dass Evolocumab zu einer medizinisch signifi kanten und anhaltenden Senkung des LDL-Cholesterins führte. Der Medianwert des LDL-Cholesterins lag nach 12 Wochen bei 0.8 mmol/L, und 63,2% der Teilnehmer erreichten unter Evolocumab ein LDL-Cholesterin unter 1.0 mmol/L. Der primäre Endpunkt zeigte eine 15%ige Reduktion von Major Adverse Cardiovascular Events (MACE) in Patienten, die in der Primärstudie bereits Evolocumab erhalten hatten, was den Vorteil einer frühen Gabe von Evolocumab hervorhebt. Die Inzidenz von schwerwiegenden unerwünschten Ereignissen blieb vergleichbar mit der bei den mit Placebo behandelten Patienten während der Hauptstudie und stieg im Laufe der Zeit nicht an. Während der FOURIER-OLE-Studie hatten Patienten, die ursprünglich in der Hauptstudie auf Evolocumab im Vergleich zu Placebo randomisiert wurden, ein um 15% geringeres Risiko für MACE, ein 20% geringeres Risiko für MACEplus und ein 23% geringeres Risiko für kardiovaskulären Tod (107 vs. 138; HR 0,77; 95% CI 0,60-0,99; p=0,04, vordefi nierte Analyse). Evolocumab ist der erste PCSK9 Inhibitor, der bei Patienten mit ASCVD über einen Zeitraum von bis zu 8,4 Jahren langfristige klinische Ergebnisse zeigt.
Fazit: Mit einem Follow-up von über 7 Jahren wird die Sicherheit und Effektivität von Evolocumab und dessen LDL-senkende Wirkung unterstrichen.
Prof. Dr. Dr. h.c. Walter F. Riesen
Neue ESC-Guidelines 2022

Folgende vier Leitlinien wurden am diesjährigen Jahreskongress vorgestellt und sind unter www.escardio.org/Guidelines abrufbar. Ebenso die Pocketguidelines, welche auch als sehr hilfreiches App z.B. im I-Phone immer zur Verfügung stehen. Auch Slide Sets sind abrufbar.
– Kardio-Onkologie – Nicht -Kardiale Chirurgie: Kardiovaskuläre Beurteilung + Management
– Pulmonale Hypertonie – Ventrikuläre Arrhythmien und die Prävention des plötzlichen Herztodes
Erstmals gibt es diese neue umfas sende Leitlinie zum Thema «Kardio-Onkologie» mit insgesamt 272 Empfehlungen vor, bei und nach einer onkologischen Therapie. Diese Guideline in enger Zusammenarbeit mit der EHA, ESTRO und IC-OS richtet sich an den Kardiologen, Onkologen, Radiotherapeuten, Gynäkologen, Internisten und weitere Ärzte, welche dieses Patientenkollektiv behandeln. Aus der Schweiz hat Prof. Dr. Thomas M. Suter aus Bern in der Task Force entscheidend mitgewirkt. Ziel ist es, Ansätze zu personalisieren, um die krebstherapiebedingte kardiovaskuläre (cv)-Toxizität zu minimieren und sowohl die Krebs- als auch die cv-Ergebnisse zu verbessern. Diese Leitlinie bietet Hilfe für die Defi nitionen, Diagnose, Behandlung und Prävention von krebstherapiebedingter cv-Toxizität und das Management von cv-Erkrankungen, die direkt oder indirekt durch Krebs verursacht werden. Durch die bessere Langzeitprognose moderner Krebstherapien ist es entscheidend potenzielle kardiotoxische Nebenwirkungen früh zu identifi zieren und korrekt zu behandeln. Neben den toxischen Kardiomyopathien müssen Arrhythmien, pulmonale Hypertonie, arterielle und venöse Thromboembolie, Klappenvitien, Perikarderkrankungen, arterielle Gefässerkrankungen und die arterielle Hypertonie als Folge der onkologischen Therapie früh erkannt und behandelt werden. Es existieren verschiedene Risikofaktoren, welche diese kardiovaskulären Ereignisse begünstigen. Patienten können mittels guter Anamnese (allgemein, kardiovaskulär + onkologisch), einer gründlichen klinischen Untersuchung und durch ein 12-Abl. EKG, eine Echokardiographie und Biomarker (cTn, NP) identifi ziert und in Risikokategorien klassifi ziert werden. In vielen Fällen mit erhöhtem kardiovaskulärem und durch onkologische Medikation induziertem Risiko kann die rechtzeitige Gabe von ACE-H. bzw. Sartanen und Betablockern kardioprotektiv wirken. Auch nach einer onkologischen Therapie muss im Langzeitverlauf der Patient resp. die Patientin auch kardiologisch regelmässig kontrolliert werden, um allfällige kardiovaskuläre Schädigungen der onkologischen Therapie zu erkennen und zu behandeln. Die Häufigkeit der kardialen Kontrollen richtet sich nach dem basalen kardio-vaskulären Risiko und der spezifi schen onkologischen Therapie und deren Nebenwirkungen. Eine gute und enge Zusammenarbeit zwischen Onkologen und Kardiologen und weiteren involvierten Ärzten ist bei diesen Patienten essentiell! Dafür ist diese umfassende Guideline eine grosse Hilfe.
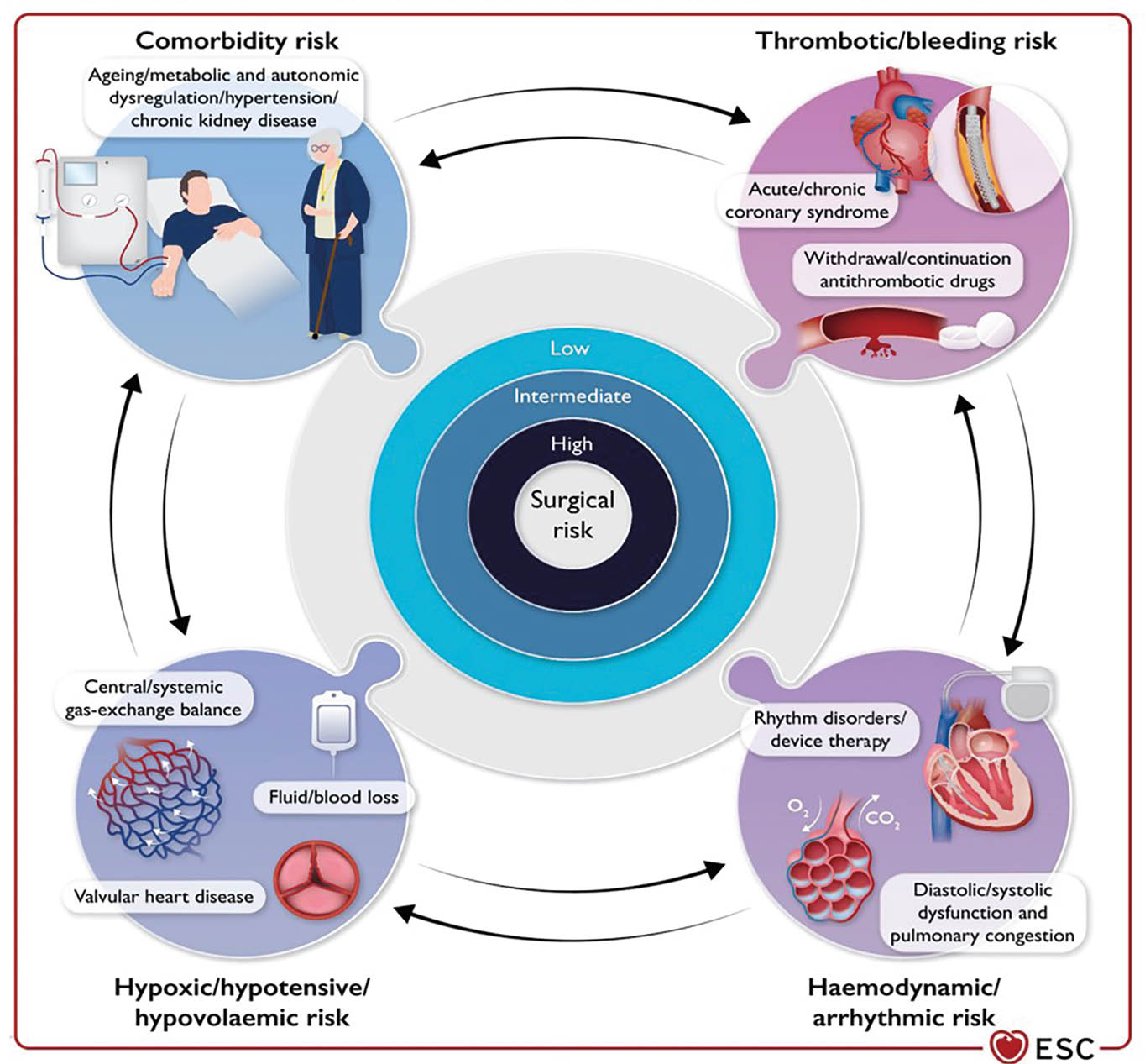
Die ESC-Leitlinien zur «kardiovaskulären Beurteilung und Behandlung von Patienten, die sich einer nicht-kardialen Operation» unterziehen wurde nach 8 Jahren erneuert. Prof. J. Mehilli erklärt: «Ziel der neuen Leitlinien ist es, einen standardisierten und evidenzbasierten Ansatz zu bieten. Sie haben das Potenzial, peri- und postoperative Komplikationen zu reduzieren und eine klare Chance zur Verbesserung der Versorgungsqualität aufzuzeigen.» Die Leitlinie umfasst 99 Seiten und 147 Empfehlungen. Davon 12% Level A. Sie richtet sich an den Kardiologen, den Internisten, den Anästhesisten und auch an den Chirurgen. Aus der Schweiz ist Prof. Dr. Christian Müller in der Task Force (Biomarker). Die Leitlinien empfehlen eine schrittweise Bewertung des Patienten, die klinische Risikofaktoren und Testergebnisse mit der geschätzten Belastung des geplanten chirurgischen Eingriffs und den mit dem Absetzen von Medikamenten verbundenen Risiken. Die kardiologischen Abklärungsmöglichkeiten werden klar bewertet. Ebenso die verschiedenen Risikoreduktionsstrategien und das Management der perioperativen kardiovaskulären Komplikationen.
Ein neues und sehr wichtiges Kapitel ist der richtige Einsatz von Biomarkern (hs-CTnT/I) vor, während und nach einer Operation bei kardiovaskulären Risikopatienten. Ein perioperativer Infarkt muss rasch erkannt und richtig behandelt werden. Ein weiteres wichtiges Kapitel ist das richtige Vorgehen bei einer antithrombotischen Therapie. Die spezifischen kardiovaskulären Erkrankungen werden in einem zusätzlichen Kapitel einzeln beleuchtet; z.B. die koronare Herzkrankheit, die verschiedenen Vitien, Arrhythmien, Devices, Hypertonie, HI, Gefässerkrankungen, onkologische Patienten. Diese Guidelines sind entscheidend; sind doch ca. 50 % aller perioperativen Todesfälle (4,2 Mio/Jahr weltweit) kardiovaskulär. Ziel ist es diese signifi kant zu vermindern und Komplikationen rasch und richtig zu behandeln.
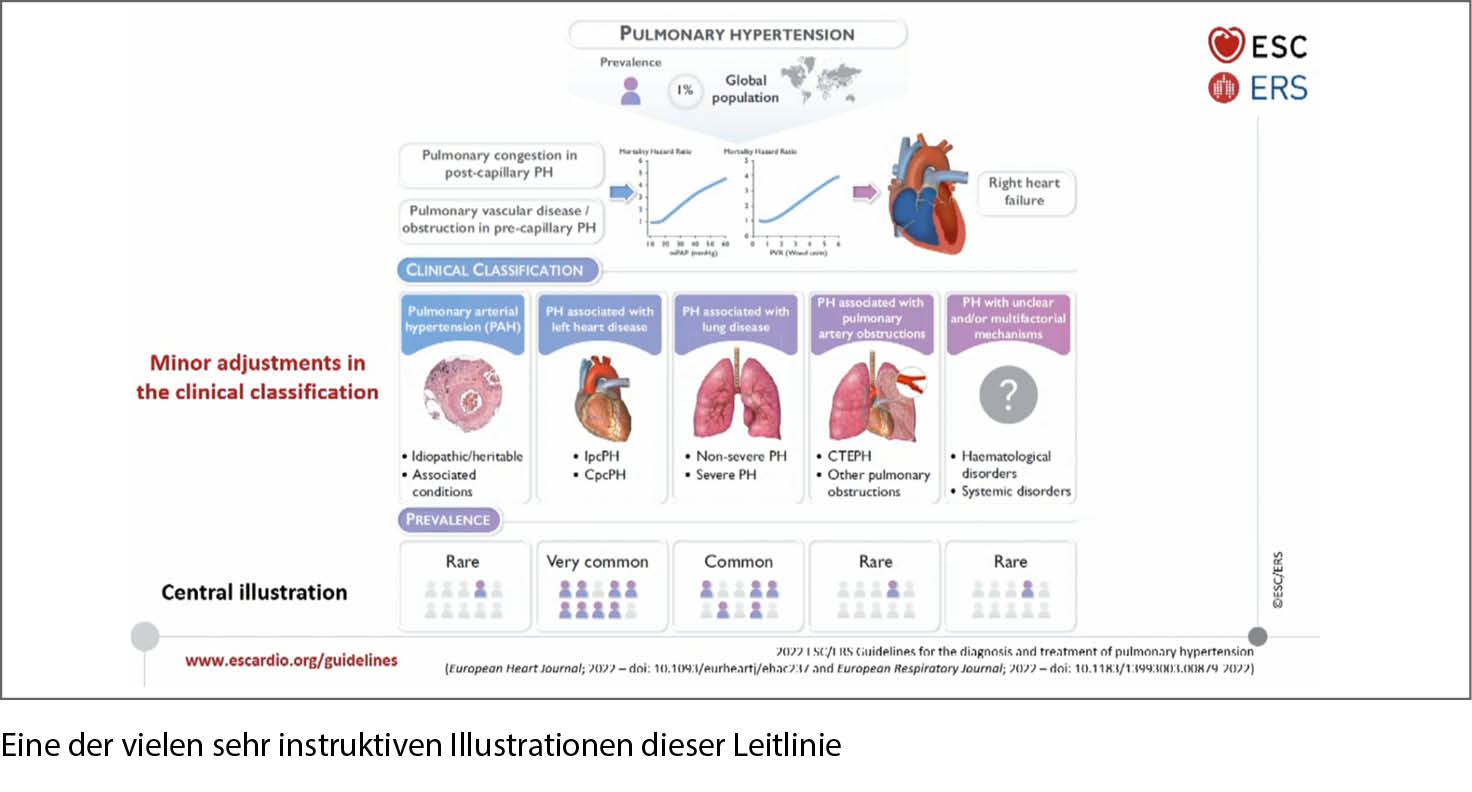
Die ESC/ERS-Leitlinien zur «pulmonalen Hypertonie (PH)» wurden letztmals 2015 publiziert. In der aktuellen Ausgabe decken diese umfassenden Leitlinien von 114 Seiten für die klinische Praxis das gesamte Spektrum der PH ab, wobei der Schwerpunkt auf der Diagnose und Behandlung der pulmonalen arteriellen Hypertonie (PAH) und der chronischen thrombo-embolischen pulmonalen Hypertonie (CTEPH) liegt. Am häufi gsten für den Kardiologen ist die PH bei Linksherzerkrankung – Gruppe 2. Hier bedarf es primär einer optimalen medikamentösen Therapie nach Guidelines. Sehr schöne Abbildungen zur primären Diagnose inkl. Echokardiographie sind für den Alltag des Kardiologen sehr hilfreich. Aus der Schweiz in der Task Force ist Dr. Tonia Thomy aus Bern. Prof. Dr. Stephan Rosenkranz aus Köln war der Leiter dieser Task Force.
Das sehr umfassende Dokument zum Thema «Ventrikuläre Arrhythmien und die Prävention des plötzlichen Herztodes» stellt die Aktualisierung der ESC Leitlinie aus dem Jahre 2015 dar. Neue Erkenntnisse über die Epidemiologie des plötzlichen Herztodes, über Genetik, Bildgebung und klinische Befunde für die Risikostratifi zierung sowie Fortschritte in der diagnostischen Bewertung und neue Therapie-Strategien führten zu dieser Überarbeitung mit insgesamt 130 Seiten. Prof. Dr. Tobias Reichlin und Prof. Dr. Christian Sticherling aus der Schweiz sind in dieser Task Force. In der diagnostischen Evaluation werden 5 klinische Szenarien dargestellt: Der Zufallsbefund einer nicht-anhaltenden VT, die Erstpräsentation mit anhaltender VT, der überlebte plötzliche Herztod, der «sudden death» und das Vorgehen bei Angehörigen eines Patienten mit plötzlichem rhythmogenem Herztod. Die Ablation wird zunehmend zur First-Line Therapie bei anhaltenden VT’s. Die medikamentöse HI Therapie muss optimiert werden. In der Diagnostik grosszügiger Einsatz von Herz-MRI und ggf. 18F-FDG PET/CT (bei Sarkoidose). Die Kardiogenetik wird wichtig in der Diagnostik und Risikostratifikation.
Auch wird in der Vollversion immer wieder auf das Textbook «Cardiovascular Medicine» verwiesen mit direkten elektronischen Links zu dem jeweiligen Kapitel. Dies ergibt dann ein sehr umfassendes Bild der jeweiligen kardiologischen Problematik resp. Fragestellung. Mit sehr vielen Flow Charts und Abbildungen wird das praktische Vorgehen gut dargestellt.
Vier meistdiskutierte Medikamente am ESC
SGLT2-Hemmer bei jeder Herzinsuffizienz
Trotz einer guten Herzinsuffizienztherapie bleibt die Hospitalisation und die cv-Mortalität weiterhin hoch. Internationale Experten empfehlen den Gebrauch von SGLT2-H. wie Empagliflozin und neu auch Dapagliflozin bei praktisch allen Patienten mit einer Herzinsuffizienz über das gesamte Spektrum der LV-EF. Dies bedeutet bei HFrEF, bei HFmrEF und bei HFpEF.
Bei einer EF<40% (HFrEF) haben Empa- und Dapa-gliflozin eine Klasse IA Indikation. Dies mit oder ohne Diabetes Typ II. Empagliflozin reduziert in der EMPEROR-Reduced Studie den cv-Tod oder die 1. Hospitalisation wegen HI um 25% resp. hat eine NNT von 19. Das Medikament sollte so schnell wie möglich in einer Dosierung von 10mg eingesetzt werden. Parallel die weiteren drei Pfeiler: ACEH/ARNI; BB; MRA. Je nach Stauung zusätzlich Diuretika. Unter SGLT2-H. bleibt der BD stabil. Das Medikament kann bei der HI bei einer GFR>20-25ml/min eingesetzt werden. Die SGLT2-H. sind nach mehreren CKD-Studien (chron. Niereninsuffizienz) nephroprotektiv mit vermindertem und deutlich verzögertem Abfall der eGFR. Die SGLT2-H. führen zu einem weniger ausgeprägten Remodeling des Herzens; zu einer besseren Lebensqualität und besseren Leistungsfähigkeit.
Bei einer EF>40% (HFmrEF, HFpEF) besteht heute nach der Emperor-Preserved Studie ein prognostischer Benefit bezüglich kardiovaskulärem Tod oder 1. Hosp. wegen HI (HR 0.79, NNT 31). Die Wirkung setzt bereits nach 18 Tagen ein. Es profitieren alle Subgruppen. Insbesondere auch sehr alte Patienten. Die Lebensqualität wird verbessert. In der am Kongress vorgestellten DELIVER Studie mit Dapagliflozin 10mg (multizentrische, randomisierte, doppelblinde Parallelgruppenstudie), zeitgleich im NEJM publiziert, bei 6263 älteren Patienten mit vielen Komorbiditäten und einer EF>40% konnte die Indikation auch für diesen SGLT2-H. bestätigt werden – HR 0.82, NNT 32 bez. cv Tod oder Verschlechterung der HI. Ausschlaggebend für den Unterschied war eine sign. relative Reduktion von HI-Verschlechterungen. Auch hospitalisierte HI-Patienten profitieren in dieser Studie von Dapagliflozin.
Somit ist die Datenbasis nun auch in dieser HI-Gruppe (>40% EF) gefestigt. In einer Metaanalyse von beiden erwähnten Studien ist die Datenlage noch klarer mit einer Senkung des primären Endpunktes cv Tod oder Herzinsuffizienz Hospitalisation von 20% (HR 0.80%). In Zukunft bekommt der SGLT2-H auch in den ESC-Leitlinien eine entsprechende Indikation.
Praktisch: Medikament früh geben in einer Dosierung von 10mg 1x tgl., bei allen 3 Gruppen der Herzinsuffizienz, auch im Alter, auch bei einer Nierenfunktionseinschränkung (GFR >20-25ml/min), auch bei grenzwertigen BD-Werten (>90-100mmHg), auch bei Diabetes Typ II. KI: bei einem Diabetes Typ I; pausiert werden sollte es 3 Tage vor einer Operation, beim Fasten resp. fehlender Nahrungsaufnahme – cave Ketoazidose! Das Problem der Genitalinfekte ist bei der HI viel geringer als beim Diabetes Typ II. Ein weiterer Vorteil: es gibt viel weniger Hyperkaliämien bei der Gabe von MRAs. Als weiterer Nebeneffekt sinkt die Harnsäure. SGLT2-H. könnten nach einer neuen kleinen Studie auch bei einer Anthrazyklin-Therapie kardioprotektiv sein.
Aktuell bestehen in der Schweiz noch gewisse Limitationen bei der Verschreibung dieser Substanzklasse.
Vericiguat bei einer sich verschlechternden HI
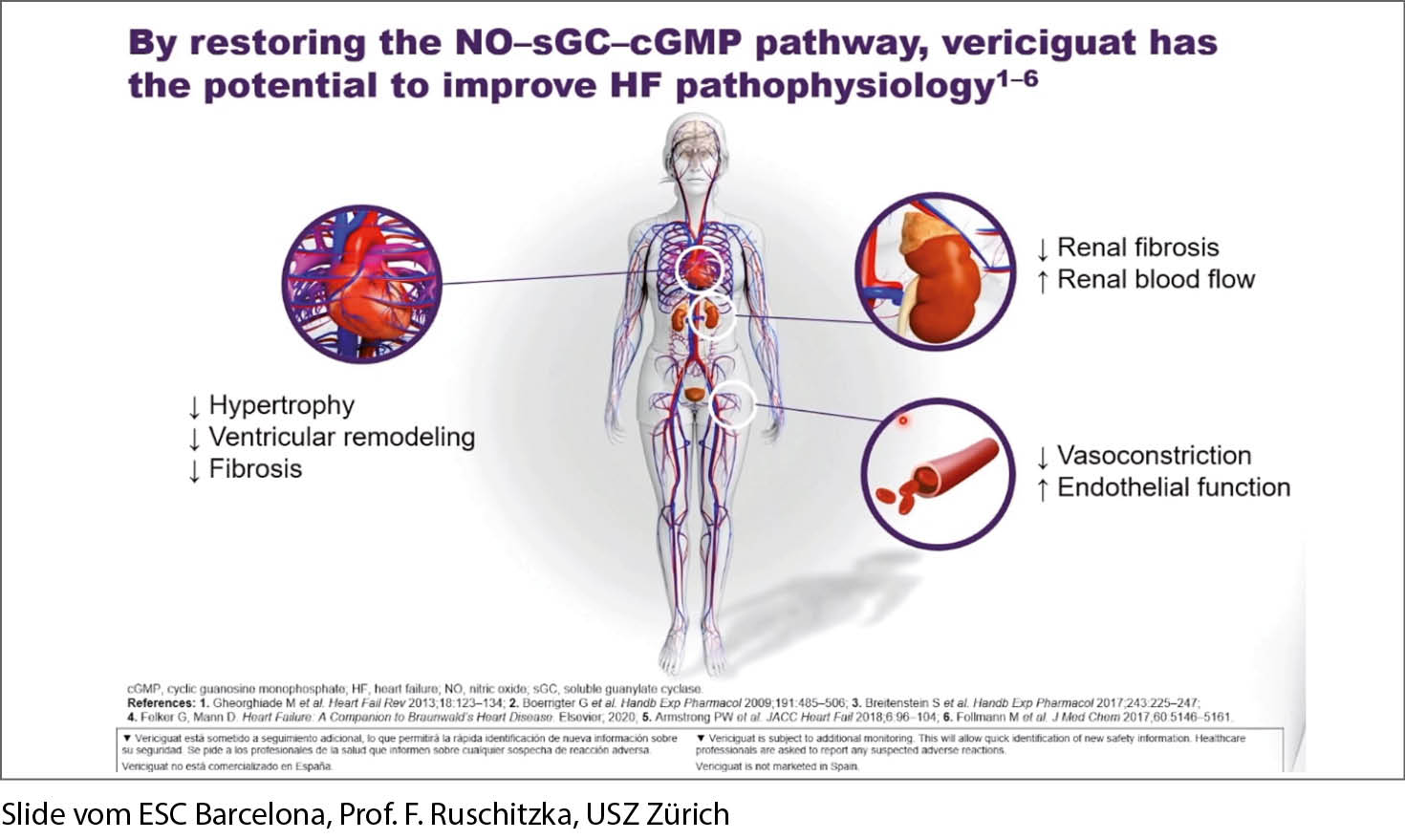
Wie erwähnt sind Patienten mit einer HFrEF (EF<40%) einem extrem hohen Risiko betreffend cv-Tod oder HI-Hospitalisation ausgesetzt. Dies trotz der modernen Vierer-Therapie. Gemäss DAPA-HF Studie dekompensierte 1 von 7 Patienten (14%). Die 1-Jahresmortalität ist bei diesen Patienten 4x höher als bei einer stabilen chron. HI. Aus diesem Grunde wird bei einer HI-Dekompensation unter der bewährten Vierer-Therapie neu Vericiguat eingesetzt. Es kommt so zu einer Wiederherstellung des NO-sGC-cGMP Pathway. Dieser wirkt dem tiefen NO bei der HI entgegen. In der VICTORIA Studie konnte bei Patienten mit NYHA II-IV und einer EF<45% und einer HI-Therapie nach Guidelines ein klarer Benefit bezüglich cv-Tod oder 1. HI Hospitalisation nachgewiesen werden. NNT 24; ARR 4,2 Events/100 PY. Das Medikament kann bei einer GFR>15ml/min. und einem BD≥100mmHg eingesetzt werden. Es hat ein gutes Sicherheitsprofil. Beginn nach Unterbruch der i.v. Diuretika für 24 Stunden mit 1x 2,5mg über 2 Wochen, bei guter Verträglichkeit dann 5mg, nach weiteren 2 Wochen 10mg.
Finerenon bei chron. Niereninsuffizienz mit Diabetes Typ II – kardio + nephroprotektiv
Der neue nicht-steroidale, selektive Mineralokortikoidrezeptor (MR)-Antagonist zeigt auf Grund dieser drei Studien (FIDELIO, FIGARO, FIDELITY) bei Patienten mit einer chronischen Niereninsuffizienz, Albuminurie und Diabetes Typ II eine deutliche Nephroprotektion und einen signifikanten kardio-vaskulären Benefit bezüglich cv-Morbidität, cv-Mortalität und HI-Hospitalisation bei guter RAAS Blockade. Die bisherigen steroidalen MRAs ergeben in den Guidelines einen klaren Benefit bei HFrEF, HFmrEF und bei HFpEF. Auch Finerenon ist nützlich bei Patienten mit einer Herzinsuffizienz. Es läuft aktuell eine Studie (FINEARTS-HF) bei einer EF≥40% und einer GFR≥25ml/min. und einem Serum Kalium <5,0mmol/l. Finerenon macht weniger Hyperkaliämien verglichen mit den bisherigen steroidalen MRAs (Spirolacton, Eplerenon). Finerenon hemmt die schädliche Wirkung einer Überaktivierung des Mineralokortikoid-Rezeptors. Dadurch kommt es zur protektiv kardiovaskulären und protektiv renalen Wirkung mit weniger Natriumretention, weniger Remodeling, weniger Hypertrophie, Entzündung und Fibrose.
Finerenon reduziert nach der FIDELITY Studie das Risiko der cv-Morbidität und Mortalität um 14% versus Placebo bei Patienten mit CKD und Diabetes II.
Revival von Diamox® – Wirkverstärker bei akut dekompensierter Herzinsuffizienz:
Durch die am Kongress vorgestellte multizentrische, randomisierte, doppelblinde, klinische Phase-IV-Studie zu den harntreibenden Wirkungen von Acetazolamid (ADVOR Studie) erlangte der gut bekannte Carboanhydrasehemmer bei akuter dekompensierter Herzinsuffizienz (ca. 2/3 HFpEF, 1/3 HFrEF) mit Volumenüberlastung (Oedeme, Pleura-Ergüsse, Ascites) und erhöhtem NT-pro BNP/BNP ein Revival. Die kleine Studie mit 519 Patienten, durchschnittlich 78 Jahre, NYHA II-IV, zeigte durch die zusätzliche i.v. Gabe von. 1x tgl.
500mg A. eine deutlich gesteigerte Diurese mit einer 46% höheren Dekongestion über 3 Tage verglichen mit der alleinigen i.v. Gabe von Schleifendiuretika. Dieses am proximalen Tubulus wirkende Diuretikum zeigt eine bis zu 75%-ige Hemmung der Natriumrückresorption.

Auf die Prognose hatte dieses Diuretikum keinen Einfluss, dafür war die Studie nicht gepowert. Es traten nicht mehr NW (Hypokaliämie, Hypotonie, Abfall der GFR) auf als bei der alleinigen Therapie mit Schleifendiuretika. Die Dauer des Klinikaufenthaltes konnte reduziert werden. In dieser Studie hatten die Patienten noch keine SGLT2-Hemmer. Gemäss Autor W. Mullens sollte aber die Gabe eines SGLT2-H. kein Hindernis sein. Additive Wirkung? Azetazolamid sollte nach dem Autor des Editorials GM. Felker vor allem bei Patientinnen und Patienten gegeben werden, die entweder eine gewisse Resistenz gegen Diuretika aufweisen oder auf Schleifendiuretika nicht ausreichend ansprechen. Inwieweit eine solche Strategie im Kontext einer zeitgemässen Herzinsuffizienztherapie eine Rolle spielen werde, müssten künftige Studien definieren, macht der Kardiologe am Ende seines Editorials deutlich, denn die Studie wurde zeitgleich im NEJM publiziert.
Dr. med. Urs Dürst, Forch
Präspezifizierte Metaanalyse von DELIVER und EMPEROR-Preserved
Sowohl DELIVER als auch EMPEROR-Preserved zeigten, dass der Einsatz der SGLT2-Hemmer Dapagliflozin bzw. Empagliflozin in Patient:innen mit Herzinsuffizienz und einer LVEF > 40% die Zahl kardiovaskulärer Ereignisse signifikant senkt. Obwohl es starke Hinweise darauf gibt, dass SGLT2-Inhibitoren in der Behandlung von Patienten mit Herzinsuffizinez und reduzierter Ejektionsfraktion (HFrEF) eingesetzt werden sollten, ist der Vorteil bei Patienten mit höheren Ejektionsfraktionen noch nicht restlos geklärt.
Eine präspezifizierte Metaanalyse von DELIVER und EMPEROR-Preserved mit 12251 Patienten (LVEF >40%), die von Prof. M. Vadugathan, Boston, in einer Hot Line Session präsentiert wurde, zeigte nach einer medianen Follow-Up-Zeit von 2,2–2,3 Jahren eine Senkung des Risikos des kombinierten Endpunktes kardiovaskuläre Mortalität oder Herzinsuffizienzhospitalisierung um 20% (HR 0,80; 95% CI 0,73–0,87; p < 0,001), der Herzinsuffizienzhospitalisierungen um 26% (HR 0,74; 95% CI 0,67–0,83), und numerisch des kardiovaskulären Todes um 12% (HR 0,88; 95% CI 0,77–1,00).
Fazit: Diese Daten zeigen einen signifikanten Benefit der Therapie, mit SGLT2-Hemmern v. a. hinsichtlich Hospitalisierung und Symptomatik bei Patienten mit Herzinsuffizienz und einer LVEF > 40% für die bislang nur eingeschränkt therapeutische Optionen vorhanden waren.
WFR
Rivaroxaban vs. VKA für rheumatisches Vorhofflimmern
INVICTUS-Studie unterstützt Standardbehandlung
Die grösste Studie bei Patienten mit rheumatischen Herzerkrankungen, die randomisierte INVICTUS-Studie wurde in einer Hot Line Session von Prof. Dr. Ganesan Karthikeyan, New Delhi, vorgestellt. Die Studie hatte zum Ziel, die Nichtunterlegenheit von Rivaroxaban im Vergleich zu Vitamin-K-Antagonisten (VKA) bei rheumatischem Vorhofflimmern zu beweisen. Es wurden 4.531 Patienten mit rheumatischem Vorhofflimmern und einer Mitralklappenöffnungsfläche von ≤ 2 cm2 oder einem CHA2DS2-VASc-Score ≥ 2 in die Gruppen Rivaroxaban oder VKA mit einer Ziel-INR zwischen 2 und 3 randomisiert. Der primäre Endpunkt war ein Komposit aus Schlaganfall/systemische Embolie, Myokardinfarkt oder Tod aufgrund vaskulärer oder unbekannter Ursache. Nach einem Follow-up von durchschnittlich 3,1 Jahren wurde der primäre Endpunkt in der Rivaroxaban-Gruppe häufiger erreicht als in der VKA-Gruppe (HR 1,25, 95% CI 1,10–1,41; p = 0,001).
Fazit: Das Antikoagulans der Wahl bei Patienten mit rheumatischem Vorhofflimmern ist weiterhin ein Vitamin-K-Antagonist.
WFR
Interview
Im Gespräch mit Prof. Dr. med. Franz Eberli

Welche neuen Studienergebnisse, die am ESC präsentiert wurden, haben Sie besonders interessiert? Welche haben Ihre Erwartungen bestätigt, welche waren enttäuschend?
Für den praktischen Alltag haben mich die Studien über den Wert der abendlichen Einnahme der Blutdruckmedikamente (TIME Studie) und den Wert der Polypill (SECURE Studie) interessiert. Die TIME Studie zeigte, dass der Zeitpunkt der Einnahme der anti-hypertensiven Medikamente keinen Einfluss auf den Behandlungserfolg hat, was für Praktiker, Kardiologen und nicht zuletzt die betroffenen Patienten bedeutend ist. Die Polypill-Studie war zwar für den primären kombinierten Endpunkt positiv, aber aufgrund der unklaren Gründe für das positive Ergebnis und der inkonsistenten Resultate eher enttäuschend.
Interessiert hat auch, ob der SGLT-2-Inhibitor Dapagliflozin bei der Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF) (DELIVER Studie) die guten Resultate der ähnlichen Studie mit Empagliflozin (EMPERER PRESERVED) bestätigen kann. Dies ist der Fall, und es scheint ein Klasseneffekt der SGLT-2 Inhibitoren vorzuliegen. Die beiden Studien haben zudem deren Stellenwert in der Behandlung von HFpEF Patienten definiert.
Bei Patienten mit Symptomen oder Verdacht auf eine koronare Herzkrankheit wird heute in den meisten Fällen als erste Untersuchung ein Koronar-CT angeordnet. Wird im Koronar-CT eine Stenose vermutet (>50% Stenose in Gefässen >2mm), kann mittels funktionellen Tests deren hämodynamische Bedeutung eruiert werden. Die DanNICAD-2 Studie hat untersucht, ob es besser ist eine Stress-MRI Untersuchung oder eine Rb-82-PET Untersuchung durchzuführen. Sie fand, dass beide Untersuchungen gleichwertig sind. Goldstandard war eine angiografische Stenose >90% oder eine bewiesene hämodynamische Signifikanz mittels fraktionierter Flussreserve. Eine schwere und hämodynamisch signifikante Stenose fand sich in 44% der in der Koronar-CT vermuteten Fälle. Überraschend und ernüchternd war die schlechte Sensitivität von MR und PET (59% resp. 64%). Das heisst bei über einem Drittel der Patienten wurde eine Ischämie verursachende Stenose mittels MR oder PET nicht diagnostiziert. Bezüglich angiografisch schwerer Stenose (>70% Lumeneinengung) waren beide Untersuchungen etwas besser (Sensitivität 83% resp. 89%). Zum sicheren Ausschluss einer Ischämie waren MR und PET ebenfalls vergleichbar (Spezifität 84% resp. 89%). Es berechnete sich ein positiver prädiktiver Wert von 76% resp. 79% und ein negativ prädiktiver Wert von 73% resp. 75% für das MR respektive das PET. Die Befunde bestätigen, dass die Koronar-CT Untersuchung vielfach den Schweregrad der Koronarstenosen nicht genau quantifizieren und deren funktionelle Bedeutung nicht abschätzen kann. Die Studie zeigt aber auch die Grenzen der nicht-invasiven funktionellen Diagnostik. Trotz bester Technik verbleibt bei über 20% der Patienten eine Unsicherheit.
Die Polypill-Studie – Ihre Meinung? Was wäre die beste Zusammensetzung der Pille?
In der Polypill-Studie führte die Polypill, welche aus Aspirin + Atorvastatin + Ramipril bestand, zu einer Reduktion des kombinierten kardiovaskulären Endpunktes (kardiovaskuläre Mortalität, Myokardinfarkt, Schlaganfall, dringende Revaskularisation) in der Sekundärprävention nach Myokardinfarkt (9.5% versus 12,7%). Damit bestätigte die Polypill-Studie frühere Studien in der Primärprävention, die einen Vorteil der Polypill gegenüber der üblichen Medikation gezeigt hatten. Die Studie zeigte auch, dass die Reduktion der Tablettenzahl zu einer Verbesserung der Medikamentenadhärenz führte.
Soll deshalb nun die Polypill im klinischen Alltag breitflächig eingeführt werden? Dazu ist es zu früh. Denn die Polypill-Studie hat wenige, streng selektionierte Patienten eingeschlossen. Zudem sind in der Nachbeobachtungszeit viele Patienten verloren gegangen und die Resultate sind nicht konsistent. Zuerst zur Patientenselektion: eingeschlossen wurden nur Patienten mit einem Alter von >75 Jahren oder >65 Jahren, wenn sie zusätzlich zum Indexinfarkt einen Diabetes, eine Niereninsuffizienz oder ein vorausgegangenes kardiovaskuläres Ereignis (Myokardinfarkt, Schlaganfall, PVI oder Bypassoperation) hatten. Es waren also alte, kranke Patienten, welche multiple andere Medikamente benötigten. Es kann erwartet werden, dass eine Reduktion der Pillenzahl bei diesen Patienten zu einer besseren Adhärenz führt. Erstaunlicherweise war aber die Medikamentenadhärenz in beiden Gruppen nicht toll. In der Polypillgruppe war die Adhärenz in 71%, in der Kontrollgruppe in 63% befriedigend. Die bessere Adhärenz in der Polypillgruppe resultierte auch nicht in einer Verbesserung des LDL-Cholesterins oder in tieferen Blutdruckwerten. Die Reduktion des Endpunktes ist daher schwer zu erklären. Ob die etwas regelmässigere Einnahme von Aspirin den Unterschied ausmachte, ist zumindest zweifelhaft. Schwer zu erklären ist auch der Umstand, dass die nicht-tödlichen kardiovaskulären Ereignisse (erneuter Myokardinfarkt, Schlaganfall, Notwendigkeit einer Revaskularisation) nur numerisch gesenkt wurden, der kardiovaskuläre Tod aber deutlich reduziert wurde (48 = 3.9% vs. 71 = 5.8%). Gleichzeitig kam es in der Polypillgruppe aber zu einer Zunahme der nicht kardiovaskulären Mortalität (67 = 5.4%) gegenüber der Kontrollgruppe (46 = 3.7%). Die Gesamtmortalität in beiden Gruppen war identisch (115 =9.3% versus 117 = 9.5%). Die Polypill hat also zu einer leichten Abnahme der nicht-tödlichen kardiovaskulären Ereignisse geführt, aber nicht zur Reduktion der Gesamtmortalität. Ein etwas enttäuschendes Resultat.
Es gibt auch technische Probleme, die einer Einführung der Polypill entgegenstehen. Valentin Fuster, der Principal Investigator der Polypill Studie hat anlässlich der Präsentation der Studienergebnisse selber vor zu grossem Enthusiasmus gewarnt. Es dauerte nach seinen Angaben 15 Jahre (!) um die in der Studie verwendete Polypill so herzustellen, dass die Absorption, Bioverfügbarkeit und Pharmakodynamik der einzelnen Komponenten mit den Originalpillen identisch waren. Es ist unwahrscheinlich, dass die Industrie die Produktion, Testung des Produkts und die Vermarktung der verschiedenen Polypills übernehmen wird.
Die Erhöhung der Medikamentenadhärenz durch die Reduktion der Pillenzahl ist jedoch unbestrittenermassen eine erstrebenswerte und wünschenswerte Massnahme. Ein erfolgversprechenderer Ansatz als die Polypill dürfte bei Patienten mit multiplen Risiken allerdings der Einsatz von Kombinationspräparaten sein. Zum Beispiel die Bündelung der cholesterinsenkenden, der anti-hypertensiven Medikamente und der Anti-diabetika in jeweiligen Kombinationspräparaten (zum Beispiel: Ezetimib+Statin, ACE-Hemmer+Kalziumantagonist, Metformin+SGLT-2 Inhibitor). Damit kann in den meisten Fällen die Pillenzahl halbiert werden und es bietet zudem den Vorteil, dass die Therapie den individuellen Bedürfnissen angepasst werden kann.
Metformin weiterhin bei jedem Patienten mit T2DM?
Metformin ist weiterhin als die erste Wahl für eine anti-diabetische Therapie bei Patienten mit Diabetes auch bei einer Herzinsuffizienz empfohlen. Metformin ist wirksam, sicher und hat wenig Nebenwirkungen. Zudem ist das Medikament kosteneffizient. Die neuen anti-diabetischen Medikamente, die GLP-1 Agonisten und die SGLT-2 Inhibitoren sind in grossen Studien getestet worden und haben ihre gute anti-diabetische Wirkung und Organprotektion bewiesen. Sie sind daher gute, aber teure Alternativen zu Metformin.
Am diesjährigen ESC wurden die Resultate der DELIVER Studie vorgestellt, welche Dapagliflozin gegen Placebo bei Patienten mit Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF) (LVEF >40%) verglich. Dapagliflozin reduzierte den kombinierten Endpunkt Hospitalisationen für Herzinsuffizienz und kardiovaskuläre Mortalität (16.4% versus 19.5%). Damit waren die Resultate fast identisch mit der Studie an HFpEF Patienten mit Empagliflozin, der EMPEROR PRESERVED Studie. Die Resultate der beiden Studien wurden denn auch in einer kombinierten Analyse ebenfalls präsentiert. Diese kombinierte Analyse zeigte, dass der positive Effekt der SGLT-2 Inhibitoren sowohl bei leicht reduzierter Auswurffraktion als auch bei vollständig erhaltener Auswurffraktion vorhanden war. Dementsprechend wurden beide Studien als «real game changer» bei der HFpEF gelobt.
Bei nüchterner Betrachtung sind die Resultate aber nicht überwältigend. In beiden Studien (DELIVER und EMPEROR PRESERVED) wurde bei den HFpEF Patienten weder die kardiovaskuläre Mortalität noch die Gesamtmortalität gesenkt. In der EMPEROR PRESERVED Studie senkte Empagliflozin zwar die Hospitalisation wegen Herzinsuffizienz, welche etwa 20% der Hospitalisationen in der Nachbeobachtungszeit ausmachten. Die Gesamtzahl der Hospitalisationen wurde aber nicht gesenkt! Die DELIVER Studie fand wie gesagt genau die gleiche Wirksamkeit mit dem SGLT-2 Inhibitor Dapagliflozin. Klugerweise wurde aber die Gesamtzahl der Hospitalisationen in der DELIVER Studie weder in der Präsentation am ESC, noch im Artikel im New England Journal of Medicine mitgeteilt. Ein Schelm ist, wer hinter dieser Unvollständigkeit eine Absicht vermutet! Es ist anzunehmen, dass SGLT-2 Inhibitoren bei Patienten mit HFpEF also ausser der Senkung der Anzahl der Hospitalisationen wegen Herzinsuffizienz keinen signifikanten Effekt auf die harten Endpunkte haben und die Gesamtzahl der Hospitalisationen unverändert hoch bleibt.
Unbestritten ist, dass die SGLT-2 Inhibitoren bei einigen Patienten mit HFpEF die Dyspnoe senken und damit die Leistungsfähigkeit verbessern. Sie stellen deshalb doch die gewünschte Erweiterung der medikamentösen Behandlung der HFpEF dar. Da die Aetiologie der HFpEF aber vielfältig ist, kann beim einzelnen Patienten der Erfolg der Therapie nicht vorausgesagt werden.
Wie beurteilen Sie eBRAVE? Werden sich Smartphones in der Kardiologie durchsetzen?
In der eBRAVE-Studie wurden beim Suchen mit der Smartwatch mehr Personen mit Vorhofflimmern gefunden als mit dem routinemässigen, symptombasierten Suchen nach Vorhofflimmern und dementsprechend mehr Patienten mit oraler Antikoagulation behandelt. Ob dies allerdings einen günstigen Effekt auf die thrombo-embolischen Ereignisse hat, ist unsicher. In der LOOP-Studie vom letzten Jahr hat diese Strategie keine Reduktion der Schlaganfälle gebracht. Dies hat insbesondere damit zu tun, dass unklar ist, ob kurze, klinisch stumme Vorhofflimmerepisoden eine orale Antikoagulation nötig machen. Smartphones erlangen also bei der Rhythmusdiagnostik eine zunehmende Bedeutung, ihr Stellenwert ist aber noch nicht klar.
Welche der neu vorgestellten Guidelines werden Einfluss auf Ihre Praxistätigkeit haben?
Die neuen Guidelines der kardialen Abklärung und Behandlung bei nicht kardialen Operationen legen weiterhin ein nach Risiko der Operation und kardiovaskulärem Risiko des Patienten abgestuftes Vorgehen vor. Bei Patienten mit kardiovaskulären Vorerkrankungen oder multiplen Risikofaktoren wird eine gründliche kardiale Anamnese, ein klinischer Untersuch, ein EKG und wenn Zeichen für eine kardiale Erkrankung (z.B. ein Herzgeräusch) vorliegen, eine Echokardiografie empfohlen. Die neuen Guidelines legen neu ein grosses Gewicht auf das Erfassen von ischämischen Ereignissen und deren perioperativer Behandlung. Perioperative Ischämien, d.h. Myokardinfarkte laufen wegen fehlenden oder nicht typischen Schmerzen häufig unerkannt ab. Es sollen daher vor der Operation mittleren und hohen Risikos die Biomarker bestimmt werden, einerseits zum Screening auf myokardiale Schäden und andererseits, um einen Ausgangswert vor der Operation zu haben. Nach der Operation sollen die Biomarker routinemässig mehrmals bestimmt werden. Bei Ansteigen der Biomarker kann die Ischämie diagnostiziert und rechtzeitig behandelt werden.
Die neuen Guidelines über die pulmonale Hypertonie werden die Praxis insofern beeinflussen, dass neu ein mittlerer pulmonal-arterieller Druck von >20 mmHg (in den letzten Guidelines >25 mmHg) zur Diagnose einer pulmonalen Hypertonie führt. Diese tiefere Schwelle ist gewählt worden, weil bei der seltenen primären pulmonalen Hypertonie und der seltenen chronisch thrombo-embolischen Hypertonie ab dieser Schwelle eine Abnahme der Lebensdauer gefunden wurde. Inwieweit dies für die viel häufigere pulmonale Hypertonie bei der Linksherzinsuffizienz zutrifft, ist allerdings nicht klar. Die Schwelle für die Verdachtsdiagnose einer pulmonalen Hypertonie in der Echokardiografie (Druckgradient zwischen RV und rechtem Vorhof: TVR>2,8 m/s) ist aber gleich belassen worden. Neu sind erstmals auch diagnostische Kriterien für die belastungsabhängige pulmonale Hypertonie festgelegt worden. Dabei wird die belastungsabhängige pulmonale Hypertonie definiert als ein Anstieg des Quotienten mittlerer PA Druck/cardiac output von >3mmHg/l/min von Ruhe zur maximalen Belastung.
Ihre persönlichen Highlights des diesjährigen ESC-Kongresses 2022?
Besonders aufgefallen an diesem ESC sind die vielen neutralen Studienresultate. Diese sogenannten negativen Studien sind aber sehr wertvoll, weil sie wie die positiven Studien Therapiestrategien definieren oder bestärken. So hat die PERSPECTIVE Studie sorgfältig untersucht, ob Sacubitril/Valsartan (Entresto) zur Entwicklung einer Alzheimer-Krankheit beiträgt und konnte dies definitiv ausschliessen. Der fehlende negative Effekt von Sacubitril/Valsartan auf die Hirnfunktion ist wichtig für die Sicherheit des Medikaments bei langjähriger Anwendung. Ein weiteres bedeutendes negatives Studienergebnis ist die fehlende Wirksamkeit von Allupurinol als ergänzende anti-oxidative Medikation bei der koronaren Herzkrankheit (ALL-Heart Studie). Die Studie ergänzt all die bisherigen negativen Studien zu Anti-oxidantien (z.B. Vitamine) bei der koronaren Herzkrankheit und weist auf die fehlende Machbarkeit des Verbesserns der Behandlung der KHK durch eine anti-oxidative Therapie hin. Ebenfalls neutral waren die Ergebnisse der REVIVED-BCIS2 Studie und die ISCHEMIA CKD Extended Studien. Die REVIVED-BCIS2 Studie untersuchte, ob eine initiale Strategie mit perkutaner Revaskularisation (PCI) einen Vorteil bringt gegenüber optimaler medikamentöser Therapie und Revaskularisation nur bei Verschlechterung der Klinik in Patienten mit reduzierter Auswurffraktion (LVEF <35%) und koronarer Mehrgefässerkrankung. Die ISCHEMIA CKD Extended untersuchte den Wert einer initial invasiven versus einer initial konservativen Strategie bei stabilen Patienten mit schwerer Niereninsuffizienz und Mehrgefässerkrankung in der Nachbeobachtungsphase von 5 Jahren. Ausgeschlossen waren Patienten mit vorausgegangenem akutem Koronarsyndrom oder stark symptomatische Patienten. Auffallend bei beiden Studien war die hohe Sterblichkeit. In der REVIVED-BCIS2 Studie betrug sie 37% in der PCI Gruppe und 38% in der medikamentösen Gruppe. In der ISCHEMIA CKD Extended Studie betrug die Gesamtmortalität nach fünf Jahren 40,5% vs 37.4% und die kardiovaskuläre Mortalität 29% vs 27% in der invasiven vs. der konservativen Gruppe. Bei der ischämischen Kardiomyopathie und bei der Niereninsuffizienz mit koronarer Dreigefässerkrankung hat also eine routinemässige initiale invasive Abklärung und/oder Revaskularisation keinen Überlebensvorteil gebracht. Allerdings haben in beiden Studien die initial konservativ behandelten Patienten im Verlauf mehr spontane Myokardinfarkte erlitten und klagten über mehr Angina pectoris und schlechtere Lebensqualität.
Eleonore E. Droux
DELIVER: Dapagliflozin bei Herzinsuffizienz mit leicht reduzierter oder erhaltener LVEF
Dapagliflozin stellt seinen klinischen Nutzen auch bei Patienten mit Herzinsuffizienz und leicht reduzierter oder erhaltener linksventrikulärer Ejektionsfraktion unter Beweis, wie Prof. Dr. S. Solomon, Boston, in einer Hot Line Session zeigte. Die doppelblinde, placebokontrollierte Studie randomisierte 6.263 symptomatische Patient:innen (NYHA-Stadium II-IV, LVEF > 40% [mittlere LVEF 54%]) zu Dapagliflozin versus Placebo. Über eine mediane Follow-Up-Zeit von 2,3 Jahren reduzierte Dapagliflozin den primären kombinierten Endpunkt, kardiovaskulärer Tod und Verschlechterung der Herzinsuffizienz, um 18% (HR 0,82; 95% CI 0,73–0,92; p < 0,001). Sekundäre Endpunkte wie Herzinsuffizienzhospitalisierungen und kardiovaskulärer Tod (RR 0,77; 95% CI 0,67-0,89), sowie Lebensqualität (mittlerer Unterschied im KCCQ-Score 2,4; 95% CI 1,6–3,2) wurden ebenfalls reduziert.
Fazit: Neben EMPEROR-Preserved ist DELIVER die zweite Landmarkstudie, die Evidenz zur Implementierung von SGLT2-Hemmern zur Behandlung von symptomatischen Herzinsuffizienz-Patient:innen mit einer LVEF > 40% belegt.
WFR
MASTER-DAPT: Ergebnisse über 15 Monate
In der von Prof. Dr. Marco Valgimigli, Lugano, in einer Hot Line Session vorgestellten MASTER-DAPT-Studie wurden Patienten mit akutem oder chronischem Koronarsyndrom und hohem Blutungsrisiko einer PCI mit biologisch abbaubaren, mit Sirolimus beschichteten Polymerstents unterzogen. Patienten, die frei von ischämischen und blutungsbedingten Ereignissen waren und einen Monat nach der PCI ein DAPT-Schema einhielten, wurden nach dem Zufallsprinzip in eine sofortige DAPT-Unterbrechung und eine Fortsetzung der Behandlung für bis zu einem Jahr eingeteilt. Die einmonatige DAPT war in Bezug auf das Auftreten von unerwünschten kardialen oder zerebrovaskulären Ereignissen nicht unterlegen und war nach 11 Monaten mit einer geringeren Anzahl schwerer oder klinisch relevanter nicht-schwerwiegender Blutungen verbunden.
Im Anschluss an die 12-monatige Studie erhielten die Patienten beider Behandlungsgruppen eine klinische Routineversorgung nach dem Ermessen ihres Arztes. Die Forscher erfassten die Medikation und die unerwünschten Ereignisse während der folgenden drei Monate. Von den 2295 bzw. 2284 Patienten, die in die verkürzte bzw. die Standard-DAPT randomisiert wurden, begannen 2205 bzw. 2186 Patienten nach 12 Monaten mit der Routineversorgung. Eine vollständige Nachbeobachtung nach 15 Monaten war bei 99,8% bzw. 99,9% der Patienten in der verkürzten bzw. der Standardtherapie möglich.
Bei der Routineversorgung tendierten die Ärzte dazu, die in der Studie zugewiesene Behandlung fortzusetzen. In den Leitlinien wird empfohlen, dass Patienten, die keine oralen Antikoagulanzien (OAK) erhalten, die DAPT absetzen sollten, aber mehr als 15% der Patienten, die keine OAC erhielten, waren nach 15 Monaten im Standard-DAPT-Arm noch auf DAPT, was etwa dreimal so hoch war wie die entsprechende Zahl im verkürzten Arm. Obwohl in den Leitlinien empfohlen wird, dass OAK-Patienten, wenn sie frei von wiederkehrenden ischämischen Ereignissen oder wiederholten Eingriffen sind, die alleinige Thrombozytenaggregationshemmer-Therapie (SAPT) absetzen sollten, nahmen mehr als ein Viertel der Patienten in der Standard-DAPT-Gruppe immer noch eine SAPT ein, verglichen mit 14% in der verkürzten Behandlungsgruppe. In der multivariaten Modellierung war die vorherige Zuteilung zur verkürzten Behandlung ein starker unabhängiger Prädiktor für die SAPT im Vergleich zur DAPT bei Patienten, die keine antithrombozytäre Therapie erhielten, und für die keine antithrombozytäre Therapie im Vergleich zur SAPT bei Patienten mit künstlicher Beatmung in Frage kommt.
Professor Valgimigli sagte: «Wir haben auch festgestellt, dass das Blutungsrisiko mit Ausnahme des Alters keinen Einfluss auf die Wahl zwischen DAPT und SAPT hatte, ebenso wenig wie frühere Blutungen. Im Gegensatz dazu veranlassten klinische oder verfahrenstechnische Marker für das Ischämierisiko die Ärzte, die DAPT über ein Jahr hinaus zu verlängern».
Die 15-Monats-Ergebnisse entsprechend der ursprünglichen Behandlungszuweisung für die drei primären Ergebnisse der Hauptstudie: 1) unerwünschte klinische Nettoereignisse (NACE; zusammengesetzt aus Todesfällen insgesamt, Myokardinfarkt, Schlaganfall und schweren oder klinisch relevanten nicht-schwerwiegenden Blutungen); 2) schwere unerwünschte kardiale und zerebrale Ereignisse (MACCE; zusammengesetzt aus Todesfällen insgesamt, Myokardinfarkt und Schlaganfall); und 3) schwere oder klinisch relevante nicht-schwerwiegende Blutungen (Blutungen vom Typ 2, 3 oder 5 des Bleeding Academic Research Consortium).
NACE trat bei 199 (8,7%) bzw. 214 (9,5%) Patienten in der verkürzten und der Standard-DAPT-Gruppe auf, was einer Hazard Ratio (HR) von 0,92 (95% Konfidenzintervall [CI] 0,76-1,12; p=0,399) und einer Risikodifferenz von -0,75 Prozentpunkten (95% CI -2,42 bis 0,93) entspricht. MACCE trat bei 158 (6,9%) bzw. 167 (7,4%) Patienten in der verkürzten und der Standard-DAPT-Gruppe auf (HR 0,94; 95% KI 0,76-1,17; p=0,579), was einer Risikodifferenz von -0,51 Prozentpunkten (95% KI -2,01 bis 1,00) entspricht. Schwerwiegende oder klinisch relevante nicht-schwerwiegende Blutungen blieben in der Kurztherapie im Vergleich zur Standardtherapie geringer (167 [7,4%] gegenüber 239 [10,7%]; HR 0,68; 95% KI 0,56-0,83; p=0,0001), was einer Risikodifferenz von -3,25 Prozentpunkten (95% KI -4,93 bis -1,58) entspricht.
Fazit: Diese Langzeitdaten stellen ein weiteres Signal für die Überlegenheit dieses Vorgehens dar. Professor Marco Valgimigli sagte: «Die Ergebnisse unterstreichen die Notwendigkeit, Patienten mit hohem Blutungsrisiko zu identifizieren, die sich einer perkutanen Koronarintervention (PCI) unterziehen, damit im Vorfeld Entscheidungen über die Thrombozytenaggregationsbehandlung und deren Dauer getroffen werden können, um das Blutungsrisiko zu mindern und die Ergebnisse zu optimieren.»
WFR
PACIFIC-AMI: Faktor XIa-Inhibition «on top of» DAPT
In der Prof. Dr. John Alexander, Durham, in einer Hot Line vorgestellten multizentrischen Phase II-Studie wurde die Wirksamkeit und Sicherheit von drei Dosierungen des selektiven Faktor XIa-Inhibitors Asundexian (10, 20 sowie 50 mg täglich) versus Placebo bei 1.600 Patienten mit Myokardinfarkt zusätzlich zu einer bereits bestehenden dualen Antiplättchentherapie (DAPT) getestet.
Unter Hochdosis-Asundexian konnte eine > 90 % Blockade der Faktor XIa-Aktivität erreicht werden, dies ohne signifikante Erhöhung relevanter Blutungsereignisse im Vergleich zur Kontrollgruppe. Es zeigten sich allerdings ebenfalls keine Unterschiede in der Reduktion kardiovaskulärer Ereignisse (Tod, Myokardinfarkte, Schlaganfälle, Stent-Thrombosen) zwischen Asundexian 50 mg und Placebo.
Fazit: Die Ergebnisse der PACIFIC-AMI-Studie deuten auf kein erhöhtes Blutungsrisiko einer Hochdosis-Faktor XIa-Inhibition «on top» einer DAPT. Endgültige Daten zur Wirksamkeit von Asundexian nach Myokardinfarkt werden in der Phase III-Folgestudie erwartet.
WFR
Können Smartphones die Erkennung von Vorhofflimmern bei älteren Erwachsenen verbessern?
DIe von Prof. Axel Bauer, Innsbruck, in einer Hot Line vorgestellte eBRAVE-AF-Studie randomisierte 5.551 Patienten mit Herzinsuffizienz-und einer LVEF > 40 zu einem routinemässigen Symptom-basierten Screening von Vorhofflimmern (VHF) im Vergleich zu einer e-Health-basierten Strategie (mit Crossover nach 6 Monaten). Diese bestand aus repetitivem 1-Minuten photoplethysmographischen Screening per Smartphone-App (Preventicus Heartbeats, Preventicus, Jena, Germany); bei Auffälligkeiten gefolgt von einem 14-Tage-EKG-Patch (CardioMem CM 100 XT, Getemed, Teltow, Germany). In die Studie eingeschlossen wurden: Versicherungsnehmer einer grossen Krankenkasse, Alter ≥ 50 Jahre, CHA2DS2-VASc ≥ 1 (bei Frauen ≥ 2). Ausschlusskriterien waren VHF, orale Antikoagulation. Der primäre Endpunkt dieser Studie war die Initiierung einer oralen Antikoagulation aufgrund von detektiertem VHF innerhalb von 6 Monaten (Einschluss 2/20 bis 7/21 mittels Anschreiben, ohne Arzt-Patienten-Kontakt). Das klinische Follow-up betrug 12 Monate mittels App-basiertem Fragebogen alle 4 Wochen.
Der primäre Endpunkt wurde in beiden Phasen (vor und nach Cross-over) erreicht. Die VHF-Detektionsrate war in der Smartphone-App-Gruppe jeweils mehr als doppelt so hoch wie in der symptombasierten, konventionellen Gruppe. Bemerkenswert ist, dass die VHF-Detektionsrate in der e-Health Gruppe nur 1,7 % war (medianes Patientenalter 65 Jahre, CHA2DS2-VASc = 3) und, dass von den angeschriebenen Patienten 61.397 (> 90 %) nicht teilnahmen.
Fazit: Diese Studie belegt die Durchführbarkeit eines grossflächigen VHF-Screenings via Smartphone-App in der älteren Bevölkerung. Dabei zeigte sich die Überlegenheit der niederschwelligen, App-basierten Methode gegenüber dem konventionellen, rein symptombasierten Screening.
WFR
SECURE Trial: Kann Polypille die Sekundärprävention nach Herzinfarkt verbessern
Nach einem Herzinfarkt nehmen weniger als 50% das für die sekundäre kardiovaskuläre Prävention verschriebene Multimedikamentenregime konsequent ein. Eine Polypille hat das Potenzial, die Compliance und damit die Ergebnisse der Patienten zu verbessern, aber wird sie auch funktionieren? Bislang fehlten jedoch Daten aus grossen randomisierten Studien, die die prognostische Überlegenheit der Polypill zeigten. In einer Hot Line Session präsentierte Prof. Dr. Valentin Fuster, Madrid, New York, die Resultate der SECURE Studie, der ersten randomisierten Studie zur Untersuchung der Effekte einer Polypille auf wiederkehrende kardiovaskuläre Ereignisse bei Patienten nach Myokardinfarkt.
In der SECURE-Studie wurden Patienten nach Myokardinfarkt und mit hohem Risikoprofil zu entweder einer Polypille (ASS + Ramipril + Atorvastatin, in unterschiedlichen Dosierungen) vs. Standardtherapie (3 Tabletten der einzelnen Substanzen) randomisiert. Bei einem 3 jährigen Follow-up nach dem Herzinfarkt zeigte sich, dass Patienten mit der „Polypill“ deutlich weniger Re-Infarkte, Schlaganfälle, Notwendigkeit einer Revaskularisation sowie kardiovaskuläre Todesfälle erlitten (9,5 % gegenüber 12,7 % in der Standardgruppe) Während alle Komponenten des primären Endpunkts zum Behandlungseffekt beitrugen, war der hauptsächliche Driver der kardiovaskuläre Tod, welcher bei 3.9% und 5.8% der Patienten in der Polypill-Gruppe und in der Kontrollgruppe mit üblicher Behandlung auftrat. Es gab auch eine 30% Reduktion des wichtigsten sekundären Endpunkts kardiovaskulärer Tod, nicht-tödlicher Myokardinfarkt, und Schlaganfall. Mit Raten von 8.2% und 11.7 % in der Polypillgruppe und der Gruppe mit üblicher Behandlung. Die Gesamtmortalität war in den beiden Gruppen gleich (HR 0.97; 0.75 bis 1.25).
Fazit: Die Polypille könnte ein integraler Bestandteil von Strategien zur Verhinderung von Herz-Kreislauf-Ereignissen bei Patienten nach einem Herzinfarkt werden, indem die Behandlung vereinfacht und die Therapietreue verbessert wird.
WFR
DANCAVAS: Effekte eines kardiovaskulären Screening-Programms bei Männern
In einer Hot Line Session präsentierte Prof. Dr. Axel Cosmus Pyndt Diederichsen, Odense, die Daten der dänischen Cardiovascular Screening (DANCAVAS)-Studie. In DanVAVAS wurden 46.611 Männer 1:2 randomisiert und zu einem kardiovaskulären Screening-Programm eingeladen. Dies bestand aus einem EKG-getriggerten Nativ-CT zur Erfassung des koronaren Calcium-Scores (CAC), aortaler und iliakaler Aneurysmen sowie Vorhofflimmern, einer Ankle-Brachial-Index (ABI)-Messung sowie der Bestimmung von HbA1c und Gesamtcholesterin. Bei positiven Resultaten wurden spezifische Massnahmen wie z. B. eine Therapie mit Aspirin und Atorvastatin 40 mg empfohlen.
Nach 5,6 Jahren zeigte sich eine nicht signifikante 5% relative Risikoreduktion für Gesamtmortalität: 12.6% der Männer in der Screening-/Interventionsgruppe und 13.1% in der Kontrollgruppe starben (p=0.062). Die Anzahl der Personen, die zum Screening eingeladen werden müssen, um einen Todesfall zu verhindern, beträgt 155.
Obschon es keinen Unterschied in den Sterberaten zwischen den Gruppen bei 70jährigen und älteren Männern gab, war das Screening-/Intervention mit einer 11% Reduktion des Mortalitätsrisikos bei zwischen 65 und 69 Jahre alten Männern. Eine post hoc Analyse zeigte eine Screening-assoziierte Reduktion des kompositen Endpunkts von Tod, Schlaganfall oder Myokardinfarkt von 7% in der Gesamtpopulation (p=0.016) und diese stieg an auf 11>% bei Männern im Alter von 65-69 Jahren.
Fazit: Vor allem bei unter 70-Jährigen könnte die Einführung eines umfassenden kardiovaskulären Screening-Programms zu einer Reduktion von kardiovaskulären Ereignissen führen.
WFR
REVIVED-BCIS2
Die in einer Hot Line Session von Prof. Dr. Divaka Perera, London, präsentierte REVIVED-BCIS2 Studie ergab die ersten randomisierten Daten zur Wirksamkeit und Sicherheit einer perkutanen Koronarintervention (PCI) bei ischämischer Kardiomyopathie mit schwer eingeschränkter linksventrikulärer Funktion (LVEF 35 % oder weniger). Verglichen wurde mit optimaler medikamentöser Therapie nach aktuellem Leitlinienstandard. Insgesamt 700 Patienten aus 40 Zentren in Grossbritannien wurden nach dem Zufallsprinzip im Verhältnis 1:1 entweder PCI mit optimaler medizinischer Therapie oder nur optimaler medizinischer Therapie zugeordnet. Das Durchschnittsalter der Teilnehmer betrug 70 Jahre, 88% waren Männer und die mittlere linksventrikuläre Ejektionsfraktion betrug 27%. Der primäre Endpunkt war die Zusammensetzung aus Todesursache oder Krankenhausaufenthalt wegen Herzinsuffizienz. Zu den sekundären Endpunkten gehörten die linksventrikuläre Ejektionsfraktion nach 6 und 12 Monaten und Massnahmen zur Lebensqualität.
Trotz der Hypothese, dass PCI das ereignisfreie Überleben innerhalb der Patientenpopulation verbessern würde, berichtete Perera, dass während einer medianen Nachbeobachtungszeit von 3,4 Jahren der primäre Endpunkt bei 129 (37,2%) Patienten in der PCI-Gruppe und 134 (38%) Patienten in der medizinischen Therapiegruppe allein für eine Hazard Ratio (HR) von 0,99 (95%-Konfidenzintervall 0,78–1,27), p=0,96) reichte. “Die wichtigste Botschaft, die ich mit nach Hause nehme, ist, dass dies jetzt ein definitives Ergebnis ist, wir haben endlich RCT-Beweise [randomisierte kontrollierte Studie], die es ermöglichen, die Richtlinien einerseits zu stärken und andererseits die klinische Praxis auf der ganzen Welt zu rationalisieren”, kommentierte Perera. Im wichtigsten sekundären Endpunkt der Studie, der linksventrikulären Ejektionsfraktion (LVEF), wurde nach sechs und 12 Monaten kein signifikanter Unterschied zwischen den Gruppen beobachtet.
Aber wie bei dieser Studie wurde (wie bei allen andern ähnlich gelagerten Studien, z.B. ISCHEMIA trial) die Strategie initial medikamentöse Therapie vs. initiale Revaskularisation gegeneinander verglichen. Es handelte sich also um eine Strategiestudie. Erstaunlich war, dass nur 10 % der initial medikamentös behandelten Patienten im Verlauf eine PCI brauchten. Aber nichtsdestotrotz ist es gefährlich zu sagen, dass man keine PCI brauche, weil sie nichts nütze. Die Studie hat nur noch einmal gezeigt, dass mit dieser Strategie bezüglich Mortalität kein Unterschied zwischen den Gruppen besteht. Die Symptomatik wurde auch in dieser Studie durch die PCI verbessert. Und würde man das Therapieversagen in den Endpunkt einbeziehen, dann wäre die PCI der medikamentösen Therapie überlegen.
WFR
Vergleich der Low-Density-Lipoprotein-Cholesterin-Gleichungen bei Patienten mit Dyslipidämie, die eine Hemmung des Cholesterin-Ester-Transferproteins erhalten
Die Senkung der Low-Density-Lipoproteine (LDL-C) ist für die Prävention von Herz-Kreislauf-Erkrankungen unerlässlich. Die wirksame Umsetzung der Erkenntnisse zur Senkung der LDL-C zur Maximierung des klinischen Nutzens, hängt von der Verfügbarkeit genauer LDLC-Ergebnisse zur Steuerung der Therapie ab. Ausserdem haben frühere Arbeiten die Möglichkeit gezeigt, dass die Hemmung des Cholesterinesterase-Transferproteins (CETP) die genaue Bestimmung des LDLC beeinträchtigen könnte.
Dies hat Prof. John Kastelein dazu veranlasst, die Genauigkeit von drei klinisch eingesetzten LDLC-Gleichungen in einer klinischen Studie zur CETP-Hemmung zu vergleichen. Die Studie war eine Kooperation zwischen der Johns Hopkins Universität, Baltimore USA und, der New Amsterdam Pharma B.V, Naarden, Niederlande und den Medpace Reference Laboratories Cincinnati, USA.
Methoden
Männer und Frauen im Alter zwischen 18 und 75 Jahren mit Dyslipidämie wurden aus 17 Einrichtungen in den Niederlanden und Dänemark rekrutiert. Die Patienten wurden nach dem Zufallsprinzip einer von neun Gruppen zugeteilt, die verschiedene Kombinationen des CETP-Inhibitors TA8995, eine Statintherapie oder Placebo erhielten. In gepoolten Messungen über 12 Wochen berechneten die Autoren das LDL-C nach den Friedewald-, Martin/Hopkins- (1) und Sampson (2)-Gleichungen und verglichen die Werte mit dem LDL-C-Wert der präparativen Ultrazentrifugation (PUZ) als Referenzwert (auch Beta-Quantifizierung genannt). Auf der Grundlage früherer Literatur und Dyslipidämie-Leitlinien untersuchten die Autoren korrekte Klassifizierungen über den LDLC-Grenzwert von 1,81 mmol/L in der Untergruppe von Patienten mit Triglyceriden von 1,69-4,51 mmol/L.
Resultate
Die Analyse umfasste 242 Patienten, die 921 Beobachtungen beisteuerten. Insgesamt waren die medianen LDLC-Unterschiede zwischen Schätzungen und PUC gering: Friedewald, 0,00 (25., 75.: 0,10, 0,08) mmol/L; Martin/Hopkins, 0,02 (0,08, 0,10) mmol/L; und Sampson, 0,05 (0,03, 0,15) mmol/L. In der Untergruppe mit geschätzten LDL-C <1.81 mmol/l und Triglyceriden 1.69mmol/l unterschätzte die Friedewald-Formel LDL-C mit einer medianen Differenz von 0.25 (0.33, 0.10) gegenüber der PUK Methode, während die Martin/Hopkins Gleichung dieses Problem mit einer medianen Differenz von 0.00 (0.08, 0.10) korrigierte, und die Sampson-Gleichung mit einer medianen Differenz von 0,06 (0,13, 0,00) mmol/L eine Tendenz zur Unterschätzung zeigte. Alle drei Gleichungen zeigten eine Genauigkeit von >95%, wenn die geschätzten LDLC-Werte ≥1,81 mmol/L waren. Allerdings war der Anteil der LDLC-Beobachtungen 93,1% bei der Sampson-Gleichung.
Schlussfolgerung
Bei Europäern mit Dyslipidämie zeigt diese Analyse eine verbesserte Genauigkeit des LDLC bei Verwendung moderner LDLC-Gleichungen gegenüber der Friedewald Gleichung, insbesondere bei Verwendung der Martin/Hopkins-Gleichung. Eine hohe Genauigkeit der Martin/Hopkins-Gleichung wurde bei Personen beobachtet, die mit einer CETP-Inhibition behandelt wurden, und dies selbst bei niedrigen LDLC- und hohen Triglyceridwerten. Diese Arbeit ist besonders wichtig im Hinblick auf die derzeitigen Zielwerte für LDL-Cholesterin <0.7mmol/l. In diesem Bereich ist die Friedewald-Formel unzuverlässig, wie Prof. Dr. Kastelein betonte. Zudem zeigte sich die frühere Annahme, dass die Friedewald-Formel bis zu einem Triglyceridwert >4.5mmol/l genaue Werte liefert, als unkorrekt. Die Friedewald-Formel ist bereits ab Triglyceridwerten >1.7mmol/l nicht mehr zuverlässig.
WFR
Literatur:
1. Martin SS et al. Comparison of a novel method vs. the Friedewald equation for estimating low density lipoprotein levels from the standard lipid profile. JAMA 2013;310:2061-68
2. Sampson M et al A new equation for calculation of low density lipoprotein cholestterol in patients with normolipidemia oand7or Hypertriglyceridemia. JAMA Cardiol 2020; 5 : 540-548
ALL-HEART: Allopurinol und kardiovaskuläre Outcomes bei KHK
Allopurinol, das zur Behandlung von Gicht eingesetzt wird, hat nachweislich sekundäre Wirkungen, die sich positiv auf Herz-Kreislauf-Erkrankungen auswirken könnten. Kann es aber die Zahl der Herz-Kreislauf-Ereignisse bei Patienten mit ischämischer Herzkrankheit verringern?
Die von Prof. Isla Mackenzie, Dundee, präsentierte ALL-HEART-Studie untersuchte nun, ob Allopurinol (Zieldosis 600 mg/Tag) zusätzlich zu einer optimalen medikamentösen Therapie zu einer Verbesserung von kardiovaskulären Outcomes (Herzinfarkt, Insult, kardiovaskulärer Tod) bei KHK-Patienten führt.
Einschlusskriterien waren ein Alter > 60 Jahre, sowie das Vorhandensein einer KHK. Es konnten 5.215 Patienten eingeschlossen und 1:1 randomisiert werden. Während eines medianen Follow-up von 4,8 Jahren traten 639 Events auf, wobei sich kein signifikanter Unterschied zwischen der Verum- und der Placebogruppe zeigte (HR 1,04; p = 0,65).
Es gab auch keine Unterschiede zwischen den Gruppen bei den sekundären Endpunkten, zu denen nicht tödlicher Myokardinfarkt, nicht tödlicher Schlaganfall, kardiovaskulärer Tod, Gesamtmortalität, Krankenhausaufenthalt wegen akutem Koronarsyndrom (ACS), koronare Revaskularisation, Krankenhausaufenthalt wegen ACS oder koronarer Revaskularisation, Krankenhausaufenthalt wegen Herzinsuffizienz und alle kardiovaskulären Krankenhausaufenthalte zählten. Insgesamt starben 288 (10,1 %) Patienten in der Allopurinol-Gruppe im Vergleich zu 303 (10,6 %) Patienten in der normalen Behandlungsgruppe, was einer HR von 1,02 (95 % CI 0,87-1,20, p=0,77) entspricht.
Fazit: Allopurinol führt zu keiner Prognoseverbesserung von KHK-Patienten und hat somit keinen therapeutischen Stellenwert in dieser Indikation
WFR
Alle Patienten mit Diabetes sollten mit Metformin behandelt werden
Zur Behandlung von Typ 2 Diabetes äusserte sich Prof. Dr. med. Dr. h.c. Heinz Drexel, Bregenz. Der Referent präsentierte zunächst die Geschichte von Metformin, die 1957 mit der ersten Einführung von Metformin in das klinische Management von Diabetes beginnt.
Geschichte von Metformin
1957 Erste Einführung in das klinische Management von Diabetes. Metformin wurde jedoch nur wenig beachtet, da es weniger wirksam war als andere Biguanide zur Senkung des Blutzuckerspiegels (Phenformin und Buformin), die Ende der 1970er Jahre wegen des hohen Risikos einer Laktatazidose generell aus dem Verkehr gezogen wurden. Die Zukunft von Metformin war ungewiss, da sein Ruf trotz offensichtlicher Unterschiede durch die Assoziation mit anderen Biguaniden beschädigt wurde. Die Fähigkeit von Metformin, der Insulinresistenz entgegenzuwirken und die Hyperglykämie bei Erwachsenen ohne Gewichtszunahme oder erhöhtes Hypoglykämierisiko zu behandeln, gewann in Europa allmählich an Glaubwürdigkeit, und nach intensiver Prüfung wurde Metformin 1995 in den USA eingeführt. Langfristige kardiovaskuläre Vorteile von Metformin wurden 1998 in der UK Prospective Diabetes Study (UKPDS) festgestellt und lieferten eine neue Begründung für die Einführung von Metformin als Ersttherapie zur Behandlung von Hyperglykämie bei Typ-2-Diabetes. Sechzig Jahre nach seiner Einführung in die Diabetesbehandlung ist Metformin das weltweit am häufigsten verschriebene Medikament zur Senkung des Blutzuckerspiegels und hat das Potenzial für weitere therapeutische Anwendungen. Im Jahre 2022 wird Metformin in den meisten Ländern als primäres Glucose-senkendes Medikament bei Typ 2 Diabetes verschrieben.
Evidenz für Metformin
UKPDS: Intensive Glucosekontrolle mit Metformin senkt das Risiko für Diabetes-bezogene Endpunkte bei übergewichtigen Patienten mit Diabetes und ist mit weniger Gewichtszunahme und weniger hypoglykämischen Attacken als Insulin und Sulfonylharnstoffe assoziiert.
Weitere RCTs in Populationen mit Typ2 Diabetes (T2DM): RCT mit 304 T2DM-Patienten (5 Jahre) → signifikante Senkung des kompositen kardiovaskulären Endpunkts für Metformin im Vergleich zu Sulfonylharnstoff. RCT mit 390 Teilnehmern mit Insulin-behandeltem T2DM mit Metformin vs. Placebo (während 4.3 Jahren) → signifikante Senkung im kompositen sekundären makrovaskulären Endpunkt.
Neuere RCTs mit GLP-1 Rezeptoragonisten, ca. 75% auf Metformin. RCTs mit SGLTs-Hemmern: ca 75% auf Metformin.
Hierarchie medizinischer Daten
Die Unterschiede zwischen RCTs und Registern bestehen darin, dass RCTs für bekannte und unbekannte Störfaktoren kontrollieren, während Register nur für bekannte Störfaktoren kontrollieren (durch «propensity matching»).
Der Referent zitierte eine Studie, die die Wirkungen von Metformin im Vergleich zu Sulfonylharnstoff Monotherapie auf Langzeit-Gesamtmortalität und kardiovaskuläre Mortalität und Morbidität untersuchte (Maratgur NM et al. Ann Intern Med 2016;164:740-751). Die bereinigte HR aus Beobachtungsstudien betrug für die Gesamtmortalität 0.5 bis 0.8 (7 Studien) mit einer niedrigen Evidenzstärke. Für kardiovaskuläre Mortalität HR 0.6 bis 0.9 (3 Studien) mit moderater Evidenzstärke und für kardiovaskuläre Morbidität HR 0.3 bis 0.9 (5 Studien) mit niedriger Evidenzstärke. Die Wirksamkeit und Sicherheit von Metformin wurde bei 51675 Patienten mit Typ2 Diabetes und verschiedenen Graden der Nierenfnktion in einer Kohortenstudie aus dem Nationalen Schwedischen Diabetes-Register untersucht. Bei diesen 51 675 Patienten, die vier Jahre lang beobachtet wurden, wies Metformin ein geringeres Risiko für Herz-Kreislauf-Erkrankungen und Gesamtmortalität auf als Insulin und ein etwas geringeres Risiko für Gesamtmortalität im Vergleich zu anderen oralen hypoglykämischen Medikamenten. Bei Patienten mit Nierenfunktionsstörungen wurde kein erhöhtes Risiko für Herz-Kreislauf-Erkrankungen, Gesamtmortalität oder Azidose/schwere Infektionen festgestellt. In der klinischen Praxis überwiegen die Vorteile der Metformin-Einnahme eindeutig das Risiko schwerer Nebenwirkungen.
Beobachtungsstudien und Meta-Analysen haben einen marginalen Nutzen gezeigt. Die Studiendauer ist kritisch. Bedeutsame >Ergebnisse wurden in der UKPDS Studie erst nach 6 Jahren erhoben, so der Referent.
Zusammenfassung und Schlussfolgerung:
Metformin und das Herz ein neues Update
Wie wir heute wissen, gibt es Beweise für den Schutz des Herz-Kreislauf-Systems durch Metformin, einschliesslich der Ergebnisse von Radionuklidstudien, vieler Beobachtungsstudien und umfangreicher experimenteller Daten.
Die Art der klinischen Studien wurde jedoch durch die neue Konstellation von Ergebnisstudien überholt, die darauf abzielen, Fragen der klinischen Sicherheit zu beantworten, die lange nach der Durchführung der randomisierten Bewertungen von Metformin formuliert wurden.Die Interpretation der aktuellen Evidenzbasis für Metformin ist zweifellos eine herausfordernde Aufgabe, aber deshalb nicht weniger wichtig
WFR
CTT-Meta-Analyse der Statineffekte auf Muskelsymptome
Die Risken von Muskelsymptomen sind viel geringer als die kardiovaskulären Vorteile, so Forscher einer gross angelegten Meta-Analyse, die am ESC vorgetragen wurde. Die Ergebnisse basierten auf einer Analyse von 23 doppelblinden Studien mit Statinen, die je mindestens 1000 Teilnehmer umfassten. Alle Studien wiesen eine geplante Behandlungsdauer von 2 Jahren auf und verglichen entweder Statintherapie mit Placebo (n=123’940 Patienten) oder intensivere Statintherapie mit weniger intensiver Statintherapie (n=30’724 Patienten). Die Gesamtresultate ergaben, dass die Statintherapie einen kleinen, relevanten Anstieg der Zahl der Berichte über Muskelsymptome um 3% verursachte, wobei die Mehrheit der Berichte im ersten Behandlungsjahr auftrat (Überschussrate von 11 Ereignissen pro 1000 Personenjahre). Mehr als 90% aller Berichte waren nicht auf das Statin zurückzuführen, so Prof. Colin Baignet, Oxford, der die Studie präsentierte. Es zeigte sich ferner, dass intensivere Statin-Regimes zu mehr Muskelsymptomen und längerer Dauer der Symptome führte als eine weniger intensive Statintherapie. Baigent et al betonten, dass die Ergebnisse auf die Notwendigkeit hindeuten, das klinische Management bei Patienten, die Statine einnehmen zu überprüfen und die Beipackhinweise zu überarbeiten.
WFR
Quelle: CTT metaanaylsis of the effects of statins on muscle symptomes, ESC Congress, Bacelona, 29.8.2022
DanNICAD-2: Funktionelle Testung nach CT-Angiografie – MR oder PET?
Die dänische DanNICAD-2-Studie untersuchte die diagnostische Wertigkeit von Stress-MR und Rb-82-PET als funktionelle Tests im Anschluss an die CT-Angiografie. Als Goldstandard wurden beide Methoden mit der invasiven Koronarangiografie mit fraktioneller Flussreserve (FFR) verglichen. 1.732 Patienten (mittleres Alter 59 Jahre, 57% Männer) mit Angina pectoris und Verdacht auf koronare Herzkrankheit wurden mit einer CT-Koronarangiografie untersucht. Davon wurden 1.277 ohne signifikante Stenosen (< 50%) nicht weiterverfolgt. 445 Patienten wiesen im CT > 50% Stenosen in Gefässen mit > 2 mm Durchmesser auf. 372 Patienten unterzogen sich anschliessend sowohl der MR- als auch PET-Untersuchung mit Adenosin-Stress. Die Studie wurde von Prof. Dr. Morton Bottcher, Aarhus, an einer Hot Line Session vorgestellt.
Ein positiver MR-Befund wurde definiert als signifikanter Perfusionsdefekt oder ein Late-Gadolinium-Enhancement oder eine Wandbewegungsstörung in jeweils ≥ 2 benachbarten Segmenten. Als positiv definiert wurde die PET-Untersuchung, wenn ein Summed-Stress-Score von ≥ 4 in ≥ 2 benachbarten Segmenten oder ein myokardialer Blutfluss von < 2 ml/g/min im Gefässgebiet der korrespondierenden Stenose oder eine globale Flussreserve von ≤ 1,8 oder eine transiente ischämische Dilatation > 1,13 nachgewiesen werden konnte. Die Untersuchungen wurden ohne Kenntnis der Koronar-CT-Daten verblindet befundet. Die invasive Koronarangiografie wurde als „hämodynamisch obstruktiv“ definiert, wenn eine > 90% Stenose visuell nachgewiesen oder eine FFR von ≤ 0,80 gemessen wurde. Zusätzlich wurde mittels 3D quantitativer Analyse eine 70% Stenose als „anatomisch obstruktiv“ definiert.
Es fanden sich 208 hämodynamisch nicht obstruktive Stenosen und 164 hämodynamisch obstruktive Stenosen (105 Eingefäss-, 28 Zweigefäss-, 31 Dreigefässerkrankung), mittlere FFR 0,81 (44,1%). Anatomisch waren 301 nicht obstruktive und 71 obstruktive Stenosen.
Es wurde eine Sensitivität von 59% (MR) und 64% (PET) (p = 0,21) und eine Spezifität von 84% (MR) und 89% (PET) (p = 0,08) berechnet, wenn die FFR als Referenz herangezogen wurde. Dagegen ergab sich eine Sensitivität von 83% (MR) und 90% (PET) und eine Spezifität von 76% (MR) und 78% (PET), wenn die koronarangiografische anatomische Stenose als Goldstandard herangezogen wurde.
Fazit: Prof Bottcher sagte, dass auf der Grundlage der Studienergebnisse, in Zukunft «die Genauigkeit der koronaren CTA verbessert werden muss, damit mehr Patienten ohne obstruktive KHK weitere Untersuchungen vermeiden können». Er schlug vor, dass dies «durch eine bessere CT-Bildqualität und vielleicht durch fortschrittlichere Bildanalysen wie nicht-invasive FFR-Schätzung und Photonenzählsysteme erreicht werden könnte».
WFR
Hohe Langzeitpersistenz bei Evolocumab-Behandlungsschemata in der europäischen klinischen Praxis: Analyse des HEYMANS-Registers
Lipidsenkende Therapien (LLTs) erfordern sowohl die Einhaltung als auch die langfristige Beibehaltung des Behandlungsschemas, um den Nutzen der Behandlung zu maximieren. Kleine Moleküle erfordern eine tägliche Selbstmedikation, aber Therapien wie Evolocumab sind für eine Behandlung alle 2 Wochen oder monatlich vorgesehen. Über die Langzeitpersistenz von Evolocumab in der klinischen Routinepraxis liegen nur begrenzte Daten vor. Ziel dieser Analyse war es, anhand von Daten aus dem HEYMANS-Register die Persistenz und das Absetzen von Evolocumab in Europa zu bewerten.
Methode
HEYMANS war ein prospektives Register, das Erwachsene umfasste, die zwischen August 2015 und Juni 2020 eine Evolocumab-Behandlung in der klinischen Routinepraxis in 12 europäischen Ländern begonnen hatten. Ursprünglich war eine Nachbeobachtungszeit von bis zu 12 Monaten vorgesehen, doch wurde das Protokoll im Februar 2018 geändert, um die Nachbeobachtungszeit auf bis zu 30 Monate zu verlängern. Patienten, die zu diesem Zeitpunkt die 12-monatige Nachbeobachtung noch nicht abgeschlossen hatten, wurden bis zu 30 Monate lang nachbeobachtet. Daher analysierten die Autoren das Absetzen von Evolocumab getrennt für die beiden Zeiträume: 0-12 Monate (alle), 12-30 Monate (Teilgruppe).
Resultate
Von den insgesamt 1951 Patienten beendeten 30 Patienten die Teilnahme an der Studie vor Ablauf von 12 Monaten (die Einnahme von Evolocumab war zum Zeitpunkt der Beendigung der Studie noch nicht abgeschlossen). Daher wurde der Status der Evolocumab-Anwendung bei 1921 Patienten nach 12 Monaten ermittelt. Von diesen nahmen 1781 (92,7%) auch nach 12 Monaten noch Evolocumab ein. Nach 12 Monaten waren die LDL-C-Werte gegenüber dem Ausgangswert im Median um 58% gesunken (Q1, Q3: 41%, 69%). Insgesamt kamen nach der Protokolländerung 1136 Patienten für eine erweiterte Nachbeobachtung in Frage. Davon beendeten 137 Patienten die Studienteilnahme vor Ablauf der 30-monatigen Nachbeobachtungszeit (bei laufender Behandlung mit Evolocumab). Daher wurde der Status der Evolocumab-Anwendung bei 999 Patienten ermittelt, von denen 92,2% (921) nach 30 Monaten der Nachbeobachtung weiterhin mit Evolocumab behandelt wurden. Die nach 12 Monaten beobachtete Senkung des LDL-C-Spiegels hielt während der gesamten Studie an, und die Patienten erreichten auch nach 30 Monaten eine mediane LDL-C-Senkung von 58% (Q1, Q3: 42%, 70%) gegenüber dem Ausgangswert.
Schlussfolgerungen
In dieser praxisnahen Studie, die für die europäische Praxis repräsentativ ist, lag der Anteil der Patienten, die in der Verlängerungsphase mit Evolocumab behandelt wurden, bei über 90%, und die Behandlung war mit einer anhaltenden LDL-C-Senkung verbunden. Diese Daten deuten darauf hin, dass das Selbstverabreichungsschema von Evolocumab in der Allgemeinbevölkerung sowohl durchführbar als auch akzeptabel ist und zu einer langfristigen, anhaltenden Senkung des LDL-C-Wertes führt, was wahrscheinlich mit gesundheitlichen Vorteilen verbunden ist.
WFR
Quelle: Ray KK et al. High long-term persistence to evolocumab treatment regimens in European clinical practice: analysis of the HEYMANS registry. ESC Congress, Barcelona 2022, 26.8.
Vergleich von Patienten mit schwerer Hypercholesterinämie mit und ohne pathogenen Varianten
Eine pathogene Variante, die ursächlich mit der familiären Hypercholesterinämie (FH) zusammenhängt, findet sich bei weniger als der Hälfte der Erwachsenen mit schwerer Hypercholesterinämie. Die Merkmale von Erwachsenen mit schwerer Hypercholesterinämie ohne pathogene Variante sind nur unzureichend beschrieben, und es bleibt unklar, ob intensive präventive Strategien empfohlen werden sollten.
In der von Prof. Dr. David Nanchen präsentierten Studie wurden die Merkmale von Erwachsenen mit schwerer Hypercholesterinämie mit und ohne pathogener FH-Variante verglichen.
Methoden
Zwischen November 2020 und Februar 2022 wurden Personen, die älter als 16 Jahre waren und einen niederländischen Lipid Clinic Network (DLCN) Score ≥6 und für LDLR, APOB und PCSK9 genotypisiert waren. Die Teilnehmer waren Teil der multizentrischen CATCH-Studie, in der die Einführung eines genetischen Kaskaden-Screenings für FH in der Schweiz getestet wird. Alle genetischen Analysen wurden in einem einzigen Zentrallabor durchgeführt. Varianten, die als wahrscheinlich pathogen oder pathogen eingestuft wurden, wurden als FH-verursachend interpretiert. Die Autoren untersuchten auch den sozioökonomischen Status, kardiovaskuläre Risikofaktoren, Lebensstil und die Einnahme von lipidsenkenden Medikamenten.
Resultate
Insgesamt wurden 150 nicht verwandte Erwachsene mit einem DLCN-Score von ≥6 eingeschlossen, von denen 62 (41,3%) eine genetisch bestätigte FH aufwiesen. Die meisten Varianten wurden im LDLR-Gen gefunden (77%). Insgesamt nahmen 70% ein lipidsenkendes Medikament ein und 20% waren Raucher. Im Vergleich zu den Erwachsenen mit genetisch bestätigter FH waren die Personen ohne pathogene Varianten älter (57,6 vs. 50,4 Jahre) und hatten niedrigere unbehandelte LDL-Cholesterinwerte (p<0,001), höhere Triglyceridwerte (p=0,032), einen höheren BMI (p=0,014) und hatten häufiger Bluthochdruck (62,5% vs. 36.1%). Es wurden keine sozioökonomischen Unterschiede festgestellt. Obwohl die Befolgung der mediterranen Diät bei den Erwachsenen ohne pathogene Variante höher war, erreichten sie seltener das empfohlene Mass an körperlicher Aktivität als Erwachsene mit genetisch bestätigter FH (66,2% vs. 82,1%). Xanthome oder Xanthelasmen, aber kein Hornhaut-Arcus, traten bei genetisch bestätigter FH häufiger auf (5,7% gegenüber 20,3%).
Schlussfolgerungen
Erwachsene mit schwerer Hypercholesterinämie und ohne eine pathogene FH-Variante hatten eine weniger optimale Kontrolle der kardiovaskulären Risikofaktoren als genetisch bestätigte FH. Ein Fünftel der Patienten waren Raucher und ein Drittel aller Patienten in der Studie nahmen keine lipidsenkende Medikamente trotz dem Vorhandensein einer pathogenen Variante.
WFR
Quelle: D Nanchen, T Von Kanel, G Ehret, N Brun, I Sudano, N Rodondi, H Rickli, G Girod, D Ballhausen, R Falciano, JH Beer, A Gallino8, ESC 2022, 28.8. , Barcelona
DANFLU-1: Hinweis auf Mortalitätsvorteil mit hochdosiertem Influenzaimpfstoff
Eine Grippeinfektion ist mit einem erhöhten Risiko für spätere kardiovaskuläre Ereignisse verbunden. Hochdosierte Influenza-Impfstoffe sind für die Verwendung bei älteren Erwachsenen zugelassen, werden aber in diesem Umfeld nicht routinemässig eingesetzt, obwohl es Hinweise auf einen zusätzlichen Schutz vor Influenza-Infektionen und grippebedingter Morbidität im Vergleich zu Standardimpfstoffen gibt. Die DANFLU-1-Studie untersuchte die Durchführbarkeit einer gross angelegten pragmatischen, individuell randomisierten Studie zur Bewertung der Wirksamkeit von QIV-HFD und QIV-SD bei älteren Menschen. In der Studie wurden 12477 Teilnehmer im durchschnittlichen Alter von 71.7 Jahren (47.1% waren Frauen) untersucht.
Ältere Erwachsene, die einen hochdosierten vierwertigen Grippeimpfstoff erhielten, hatten 64,4 % weniger Hospitalisierungen aufgrund von Influenza oder Pneumonie (10 [0,2 %] vs. 28 [0,4 %]). Die Mortalität war bei Patienten der Hochdosisgruppe um 49 % geringer (21 [0,3 %] vs. 41 [0,7 %] Ereignisse). Es fand sich kein Unterschied hinsichtlich der Hospitalisierung aufgrund von kardiovaskulären Erkrankungen oder Serious Adverse Events in den beiden Gruppen.
Dr. Niklas Dyrby Johanson, Copenhagen, der die Studie präsentierte, betonte, dass diese Studie nicht gepowert für diese Endpunkte war und die Ergebnisse daher nur hypothesengenerierend sind. Prof. Tor Biering-Sorensen, der Senior Autor der Studie, betonte in seinem Interview mit ESC-TV, dass nun eine ausreichend gepowerte, gross angelegte Studie geplant ist. Die erforderliche Studienpopulation wird mit 200.000 Teilnehmern angenommen. Das erfolgreiche Studiendesign kann auch leicht auf andere Fragestellungen ausgeweitet werden.
Fazit: Die Reduktion der Hospitalisierungen und der Gesamtmortalität ist vielversprechend, auch wenn sie noch durch eine grössere Studie bestätigt werden muss. Die Daten passen zu vorangegangenen Studien, die einen besseren Impfschutz durch eine Hochdosisinfluenzaimpfung bei älteren Patienten gezeigt hatten.
WFR
FRAME-AMI: FFR- vs. Angiografie-gestützte Revaskularisierung im akuten Myokardinfarkt
Die Auswahl von Läsionen in nicht-infarktnahen Arterien (IRA) für eine Intervention unter Verwendung der fraktionellen Flussreserve (FFR) ist der routinemässigen angiographischen Auswahl bei Patienten mit akutem Myokardinfarkt und Mehrgefässerkrankung überlegen. Dies ist das Ergebnis einer aktuellen Forschungsarbeit, die in einer Hot-Line-Sitzung von Prof. Joo Yong Hahn, Seoul, vorgestellt wurde.
FRAME-AMI wurde als Investigator-initiated Trial in 14 Zentren in Korea bei Patienten mit akutem Myokardinfarkt und Mehrgefässerkrankung durchgeführt. Nach erfolgreicher perkutaner Koronarintervention (PCI) der Targetläsion erfolgte eine Randomisierung der Non-Culprit-Arterien zu FFR-gestützter (FFR ≥ 0,8) versus angiografisch-geleiteter (≥ 50 % Stenosen) kompletter Revaskularisierung. Es wurde für NSTEMI versus STEMI stratifiziert. Chronisch totale Koronarverschlüsse waren ausgeschlossen.
Der primäre Studienendpunkt, bestehend aus Tod, Myokardinfarkt und neuerlicher Revaskularisierung war in der FFR-gestützten Gruppe (n = 284) signifikant reduziert im Vergleich zur konventionellen angiografisch-geleiteten Gruppe (n = 278): 7,4% versus 19,7% (p = 0,03). Dies, obwohl die kalkulierte Fallzahl von 646 Patienten pro Gruppe wegen COVID-19 nicht erreicht wurde.
Fazit: Die Studie zeigt, dass FFR-gestützte PCI von Non-Culprit-Lesions im akuten Myokardinfarkt der angiografisch-geleiteten kompletten Revaskularisierung überlegen sind. Die Daten unterstützen die physiologische Evaluierung von Koronarstenosen auch im Setting des akuten Koronarsyndroms.
WFR
EchoNet-RCT: Künstliche Intelligenz verbessert LVEF-Messung
Die linksventrikuläre Auswurffraktion (LVEF) in der Echokardiografie ist zentraler Bestandteil vieler klinischer Entscheidungen in der Kardiologie. Die LVEF wird derzeit entweder durch manuelle Analyse oder semi-automatisch mit manueller Korrektur einer vorgegebenen Konturanalyse durchgeführt. Die in einer Hot Line Session von Dr. David Ouyang, Los Angeles, präsentierte EchoNET-RCT-Studie ist die erste prospektive, randomisierte und verblindete Studie, die künstliche Intelligenz (KI) in der kardiovaskulären Bildgebung in grossem Stil einsetzt. Die LVEF der KI wurde mit jener von «Sonographers» (in Österreich am ehesten Radiologietechnologen entsprechend) verglichen, wobei Fachärzte für Kardiologie alle Fälle noch einmal begutachteten, ohne zu wissen, wer die LVEF zuvor gemessen hatte.
Die Kardiologen korrigierten bei den insgesamt 3495 Patienten deutlich häufiger die Befunde der sonographers (27,2% vs. 16,8% der KI; definiert als Abweichung von über 5% der LVEF). Interessant ist, dass die Spezialisten nicht unterscheiden konnten, welche Konturanalyse von der KI und welche von Sonographers gemacht wurde. Der Zeitaufwand zum Korrigieren der LVEF-Analyse war bei den KI-Fällen deutlich geringer gegenüber jenen der Sonographers (64 gegenüber 54 Sekunden).
Fazit: EchoNET-RCT ist die erste grosse prospektive, randomisierte und verblindete Studie in der medizinischen Bildgebung. Sie zeigt eine Überlegenheit künstlicher Intelligenz bei der Messung von LVEF gegenüber Radiotechnologen («Sonographers»). Die Autoren betonen, dass künstliche Intelligenz medizinisches Fachpersonal nicht ersetzen wird, sondern vielmehr die Arbeit erleichtern und Zeitabläufe optimieren kann.
WFR
Kausale künstliche Intelligenz verbessert Abschätzung des CV-Risikos
Der optimale Zeitpunkt, die Dauer und die Intensität der Senkung des LDL-Cholesterins und des systolischen Blutdrucks (SBP) zur Prävention kardiovaskulärer Ereignisse ist unbekannt. Die Komplexität der Berechnung verlangt nach Artificial Intelligence (AI)-Unterstützung im Erfassen und Bearbeiten dieser Datenflut.
Prof. Brian Ference, Cambridge, berichtete an der Hot Line Session, wie mittels Machine und Deep Learning mit 1,8 Millionen Datensätzen, 1,3 Millionen Teilnehmern nach Mendel`scher Randomisierung und > 1/2 Million Teilnehmern an randomisierten Studien versucht wurde, den kausalen Langzeiteffekt von LDL und SBP abzuschätzen. Es wurden hierbei Gruppen mit niedrigem und hohem LDL/SBP und Kombinationen generiert. In der Studie konnte gezeigt werden, dass derzeitige Risiko-abschätzende Algorithmen für die individuelle Risikoabschätzung nicht ausreichend nützlich sind, weil sie kausale Effekte nicht berücksichtigen.
Fazit: Gängige Richtlinien (basierend auf randomisierten Studien) können keine exakte Aussage treffen, wann individuell mit einer primär-präventiven Massnahme begonnen werden sollte. Das allgemeine Ziel muss daher sein, eine neue Generation an AI-Algorithmen zu schaffen, die kausalen Effekte von z. B. LDL und SBP über diskrete Zeitintervalle individuell abschätzen, womit die Genauigkeit der persönlichen Risikoabschätzung und der primär präventiven Behandlungsoption erhöht werden.
WFR