Herz-Kreislauf-Erkrankungen gehören zu den häufigsten Ursachen von Mortalität und Morbidität in der Schweiz. Auch psychische Störungen wie Depressionen und Angstzustände sind weit verbreitet und gehören zu den häufigsten Erkrankungen, welche die Lebensqualität der Patienten beeinträchtigen. Die Komorbidität von kardiovaskulären und psychischen Erkrankungen stellt somit eine enorme Herausforderung für die moderne Medizin dar, allein schon wegen der grossen Zahl der betroffenen Patient*innen. In den letzten Jahren hat eine zunehmende Zahl von Studien wiederholt die Wechselwirkung zwischen Herzerkrankungen und psychosozialen Aspekten aufgezeigt. Dementsprechend ist die Berücksichtigung und das Verständnis der biopsychosozialen Aspekte bei der Entstehung von Herzkrankheiten einerseits und der psychologischen und sozialen Dimensionen des Krankseins aufgrund von Herzkrankheiten andererseits für die tägliche klinische Praxis wichtig. Darüber hinaus ist die Behandlung von Herzpatienten oft komplex und erfordert einen multidisziplinären und integrativen Ansatz, um ein effektives Langzeitmanagement zu gewährleisten. Der vorliegende Artikel gibt einen Überblick über die psychosozialen Aspekte von Herzkrankheiten und den Zusammenhang zwischen kardiovaskulären und psychologischen Erkrankungen.
Cardiovascular diseases are among the leading causes of death and illness-related disability in Switzerland. Similarly, psychological disorders such as depression and anxiety, are highly prevalent and are leading conditions limiting patient’s quality of life. The comorbidity of cardiovascular and mental illnesses thus represents an enormous challenge for modern medicine, if only because of the large number of patients affected. In recent years, a growing number of studies have repeatedly shown the reciprocal interaction between heart disease and psychosocial aspects. Accordingly, considering and understanding biopsychosocial aspects in the development of heart diseases on one side, and psychological and social dimensions of being ill due to heart disease on the other side is important for daily clinical practice. Furthermore and most importantly, the treatment of cardiac patients is often complex and requires a multidisciplinary and integrative approach to emphasize effective long-term management.
The present article provides a comprehensive overview on the psychosocial aspects of heart disease and the link between cardiovascular and psychological diseases.
Key Words: psychological disorders, Cardiovascular diseases, mental illness, depression, anxiety
Einleitung
Herzkreislauferkrankungen gehören nach wie vor zu den häufigsten Ursachen von Morbidität und Mortalität in der Schweiz. Ihre Entstehung und ihr Verlauf lassen sich häufig durch geeignete primär- und sekundärpräventive Massnahmen besser beeinflussen als es bei vielen anderen Erkrankungen der Fall ist. In den letzten Jahren hat die Evidenz darüber, welchen Einfluss psychosoziale Faktoren auf die Entstehung und den Verlauf von Herzerkrankungen haben, deutlich zugenommen. Entsprechend wird die Relevanz des Zusammenhanges und der Wechselwirkung von Herz und Psyche immer mehr erkannt und hat konsequenterweise dazu geführt, dass diese Aspekte in den europäischen und amerikanischen Leitlinien etabliert sowie mit aktuellen und dedizierten Positionspapieren verankert wurden (1-4). Bei der koronaren Herzkrankheit (KHK), Herzinsuffizienz, arteriellen Hypertonie und bei Herzrhythmusstörungen besteht eine robuste Evidenz hinsichtlich der Bedeutung psychosozialer Faktoren, die eine Berücksichtigung in der kardiologischen Versorgung sinnvoll machen (2, 3). Der Grad der Umsetzung in den klinischen Alltag ist jedoch noch defizitär. Es wird empfohlen, psychosoziale Belastungen und psychische Begleiterkrankungen routinemässig zu erfassen, so dass gezielt weitere Behandlungen angeboten werden können.
Biopsychosozialer Zusammenhang
In der jüngsten Vergangenheit konnten etliche Studien die Wichtigkeit der Psyche und des akuten und chronischen Stresses sowohl bei der Entstehung als auch im weiteren Verlauf von kardiovaskulären Erkrankungen belegen. Unter anderem hat eine Studie während der Fussball-Weltmeisterschaft 2006 in Deutschland gezeigt, dass sich die Rate von akuten kardiovaskulären Ereignissen (akutes Koronarsyndrom und symptomatische kardiale Arrhythmien) in und um München an den Tagen, an welchen die deutsche Nationalmannschaft spielte, vervielfacht hat (5). Die Autoren schlossen daraus, dass der intensiv empfundene emotionale Stress im Rahmen eines wichtigen Fussballspiels kardiovaskuläre Ereignisse triggern kann – ein ähnliches Phänomen, welches bei Naturereignissen (z.B. Erdbeben) oder bei Kriegen gezeigt werden konnte (6, 7).
In einer weiteren Longitudinalstudie bei über 290 Personen ohne kardiovaskuläre Erkrankungen wurde die Aktivität in der Amygdala (welche in der Entstehung von Emotionen und Stress eine zentrale Rolle spielt), im Knochenmark und die arterielle Inflammation mittels 18F-Fluorodexoyglucose Positronen-Emissions-Tomographie (18F-FDG-PET) erfasst und die Patient*innen während einem Beobachtungszeitraum von 3.7 Jahren nachverfolgt (8). In dieser ersten Studie zum Zusammenhang regionaler Gehirnaktivität mit nachfolgenden Herz-Kreislauf-Erkrankungen prognostizierte die Aktivität der Amygdala unabhängig und robust kardiovaskuläre Ereignisse. Es konnte gezeigt werden, dass die erhöhte Amygdala-Aktivität über eine erhöhte Knochenmarkaktivität zu einer arteriellen Inflammation führt (8). Die Amygdala scheint somit eine entscheidende Rolle in der Entstehung von kardiovaskulären Ereignissen ausgelöst durch Stress zu spielen.
Eine weitere, kürzlich publizierte Studie wies bei Patient*innen unmittelbar nach einem akuten Myokardinfarkt verglichen mit Kontrollpatient*innen ebenfalls eine erhöhte Amygdala- und Knochenmark-Aktivität nach (9). Sechs Monate nach dem Myokardinfarkt war die Amygdala- und Knochenmark-Aktivität wieder auf dem gleichen Niveau wie bei Kontrollpatient*innen. Die Autoren kamen zum Schluss, dass die Stress-assoziierte neurobiologische Aktivität womöglich die Makrophagenaktivität fördert und dies in Verbindung mit akuter Plaqueinstabilität im Rahmen des Myokardinfarktes steht (9), was somit auch ein potentielles Ziel für künftige Behandlungen darstellen könnte.
Der psychosoziale Stress wurde neu als «risk modifier» für kardiovaskuläre Erkrankungen in den aktuellen Guidelines der European Society of Cardiolgy (ESC) aufgenommen mit der damit verbundenen Empfehlung um entsprechende präventive Massnahmen (1).
Wechselwirkung am Beispiel der Depression und der koronaren Herzkrankheit
Ungefähr 70% aller KHK-Patient*innen zeigen psychopathologische Auffälligkeiten in der Folge eines stattgehabten Akutereignisses (10). In vielen Fällen kommt es bei Patient*innen nach einem belastenden Ereignis (z.B. einem Herzinfarkt, einer Herzoperation, einer ICD-Schockabgabe) zu einer vorübergehenden psychischen Reaktion, der sogenannten «Anpassungsstörung»: Die Betroffenen haben häufig Mühe mit der Verarbeitung des akuten Ereignisses und machen sich viele Gedanken (u.a. Zukunftsängste, Angst vor dem Tod). In der Regel handelt es sich dabei um einen vorübergehenden Zustand, der sich innerhalb einiger Wochen bis wenigen Monaten wieder normalisiert. Hingegen kann es nicht selten auch zu schwerwiegenderen psychischen Folgen kommen: Neben der Angst- und Panikstörung und der posttraumatischen Belastungsstörung gehört die Depression zu den am meisten erforschten psychiatrischen Erkrankungen im Zusammenhang mit kardiovaskulären Erkrankungen.
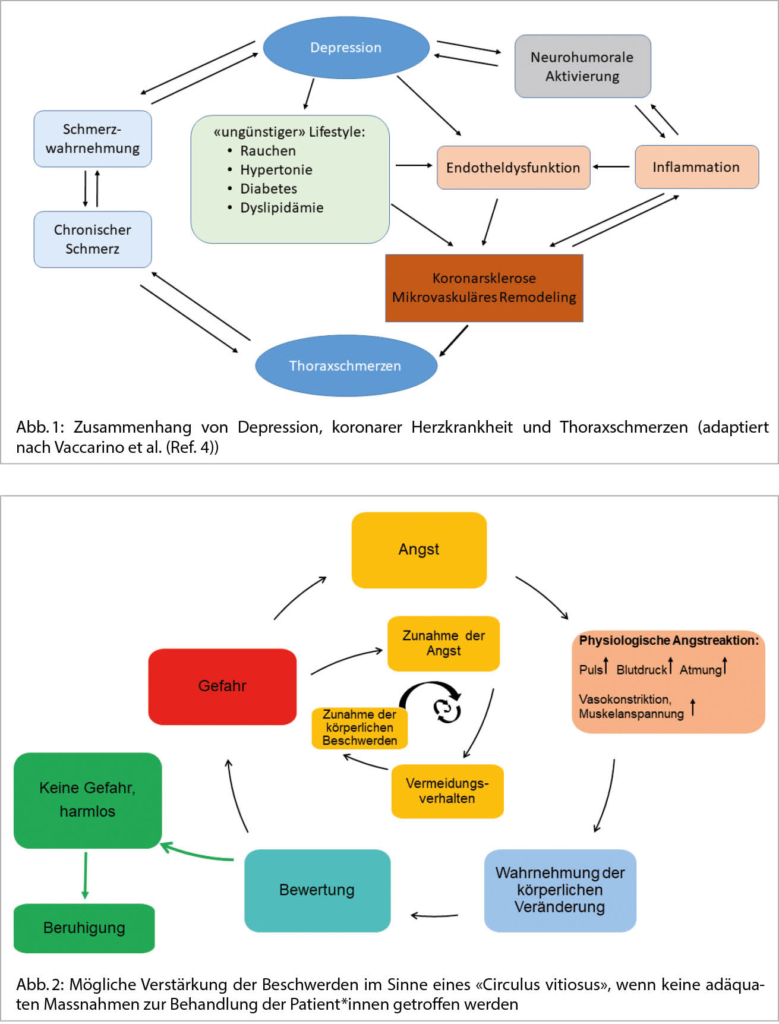
Die Prävalenz der Depression bei Patient*innen mit einer koronaren Herzkrankheit (KHK) beträgt 15–30% (4) und ist somit zwei- bis dreimal häufiger als in der Allgemeinbevölkerung. Insbesondere scheinen vor allem Frauen nach einem Herzinfarkt etwa zweimal mehr betroffen zu sein als Männer (11). Bei Personen, die bereits einen Herzinfarkt erlitten haben, scheint die Depression trotz etwas heterogener Datenlage das Wiederauftreten kardialer Ereignisse zu begünstigen (12). Umgekehrt erhöht sich auch das Risiko für ein erstes kardiales Ereignis bei depressiven Personen ohne bekannte KHK um bis zu 30% (13). Eine Depression wirkt vielseitig auf das kardiovaskuläre System ein. Neben der neurohumoralen Aktivierung spielt sicherlich auch die Endotheldysfunktion eine Rolle, was zu einem mikrovaskulären Remodeling und schliesslich zur Atherosklerose führen kann (Abbildung 1). Dazu kommt, dass Patient*innen mit KHK und Depression Therapieempfehlungen schlechter befolgen und Lebensstilveränderungen nicht optimal umsetzen können. Deshalb werden in den ESC-Guidelines verhaltenstherapeutische und psychologische Interventionen (Klasse I, Level B) der Depression bei Patient*innen mit KHK empfohlen (14). Während ein guter Effekt psychotherapeutischer bzw. pharmakologischer Interventionen auf psychische Symptome gezeigt werden konnte, ist der Effekt hinsichtlich der kardialen Prognose jedoch noch unklar. Entsprechend sind sowohl weitere Behandlungsstudien als auch intensivierte Fort- und Weiterbildungsangebote erwünscht.
Sowohl die aktuellen ESC-Guidelines als auch ein kürzlich erschienenes Positionspapier der Deutschen Gesellschaft für Kardiologie empfehlen zudem generell, psychosoziale Belastungen und psychische Begleiterkrankungen routinemässig nach einem Herzinfarkt zu erfassen (z.B. mittels Screening Fragebögen), so dass sich frühzeitig und gezielt weitere Diagnostik und Therapie anschliessen können (1, 2). Patient*innen kann dadurch ein Behandlungsangebot gemacht werden, das alters- und geschlechtsspezifische Aspekte sowie die individuellen Präferenzen berücksichtigt. Multimodale Behandlungsansätze sollen Wissensvermittlung, Sport- und Bewegungstherapie, Motivationsförderung sowie Entspannungsverfahren bzw. Stressmanagement umfassen (2).
Angst und Herzkrankheiten – ein Teufelskreis
Für viele Betroffene ist eine kardiologische Erkrankung mit einem hohen psychischen Leidensdruck verbunden. Die Betroffenen müssen lernen mit der Endlichkeit des eigenen Lebens und der plötzlichen Erschütterung der eigenen Unversehrtheit umzugehen und as Vertrauen in den eigenen Körper wiederzugewinnen. Die vitale Bedrohung durch eine akute Herzerkrankung kann bei betroffenen Patient*innen häufig ein Gefühl von Hilflosigkeit und Angst, bin hin zur Todesangst auslösen. Ängste können ihrerseits durch die begleitende vegetative Reaktion die Belastung des Herz-Kreislauf-Systems erhöhen. Die resultierende Steigerung von Herzfrequenz, Blutdruck, Atmung und Arrhythmieneigung können in einem Teufelskreis zur weiteren Steigerung der Angst führen, wenn keine adäquaten Massnahmen getroffen werden (Abb. 2). Hierzu können bereits einfache Konzepte in der Behandlung hilfreich sein (Tab. 1).
Neben der Angstsymptomatik kann ein akutes Herzereignis auch eine posttraumatische Belastungsstörung (PTBS) auslösen. In einer Metaanalyse aus dem Jahr 2019 wurde der Zusammenhang zwischen PTBS und akutem Koronarsyndrom (ACS) untersucht (15). Demnach wurden klinisch signifikante PTBS-Symptome in 4-16% aller ACS Patient*innen gefunden. Eine KHK führt also nicht selten zur PTBS, die dann wiederum die Gefahr für weitere Herzerkrankungen erhöht.
Copyright bei Aerzteverlag medinfo AG
Facharzt für Kardiologie FMH, spez. Psychosomatische und
Psychosoziale Medizin (SAPPM)
Oberarzt meV Kardiale Bildgebung (CT/NUK/MRI),
Klinik für Nuklearmedizin
Oberarzt Echokardiographie und Psychokardiologie
Klinik für Kardiologie, Klinik für Konsiliarpsychiatrie und Psychosomatik
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
aju.pazhenkottil@usz.ch
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Visseren FLJ, Mach F, Smulders YM, Carballo D, Koskinas KC, Back M, Benetos A, Biffi A, Boavida JM, Capodanno D, Cosyns B, Crawford C, Davos CH, Desormais I, Di Angelantonio E, Franco OH, Halvorsen S, Hobbs FDR, Hollander M, Jankowska EA, Michal M, Sacco S, Sattar N, Tokgozoglu L, Tonstad S, Tsioufis KP, van Dis I, van Gelder IC, Wanner C, Williams B, Societies ESCNC, Group ESCSD. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021;42(34):3227-337.
2. Albus C., Waller C., Fritzsche K., al. e. Bedeutung von psychosozialen Faktoren in der Kardiologie – Update 2018. Positionspapier der Deutschen Gesellschaft für Kardiologie. Kardiologe. 2018;12:312.
3. Ladwig KH, Baghai TC, Doyle F, Hamer M, Herrmann-Lingen C, Kunschitz E, Lemogne C, Beresnevaite M, Compare A, von Kanel R, Sager HB, Kop WJ.
Mental health-related risk factors and interventions in patients with heart failure: a position paper endorsed by the European Association of Preventive Cardiology (EAPC). Eur J Prev Cardiol. 2022;29(7):1124-41.
4. Vaccarino V., Badimon L., Bremner JD. ea, al. e. Depression and coronary heart disease: 2018 position paper of the ESC working group on coronary pathophysiology and microcirculation. Eur Heart J. 2020 May 1;41(17):1687-1696.
5. Wilbert-Lampen U, Leistner D, Greven S, Pohl T, Sper S, Volker C, Guthlin D, Plasse A, Knez A, Kuchenhoff H, Steinbeck G. Cardiovascular events during World Cup soccer. N Engl J Med. 2008;358(5):475-83.
6. Leor J, Poole WK, Kloner RA. Sudden cardiac death triggered by an earthquake. N Engl J Med. 1996;334(7):413-9.
7. Meisel SR, Kutz I, Dayan KI, Pauzner H, Chetboun I, Arbel Y, David D. Effect of Iraqi missile war on incidence of acute myocardial infarction and sudden death
in Israeli civilians. Lancet. 1991;338(8768):660-1.
8. Tawakol A, Ishai A, Takx RA, Figueroa AL, Ali A, Kaiser Y, Truong QA, Solomon CJ, Calcagno C, Mani V, Tang CY, Mulder WJ, Murrough JW, Hoffmann U, Nahrendorf M, Shin LM, Fayad ZA, Pitman RK. Relation between resting amygdalar activity and cardiovascular events: a longitudinal and cohort study. Lancet. 2017;389(10071):834-45.
9. Kang DO, Eo JS, Park EJ, Nam HS, Song JW, Park YH, Park SY, Na JO, Choi CU, Kim EJ, Rha SW, Park CG, Seo HS, Kim CK, Yoo H, Kim JW. Stress-associated neurobiological activity is linked with acute plaque instability via enhanced macrophage activity: a prospective serial 18F-FDG-PET/CT imaging assessment. Eur Heart J. 2021;42(19):1883-95.
10. Whitehead DL, Strike P, Perkins-Porras L, Steptoe A. Frequency of distress and fear of dying during acute coronary syndromes and consequences for adaptation. Am J Cardiol. 2005;96(11):1512-6.
11. Vaccarino V, Bremner JD. Behavioral, emotional and neurobiological determinants of coronary heart disease risk in women. Neurosci Biobehav Rev. 2017;74(Pt B):297-309.
12. Lichtman JH, Froelicher ES, Blumenthal JA, Carney RM, Doering LV, Frasure-Smith N, Freedland KE, Jaffe AS, Leifheit-Limson EC, Sheps DS, Vaccarino V, Wulsin L. Depression as a risk factor for poor prognosis among patients with acute coronary syndrome: systematic review and recommendations: a scientific statement from the American Heart Association.
Circulation. 2014;129(12):1350-69.
13. Gan Y., Gong Y., Tong X., al. e. Depression and the risk of coronary heart disease: a metaanalysis of prospective cohort studies. BMC Psychatry. 2014;14:371.
14. Knuuti J, Wijns W, Saraste A, Capodanno D, Barbato E, Funck-Brentano C,
Prescott E, Storey RF, Deaton C, Cuisset T, Agewall S, Dickstein K, Edvardsen T, Escaned J, Gersh BJ, Svitil P, Gilard M, Hasdai D, Hatala R, Mahfoud F, Masip J, Muneretto C, Valgimigli M, Achenbach S, Bax JJ, Group ESCSD. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41(3):407-77.
15. Edmondson D, Richardson S, Falzon L, Davidson KW, Mills MA, Neria Y.
Posttraumatic stress disorder prevalence and risk of recurrence in acute coronary syndrome patients: a meta-analytic review. PLoS One. 2012;7(6):e38915.