Im Zentrum des dritten Hauptthemas stand die Vulva. Dr. med. Martine Jacot-Guillarmod, Lausanne, ging in ihrem Vortrag insbesondere auf die Vulvodynie als die häufigste Ursache einer Dyspareunie ein. Sie erläuterte die unterschiedlichen Formen, das grundsätzliche diagnostische Vorgehen und Behandlungsoptionen.
«Unter Dyspareunie werden alle Schmerzen verstanden, zu denen es während einer sexuellen Aktivität mit vaginaler Penetration kommt», erklärte Dr. med. Martine Jacot-Guillarmod, CHUV, Lausanne. Die Prävalenz dieser Beschwerden zu definieren sei allerdings schwierig, da in der Literatur unterschiedliche Angaben zu finden seien. «Gemäss Daten aus den USA sind 17 bis 19% der Frauen betroffen», sagte sie. Untersuchungen in Grossbritannien fanden dagegen eine Prävalenz von 7,5% (1). «Wir wissen jedoch, dass 40 bis 49% der Frauen mit chronischen vulvären Schmerzen keine medizinische Hilfe in Anspruch nehmen. Deshalb können wir davon ausgehen, dass die Prävalenz wahrscheinlich unterschätzt wird», sagte sie. Die möglichen Ursachen einer Dyspareunie sind vielfältig: von vulvären Dermato-Pathologien, über Fehlbildungen und Tumore, aber auch als Folge von Verletzungen (z.B. durch Geburt, Unfälle), Operationen oder Missbrauch. In vielen Fällen erweist sich die Dyspareunie als idiopathisch.
Häufige vulväre Pathologien als Ursache
Im Weiteren stellte Dr. Jacot-Guillarmod drei vulväre Pathologien vor, die zu einer Dyspareunie führen können. Als chronisch-entzündliche Hauterkrankung führt Lichen sclerosus zu Schrumpfungen an der Vorhaut der Klitorisspitze, der kleinen Labien und der Dammregion, gelegentlich auch der Perianalhaut, sowie zu einer Atrophie der Haut mit Läsionen und Einrissen. Als Folge der Erkrankung kann es zu Verengungen des Scheideneinganges kommen, die beim Geschlechtsverkehr einreissen und zu Schmerzen führen oder eine Penetration sogar verunmöglichen. Als zweite häufige Ursache einer Dyspareunie erwähnte die Rednerin Lichen planus, eine chronisch-entzündliche mukokutane Erkrankung. «Lichen planus weist häufig eine errosive Komponente auf», betonte sie. Diese kann zu beträchtlichen Schmerzen führen. Als dritte Erkrankung, die mit Symptomen wie Pruritus, Brennen und einer Dyspareunie einhergehen kann, nannte die Rednerin die Vulvitis plasmacellularis (M. Zoon). «Sie ist besonders bei Frauen nach der Menopause häufig anzutreffen», ergänzte Dr. Jacot-Guillarmod.
Vulvodynie häufig bei unter 50-Jährigen
Die häufigste Ursache für eine Dyspareunie bei Frauen unter 50 stellt die Vulvodynie dar. «Sie weist zwei Charakteristiken auf, die für uns im Rahmen einer kurzen Konsultation, zum Beispiel bei einer Jahreskontrolle, häufig schwierig anzusprechen sind. Einerseits ist das das Thema Sexualität, andererseits handelt es sich um eine chronische Erkrankung», erläuterte Dr. Jacot-Guillarmod.
Bei der Vulvodynie wird zwischen einer lokalisierten und einer generalisierten Form unterschieden werden. Die lokalisierte Vulvodynie (auch Vestibulodynie/Klitorodynie) betrifft vor allem junge Frauen (20- bis 40-Jährige), mit der höchsten Inzidenz bei den 20-bis 29-Jährigen (2). Unter einer generalisierten Vulvodynie leiden dagegen vor allem postmenopausale Frauen. Die chronische Erkrankung kann als primäre Vulvodynie auftreten (20% der Fälle). Hier treten Schmerzen ab dem ersten Versuch einer Penetration auf oder dem Versuch, einen Tampon oder ein Spekulum einzuführen. Zur sekundären Form kommt es nach einer Phase einer harmonischen sexuellen Beziehung. Diese Frauen klagen auch nicht über Schmerzen im Zusammenhang mit der Anwendung von Tampons. «Kommt eine Frau mit Vulvodynie zu Ihnen, geht es also in einem ersten Schritt darum zu unterscheiden, ob es sich um eine lokalisierte oder generalisierte Form handelt», beschrieb Dr. Jacot-Guillarmod das Vorgehen. Danach gelte es herauszufinden, ob der Schmerz durch Berührung provoziert werden kann oder ob es sich um einen spontanen Schmerz handelt. Und schliesslich sei zwischen primärer und sekundärer Form zu unterscheiden. «Die häufigste Form stellt die lokalisierte, provozierte, sekundäre Vulvodynie dar», erklärte die Rednerin. Sie macht 72,6% aller Vulvodynien aus (2).
Starke Auswirkungen auf Lebensqualität
Wie bei der Dyspareunie kommen als auslösende Faktoren für eine Vulvodynie rezidivierende Genitalinfektionen (Mykosen), vulväre Dermatopathologien (Lichen sclerosus), (sexuelle) Traumata aber auch die hormonellen Veränderungen während der Menopause in Frage. «Verschiedene Faktoren wie emotionaler Stress, Beziehungsschwierigkeiten oder Traumata können zudem dazu führen, dass die zentrale Schmerzschwelle moduliert wird», führte Dr. Jacot-Guillarmod weiter aus. Untersuchungen weisen ausserdem darauf hin, dass Veränderungen im serotonergen System einen Beitrag zur Erstehung einer provozierten Vulvodynie leisten könnten (3).
Eine Studie machte deutlich, dass Frauen mit Vulvodynie eine deutlich schlechtere Lebensqualität aufwiesen als Patientinnen mit vielen anderen dermatologischen Erkrankungen und eine schlechtere Funktionsfähigkeit als Frauen mit anderen vulvären Erkrankungen (4). «Der Verlust an Selbstwertgefühl bei den betroffenen Frauen ist oft enorm», ergänzte die Rednerin.
Genügende Zeit für Anamnese nehmen
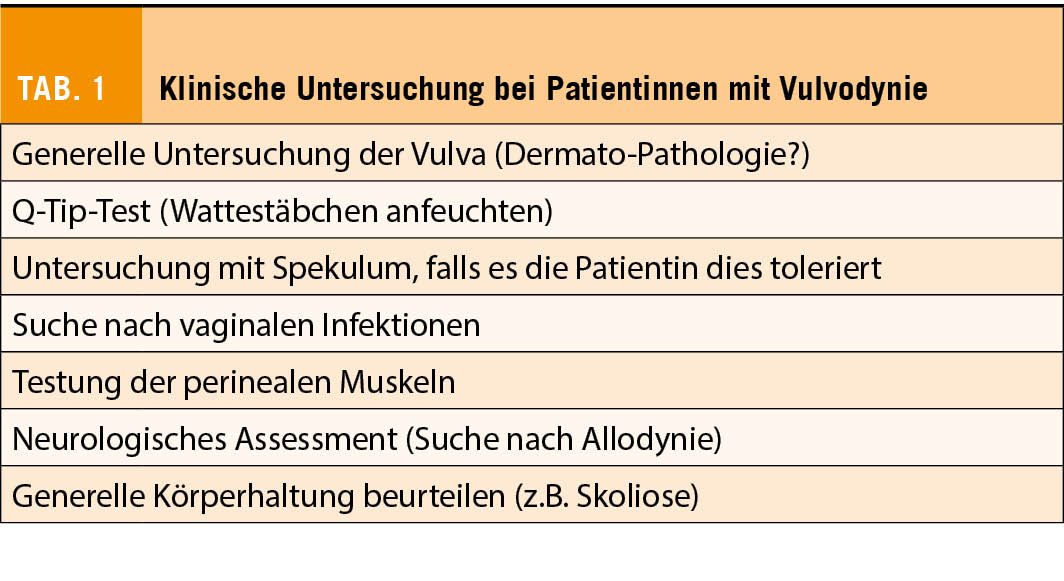
Wie Dr. Jacot-Guillarmod erklärte, sei es im Management von Patientinnen mit Vulvodynie von grosser Bedeutung, sich die Zeit für ein ausführliches Anamnesegespräch zu nehmen, in dem neben medizinischen auch psychologische und soziale Aspekte angesprochen werden. Danach folge die klinische Untersuchung (Tab. 1). «Die Reproduzierbarkeit der Schmerzen während der klinischen Untersuchungen zeigen den Patientinnen, dass ihre Schmerzen real sind. Dies empfinden sie oft als eine Art Erleichterung.
Denn meist mussten sie über längere Zeit die Erfahrung machen, dass sie mit ihrem Problem nicht ernst genommen werden», so Dr. Jacot-Guillarmod. Im weitere Verlauf der Abklärungen sollte auch die Beckenbodenmuskulatur untersucht werden. «Dies ist wichtig, da eine Vulvodynie häufig mit einem erhöhten Tonus der Beckenbodenmuskeln, v.a. der oberflächlichen, einhergeht», betonte die Rednerin. Umgekehrt könne es als eine Folge der Vulvodynie zu Veränderungen der Beckenbodenmuskulatur kommen.
Wenig Evidenz zu den Behandlungsoptionen
«Im Sinne eines multidisziplinären Vorgehens geht es bei der Therapie der lokalisierten, provozierten Vulvodynie nicht nur darum, den Schmerz im Bereich der Vulva und allfällige Myalgien des Beckenbodens zu lindern, sondern auch um das Wiederherstellen des sexuelle Selbstvertrauens und der sexuellen Identität», sagt die Rednerin. Kann eine spezifische Ursache für die Vulvodynie identifiziert werden, z.B. eine Infektion, ist diese gezielt zu therapieren. In allen anderen Fällen bzw. als Ergänzung empfehlen internationale Richtlinien als Erstlinientherapie eine Physiotherapie (Beckenbodentraining) und psychosoziale Interventionen (Schmerzmanagement, Sexualtherapie) (2). Die Physiotherapie hat sich in randomisierten Studie gegenüber einer topischen Lidocainbehandlung als überlegen erwiesen (5).
Zur pharmakologischen Behandlung stehen mehrere Optionen zur Verfügung. «Allerdings gibt es für viele von ihnen nur wenig Evidenz», schränkte Dr. Jacot-Guillarmod hier ein. So fehlen unter anderem für die Anwengund topischer Anästhetika (Lidocain) Daten aus randomisierten, kontrollierten Studien. «In der Klinik können topische Anästhetika ein über einen begrenzten Zeitraum eingesetztes Hilfsmittel darstellen, dass zum Beispiel die Physiotherapie unterstützt», schlug die Rednerin vor. Entzündungshemmende Substanzen wie Steroide werden nicht empfohlen. «Botulinumtoxin wird aktuell als Zweitlinientherapie angesehen. Es laufen jedoch einige Studien, die dazu beitragen sollen, gute Anwendungsprotokolle zu finden und diese zu validieren, so dass Botulinumtoxin in Zukunft systematischer in die Behandlung dieser Patientinnen integriert werden könnte», berichtete die Rednerin. Für Antikonvulsiva (Gabapentin) gebe es in der Literatur kontroverse Resultate. Ein Versuch als Drittlinientherapie könne sich aber lohnen. Keine Bedeutung in der Behandlung der Vulvodynie haben dagegen trizyklische Antidepressiva. Für eine topische Behandlung mit Östradiol 0,01% und Testosteron 0,1% liegen bisher keine Resultate randomisierter kontrollierter Studien vor. Eine Untersuchung mit 50 Frauen, deren Schmerzen unter Anwendung kombinierter hormoneller Kontrazeptiva begannen, lieferte Hinweise auf einen schmerzlindernden Effekt (6). «Chirurgische Therapien wie eine Vestibulektomie sollten als letztmögliche Option angesehen werden, denn auch zu ihnen gibt es keine Resultate aus randomisierten, kontrollierten Studien», schloss Dr. Jacot-Guillarmod
Dr. Therese Schwender
1. Mitchell KR et al. Painful sex (dyspareunia) in women: prevalence and associated factors in a British population probability survey. BJOG. 2017;124:1689-1697.
2. Bautrant E et al. Provoked vulvar vestibulodynia: Epidemiology in Europe, physio-pathology, consensus for first-line treatment and evaluation of second-line treatments. J Gynecol Obstet Hum Reprod. 2019;48:685-688.
3. Heddini U et al. Serotonin receptor gene (5HT-2A) polymorphism is associated with provoked vestibulodynia and comorbid symptoms of pain. J Sex Med. 2014;11:3064-71.
4. Ponte M et al. Effects of vulvodynia on quality of life. J Am Acad Dermatol. 2009;60:70-6.
5. Morin M et al. Multimodal physical therapy versus topical lidocaine for provoked vestibulodynia: a multicenter, randomized trial. Am J Obstet Gynecol 2021;224:189.e1-189.e12.
6. Burrows LJ, Goldstein AT. The treatment of vestibulodynia with topical estradiol and testosterone. Sex Med. 2013;1:30-3.