Das sogenannte vierte Trimester ist eine wichtige Phase der Schwangerschaft, die einen interdisziplinären medizinischen Ansatz erfordert. Die postpartale Hypertonie (PPHT) ist eine wichtige Erkrankung, die häufig ihren Ursprung schon in der Schwangerschaft hat, sich jedoch auch erst nach der Geburt manifestieren kann und bis zu 10% aller Schwangerschaften betrifft. Die PPHT wird durch eine Reihe von Ursachen begünstigt, die vor, während oder nach der Schwangerschaft auftreten können. Die PPHT ist eine der häufigsten Ursachen für Rehospitalisationen nach der Entbindung und stellt daher ein wichtiges Ziel für die Senkung der mütterlichen Mortalität und Morbidität dar. Nur 40 % der Frauen nehmen an den geplanten Gesundheitsuntersuchungen nach der Geburt teil, was zum Teil auf die Belastungen im Leben mit einem Neugeborenen, Schlafmangel, mangelndes Verständnis der Wichtigkeit der Untersuchungen und psychische Probleme zurückzuführen ist. Langfristig kann sich dies negativ auf die Gesundheit der Mütter auswirken, insbesondere im Falle einer anhaltend ungenügend kontrollierten oder persistierenden Hypertonie. Korrekte Diagnose, Überwachung, Behandlung und ein Patientinnen-freundliches Behandlungskonzept für die Zeit nach der Entlassung sind der Schlüssel zur Sicherung der künftigen kardiovaskulären Gesundheit dieser Frauen. In diesem Artikel beschreiben wir die Ursachen, die frühzeitige klinische und labortechnische Beurteilung und poststationäre Behandlungskonzepte der PPHT.
The so-called fourth trimester is an important phase of pregnancy that requires an interdisciplinary medical approach. Postpartum hypertension (PPHT) is an important disease that often originates during pregnancy, but may also manifest after birth, affecting up to 10% of all pregnancies. PPHT manifests from various etiologies that can occur before, during or after pregnancy. PPHT is one of the most common causes of re-hospitalization after delivery and therefore represents an important target for reducing maternal mortality and morbidity. Only 40% of women attend scheduled postpartum health checkups, due in part to the stresses of living with a newborn, sleep deprivation, lack of understanding of its importance, and mental health issues. This can have a long-term negative impact on maternal health, especially in the case of persistent inadequately controlled or persistent hypertension. Correct diagnosis, monitoring, treatment, and a patient-friendly approach to postdischarge care are key to ensuring the future cardiovascular health of these women. In this article, we describe the causes, early clinical and laboratory assessment, and postdischarge treatment concepts of PPHT.
Key Words: postpartale Hypertonie, viertes Trimester, hypertensive Störungen in der Schwangerschaft, kardiovaskuläre Gesundheit
Die postpartale Hypertonie (PPHT) ist definiert als erhöhter Blutdruck (systolischer Druck ≥ 140mmHg und/oder diastolischer Blutdruck von ≥ 90mmHg) nach der Entbindung. Die PPHT, die häufig aus den «hypertensive diseases of pregnancy» (HDP) hervorgeht, betrifft etwa 10 % aller Schwangerschaften und erfordert ein tieferes Verständnis und eine spezifische Behandlungsstrategie (1, 2). Wenn sie nicht angemessen behandelt wird, ist die PPHT kurzfristig eine der Hauptursachen für eine erneute Hospitalisierung nach der Entbindung (3). Langfristig haben diese Frauen ein erhöhtes Risiko für kardiovaskuläre Komplikationen wie Bluthochdruck, ischämische Herzkrankheiten und Schlaganfälle. Leider ist die tatsächliche Inzidenz der postpartalen Hypertonie nicht bekannt, da die Blutdruckerhöhung häufig asymptomatisch ist und unerkannt bleibt, die Mütter keine Vorsorgeuntersuchungen wahrnehmen, oder in manchen Fällen eine gestresste Mutter wichtige Symptome nicht korrekt wahrnimmt. Auch sind nicht immer entsprechende Programme zur Nachbehandlung vorhanden. In den National Institute for Health and Care Excellence (NICE)-Leitlinien wird eine strenge Kontrolle dieser Patientinnen empfohlen, was jedoch aufgrund der oben genannten Faktoren nicht immer eingehalten wird (4).
Blutdruck während der Schwangerschaft
Die Hämodynamik und damit auch der Blutdruck haben während der Schwangerschaft normale Schwankungen, die es zu kennen gilt. Das Blutvolumen nimmt während der Schwangerschaft um rund 40% zu, wobei der schnellste Anstieg im ersten Trimester zu verzeichnen ist. Auch das Herzzeitvolumen nimmt während der Schwangerschaft um bis zu 50% zu, wobei es im ersten Trimester stetig ansteigt und im fünften Monat einen Höchstwert erreicht. Im Allgemeinen sinkt der Blutdruck trotz des Anstiegs des Herzzeitvolumens im ersten Trimester um 5-10mmHg und sinkt dann bis zur Mitte der Schwangerschaft aufgrund der Progesteron-vermittelten Entspannung der glatten Muskulatur (5). Bei der Erstbewertung des Blutdrucks in der Schwangerschaft sollten die Blutdruckmessungen mit den Werten vor der Schwangerschaft verglichen werden, da bereits physiologische Veränderungen stattgefunden haben. Im dritten Trimester ist ein allmählicher Anstieg des Blutdrucks zu beobachten, der dann im Allgemeinen 3-6 Tage nach der Entbindung seinen Höhepunkt erreicht und dann wieder abfällt.
Ursachen für postpartale Hypertonie
In den meisten Fällen wird die postpartale Hypertonie durch eine zugrundeliegende HDP verursacht, aber es gibt auch immer wieder Patientinnen mit späten Präeklampsien oder auch Patientinnen mit einer unkomplizierten Schwangerschaft und erst postpartal erhöhten Blutdruckwerten. Die HDP umfassen fünf Situationen: chronische Hypertonie, Schwangerschaftshypertonie oder schwangerschaftsinduzierte Hypertonie, Präeklampsie, HELLP-Syndrom und Eklampsie (6). Neben der klassischen PPHT, die durch HDP verursacht wird, können Frauen eine vorübergehende postpartale Hypertonie haben, die z.B. durch Schmerzen, intravenöse Flüssigkeitszufuhr, generalisierte Ödeme aufgrund der Schwangerschaft und nichtsteroidale entzündungshemmende Medikamente ausgelöst wird. Sehr wichtig ist es späte Manifestationen einer Präeklampsie nicht zu verpassen.
All diese unterschiedlichen klinischen Situationen können zu einem anhaltend erhöhten Blutdruck nach der Geburt führen und erfordern eine besondere Überwachung auf der Entbindungsstation, eine geeignete Behandlung während der Stillzeit und eine gut geplante Überwachung nach der Entlassung, da die Normalisierung des Blutdrucks sich rasch einstellen kann und ggf. eingesetzte antihypertensive Medikamente schrittweise reduziert werden müssen.
Messung des Blutdrucks
Bei allen Frauen sollte spätestens 6 Stunden nach der Geburt der Blutdruck gemessen werden. Bei Frauen, die wiederholt Blutdruckwerte ≥ 140/90 oder einmal > 160/100mmHg haben, ist eine besondere Überwachung erforderlich (4, 6). Der Blutdruck sollte mindestens drei- bis viermal pro Tag mit einem automatischen Blutdruckmessgerät gemessen werden. Jede Messreihe sollte aus 3-5 Blutdruckmessungen im Abstand von mindestens 1 Minute bestehen. Die Messungen sollten mit einem kalibrierten und validierten Oberarm Blutdruckmessgerät in Höhe des Herzens durchgeführt werden. Obwohl Messungen im Krankenhaus nie die ideale Umgebung für Blutdruckmessungen sind, können und sollten einige der bekannten Störfaktoren minimiert werden. Wir schlagen vor, dass die Messungen nach Möglichkeit mit der Patientin allein im Zimmer durchgeführt werden, ohne dass sie redet, stillt oder ihr Baby hält. Automatisierte und unbeobachtete Messungen können dabei die Häufigkeit einer Weisskittelkomponente weiter reduzieren Auf diese Weise erhalten die behandelnden Ärzte genauere Messungen, um korrekte therapeutische Entscheidungen treffen zu können. Wenn die Diagnose einer postpartalen Hypertonie unklar ist, sollte eine 24-Stunden-Blutdruckmessung im Krankenhaus in Betracht gezogen werden.
Klinische und labortechnische Erstuntersuchung
Bei unklarer Ätiologie der PPHT empfehlen wir, falls vorhanden, die Histologie der Plazenta und die anschliessende Klassifizierung nach Amsterdam anzuschauen. Obwohl diese Klassifizierung komplex ist und im Zusammenhang mit dem Gestationsalter, der klinischen Vorgeschichte und dem Gewicht des Neugeborenen interpretiert werden muss, hat sie sich als wertvoll erwiesen (7). Die Informationen können dazu beitragen, die Ursache der PPHT zu klären, was Auswirkungen auf das Management in der aktuellen postpartalen Phase und bei zukünftigen Schwangerschaften haben kann.
Wir empfehlen ausserdem, vor der Entlassung das poststationäre Management der Patientin durch eine Überweisung an einen entsprechend erfahrenen Gynäkologen, Internisten oder Kardiologen zu organisieren. Bei dieser Konsultation sollte eine Anamnese erhoben werden, die sich auf das vorbestehende Präeklampsierisiko, die kardiovaskuläre und renale Vorgeschichte, kardiovaskuläre Risikofaktoren, die Familienanamnese und den aktuellen und ggf. früheren Schwangerschaftsverlauf konzentriert. Zu den zu erhebenden kardiovaskulären Risikofaktoren gehören: Rauchen, Adipositas, Diabetes, Dyslipidämie, Autoimmun- und rheumatoide Erkrankungen, Ernährung, Aktivitätsniveau und ggf. weitere Faktoren wie Umwelteinflüsse.
Eine körperliche Untersuchung mit Fokus auf dem kardiovaskulären, pulmonalen und neurologischen Status sollte durchgeführt werden. Bei Sehstörungen oder Kopfschmerzen, die nicht mit einem erhöhten Blutdruck korrelieren, wird auch eine neurologische Untersuchung empfohlen, um postdurale Kopfschmerzen (nach Periduralanästhesie) und ein posteriores reversibles Enzephalopathie-Syndrom auszuschliessen (8).
Die Laboruntersuchung umfasst mindestens ein hämatologisches Panel, Leber- und Nierenfunktion sowie Elektrolyte, Urinanalyse mit Albumin/Kreatinin-Quotient und Protein/Kreatinin-Quotient (9). In unserer Institution erfolgt diese Erstuntersuchung im Hinblick auf die PPHT und die Transition in die ambulante Behandlung noch im stationären Setting, damit in diesem Rahmen mit den Frauen die verschiedenen Möglichkeiten des poststationären Managements inkl. Telemonitoring und telemedizinischer Betreuung diskutiert werden können.
Antihypertensive Behandlung
Sobald eine postpartale Hypertonie diagnostiziert wurde, ist eine medizinische Behandlung angezeigt und sollte nicht aufgeschoben werden (6). Dazu gehören das Absetzen von NSAR, die Beurteilung und konsequente Behandlung von Schmerzen und das Absetzen unnötiger intravenöser Flüssigkeiten (6). Die Patientinnen sollten beruhigt und darüber aufgeklärt werden, dass die eingesetzten Medikamente für Mutter und Kind sicher sind.
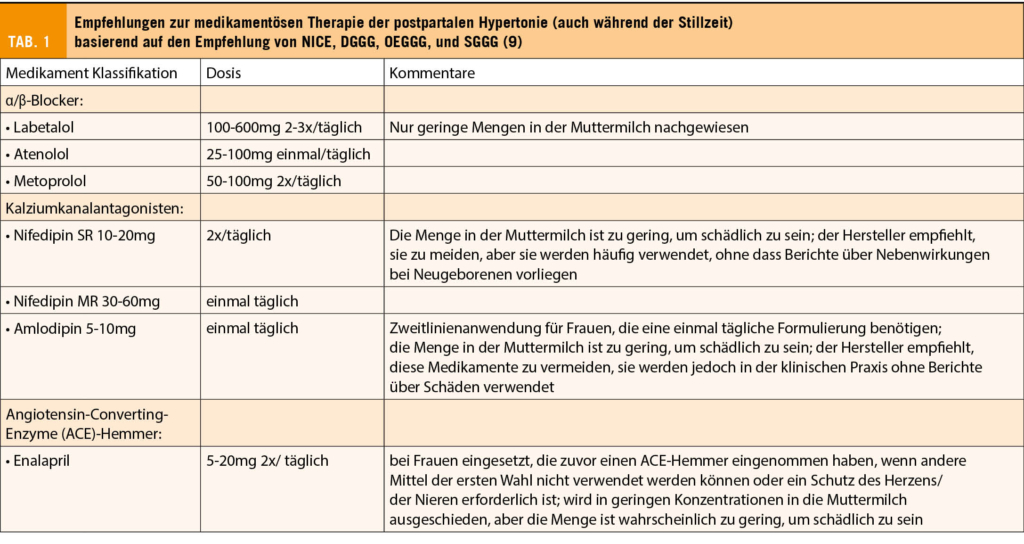
In Fällen, in denen Patientinnen während der Schwangerschaft blutdrucksenkende Medikamente wie Labetalol oder Methyldopa eingenommen haben, empfehlen wir, diese auf ein länger wirksames Medikament umzustellen (6). Leider gibt es nur wenige Daten zur blutdrucksenkenden Therapie bei PPHT und die Behandlung beruht weitgehend auf klinischen Erfahrungen. Im Allgemeinen ist es weniger wahrscheinlich, dass Medikamente mit hoher Proteinbindung und geringer Lipidlöslichkeit in relevanten Mengen in der Muttermilch vorhanden sind (4). Wir empfehlen bei Albuminurie, Proteinurie und/oder erhöhtem diastolischen Blutdruck mit Enalapril zu beginnen (9). Im Setting der Präeklampsie zeigte Enalapril in einer Pilotstudie einen kardioprotektiven Effekt (10, 11).
Metoprolol kann in Kombination mit Enalapril oder allein verwendet werden. Nifedipin sollte als Mittel der dritten Wahl oder als Notfallmedikament in Betracht gezogen werden, wenn die Blutdruckwerte ≥ 160/100mmHg sind oder wenn die maximale Dosierung von Enalapril und Metoprolol nicht ausreicht. Bei Frauen mit afrikanischer Herkunft sollte Nifedipin frühzeitig und als Basistherapie in Betracht gezogen werden, wenn der Blutdruck auf Enalapril oder Metoprolol nicht adäquat anspricht, da diese beiden pharmakologischen Klassen bei Frauen mit diesem Hintergrund einen geringeren Nutzen haben können. Mögliche Medikamente in der postpartalen Phase mit einem vertretbaren Sicherheitsprofil sind in Tabelle 1 aufgeführt (4, 6).
Nach der Entlassung/ambulante Behandlung der postpartalen Hypertonie
In der unmittelbaren postpartalen Periode ist der Blutdruck sehr dynamisch. Bei einigen Frauen steigt der Blutdruck unerwartet an, bei anderen normalisiert er sich schnell. In beiden Fällen besteht die Gefahr, dass der Blutdruck entweder nicht angemessen oder übermässig behandelt wird.
Um eine optimale Transition von der stationären zur ambulanten Behandlung zu ermöglichen, empfehlen wir, dass Frauen mit PPHT innerhalb einer Woche Kontakt mit ihrem nachbehandelnden Arzt aufnehmen. Im Allgemeinen kann in den nächsten Wochen die Medikation schrittweise reduziert und im günstigsten Fall abgesetzt werden. Üblicherweise bietet sich an zuerst den Betablocker schrittweise zu reduzieren und zu beenden und in einem weiteren Schritt das Enalapril zu reduzieren und wenn möglich zu stoppen. Durch dieses schrittweise Vorgehen erhält die Patientin eine längere Exposition des ACE-Hemmers, was aufgrund einer postulierten kardio-renalen Schutzwirkung von Vorteil sein kann (10).
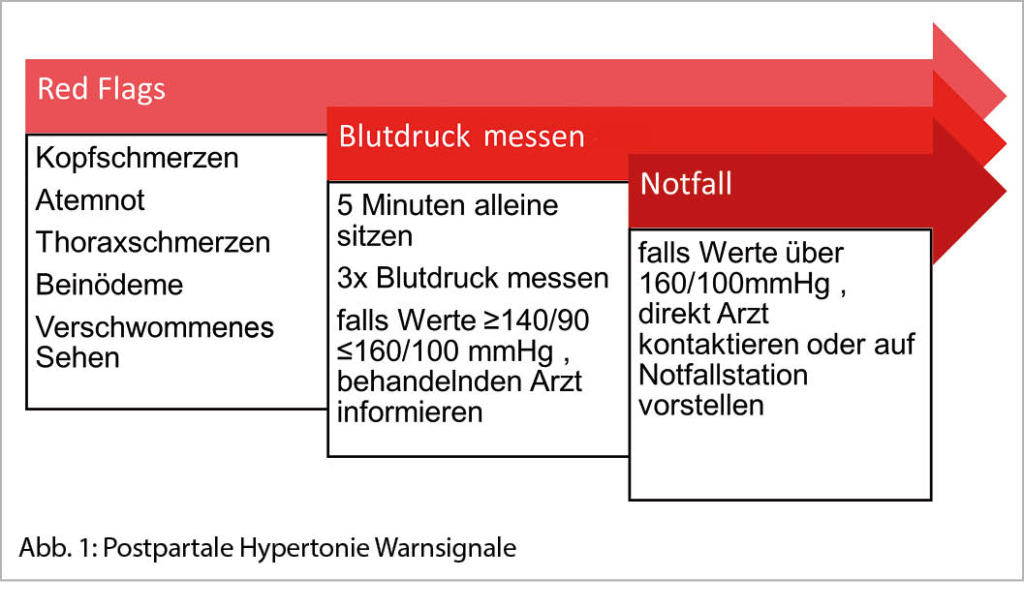
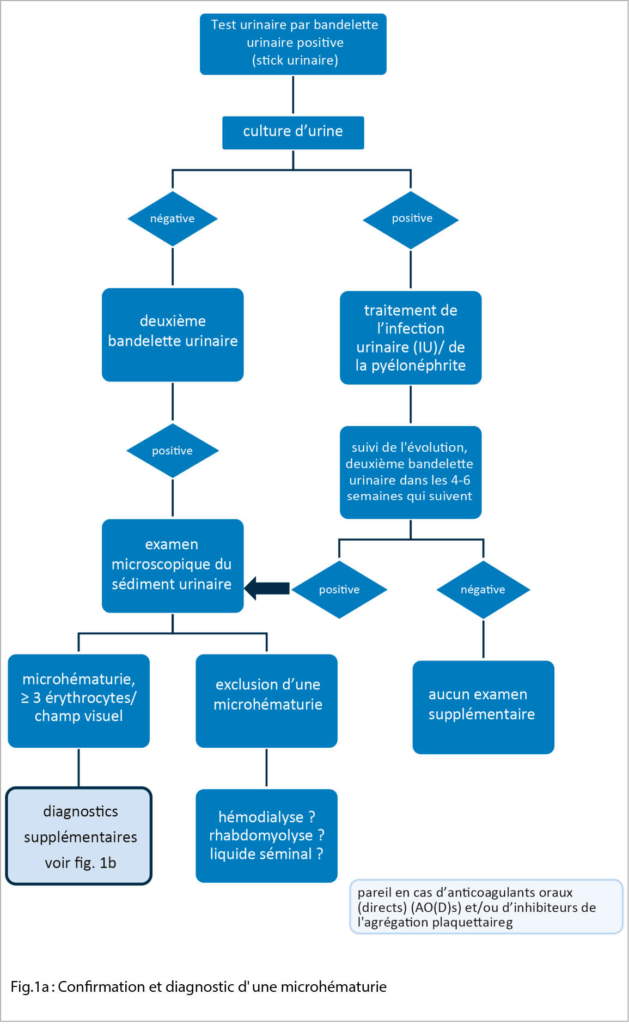
Die medizinischen Kontakte, die eine Woche nach der Entlassung stattfinden sollten, können persönlich wahrgenommen werden. Alternativ können telemedizinische Methoden und Telemonitoring für das poststationäre Management verwendet werden. Dies gilt vor allem dann, wenn vor der Entlassung eine gute Kommunikation mit der Patientin und ein Verständnis für Warnzeichen des Bluthochdrucks erreicht werden kann (Abb. 1). Essentiell in diesem Fall sind technisch korrekte Heimblutdruckmessungen, um eine optimale Datengrundlage für Behandlungsentscheide zu haben. Hier empfehlen wir die Patientin entsprechend zu instruieren. Je nach Institution stehen auch Gesundheits-Applikationen zur Verfügung, die die Patientin anleiten, standardisierte Messungen durchzuführen. Aus unserer Erfahrung heraus kann durch den Einsatz von telemedizinischen Methoden die Anzahl von physischen Konsultationen im Spital minimiert werden.
Für Patientinnen mit grenzwertigen Blutdruckwerten, bei denen das Risiko besteht, dass sie eine postpartale Hypertonie entwickeln, empfehlen wir, diese mit einem Rezept für ein Oberarm-Blutdruckmessgerät und ggf. für Medikamente (Einnahme jedoch nur nach Rücksprache mit einem Arzt) zu entlassen. Gefährdet sind insbesondere Frauen, die während der Schwangerschaft eine Präeklampsie oder schwangerschaftsinduzierte Hypertonie hatten und direkt nach der Geburt wieder normotensive Werte aufweisen. Dies ist darauf zurückzuführen, dass grenzwertige Blutdruckwerte im Krankenhaus oft nicht wahrgenommen werden.
Drei Monate nach der Geburt empfehlen wir eine 24h-Blutdruckmessung, um zu dokumentieren, ob sich der Blutdruck wieder normalisiert hat, oder ob eine Hypertonie persistiert. Zu diesem Zeitpunkt sollte auch der Albumin-Kreatinin-Quotient im Urin bestimmt werden, um eine anhaltende Albuminurie zu überprüfen und eine Leberwerte Kontrolle, falls diese nach Geburt erhöht waren (4).
Wenn die postpartale Hypertonie 3 Monate nach der Entbindung persistiert, empfehlen wir eine Wiederholung der ambulanten 24-Stunden-Blutdruckmessung nach 6 Monaten. Sollte die Hypertonie sechs Monate nach der Geburt weiterhin vorhanden sein, so besteht bei der Patientin der Verdacht auf eine essenzielle oder sekundäre Hypertonie, und sekundäre Ursachen der Hypertonie sollten ausgeschlossen und die Medikation entsprechend umgestellt werden, sobald die Mutter nicht mehr stillt. Insbesondere auf die Abklärung von sekundären Hypertonieursachen sollte ein Hauptaugenmerk gelegt werden, da diese gemäss den NICE-Leitlinien häufig unterdiagnostiziert werden (4).
Patientinnen mit einer Perstistenz einer Albuminurie nach 6 Monaten sollten durch einen Neurologen mitbeurteilt werden.
Die COVID-19-Pandemie hat uns in unserem Behandlungsmanagement zu neuen Wegen gezwungen. Schon vor Beginn der Pandemie boten wir an unserer Institution den Patientinnen mit PPHT zunehmend an, klassische physische Konsultationen in der Hypertoniesprechstunde durch den Einsatz eines standardisierten, virtuellen Behandlungskonzeptes mit Telemonitoring und Telekonsultationen maximal zu reduzieren. Die ersten Ergebnisse der wissenschaftlichen Begleitung dieses virtuellen Behandlungsmanagements stimmen uns sehr positiv bei einer hohen Praktikabilität und Patientenakzeptanz (noch unpublizierte Daten). Unterstützt werden virtuelle Behandlungskonzepte der arteriellen Hypertonie auch durch aktuelle Empfehlungen verschiedener Fachgesellschaften, wobei es essentiell ist, dass durch die virtuelle Behandlung die Behandlungsqualität nicht leidet (12).
Änderung des Lebensstils in der Postpartum-Phase
Parallel zur Überwachung und medikamentösen Behandlung sollten Frauen im Wochenbett über einen gesunden Lebensstil und dessen positive Auswirkungen im Wochenbett aufgeklärt werden. Schlafen, wann immer es möglich ist, einschliesslich Nickerchen, wenn das Baby schläft, 10.000 Schritte Bewegung pro Tag und eine natriumarme und ballaststoffreiche Ernährung werden generell empfohlen. Das American College of Obstetricians and Gynecologists (ACOG) ermutigt Frauen im vierten Trimester jede verfügbare zusätzliche nicht-medizinische Hilfe in Anspruch zu nehmen, um diese komplexe Phase zu bewältigen. Dazu gehört z.B. die Unterstützung durch Hebammen, Schlaf-Doulas, Familie und Freunde (13).
Zukünftige Schwangerschaften und kardiovaskuläres Risiko
Der dreimonatige Kontrolltermin ist ein guter Zeitpunkt, um mit den Patientinnen über die PPHT und den Krankheitsverlauf zu sprechen. Die Patientinnen sollten über Ursachen der PPHT und die möglichen Auswirkungen auf das kardiovaskuläre Risiko aufgeklärt werden. Insbesondere über das erhöhte Risiko einer arteriellen Hypertonie sollte gesprochen werden, da 1 Jahr nach der Geburt rund 40% der Frauen eine essentielle Hypertonie entwickeln, selbst wenn sich die Werte initial schnell wieder auf einen normalen Blutdruck eingestellt haben (14). Insofern gilt es regelmässig und langfristig ein besonderes Augenmerk auf die kardiovaskulären Risikofaktoren und insbesondere die Blutdruckwerte zu haben.
Im Falle einer erneuten Schwangerschaft wird die frühzeitige Einnahme von Aspirin empfohlen, um das Risiko einer frühen Präeklampsie zu verringern.
Abkürzungen:
HDP hypertensive diseases of pregnancy, HELLP haemolysis, elevated liver enzyme levels, low platelet count, PPHT postpartale Hypertonie, ACOG American College of Obstetricians and Gynecologists
Copyright bei Aerzteverlag medinfo AG
Oberärztin Medizinische Poliklinik
Medizinische Poliklinik, Universitätsspital Basel
Petersgraben 4
4031 Basel
thenral.socrates@usb.ch
Stv. Chefarzt medizinische Poliklinik
und Leiter Hypertoniesprechstunde
Universitätsspital Basel
Petersgraben 4
4031 Basel
thilo.burkard@usb.ch
Dr. Socrates und Dr. Burkard haben von Roche Diagnostics einen Research Grant und Materialsupport (Laborkits) zur Unterstützung des Basel Postpartum Hypertension Registers erhalten
1. Giorgione V, Ridder A, Kalafat E, Khalil A, Thilaganathan B. Incidence of postpartum hypertension within 2 years of a pregnancy complicated by pre-eclampsia:
a systematic review and meta-analysis. Bjog. 2021;128(3):495-503.
2. Gestational Hypertension and Preeclampsia: ACOG Practice Bulletin, Number 222. Obstet Gynecol. 2020;135(6):e237-e60.
3. Clapp MA, Little SE, Zheng J, Robinson JN. A multi-state analysis of postpartum readmissions in the United States. Am J Obstet Gynecol. 2016;215(1):113.e1-.e10.
4. Webster K, Fishburn S, Maresh M, Findlay SC, Chappell LC. Diagnosis and
management of hypertension in pregnancy: summary of updated NICE guidance. Bmj. 2019;366:l5119.
5. Klein HH, Pich S. [Cardiovascular changes during pregnancy]. Herz. 2003;28(3):173-4.
6. Bramham K, Nelson-Piercy C, Brown MJ, Chappell LC. Postpartum management of hypertension. BMJ : British Medical Journal. 2013;346:f894.
7. Redline RW, Ravishankar S, Bagby CM, Saab ST, Zarei S. Four major patterns of placental injury: a stepwise guide for understanding and implementing the 2016 Amsterdam consensus. Mod Pathol. 2021;34(6):1074-92.
8. Sudulagunta SR, Sodalagunta MB, Kumbhat M, Settikere Nataraju A. Posterior
reversible encephalopathy syndrome(PRES). Oxf Med Case Reports. 2017;2017(4):omx011.
9. Schlembach D, Stepan H, Groten T. S2k Leitlinie: Hypertensive Schwangerschaftserkrankungen: Diagnostik und Therapie. Deutsche Gesellschaft für Gynäkologie und Geburtshilfe, Österreichische Gesellschaft für Gynäkologie und Geburtshilfe, Schweizerische Gesellschaft für Gynäkologie und Geburtshilfe. 2019.
10. Ormesher L, Higson S, Luckie M, Roberts SA, Glossop H, Trafford A, et al. Postnatal Enalapril to Improve Cardiovascular Function Following Preterm Preeclampsia (PICk-UP):: A Randomized Double-Blind Placebo-Controlled Feasibility Trial. Hypertension. 2020;76(6):1828-37.
11. Staff AC, Dechend R. Will Postnatal Renin-Angiotensin System Blockade Improve
Long-Term Maternal Cardiovascular Health After Preeclampsia? Hypertension. 2020;76(6):1704-6.
12. Khan NA, Stergiou GS, Omboni S, Kario K, Renna N, Chapman N, et al. Virtual management of hypertension: lessons from the COVID-19 pandemic-International Society of Hypertension position paper endorsed by World Hypertension League and European Society of Hypertension. J Hypertens. 2022.
13. ACOG Committee Opinion No. 736: Optimizing Postpartum Care. Obstet Gynecol. 2018;131(5):e140-e50.
14. Melchiorre K, Sutherland GR, Liberati M, Thilaganathan B. Preeclampsia is
associated with persistent postpartum cardiovascular impairment. Hypertension. 2011;58(4):709-15.