Der Nutzen von digitalen Hilfsmitteln erscheint auf den ersten Blick in der Palliative Care nicht naheliegend. In Ländern mit grossen geographischen Distanzen werden sie bereits flächendeckend eingesetzt. Die häufigsten klinischen Anwendungsgebiete sind die direkte Kommunikation zwischen Fachperson und Patient:in (virtuelle Visiten), und die Koordination (virtuelle Besprechungen z.B. Tumorboards, interprofessionelle Kommunikation). Vorteile sind Verbesserung der Kommunikation und Koordination, Reduktion von Symptomen durch rasche Beratung und geringerer Aufwand durch Vermeidung von Wegzeiten. Andere Anwendungen wie digitale Apps und psychologische Unterstützung mittels virtueller Realität werden auch bereits klinisch eingesetzt. Zwangsläufig hat die digitale Medizin in der Onkologie und Palliative Care während der COVID-Pandemie einen Aufschwung erhalten; ob dieser Aufschwung anhält, ist unklar.
Im Kontext der Schweiz sehen wir vor allen die folgenden Anwendungen als potentiell hilfreich: virtuelle Kommunikation (digitale interprofessionelle Besprechungen, virtuelle Visiten), Digitales Monitoring und Anwendungen der virtuellen Realität. Bei der virtuellen Kommunikation sind insbesondere die digitalen interprofessionellen Besprechungen interessant, da diese zu einer Verbesserung der interprofessionellen Koordination beitragen können. Beim digitalen Monitoring steht die Unterstützung der Patient:in im häuslichen Umfeld mittels automatischer Übermittlung von Gesundheitsdaten an die Fachpersonen im Vordergrund. Die virtuelle Realität zeigt ihr Potential in der psychologischen Unterstützung. Haupthindernisse sind aktuell die fehlende Standardisierung der Infrastruktur und die unvorhersehbare Akzeptanz bei den Fachpersonen und Patient:innen. Nicht zuletzt ist auch aus der Datenschutzperspektive Skepsis bezüglich einer raschen Verbreitung in der Zukunft angebracht. Die drei aktuellen Einsatzbereiche der digitalen Hilfsmittel werden bezüglich ihres klinischen Nutzens im schweizerischen Kontext analysiert.
At first glance, the use of digital aids in palliative care does not seem obvious. In countries with large geographic distances, they are already being used extensively. The most common clinical applications are direct communication between specialist and patient (virtual visits) and coordination (virtual meetings, e.g. tumor boards, interprofessional meetings). Advantages are improvement of communication and coordination, reduction of symptoms through rapid consultation, and less effort by avoiding travel time. Other applications such as digital apps and psychological support using virtual reality are also already being used clinically. Inevitably, digital medicine in oncology and palliative care received a boost during the COVID pandemic; whether this boost will continue is unclear.
In the context of Switzerland, we see the following applications in particular as potentially helpful : virtual communication (digital interprofessional meetings, virtual visits), digital monitoring, and virtual reality applications. In the case of virtual communication, digital interprofessional meetings are of particular interest, as they can contribute to an improvement of interprofessional coordination. In digital monitoring, the focus is on supporting the patient in the home environment by means of automatic transmission of health data to the professionals. Virtual reality shows its potential in psychological support. The main obstacles are currently the lack of standardization of the infrastructure and the unpredictable acceptance by professionals and patients. Last but not least, skepticism is also warranted from a data protection perspective with regard to rapid dissemination in the future. The three current areas of application of digital aids are analyzed in terms of their clinical benefits in the Swiss context.
Key Words: Telemedicine, Digital health interventions, Palliative Care, Oncology Interprofessional Care
Telemedizin und Palliative Care erscheinen vordergründing nicht sehr kompatibel, da die Idee eines digital-elektronischen Werkzeugs in einem beziehungsbasierten Fachgebiet nicht naheliegend erscheint.
Eine breite Palette von digitalen Werkzeugen/Interventionen wird jedoch bereits in der Palliative Care angewendet. Diese reichen von der klassischen virtuellen Visite, über virtuelle Realität (beispielsweise 3-D-Reisen bis zu Entscheidungsfindung mittels künstlicher Intelligenz (1, 2)). Weitere Anwendungsgebiete der Telemedizin beziehen sich auf die digitale Überwachung des Gesundheits-zustandes, die Übertragung von Daten zur Fachperson und die Fallbesprechungen (Fachperson zu Fachperson) (3, 4). Bei onkologischen Patient:innen hat nicht zuletzt die Corona-Pandemie dazu beigetragen, dass Interventionen der Palliative Care vermehrt telemedizinisch erfolgen. Dies betrifft insbesondere die Beratung und das Monitoring bei der Symptombehandlung, aber auch die Instruktion und Koordination des betreuenden Netzwerks und der Angehörigen. Hier handelt die Palliative Care gemäss ASCO mit einem problem- und patientenbezogenen Vorgehen im Sinn der «Concurrent care», also in der Regel parallel zur krankheitsmodifizierenden Therapie mit supportiven Therapien (5).
Die Vorteile der Telemedizin, insbesondere der virtuellen Visite, zeigen sich vor allem im Bereich des erleichterten Zugangs zu Dienstleistungen, einer Verbesserung der Kommunikation durch rasche Erreichbarkeit, und dadurch nicht zuletzt einer Reduktion der psychischen Symptome, vor allem der Angst, und in geringeren Kosten (6). In Ländern mit grossen geographischen Distanzen wie Canada oder Australien ist die Akzeptanz bei den Patienten, aufgrund jahrzehntelanger Vorerfahrung, grundsätzlich sehr gut. Die Fachpersonen zeigen eine gesunde Skepsis gegenüber der Telemedizin, akzeptieren diese aber gut, wenn sie die notwendige Logistik und Schulung erhalten (4, 7). Die Evidenz dafür basiert aber häufig auf Evaluationen von bestehenden Projekten, oder solchen aus der Notwendigkeit (geographische Distanz, Fachkräftemangel) entstandenen Projekte. Eine Bedürfnisabklärung bei allen Beteiligten vor der Planung und Implementation wurde nur sehr selten durchgeführt (7).
Die geographischen Distanzen existieren in der Schweiz nicht und die pandemiebedingten Zugangsbeschränkungen zum Gesundheitssystem sind und waren nicht sehr ausgeprägt.
Parallel dazu zeigte sich, dass sich einige der geplanten oder existierenden digitalen Hilfsmittel trotz des Digitalisierungsschubs während der Pandemie nur schleppend entwickelt haben. Das bekannteste Beispiel ist das elektronische Patienten-Dossier. Bei einigen sind sogar schwerwiegende Datenschutzlücken erkannt worden, man denke an das digitale Impfbuch oder das Organspende-
Register. So stellt sich die Frage aus Sicht der Palliative Care, in welchen Anwendungsbereichen der Einsatz telemedizinischer Vorgehensweisen in der Zukunft insbesondere aus Sicht der Patient:innen sinnvoll ist (8). Ein hoher Anspruch an den Datenschutz ist hierbei selbstverständlich.
Wir möchten in diesem Beitrag die telemedizinischen Hilfsmittel aus der klinisch-praktischen Perspektive der Palliative Care beleuchten und hinsichtlich der Zukunft kritisch hinterfragen.
Methoden
Die vorliegende Arbeit basiert auf einem Scoping review (7) und zwei Positionspapieren (4, 8) der Autoren. Die beschriebene Zukunftsperspektive basiert einerseits auf der klinischen Erfahrung/Einschätzung der Autoren, andererseits auf selektionierten Artikeln einer Literatursuche (Pubmed: Telemedicine AND Palliative Care, ab 2022).
Einsatzbereiche der digitalen Hilfsmittel
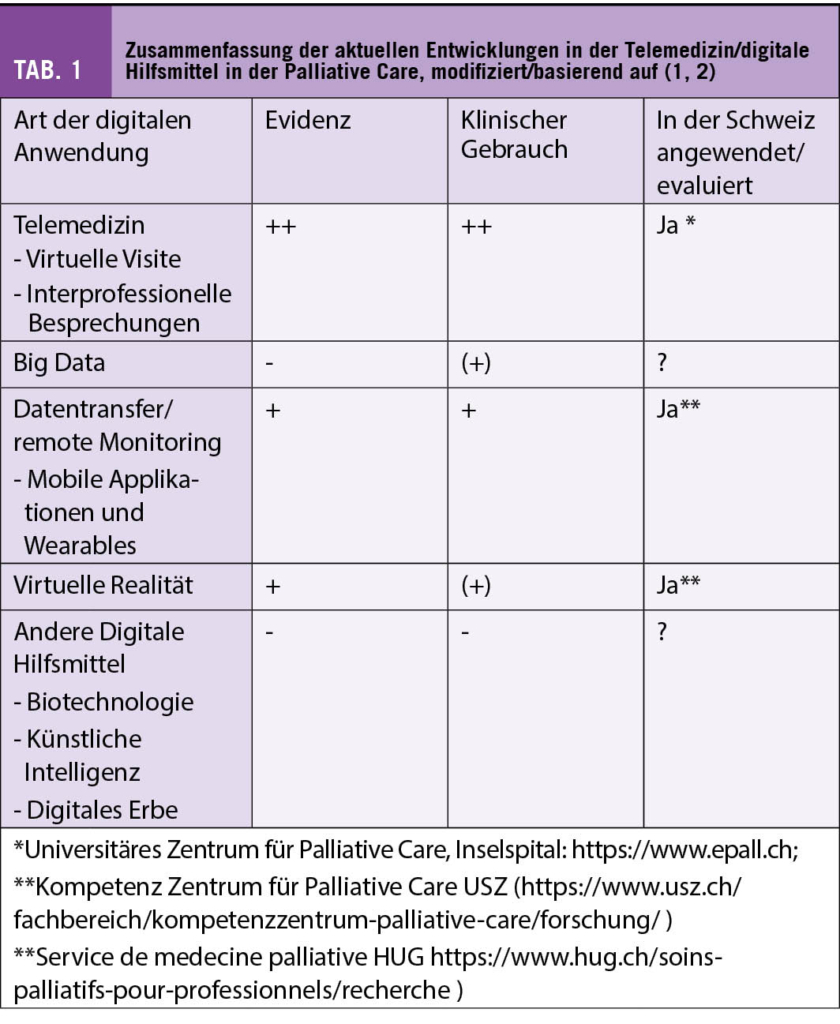
Im Folgenden werden wir den Nutzen und die Herausforderungen der verschiedenen digitalen Hilfsmittel in der Palliative Care aufzeigen. Tabelle 1 fasst die aktuellen Entwicklungen bezogen auf die Palliative Care zusammen.
Virtuelle Visite
Die virtuelle Visite, also eine Visite über eine Videokonferenz, ist die am weitesten verbreitete Form der Telemedizin. Sie ist gut akzeptiert, relativ einfach machbar und hat bewiesenermassen Vorteile für den Patienten auf der Ebene der Kommunikation, Symptomreduktion (teilweise) und der Reduktion von Reisezeit und -aufwand (4, 7). Wie oben erwähnt, gilt diese Evidenz aber nur für Länder mit geographischen Hindernissen/grossen Distanzen.
Die technologischen Grundvoraussetzungen sind in der Schweiz mehrheitlich gegeben. Mögliche Hindernisse orten wir in zwei Bereichen: in einer der Telemedizin gegenüber eher zurückhaltenden Einstellung der Patient:innen, Angehörigen und Fachpersonen, und die fehlende technische Standardisierung. Letztere (z.B. bei der Identifikation/Datenschutz/Interkompatibilität) führt zu einer schlechteren Benutzbarkeit, was die Motivation der Patienten nicht fördert.
Zusätzlich gibt es aktuell keine klar definierten Verrechnungsmöglichkeiten. Die Abrechnung als klassische Telefonkonsultation ist zwar möglich, bildet aber den Aufwand nur unzureichend ab, was eine nachhaltige Verwendung in der Zukunft insbesondere für den ambulanten Bereich erschwert (9).
Aus diesen Gründen sehen wir die Zukunft für eine virtuelle Visite zwiespältig: der Nutzen für schwerkranke Menschen, die möglichst viel Lebenszeit zuhause verbringen möchten und für die der Energieaufwand für eine externe Konsultation enorm ist, könnte sehr gross sein. Dies betrifft auch das Sicherheitsgefühl nicht nur für die Patient:innen sondern auch für die Angehörigen: der rasche «Kanal» zum Betreuungsnetz, nicht nur als schwer zuordenbare Stimme, sondern als sichtbare Person. Auf der anderen Seite stehen die regulatorischen Anforderungen, und die Zurückhaltung in der schweizerischen Gesellschaft, individuelle Daten preiszugeben unter Einschluss einer E-Mail-Adresse, die Voraussetzung für den telemedizinischen Link ist.
Interprofessionelle Kommunikation
Palliative Care gilt als eine der Vorreiterdisziplinen der Interprofessionalität. Eines der wichtigsten Elemente der Interprofessionalität ist die transparente Definition von gemeinsamen Zielen und die Koordination von verschiedenen Fachkompetenzen und -personen. Dies ist zeitlich und ressourcentechnisch eine sehr aufwändige Aufgabe. Deshalb erscheint die Telemedizin mit der Möglichkeit von Video-Konferenzen und einer zeitnahen, zentralen Dokumentation als ein interessanter Lösungsansatz (8).
Als Hindernis sehen wir hier wiederum die fehlende technische Standardisierung (Identifikation, Kompatibilität der Systeme) und das Fehlen eines funktionierenden, von der Bevölkerung akzeptierten digitalen Patient:innen-Dossiers.
Wie bei den virtuellen Visiten gibt es auch für diese Modalität keine spezifischen Verrechnungsmöglichkeiten im aktuellen Vergütungssystem.
Abgesehen von den technischen Hindernissen, sehen wir in dieser Art der Telemedizin im Bereich der Palliative Care ein grosses Potential: bei der Koordination der Betreuung der Patient:innen im häuslichen Umfeld, insbesondere bei der Interaktion im regionalen Palliativnetz zwischen Patient:innen, Angehörigen, Spitex und Hausärztin, sowie dem Mobilen Palliativdienst und den stationären Strukturen.
Datentransfer/remote Monitoring
Der Transfer von Daten über den Gesundheitszustand inklusive Daten über die aktuelle Lebensqualität (z.B. PROM’S) an Fachpersonen, entweder durch einen aktiven Prozess (Smartphone-Applikation/Internet basiert) oder passiv mit automatischer Informationsübermittlung («Wearables») wird seit einigen Jahren auch in der Palliative Care insbesondere bei Tumorpatienten untersucht (2, 10). Der Fokus liegt dabei auf den Symptomen oder der Sicherheit (Bewegungsmuster) mit den Zielen Reduktion von Unsicherheiten, Verbesserung des Selbst-Managements und Datengrundlagen für die Entscheidungsfindung (10).
Obwohl die Studien vielversprechend sind, müssen diese Technologien ihre Nützlichkeit und Akzeptanz in der Praxis noch beweisen (1).
Als Hindernis sehen wir hier drei Hauptpunkte. Die Machbarkeit steht zur Diskussion: Digitale PROMS benötigen eine relativ komplexe Mitarbeit des Patienten/Angehörigen. Ob diese möglich und gewünscht ist, insbesondere bei den vielen vulnerablen Menschen in der Palliative Care mit ausgeprägter Fatigue, muss noch bewiesen werden. Daneben geht es um die Akzeptanz einer standardmässigen Übermittlung von Gesundheitsdaten, sei es aktiv oder passiv. Und drittens, wie schon erwähnt, geht es auch hier um die fehlende technische Standardisierung. Diese Technologie macht nur Sinn, wenn die Fachpersonen einfach und schnell auf besorgniserregende Daten reagieren können. Grundlage hierfür wären ein einfacher und sicherer Zugang zu den Individualdaten und die notwendigen technischen und personellen Ressourcen für das Monitoring und die zeitgerechte Evaluation und Reaktion.
Andere digitale Hilfsmittel
Während der Pandemie standen und stehen digitale Kommunikationstools im gesellschaftlichen Fokus. Es ging und geht darum, schnell und pragmatisch eine Kommunikationsmöglichkeit für die Bevölkerung von der Schule bis zur Altersbetreuung herzustellen. Dies betrifft auch das Gesundheitswesen. Pilot-Projekte wurden ausgebaut, viele Spitäler planten und implementierten neue Telemedizinprogramme.
Zukunftsträchtige digitale Tools für die Palliative Care wurden kürzlich durch einen Delphiprozess definiert (1).
Grosses Interesse besteht aktuell für «virtual reality». Bei dieser Intervention wird der Patient durch eine Fachperson (meist eine Psychologin) auf einer virtuellen Reise mittels einer VR-Brille begleitet. Dies erlaubt es der betroffenen Person, zumindest kurzzeitig, der oft schwer erträglichen Realität zu entfliehen. Eine schweizerische Pilot-Studie von Seiler et al. zeigte kürzlich eine gute Akzeptanz und sehr vielversprechende Resultate bezüglich Symptom-Reduktion (11).
Künstliche Intelligenz, insbesondere im Zusammenhang mit grossen Datensätzen (Big Data) und Smart Home wird erforscht, hat aber noch keinen klinischen Stellenwert.
Big Data und Datamonitoring könnte allenfalls eine gewisse Hilfestellung bei der Prognosefindung und beim Monitoring von Risikofaktoren in der Prävention von schwierigen Symptomen wie einem Delirium bieten; aktuell steht hier immer noch die klinische Einschätzung im Vordergrund (1).
Die Frage nach dem digitalen Erbe ist mit dem rasanten Anstieg von Cloud-Diensten, sozialen Medien und anderen, physisch nicht greifbaren Dokumentationsarten sehr reell geworden. Das Bewusstsein für diesen in der heutigen digitalen Zeit notwendigen Schritt der Vorausplanung ist bei den Patient:innen und Fachpersonen noch wenig vorhanden (12). Die persönliche und gesellschaftliche Frage, was mit personenbezogenen Daten nach dem Tod passiert, wird sicherlich immer wichtiger.
Copyright bei Aerzteverlag medinfo AG
Universitäres Zentrum für Palliative Care
Inselspital Bern
Freiburgstrasse
3010 Bern, Schweiz
HFR Tafers
Abteilung Innere Medizin
1712 Tafers
andreas.ebneter@h-fr.ch
Chefarzt
Universitäres Zentrum für Palliative Care
Inselspital Bern, SWAN Haus
Freiburgstrasse 38
3010 Bern
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Beitrag deklariert.
1. 1Nwosu AC, McGlinchey T, Sanders J, Stanley S, Palfrey J, Lubbers P, et al. Identification of Digital Health Priorities for Palliative Care Research: Modified Delphi Study. JMIR Aging. 2022;5(1):e32075.
2. Amann M, Blum D. Digitale Palliative Care. Praxis. 2021;110(15):851-4.
3. WHO. WHO | Classification of digital health interventions v1.0 [Available from: http://www.who.int/reproductivehealth/publications/mhealth/classification-digital-health-interventions/en/.
4. Ebneter AS, Fliedner M, Trapp D, Ramseier F, Sauter TC, Eychmüller S. [Telemedicine in Palliative Care: Digital Communication in a Relationship-Based Speciality – Does It Make Sense?]. Praxis (Bern 1994). 2021;110(15):845-50.
5. Ferrell BR, Temel JS, Temin S, Alesi ER, Balboni TA, Basch EM, et al. Integration of Palliative Care Into Standard Oncology Care: American Society of Clinical Oncology Clinical Practice Guideline Update. Journal of Clinical Oncology. 2017;35(1):96-112.
6. Finucane AM, O’Donnell H, Lugton J, Gibson-Watt T, Swenson C, Pagliari C. Digital health interventions in palliative care: a systematic meta-review. NPJ Digit Med. 2021;4(1):64.
7. Ebneter AS, Sauter TC, Christen A, Eychmueller S. Feasibility, acceptability and needs in telemedicine for palliative care. Swiss Med Wkly. 2022;152(9-10).
8. Ebneter AS, Eychmueller S, Sauter TC, A. A. Einsatz von Telemedizin in der Palliative Care. SAEZ. 2022.
9. Tang M, Reddy A. Telemedicine and Its Past, Present, and Future Roles in Providing Palliative Care to Advanced Cancer Patients. Cancers (Basel). 2022;14(8).
10. Ansari N, Wilson CM, Heneghan MB, Supiano K, Mooney K. How technology can improve communication and health outcomes in patients with advanced cancer: an integrative review. Support Care Cancer. 2022.
11. Seiler A, Schettle M, Amann M, Gaertner S, Wicki S, Christ SM, et al. Virtual Reality Therapy in Palliative Care: A Case Series. Journal of palliative care.0(0):08258597221086767.
12. Coop H, Marlow C. Do we prepare patients for their digital legacy? A survey of palliative care professionals. Palliative Medicine. 2019;33(1):114-5.