Die beiden häufigsten chronisch rezidivierenden vaginalen Infektionen sind die bakterielle Vaginose (BV) und die chronisch rezidivierende Vulvovaginalcandidose (VVC). Diese Erkrankungen verursachen bei vielen Frauen hohen Leidensdruck und Therapiebedarf. Eingesetzt werden bei der VVC lokal oder systemisch angewandte Antimykotika und bei der BV eine lokale Erhaltungstherapie mit Antibiotika. Obgleich Studien zu Impfungen bei VVC oder die Einnahme eines neuen Biotherapeutikums (lebende Lactobacillus-Stämme) Hoffnung auf therapeutische Möglichkeiten geben, sind neue, erfolgsversprechende Medikamente oder Therapiemöglichkeiten leider noch nicht auf dem Markt zugelassen.
The two most common chronic recurrent vaginal infections are bacterial vaginosis (BV) and chronic recurrent vulvovaginal candidosis (RVVC). These diseases cause high suffering and need for therapy in many women. Antifungal agents applied locally or systemically are used for the VVC, and local maintenance therapy with antibiotics is used for BV. Although studies on vaccination in VVC or the use of a new biotherapeutic (live Lactobacillus strains) give hope for therapeutic possibilities, new promising drugs or therapeutic options are unfortunately not yet approved on the market.
Key Words: Chronic recurrent vaginal infections, bacterial vaginosis, recurrent vulvovaginal candidosis
Eine Vaginitis ist eine Entzündung der Vaginalschleimhaut entweder infektionsbedingt oder nicht-infektionsbedingt, gelegentlich ist auch die Vulva mitbeteiligt.
Vaginale Entzündungen mit den Symptomen Juckreiz, vaginales Brennen und veränderter Ausfluss gehören zu den häufigsten Gründen, warum Frauen sich in der gynäkologischen Praxis vorstellen.
Es kann sich hierbei um ein akutes und einmaliges Ereignis oder um ein rezidivierendes oder auch chronisch rezidivierendes Krankheitsbild handeln.
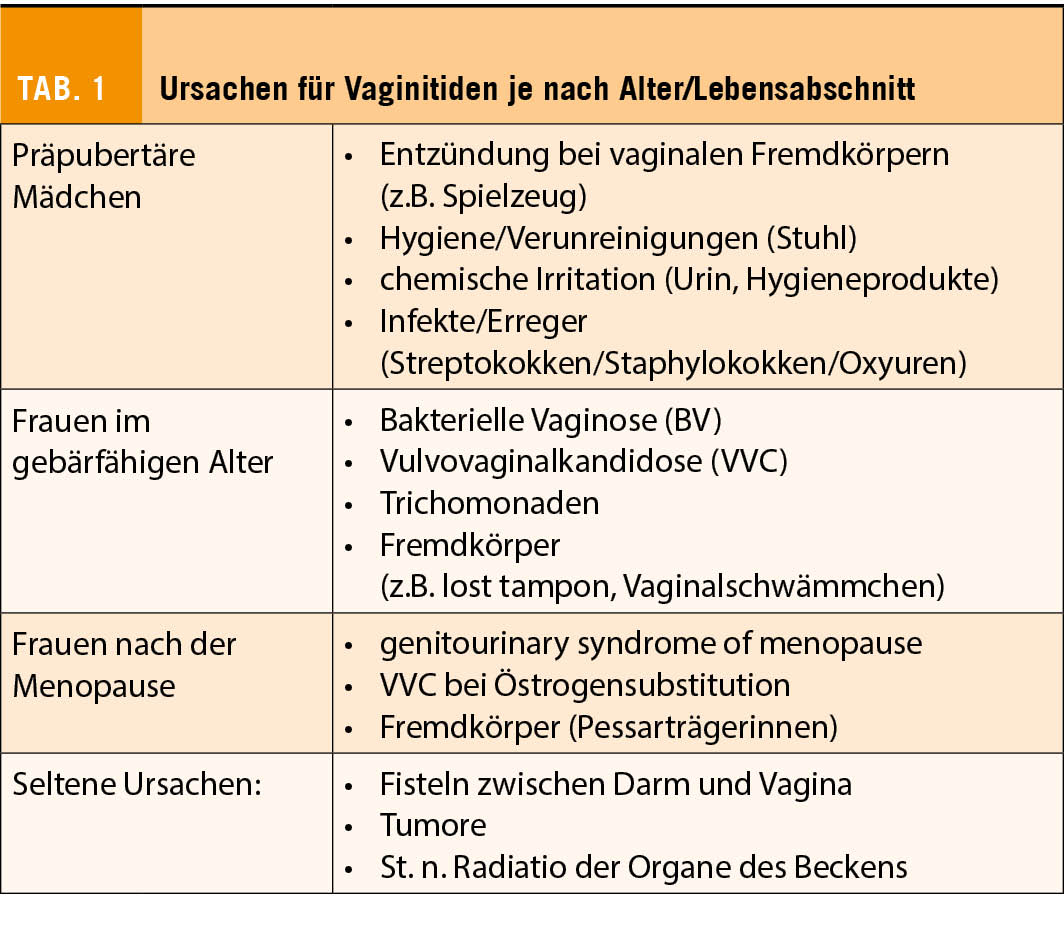
Je nach Alter und Lebensabschnitt kommen verschiedene Formen der Vaginitiden vor. Tabelle 1 zeigt die häufigsten Krankheitsbilder, unabhängig vom akuten oder chronischen Verlauf.
Im Folgenden wird hier nur auf die vaginalen Infektionen eingegangen, insbesondere auf die zwei häufigsten, die BV und die VVC und deren chronisch rezidivierende Krankheitsverläufe.
Die bakterielle Vaginose (BV)
Per definitionem ist die BV eine vaginale Dysbiose, gekennzeichnet durch das Überwachsen der normalen Vaginalflora mit opportunen Bakterien. Entgegen der Erwartung zeichnet sich die Vaginalflora der Dysbiose durch eine hohe Diversität und das Vorhandensein von fakultativ anaeroben Bakterien, wie z.B. Gadnerella vaginalis, Prevotella species, Bacteroides species und vielen mehr aus.
Ausserdem kommt es zu einer relativen Abnahme der physiologisch vorkommenden Vaginalbakterien, d.h. der Lactobazillen.
Die Rolle des Biofilms
Die gesunde Vaginalflora zeichnet sich unter anderem durch eine die Vaginalschleimhaut bedeckende Bakterienschicht aus. Diese Bakterien (aus der Gruppe der Lactobacillen) bilden eine Vielzahl von antimikrobiell wirkenden Proteinen und Enzymen wie z.B. Wasserstoffperoxid und Milchsäure, welche helfen, die natürliche Barrierefunktion der Vagina aufrecht zu halten.
Wenn diese Vaginalflora gestört wird und es zur sogenannten Dysbiose kommt, entsteht ein verändertes «neues» Mikrobiom. Synergistische Faktoren verschiedener pathogener Bakterienstämme begünstigen die Degradierung der normalen, schützenden Bakterienschicht und bewirken ein besseres Anhaften von weiteren pathogenen Bakterien am Vaginalepithel.
Es entsteht in der Folge ein neuer, für die BV typischer Biofilm.
Das Vorhandensein des Biofilms scheint auch Konsequenzen für die Therapie zu haben, so ist beim Vorliegen des Biofilms die Behandlung der BV erschwert und die Rezidivrate erhöht.
Eine Studie von Swidinski et al konnte zeigen, dass der pathologische Biofilm nicht nur in der Vagina vorliegt, sondern auch bis in das Endometrium des Uterus vordringt (1).
Die Äthiologie der BV ist nicht vollständig geklärt, obwohl seit über 60 Jahre aktiv daran geforscht wird.
Symptome/Klinik
50-75% der Frauen mit einer BV sind asymptomatisch.
Die Symptome der bakteriellen Vaginose sind im akuten Ereignis die gleichen wie im chronisch rezidivierenden Setting:
- Vermehrter dünnflüssiger Ausfluss
- Fischiger Geruch des Ausflusses
- Vaginale Irritation und Brennen (selten bei alleiniger BV)
Prävalenz der BV
Bei Frauen im reproduktiven Alter liegt die Prävalenz bei ca. 23-29% (siehe uptodate), weltweit bestehen aber grosse Unterschiede. Die Prävalenz variiert zwischen ca. 20-60 %, die höchste Prävalenz mit 58,3% besteht in Afrika (Subsahara), die niedrigste Prävalenz in Australien (4-8%) (2).
Begünstigende Faktoren für die Entwicklung einer BV
Es gibt eine Vielzahl von Faktoren, welche mit dem Auftreten einer bakteriellen Vaginose in Zusammenhang gebracht werden, z.B. sexuelle Aktivität, mehrere Sexualpartner, frühe Kohabitarche, Häufigkeit von vaginal-penetrativem Geschlechtsverkehr und WSW (women having sex with women). Diese Faktoren erhöhen das Risiko eine BV zu entwickeln. Die BV gilt nicht als STD aber ist mit sexueller Aktivität assoziiert (2).
Diagnose
Diese wird entweder über die klinischen Amsel-Kriterien (Tab. 2) oder das mikrobiologische Gram-Präparat mittels Nugent-Score gestellt. Der Nugent Score wird durch Charakterisierung der verschiedenen Bakterienarten (grampositive Lactobazillen, gramnegative bzw. labile Stäbe, und gramlabile gebogene Stäbe), welche im Grampräparat beurteilt und ausgezählt werden, erhoben. Beim Vorliegen verschiedener Stämme werden unterschiedliche Punktwerte verteilt. Je höher der Punktwert, desto wahrscheinlicher ist das Vorliegen einer bakteriellen Vaginose. Diese Nachweismethode zur bakteriellen Vaginose gilt als Goldstandard, wird aber im klinischen Alltag selten durchgeführt, da sie sehr zeit- und kostenintensiv ist. Diese Nachweismethode findet hauptsächlich Anwendung in der Forschung.
Behandlung der BV
Sowohl eine systemische antibiotische Therapie (z.B. Metronidazol 500mg 2×1 Tbl pro Tag über 7 Tage oder Clindamycin 300mg 2×1 Tbl. Pro Tag für 7 Tage) steht zur Verfügung, als auch die lokale Anwendung eines Antiseptikums (z.B. Fluomizin vaginal 1×1 Tbl für 7 Tage). Die Behandlung der akuten BV ist in den meisten Fällen erfolgreich. In der Literatur ist eine 80-90% Heilungsrate nach einem Monat angegeben (3). Eine Partnertherapie bei asymptomatischen Partnern ist nicht empfohlen.
Rezidivierende BV
Nach erfolgreicher Behandlung der BV ist die Rate an rekurrierenden Infektionen hoch mit ca. 58% im ersten Jahr (4). Leider gibt es in der Literatur keine einheitliche Definition der rezidivierenden BV, was die korrekte Diagnosestellung schwierig gestaltet. Im klinischen Alltag gilt das mehrmalige Wiederauftreten einer BV nach Behandlung als Hinweis für das Vorliegen einer rezidivierenden BV. So geht man bei mindestens drei Episoden einer BV innerhalb von 12 Monaten vom Vorliegen einer chronisch rezidivierenden BV aus. Es ist nicht klar, ob es sich bei der chron. rez. BV um eine Reinfektion oder um ein Rezidiv der Primärinfektion handelt. Für beide Hypothesen gibt es Argumente.
Für eine Reinfektion sprechen die Resultate einer Studie, bei der gezeigt wurde, dass Frauen, welche nach einer durchgeführten Therapie für eine gewisse Zeit sexuell abstinent waren, weniger Rezidive hatten (5).
Für die Reaktivierung einer persistenten Infektion sprechen die Resultate einer anderen Studie, bei der es nach Partnerbehandlung nicht zu einer Senkung der Rate an Rezidiven kam (6). Weitere Gründe, warum es zu einer chron. rez. Erkrankung kommt, sind die Persistenz des Biofilms durch die pathogenen Bakterien und die fehlende Restitution der lactobazillenreichen Vaginalflora. Wahrscheinlich ist die Entstehung einer chron. rezidivierenden Erkrankung demnach multifaktoriell.
Implikationen auf die Gesundheit
Neben der grossen Belastung, welche eine chronisch rezidivierende bakterielle Vaginose für die Patientinnen, ihre Partner/innen und die behandelnden Ärzt/innen bedeutet, hat das Vorliegen dieser Erkrankung auch zusätzlich negative gesundheitliche Folgen. So steigt beispielsweise beim Vorliegen einer BV das Risiko, sich an einer anderen sexuell übertragbaren Krankheit wie HIV, Chlamydien, Trichomonaden, Gonokokken oder Herpes simplex zu infizieren (7). Bei HIV-positiven Frauen, welche gleichzeitig an einer BV leiden, steigt das Risiko der Transmission von HIV an männliche Partner; dies erklärt man sich über vermehrtes «viral shedding» beim gleichzeitigen Vorliegen einer HIV-Infektion und einer bakteriellen Vaginose (8). Bei Schwangeren mit chron. rezidivierenden Vaginosen steigen die geburtshilflichen Risiken, z.B. das Frühgeburtsrisiko, das Spätabort- und IUFT-Risiko, das Risiko eines vorzeitigen Blasensprungs und das Risiko eines Amnioninfektionssyndroms. Ausserdem steigen die Risiken einer genitalen Infektion nach Abort und in der Postpartumperiode (9). Nicht bei allen Risiken ist geklärt, ob es eine Assoziation oder tatsächlich ein Kausalzusammenhang ist.
Behandlung der chronisch rezidivierenden bakteriellen Vaginose
Die Behandlung der rezidivierenden BV besteht momentan aus einer länger andauernden topischen Applikation von Metronidazol im Sinne einer Suppressionstherapie (2x wöchentlich über 6 Monate). Als Alternative kann auch Clindamycin eingesetzt werden, welches aber im Vergleich zum Metronidazol die Lactobazillenflora stärker angreift und somit die Restaurierung der normalen Vaginalflora verzögert. Auch bei länger anhaltenden Suppressionstherapien zeigen sich nach Abschluss häufig Rezidive resp. Reinfektionen (10). Ausserhalb der Schweiz (z.B. in den USA) wird die lokale Applikation von borsäurehaltigen Vaginalzäpfchen ergänzend vorgeschlagen, diese sollen den Biofilm zerstören und somit die Wirkung des Antibiotikums auf die Eradikation der die BV begünstigenden Keime verbessern. Borsäurehaltige Produkte sind jedoch in der Schweiz nicht verfügbar und nicht zugelassen. Die hohe Rezidivrate nach einer Behandlung erfordert dringend die Erforschung von neuen therapeutischen Möglichkeiten. Ein erfolgsversprechendes Produkt ist das Biotherapeutikum Lactin-V (lebende Lactobacillus crispatum Stämme). In einer randomisierten, doppel-blinden, plazebo-kontrollierten Studie (Phase 2a Studie), welche im Mai 2020 im New England Journal of Medicine publiziert wurde, konnte gezeigt werden, dass die 12-wöchige lokale vaginale Anwendung von LactinV nach Behandlung mit Metronidazol die Rezidivrate der BV im Vergleich zu Plazebo signifikant reduziert, nach 12 Wochen hatten 30% in der Lactin-V Gruppe ein Rezidiv der BV versus 45% in der Placebo-Gruppe, nach 24 Wochen waren es 39% Rezidive in der Lactin-V Gruppe und 54% in der Placebo-Gruppe (11).
Die vulvovaginale Candidose (VVC)
Die VVC ist die zweithäufigste Ursache für eine Vaginitis nach der BV, ca. 75% aller Frauen leiden mindestens einmal im Leben an einer VVC.
Definition
Eine VVC liegt vor, wenn eine Entzündung der Vagina und der Vulva (gel. auch übergreifend auf die Perineal- und Perianalregion) besteht und gleichzeitig Candiaerreger (Hyphen oder Pseudohyphen) in der Nativ-Mikroskopie nachgewiesen werden können. Die Diagnose wird daher meist klinisch und mit Hilfe der Nativ-Mikroskopie gestellt. Wenn die Nativ-Mikroskopie nicht aufschlussreich ist, kann eine Pilzkultur abgenommen werden. Dies ist besonders wichtig im Falle der chronisch rezidivierenden Erkrankungen, da nur beim tatsächlichen Vorliegen einer Candidainfektion eine chronische Erhaltungstherapie indiziert ist. Zu differenzieren sind hierbei insbesondere andere Ursachen für (meist) vulvären Juckreiz wie z.B. das atopische Vulvaekzem, als Dermatose oder Kondylombefall.
Äthiologie
Die Erreger bei der VVC sind in den meisten Fällen Hefepilze der Spezies Candida albicans (85-95 % der Fälle bei akuter VVC). In besonderen Situationen z.B. Immunsuppression, Diabetes mellitus können auch seltenere Nicht-Albicans Arten wie z.B. Candida glabrata oder Candida krusei für die Erkrankung verantwortlich sein. Es ist bekannt, dass bei einigen Frauen eine asymptomatische Kolonisation der Vagina mit Candida ohne Entzündungszeichen vorliegt. Der Übergang von Kolonisation zu Entzündung ist abhängig von verschiedenen Faktoren, diskutiert werden hier die individuelle Immunlage, die Infektabwehr und Virulenzfaktoren der Hefepilze. Unter Virulenzfaktoren versteht man bestimmte Enzyme oder Proteine der Candia-Hefen, welche eine Inflammation im Vaginalgewebe der Frau hervorrufen können. Dies sind z.B. verschiedene Proteasen, Lipasen und das Candidalysin. Invasion der Candida-Pilzen in das Gewebe, hierfür muss sich der Pilz von der Hefeform in die Hyphenform umwandeln, dieser Schritt wird durch das Vorhandensein von Östrogen erleichtert.
Prädisponierende Faktoren
Bestimmte Bedingungen, Erkrankungen oder Lebensabschnitte gelten als prädisponierend für eine VVC. Darunter zählt man unter anderem den Diabetes mellitus. Die erhöhten Serumglukosewerte (besonders bei schlecht eigestelltem Diabetes) erleichtern die Adhäsion der Pilze am Vaginalepithel und verlangsamen gleichzeitig wichtige Mechanismen der Abwehr wie zum Beispiel die Migration von neutrophilen Granulozyten.
Andere Faktoren, welche die Entstehung einer VVC begünstigen sind z.B. die Durchführung einer antibiotischen Behandlung, verändertes vaginales Mikrobiom mit geringer Anzahl von Lactobacillen, hormonelle Faktoren wie Schwangerschaft, Einnahme von hormonellen Kontrazeptiva und Hormontherapie in der Menopause. Zusätzlich gibt es noch genetische Prädispositionen, welche eine VVC begünstigen wie z.B. atopische Diathese und angeborene Störungen des Immunsystems mit Immunsuppression. Nicht zuletzt werden Life-Style Faktoren diskutiert wie z.B. spezielle zuckerreiche Ernährung, psychosozialer Stress und sexuelle Praktiken. Hier ist die Evidenz jedoch gering (12).
Symptome
Das Hauptsymptom der VVC ist der Juckreiz und die vaginale Rötung mit Brennen. Oft besteht ein vermehrter und krümmelig-weisslicher Ausfluss. Zusätzlich geben Patientinnen das Gefühl von Wundsein an und leiden häufig an Dyspareunie und Dysurie.
Behandlung der chronischen VVC
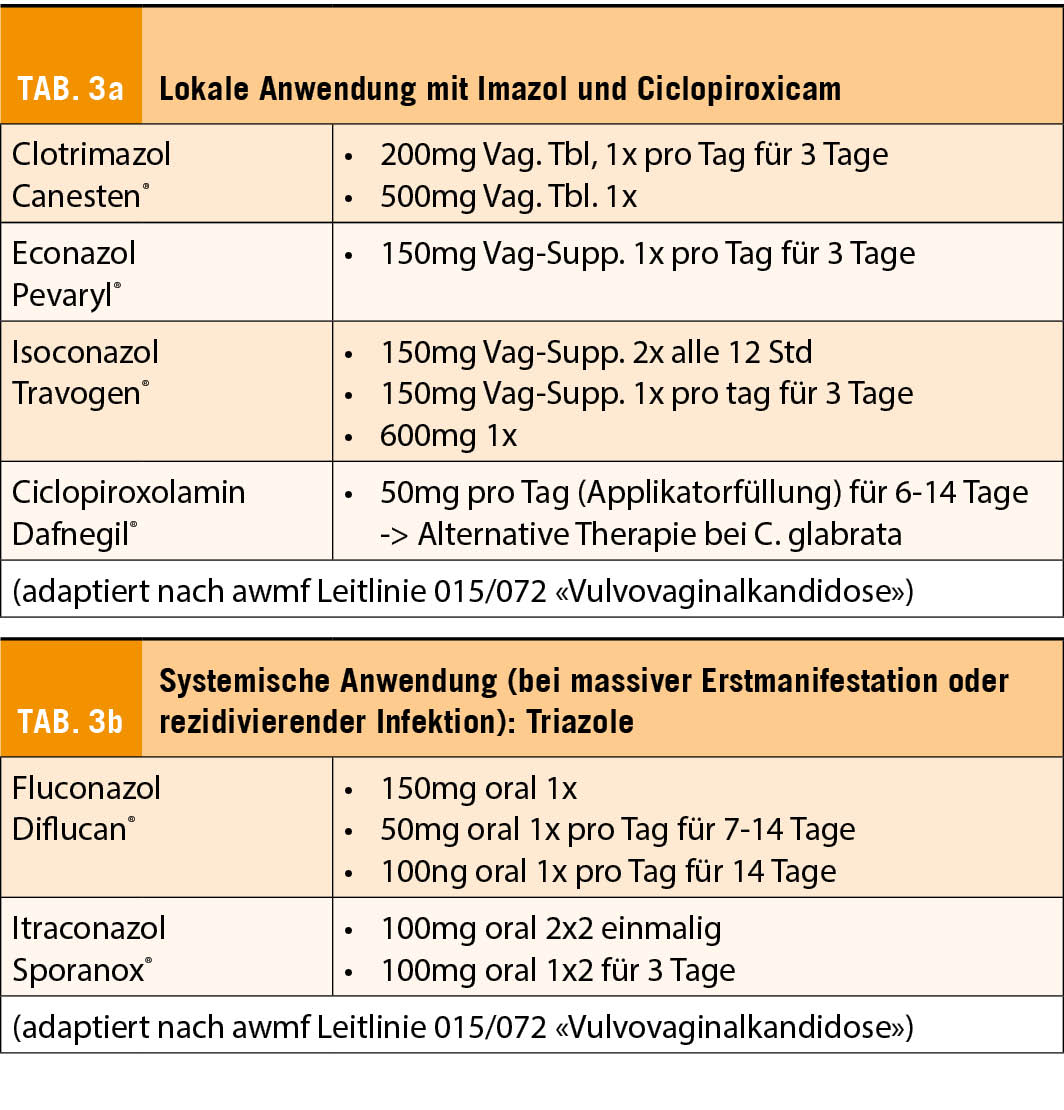
Diese besteht immer aus einem Antimykotikum. Diese können sein: Imazolderivate für die topische Anwendung, Triazole für die systemische Applikation, ausserdem noch alternative Antimykotika wie Nystatin (Polyen) und Ciclopiroxicam. Ähnlich wie bei der bakteriellen Vaginose ist die Behandlung eines symptomlosen Sexualpartners nicht empfohlen. Die verschiedenen Präparate mit den entsprechenden Dosierungen sind in den Tabellen 3a und 3b aufgeführt.
Medikamentöse Therapie der VVC
Chronisch rezidivierende VVC
Wenn es nach der Behandlung einer VVC zu einem Rezidiv kommt und Frauen mindestens 4 Krankheits-Episoden innerhalb eines Jahres erleiden, besteht eine chronisch rezidivierende VVC. Die Behandlung der chron. rezidivierenden VVC ist eine Erhaltungs- bzw. Suppressionstherapie und es kommen die gleichen (meist oralen) Antimykotika zum Einsatz wie bei der akuten Erkrankung. Im klinischen Alltag existieren verschiedene Schemata, insgesamt gibt es wenig Evidenz, welches Schema am besten ist. Aber allgemein gilt, dass ungefähr ein Jahr lang deeskalierend, in der Regel mit einem azolhaltigen Antimykotikum behandelt werden sollte.
Zu den off-label Alternativen bei der Behandlung der VVC gehören borsäurehaltige Rezepturen und jodhaltige Desinfektiva, sowie Propolis (Bienenprodukt, harzartiger Masse mit antimykotischer Wirkung) und die Heilpflanze Salvia officinalis. Allen Präparaten ist gemeinsam, dass es keine wissenschaftliche Evidenz zur Wirksamkeit gibt.
Neue Therapieansätze, insbesondere immunologische Therapie werden untersucht. Leider ist bislang jedoch noch kein neues Präparat zur Behandlung der chron. rez. VVC zugelassen.
Erwähnenswert ist der Ansatz der Hyposensibilisierung gegen ein Candida abicans-Antigen und die Idee der Impfung. Im Tierversuch und bei ersten Studien an Menschen konnte nach Impfung die Bildung von Antikörpern nachgewiesen werden. In einer klinischen Studie konnte gezeigt werden, dass die Impfung mit einem rekombinant hergestellten Impfstoff, welcher aus einem spezifischen Candida-Protein und einem aluminiumhaltigen Adjuvans besteht, sicher, immunogen und therapeutisch wirksam ist. Es kam zu einer Reduzierung von symptomatischen VVC Episoden innerhalb von 12 Monaten (13).
Copyright bei Aerzteverlag medinfo AG
Stadtspital Waid und Triemli
Frauenklinik
Birmensdorferstrasse 497
8063 Zürich
nina.manz@triemli.zuerich.ch
Es besteht kein Interessenkonflikt in Verbindung mit dem vorgelegten Artikel.
1. Swidsinski A, Verstraelen H, Loening-Baucke V, Swidsinski S, Mendling W,
Halwani Z. Presence of a polymicrobial endometrial biofilm in patients with bacterial vaginosis. PLoS One. 2013;8(1):e53997. doi: 10.1371/journal.pone.0053997. Epub 2013 Jan 8. PMID: 23320114; PMCID: PMC3540019.)
2. Coudray MS, Madhivanan P. Bacterial vaginosis-A brief synopsis of the literature. Eur J Obstet Gynecol Reprod Biol. 2020 Feb;245:143-148. doi: 10.1016/j.ejogrb.2019.12.035. Epub 2019 Dec 24. PMID: 31901667; PMCID: PMC6989391.
3. Joesoef MR, Schmid GP. Bacterial vaginosis: review of treatment options and
potential clinical indications for therapy. Clin Infect Dis. 1995 Apr;20 Suppl 1:S72-9. doi: 10.1093/clinids/20.supplement_1.s72. PMID: 7795111.
4. Bradshaw CS, Morton AN, Hocking J, Garland SM, Morris MB, Moss LM, Horvath LB, Kuzevska I, Fairley CK. High recurrence rates of bacterial vaginosis over the course of 12 months after oral metronidazole therapy and factors associated with recurrence. J Infect Dis. 2006 Jun 1;193(11):1478-86. doi: 10.1086/503780. Epub 2006 Apr 26. PMID: 16652274
5. Chen JY, Tian H, Beigi RH. Treatment considerations for bacterial vaginosis and the risk of recurrence. J Womens Health (Larchmt). 2009 Dec;18(12):1997-2004. doi: 10.1089/jwh.2008.1088. PMID: 20044862.
6. Wilson J. Managing recurrent bacterial vaginosis. Sex Transm Infect. 2004 Feb;80(1):8-11. doi: 10.1136/sti.2002.002733. PMID: 14755028; PMCID: PMC1758381
7. Gallo MF, Macaluso M, Warner L, Fleenor ME, Hook EW 3rd, Brill I, Weaver MA. Bacterial vaginosis, gonorrhea, and chlamydial infection among women
attending a sexually transmitted disease clinic: a longitudinal analysis of
possible causal links. Ann Epidemiol. 2012 Mar;22(3):213-20. doi: 10.1016/j.
annepidem.2011.11.005. Epub 2011 Dec 20. PMID: 22192490.
8. Bradshaw CS, Brotman RM. Making inroads into improving treatment of bacterial vaginosis – striving for long-term cure. BMC Infect Dis. 2015 Jul 29;15:292. doi: 10.1186/s12879-015-1027-4. PMID: 26219949; PMCID: PMC4518586.
9. Abou Chacra L, Fenollar F, Diop K. Bacterial Vaginosis: What Do We Currently Know? Front Cell Infect Microbiol. 2022 Jan 18;11:672429. doi: 10.3389/fcimb.2021.672429. PMID: 35118003; PMCID: PMC8805710.
10. Surapaneni S, Akins R, Sobel JD. Recurrent Bacterial Vaginosis: An Unmet
Therapeutic Challenge. Experience With a Combination Pharmacotherapy Long-Term Suppressive Regimen. Sex Transm Dis. 2021 Oct 1;48(10):761-765. doi: 10.1097/OLQ.0000000000001420. PMID: 34110746; PMCID: PMC8460079.
11. Cohen CR, Wierzbicki MR, French AL, Morris S, Newmann S, Reno H, Green L, Miller S, Powell J, Parks T, Hemmerling A. Randomized Trial of Lactin-V to Prevent Recurrence of Bacterial Vaginosis. N Engl J Med. 2020 May 14;382(20):1906-1915. doi: 10.1056/NEJMoa1915254. PMID: 32402161;
PMCID: PMC7362958.
12. Gonçalves B, Ferreira C, Alves CT, Henriques M, Azeredo J, Silva S. Vulvovaginal candidiasis: Epidemiology, microbiology and risk factors. Crit Rev Microbiol. 2016 Nov;42(6):905-27. doi: 10.3109/1040841X.2015.1091805. Epub 2015 Dec 21. PMID: 26690853.
13. Edwards JE Jr, Schwartz MM, Schmidt CS, Sobel JD, Nyirjesy P, Schodel F,
Marchus E, Lizakowski M, DeMontigny EA, Hoeg J, Holmberg T, Cooke MT, Hoover K, Edwards L, Jacobs M, Sussman S, Augenbraun M, Drusano M,
Yeaman MR, Ibrahim AS, Filler SG, Hennessey JP Jr. A Fungal Immunotherapeutic Vaccine (NDV-3A) for Treatment of Recurrent Vulvovaginal Candidiasis-A Phase 2 Randomized, Double-Blind, Placebo-Controlled Trial. Clin Infect Dis. 2018 Jun 1;66(12):1928-1936. doi: 10.1093/cid/ciy185. PMID: 29697768;
PMCID: PMC5982716.