Lors de l’Update Refresher à Lausanne le 12.02.2021, les spécialistes du CHUV ont donné des conférences sur les maladies de la thyroïde, les maladies de l’hypophyse et des glandes surrénales, ainsi que sur le diagnostic et le traitement des complications diabétiques. Ce rapport résume l’exposé sur les progrès, défis et options de traitement du diabète de type 2.
Les patients atteints de diabète sont plus exposés aux complications macrovasculaires et microvasculaires. La prévalence des maladies coronariennes est de 14 à 21 %, celle de l’ insuffisance cardiaque de 19 à 26 %, celle de la maladie artérielle périphérique de 16 à 29 % et celle des accidents vasculaires cérébraux de 8 à 12 %. Parmi les maladies microvasculaires, la prévalence de la rétinopathie est de 34 %, celle de la neuropathie cardiaque autonome de 31 à 73 % et celle de la néphropathie de 29 à 61 %, a indiqué la Pre Anne Wojtusciszyn, Service d’ endocrinologie, diabétologie et métabolisme du CHUV.
« Optimisez le time in range chez les patients avec diabète de type 2 (DT2) pour minimiser les complications microvasculaires ! », a-t-elle proposé. Avec moins de 51 % de time in range, la prévalence de la rétinopathie diabétique altérant la vision est de 9,7% ; avec un time in range de plus de 86 %, elle est à 3,5 %.
Complications et diabète – les défis
La morbidité/mortalité cardiovasculaire a baissé chez le DT2 depuis 1998/1999 – 2012/2013. Elle reste pourtant supérieure à celle d’ un patient témoin non diabétique. MACE prend principalement en compte les décès d’ origine cardiovasculaire, les accidents vasculaires cérébraux et les infarctus du myocarde. Cependant, les deux complications prédominantes chez les patients diabétiques semblent être l’ artériopathie périphérique et l’ insuffisance cardiaque, a expliqué l’ oratrice.
Diabète type 2 et NAFLD/NASH
On estime à 18,2 millions le nombre de personnes vivant avec le DT2 et la stéatose hépatique non alcoolique (NAFLD) aux États-Unis, dont 6,4 millions souffrent de stéatohépatite non alcoolique (NASH). Le coût sur vingt ans de la NAFLD chez ces patients s’ est élevé à 55,8 milliards de dollars. Au cours des 20 prochaines années, la NASH dans le DT2 sera responsable de 65 000 transplantations, de 1,37 millions de décès liés à la maladie CV et 812 000 décès liés au foie, a indiqué l’ oratrice.
Diabète type 2 et COVID-19
Le risque global de décès ou de traitement par COVID-19 en unité de soins intensifs est sensiblement plus élevé chez les personnes atteintes de DT2 que dans la population générale. Le risque de décès par COVID-19 ou par traitement en soins intensifs, et donc la nécessité de mesures de protection spéciales, varie considérablement d’ un patient diabétique à l’ autre, mais peut être raisonnablement prédit en utilisant l’ histoire clinique. (McGurnaghan SJ et al. Lancet Diabetes Endocrinol. 2021;9:82-93.)
Les progrès
De nouveaux sous-groupes de DT2 chez l’ adulte
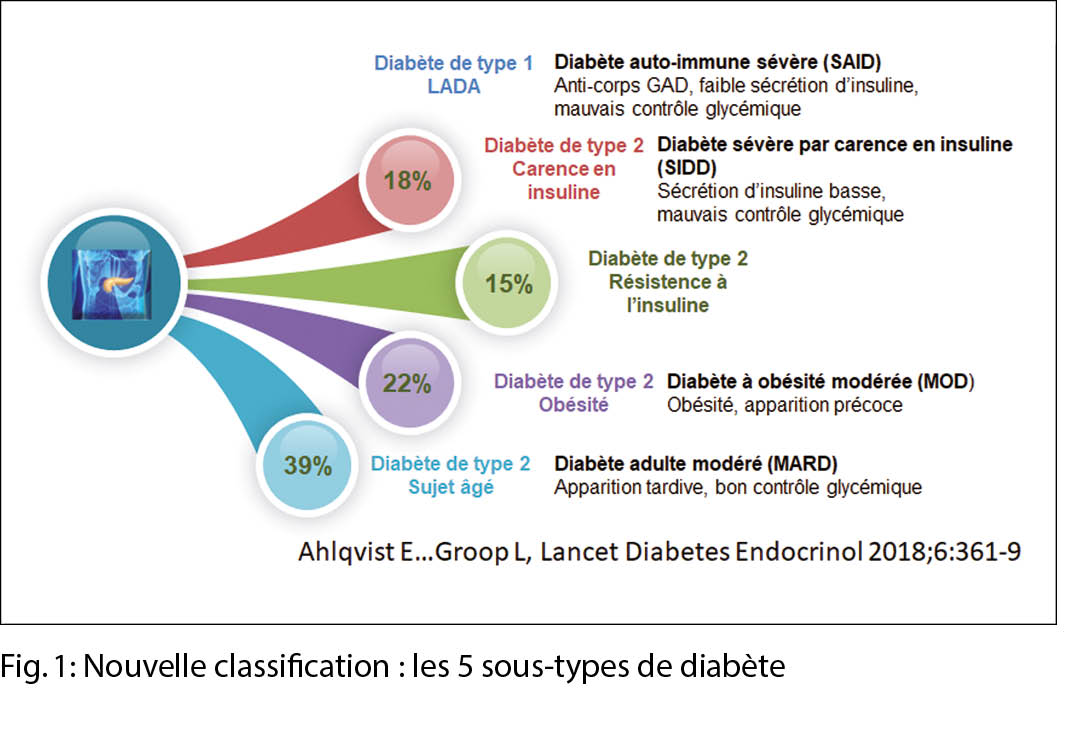
Le diabète est actuellement classé en deux formes principales, le DT1 et le DT2, ce dernier en particulier étant très hétérogène. Une classification affinée pourrait fournir un outil puissant pour individualiser les schémas de traitement et identifier les individus présentant un risque accru de complications au moment du diagnostic (Ahlqvist E et al Lancet Diabetes and Endocrinology 2018; 6:361-369). Les auteurs ont identifié cinq groupes reproductibles de patients diabétiques qui présentaient des caractéristiques et des risques de complications diabétiques très différents (fig. 1). En particulier, les individus du groupe 3 (le plus résistant à l’ insuline) présentaient un risque significativement plus élevé de maladie rénale diabétique que les individus des groupes 4 et 5, mais ils avaient tous reçu un traitement similaire contre le diabète. Le groupe 2 (carence en insuline) présentait le plus grand risque de rétinopathie. Pour soutenir ce regroupement, les associations génétiques dans les groupes étaient différentes de celles observées dans le DT2 traditionnel. Cette nouvelle classification pourrait permettre d’ adapter le traitement précoce aux patients qui en bénéficieraient le plus, ce qui représente un premier pas vers une médecine de précision dans le domaine du diabète.
Effet des GLP-1 RA sur les complications macrovasculaires
Les GLP-1 RA ont montré un bénéfice significatif sur l’ infarctus du myocarde et l’ accident vasculaire cérébral et la mortalité cardiovasculaire dans l’ étude LEADER (liraglutide) et dans l’ étude HARMONY (albiglutide). Dans l’ étude SUSTAIN 6 le taux de mortalité cardiovasculaire, d’ infarctus du myocarde non mortel ou d’ accident vasculaire cérébral non mortel était significativement plus faible chez les patients recevant le GLP-1 RA sémaglutide que chez ceux recevant un placebo. Dans l’ étude REWIND, le dulaglutide a réduit de manière significative le critère d’ évaluation combiné MACE-3 dans une population d’ étude dont la majorité des patients présentaient des facteurs de risque cardiovasculaire mais aucune maladie cardiovasculaire manifeste.
Effet des inhibiteurs SGLT-2 sur l’ insuffisance cardiaque
L’ année 2020 est l’ année des inhibiteurs SGLT-2 comme thérapie dans l’ insuffisance cardiaque chez les patients non diabétiques. Les inhibiteurs SGLT-2 se sont révélés être efficaces pour prévenir l’ insuffisance cardiaque et le dysfonctionnement rénal, même chez les patients non diabétiques, comme le démontraient les études DAPA HF (dapagliflozine) et EMPA REG (empagliflozine), l’ étude DAPA CKD et l’ étude EMPEROR, respectivement. Dans ces essais, 50 % des patients n’ étaient pas diabétiques. La canagliflozine a également réduit le risque d’ insuffisance rénale et d’ événements cardiovasculaires chez les patients atteints de DT2 et de maladies rénales par rapport au placebo dans l’ étude CREDENCE, avec un suivi médian de 2,62 ans.
Les progrès en 2020
- Une pratique plus personnalisée, axée sur les besoins du patient.
- Metformine en première ligne.
- En association rapide les inhibiteurs SGLT-2 ou les GLP-1 RA sans regarder l’ HbA1c en fonction des facteurs de risque.
- Les inhibiteurs SGLT-2 font la démonstration de leur efficacité pour prévenir l’ insuffisance cardiaque et la dégradation de la fonction rénale, y compris chez les non-diabétiques.
- En troisième ligne les GLP-1 RA ou les SGLT-2 inhibiteurs – les nouvelles «stars» de nos ordonnances !
- Selon les nouvelles recommandations suisses, 3 questions doivent être posées en premier lieu : 1) Déficience en insuline ? 2)
- Traitement ou prévention de l’ insuffisance cardiaque ? 3) Fonction rénale (eGFR) ?
Les principales recommandations pour les médecins généralistes sont les suivantes : Motivation pour un changement de mode de vie, traitement multifactoriel : l’ hypertension, les lipides, le sevrage tabagique et le diabète.
Les options (nouveautés pharmacologiques)
L’ insuline
Insuline hebdomadaire (insuline Icodec) pour le DT2 sans traitement préalable à l’ insuline. Ce traitement a eu une efficacité hypoglycémiante et un profil de sécurité similaire à celui de l’ insuline glargine U100 à prise unique quotidienne chez les patients atteints DT2 (Rosenstock J et al. N Engl J Med. 2020;383:2107-2116).
Le tirzepatide
Dans le traitement du DT2, le tirzepatide est un agoniste du double récepteur GIP-GLP-1 qui est un peptide synthétique basé sur la séquence GIP native (GIP = peptide insulinotrope glucose-dépendant). Il est administré une fois par semaine en raison de sa demi-vie de 5 jours. Dans les études PROGRESS de phase 1 et de phase 2, le tirzepatide a démontré une réduction de l’ HbA1c proportionnelle à la dose jusqu’ à 2,4% et une réduction du poids corporel jusqu’ à 11,3 kg chez les patients atteints DT2. L’ efficacité clinique du tirzepatide est supérieure à celle du GLP-1 RA dulaglutide.
Le système de surveillance du glucose en continu (CGMS)
L’ utilisation du CGMS (continuous glucose monitoring system) continue à devenir de plus en plus courant dans la pratique clinique. En tant que composante de l’ autogestion du diabète, son utilisation quotidienne permet d’ obtenir un retour d’ information immédiat sur les taux de glycémie actuels ainsi que sur la direction et les changements des taux de glycémie. Ces informations permettent aux personnes diabétiques d’ optimiser leur consommation alimentaire et leur activité physique, de prendre des décisions de traitement éclairées concernant les repas et la correction du dosage d’ insuline et, surtout, de réagir immédiatement et de manière appropriée pour atténuer ou prévenir les événements glycémiques aigus.
Le CGMS et le DT2 – publications au congrès de l’ American Diabetes Association (ADA)
E. Miller : 84-LB – ADA 2020 : évaluation des niveaux d’ HbA1c avant, à 6 et 12 mois après le régime libre dans le DT2 sous insuline ou NON dans 3 ensembles de données croisées (FSL/Quest/DRG).
E. Wright : 78-LB – ADA 2020 : évaluation du taux d’ HbA1c après un régime libre dans les cas de DT2 ne se situant pas dans la fourchette cible (HbA1c > 8 %) d’ après une autre base de données IBM explorée (n = 1034). La valeur de l’ HbA1c était de 10,11 % avant la prescription d’ un régime libre, 8,63% après la prescription. Avec insuline 10,13 % avant et 8,98 % après, sans insuline 10,11 % avant et 8,49 % après. L’ effet était encore meilleur sans insuline.
CGMS et santé publique
E. Miller 85-LB-ADA 2929 : Evaluer s’ il existe un registre continu des complications liées au diabète (hypo/hyper, DKA, HPA ou coma) et des hospitalisations dans le DT2 sans insuline rapide. Evénements de diabète aigu avant vs. après : HR 0,70 (0,57-0,85), p < 0,001. Le total des hospitalisationsv : avant vs. après HR 0,87 (0,78-0,98) p = 0,025.
R. Bergenstal 69-OR-ADA2020. Evaluer s’ il existe un registre continu des complications liées au diabète (hypo/hyper, DKA, HPA ou coma) et des hospitalisations dans le DT2 sous insuline rapide. (« Ancien » diabète avec comorbidités) (n = 2463). Evénements de diabète aigu avant vs. après HR 0,40 (0,31-0,51), p<0,001. Le total des hospitalisations avant vs. après HR 0,67 (0,58-0,77), p < 0,001.
CGMS et patients âgés
L’ étude DIAMOND rapporte une amélioration de l’ HbA1c (100 patients 67 + /- 5 ans), et dans l’ étude WISDOM (203 patients en dessus de 60 ans, 30% >70 ans), le glucose self monitoring (SGM) a été testée vs le CGMS pendant 6 mois. Les résultats ont été une amélioration de l’ HbA1c, une réduction du temps d’ hypoglycémie, une hypoglycémie moins sévère et moins de fractures (p = 0.08) pour le CGMS.
Conclusion
- La prévention du diabète, le dépistage et l’ éducation des patients continuent à être au centre du traitement initial et de la prévention des complications. Cela est particulièrement vrai pour les personnes à risque dans le contexte de l’ épidémie de SRAS-CoV-2.
- Les GLP-1 RA oraux hebdomadaires confirment leur efficacité dans la prévention de la maladie cardiovasculaire athéromateuse.
- Les inhibiteurs SGLT-2 ont prouvé un effet préventif dans les maladies athéromateuses, l’ insuffisance rénale ainsi que l’ insuffisance cardiaque, ceci également chez les sujets non-diabétiques.
- L’ embuscade de l’ agoniste du double récepteur GIP-GLP-1 a montré un effet spectaculaire sur l’ HbA1c, le poids, et la NASH.
Plus que la pharmacologie, la technologie va également révolutionner le traitement des personnes atteintes de DT2.
Source : FOMF Update Refresher Médecine interne, Endocrinologie et diabète, Lausanne 12.02. 2021.
riesen@medinfo-verlag.ch