Die trainingsbasierte kardiovaskuläre Rehabilitation (KVR) stellt neben der Implementierung moderner interventioneller und medikamentöser Therapien eine wichtige Säule des Behandlungskonzeptes von Patienten mit kardiovaskulären Erkrankungen dar. Die COVID-19-Pandemie hat die Umsetzung rehabilitativer Massnahmen massgeblich erschwert. Der folgende Beitrag erläutert die Implementierung einer Telerehabilitation und mögliche Trainingskonzepte am Beispiel einer Umsetzung aus dem kardiovaskulären Präventionszentrum des Universitätsspitals Basel. (Solche Programme bestehen bereits, Fragen zur praktischen Umsetzung werden diskutiert).
Die trainingsbasierte kardiovaskuläre Rehabilitation (KVR) stellt neben der Implementierung moderner interventioneller und medikamentöser Therapien eine wichtige Säule des Behandlungskonzeptes von Patienten mit kardiovaskulären Erkrankungen dar (1), was in den Leitlinien durch den Evidenzgrad IA abgebildet ist (2). Hierbei werden durch physische, psychische, edukative und medikamentöse Verbesserungen sowie die positive Beeinflussung der bestehenden Risikofaktoren (Rauchstopp, Diabetes-, Dyslipidämie-, und Hypertonie-Behandlung (3)) eine Reduktion der Mortalität, Hospitalisationsrate (4) und psychischen Belastungen (5) erreicht.
Die COVID-19-Pandemie hat die Umsetzung rehabilitativer Massnahmen massgeblich erschwert, so dass diese teils nicht mehr oder nur in sehr eingeschränktem Umfang möglich sind. Die Einschränkungen ergeben sich durch die kantonalen Hygienemassnahmen, welche das erhöhte Infektions-Risiko von Patienten mit kardiovaskulären Erkrankungen (Infarkt, Herzoperation, Herzinsuffizienz) sowie fortgeschrittenem Alter (6) berücksichtigen. Dadurch sollen schwere Krankheitsverläufe auf ein Minimum reduziert werden.
Die Indikation für eine häuslich basierte KVR (HB-KVR) in sekundärpräventiver Absicht ist daher grösser denn je (7). Ein Verschub der rehabilitativen Massnahmen in eine «Corona-freie Zeit» ist keine Alternative, da der verzögerte Beginn einer KVR um eine Woche bereits einen um 4 Wochen verlängerten Trainingsaufwande verlangt, um die gleichen Benefits im Vergleich zu einem unmittelbaren Beginn zu erreichen (8). Das Ziel einer optimalen Behandlung von Herzpatienten ist daher bei gegebener Indikation der schnellstmögliche Start einer trainingsbasierten KVR unter gleichzeitigem Schutz vor Ansteckung. Die international wiederkehrenden Lockdowns im vergangenen Jahr waren ein Motor zur Etablierung von HB-KVR-Programmen (7), allerdings bestehen, trotz der erwiesenen Erkenntnis bzgl. der Vorteile einer HB-KVR (9), weiterhin Fragen bzgl. der praktischem Umsetzung einer Telerehabilitation.
Indikation und Ziele einer kardiovaskulären Rehabilitation
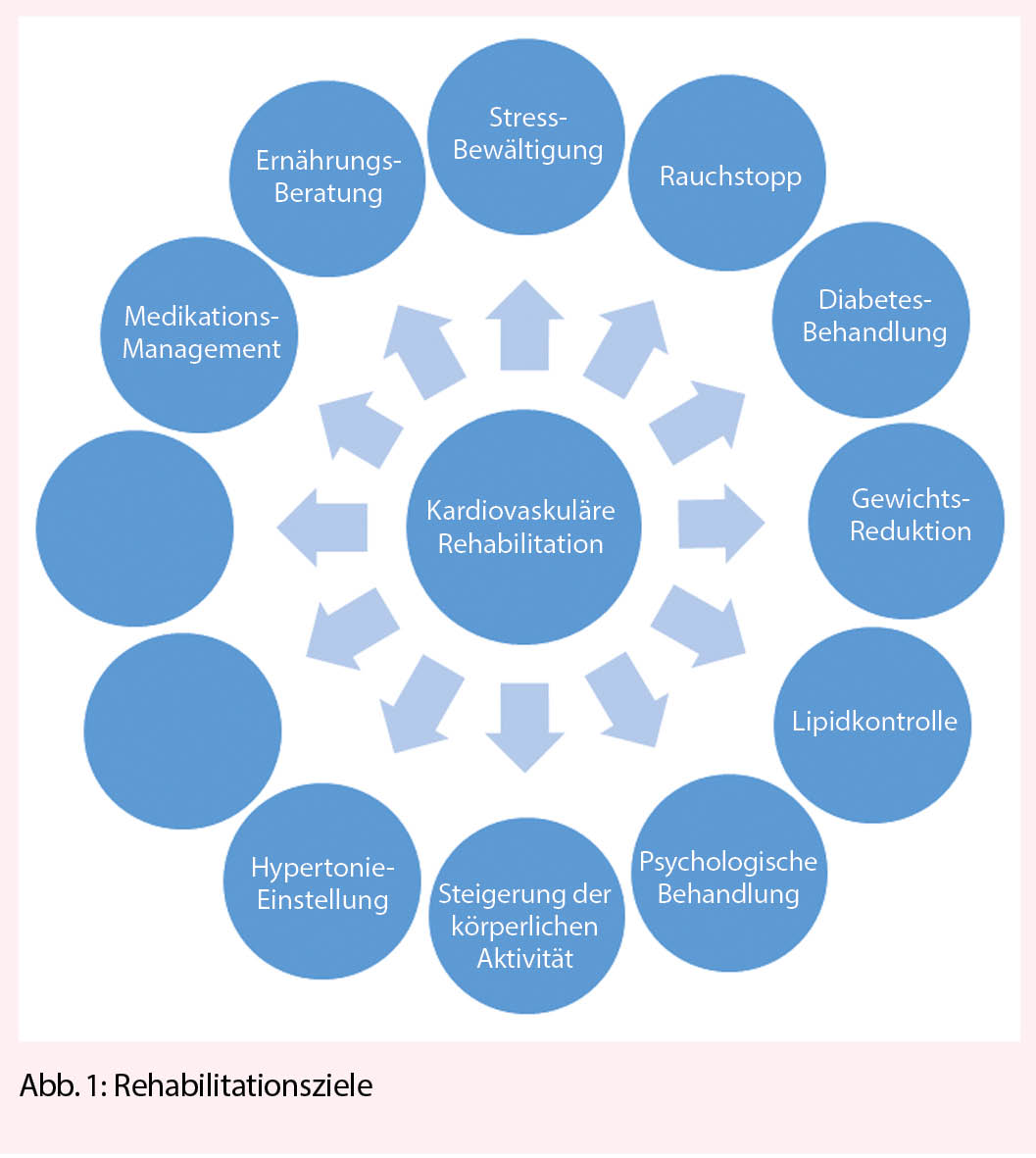
Die «Swiss Working Group for Cardiovascular Prevention, Rehabilitation and Sports Cardiology» (SCPRS) hat in einer online verfügbaren Empfehlung (10) die Indikationen zur KVR veröffentlicht. Hierzu zählen u.a. Patienten und Patientinnen mit St.n. nach Herzinfarkt, akutem/chronischem Koronarsyndrom mit/ohne PCI, Patienten und Patientinnen nach Operationen am Herzen und an den Gefässen sowie das Vorhandensein multipler Risikofaktoren (z.B. metabolisches Syndrom mit/ohne chronischer Herzkrankheit) und Herzinsuffizienz. Ziele und Inhalte der Rehabilitation sind dabei sowohl die Risikostratifizierung für Rezidive als auch die Umsetzung einer adäquaten medikamentösen Sekundärprophylaxe, Information über Krankheit (Diagnostik und Therapie) und Risikofaktoren, Rekonditionierung nach Immobilisierung sowie Korrektur eines vorbestehenden Bewegungsmangels. Ausserdem sollen Lebensstilveränderungen mit Aneignung eines gesunden Lebensstils angestrebt werden (u.a. Ernährungsberatung, Stressbewältigung, Raucherentwöhnung).
Unterschied zwischen stationärer & konventionell ambulanter kardiovaskulärer Rehabilitation
Zur Differenzierung zwischen einer ambulanten Rehabilitation und einer stationären Rehabilitation stellt die SCPRS fest, dass eine ambulante Einrichtung den Vorteil der Wohnortnähe, den möglichen Einbezug von Angehörigen, die Durchführung über längere Zeit sowie des Weiteren die Möglichkeit einer Teilzeit-Berufstätigkeit ergibt. Für eine stationäre Rehabilitation sprechen ein komplikationsreicher Verlauf, ausgeprägte Komorbidität (Begleiterkrankungen), ein erhöhter Pflegebedarf, die Notwendigkeit intensiver medizinischer Überwachung und Kontrolle sowie eine fehlende Betreuung zu Hause.
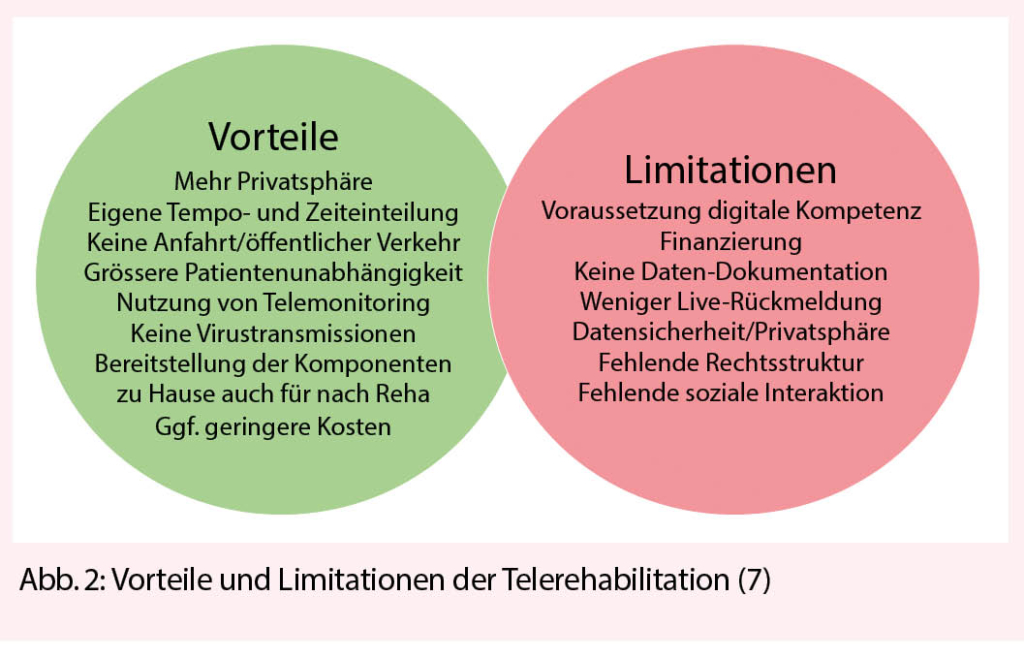
Vorteile und Limitationen der Telerehabilitation
Neben einer ubiquitären Verfügbarkeit mit grosser Reichweite besticht die Telerehabilitation durch eine hohe Kosteneffizienz und schnelle Implementierung individueller rehabilitativer Massnahmen (11) zu Zeiten eines Lockdowns. Idealerweise wird sie im Sinne einer effektiven «Hybridrehabilitation» praktiziert. Das bedeutet: Training und Weiterbildung werden zu Hause durchgeführt, während zur adäquaten medizinischen Beurteilung der Patienten zusätzlich Sprechstunden und Diagnostik im Zentrum stattfinden (12). Die hohe Akzeptanz der Telerehabilitation seitens der Patienten konnte nachgewiesen werden (9) und bestätigte sich auch durch unsere persönlichen Beobachtungen während der Lockdown-Phasen. Es bestätigte sich erwartungsgemäss, dass insbesondere Patienten nach Herzoperation häufiger als nach Katheterintervention und jüngere Patienten häufiger als ältere an Telerehabilitationsprogrammen teilnehmen. Keine Rolle spielten dagegen das Geschlecht, die persönliche Herkunft sowie die Wohnorte (Stadt versus Land) (13). Leider bestehen bisher Softwaresysteme hauptsächlich für muskuloskelettale, neurologische und pneumologische Heimprogramme, nicht jedoch für die HB-KVR (14), obschon zum Beispiel die Implementierung eines Handgelenk-Monitors für die HB-KVR zeigen konnte, dass sie einer zentrumsbasierten kardiovaskulären Rehabilitation (ZB-KVR) nicht unterlegen ist (15). Bzgl. der Verfügbarkeit eines Onlinezuganges bestehen in der Schweiz nur noch geringe Limitationen, die allergrösste Mehrheit der schweizerischen Bevölkerung besitzt ein Smartphone bei jährlich weiteren Zuwächsen (16). Selbst die vermeintlich am wenigsten digitalisierte Gruppe der herzinsuffizienten Patienten nutzte bereits 2016 (allerdings in den USA) das Smartphone durchschnittlich 120 min pro Tag (17). Die Einschätzung der Sicherheit, des Einflusses auf die Lebensqualität und auf Ängste der Teilnehmer, sowie die Akzeptanz und Adhärenz an HB-KVR herzinsuffizienter Patienten wird weiter untersucht und ist Gegenstand der aktuellen TELEREH-HF-Studie (18).
Es kann zusammengefasst werden, dass die HB-KVR verglichen zur konventionellen ZB-KVR äquivalente Erfolge erzielt und daher insbesondere in Zeiten der COVID-19-Pandemie unbedingt forciert eingesetzt werden sollte (19).
Implementierung einer Telerehabilitation am Beispiel des kardiovaskulären Präventionszentrums am USB
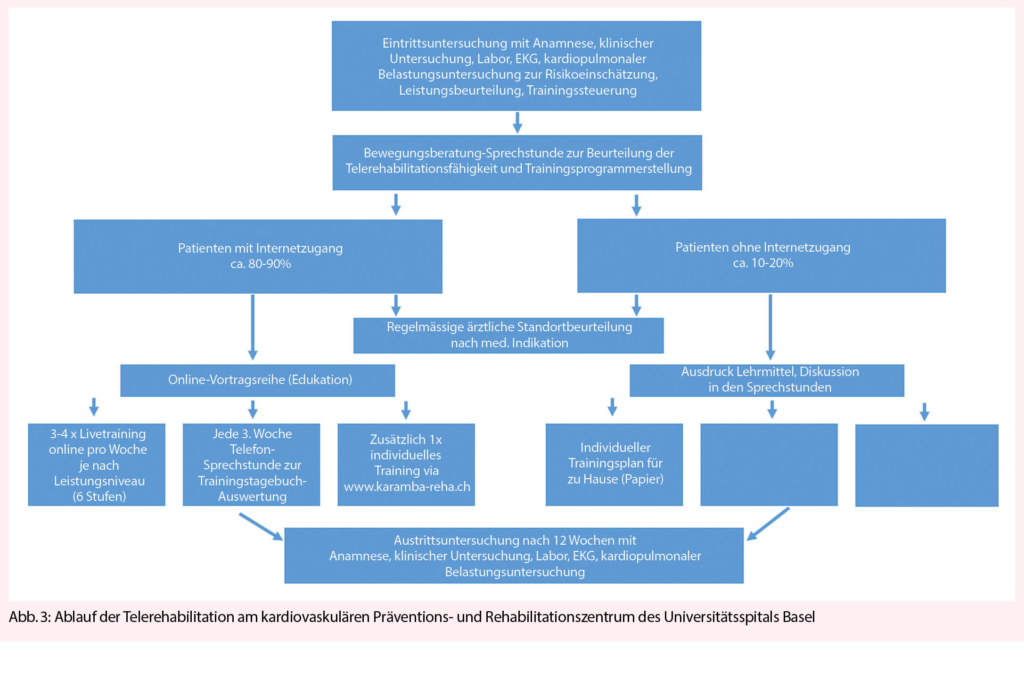
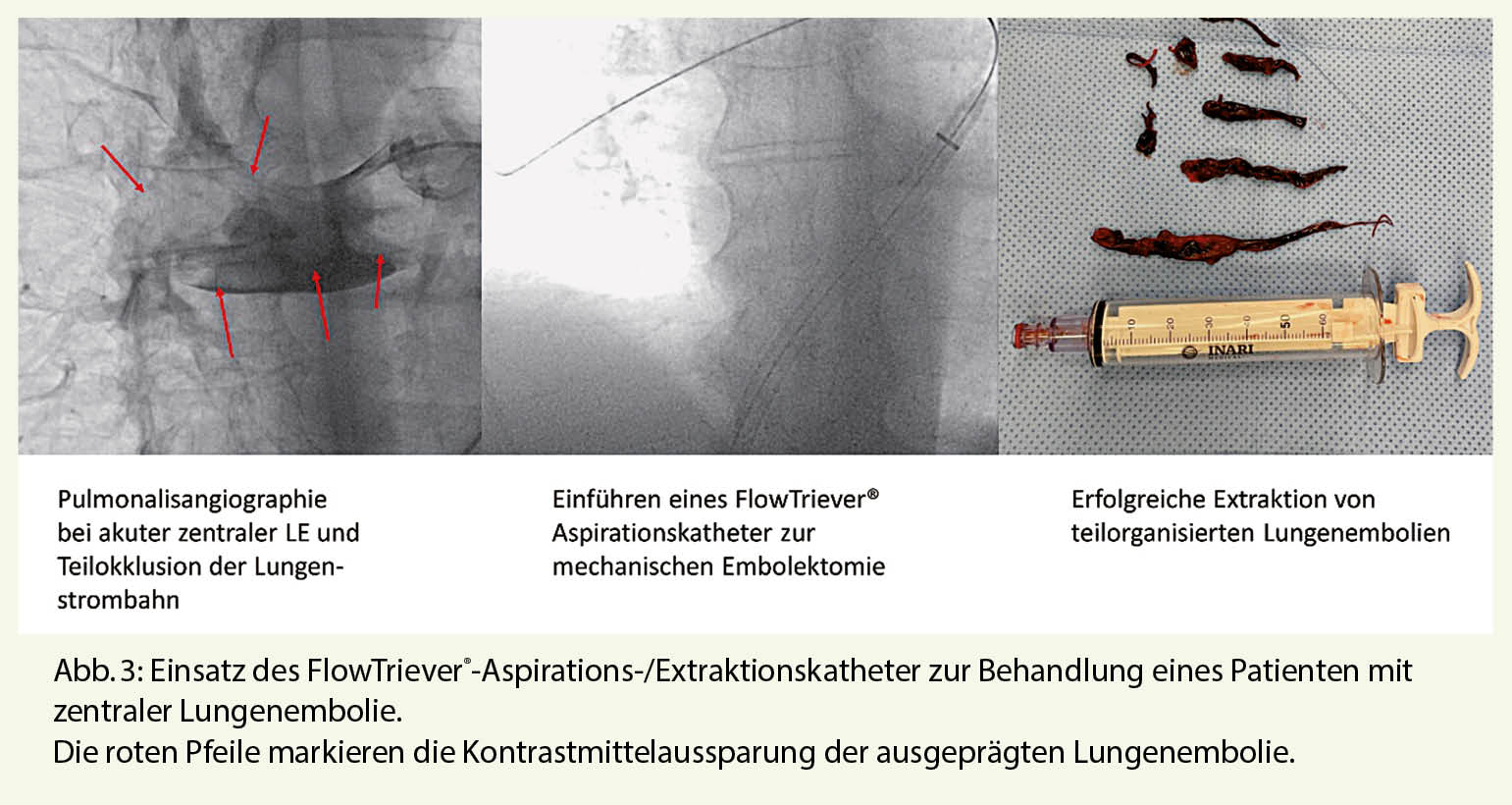
Basierend auf den Erkenntnissen des Lockdowns im Frühjahr 2020 in der Schweiz wurde auf der Grundlage aktueller Empfehlungen bzgl. relevanter Inhalte für ein HB-KVR-Programm der Phase II (5) ein Online-Hybrid-Rehabilitationsprogramm (HB-KVR) für den Fall eines weiteren Lockdowns entwickelt. Die Schliessung der ZB-KVR wurde durch erneut stark steigende Corona-Fallzahlen im Dezember 2020 nötig, sodass die HB-KVR zur Umsetzung kam (vgl. Abb. 3):
Es erfolgt jeweils primär eine ärztliche Eintrittsuntersuchung mit Anamnese, klinischer Beurteilung, Labor, EKG und Spiroergometrie, woraufhin der Patient/die Patientin in eine Leistungsgruppe eingeteilt wird. Im Anschluss erfolgt eine Bewegungssprechstunde bei einem/einer Sporttherapeut/-in, um einen Trainingsplan für die HB-KVR auszuarbeiten. Mit aeroben Ausdauertrainingseinheiten und zusätzlichen Kräftigungstrainings für die grossen Muskelgruppen folgt dieses Vorgehen den Standards der SCPRS. Hierbei wird festgelegt, ob die technischen und kognitiven Voraussetzungen gegeben sind für die Beteiligung an einem online-live-Training, oder ob auf ein Papierformat zurückgegriffen werden muss:
1. Das Online-live-Training der HB-KVR, für welches am Vortag jeweils via Email ein Link verschickt wird, basiert auf 3-4 Trainingseinheiten pro Woche à 30-45 Minuten und beinhaltet Kraft, Ausdauer, Beweglichkeit und Gleichgewichtsübungen. Zusätzlich werden den Patienten individualisiert Übungen und Trainingsoptionen aufgezeigt, die jederzeit selbstständig durch Zugriff auf www.karamba-reha.ch ohne Kosten, Passwort oder Anmeldung aufgerufen und absolviert werden können (diverse 20-30 Minuten Trainingsvideos für Ausdauer, Kraft, Beweglichkeit und Koordination). Die absolvierten Trainingseinheiten werden in einem Bewegungstagebuch mit Dauer, Intensität und subjektiver Beanspruchung (nach Borg) dokumentiert und, falls vorhanden, mittels Herzfrequenzmessungen und Schrittzähler unterstützt. Nach 3 Wochen werden (in der Regel wieder telefonisch) mögliche Probleme und Barrieren thematisiert und evtl. Anpassungen durchgeführt.
2. Für Patienten ohne Internet-Zugang wurden Übungsformen mit Haushaltsmaterialien entwickelt und in einem anleitenden Papierformat festgehalten, welche dann jedoch nach Umsetzung ebenfalls in einem Bewegungstagebuch notiert werden. Die Patienten ohne Internet-Zugang werden während der Rehabilitation engmaschiger telefonisch und durch Konsultationen betreut.
Begleitend zum Onlinetraining finden Online-Schulungen und ärztliche Konsultationen sowie individuelle Beratungen wie z.B. Rauchstoppsprechstunden (letztere bedarfsorientiert im Zentrum) statt. Am Ende der Rehabilitation, nach 12 Wochen, schliesst sich eine Austrittsuntersuchung an. Die Ergebnisse werden nach Abschluss des Lockdowns wissenschaftlich untersucht und mit einer konventionellen ZB-KVR verglichen.
Copyright bei Aerzteverlag medinfo AG
Herzzentrum Universitätsspital Basel
Petersgraben 4
4031 Basel
Rupprecht.Wick@usb.ch
Herzzentrum Universitätsspital Basel
Petersgraben 4
4031 Basel
Herzzentrum Universitätsspital Basel
Petersgraben 4
4031 Basel
Die Autoren haben deklariert, dass in Zusammenhang mit diesem Artikel keine Interessenskonflikte vorliegen.
1. Rauch B. The prognostic effect of cardiac rehabilitation in the era of acute revascularisation and statin therapy: A systematic review and meta-analysis of randomized and non-randomized studies – The Cardiac Rehabilitation Outcome Study (CROS). European Journal of Preventive Cardiology 2016, Vol. 23(18) 1914-1939
2. 2016 European Guidelines on cardiovascular disease prevention in clinical practice; European Heart Journal, June 8, 2016
3. S3-Leitlinie zur kardiologischen Rehabilitation (LL-KardReha) im deutschsprachigen Raum Europas Deutschland, Österreich, Schweiz (D-A-CH); Gesamtversion Version 1.1 (10.12.2020). AWMF-Registernummer: 133-001
4. Anderson L. Exercise-based cardiac rehabilitation for coronary heart disease. Cochrane Database Syst Rev 2016;CD001800
5. Verschueren S. The effect of exercise therapy on depressive and anxious symptoms in patients with ischemic heart disease: a systematic review. J Psychosom Res 2018;105:80-91.
6. Inciardi RM. Characteristics and outcomes of patients hospitalized for COVID-19 and cardiac disease in Northern Italy. European Heart Journal (2020) 41, 1821–1829
7. Scherrenberg M. The future is now: a call for action for cardiac telerehabilitation in the COVID-19 pandemic from the secondary prevention and rehabilitation
section of the European Association of Preventive Cardiology. European Journal of Preventive Cardiology 0(0) 1–21
8. Haykowsky M. A meta-analysis of the effects of exercise training on left
ventricular remodeling following myocardial infarction: start early and go longer for greatest exercise benefits on remodeling. Trials 2011;12:92.
9. Subedi N. Implementation of Telerehabilitation Interventions for the Self-Management of Cardiovascular Disease: Systematic Review. JMIR Mhealth Uhealth.
2020 Nov 27;8(11):e17957. doi: 10.2196/17957
10. https://www.scprs.ch/DOCS_PUBLIC/Empfehlungen%20zur%20Indikation%20und%20Durchfuhrung.pdf
11. Maddison R. Effects and costs of real-time cardiac telerehabilitation:
randomised controlled non-inferiority trial. Heart 2019;105:122–129.
12. Frederix I. Effect of comprehensive cardiac telerehabilitation on one-year cardiovascular rehospitalization rate, medical costs and quality of life: A cost-effectiveness analysis. European Journal of Preventive Cardiology 2016,
Vol. 23(7) 674–682
13. Krishnamurthi N. Predictors of Patient Participation and Completion of Home-Based Cardiac Rehabilitation in the Veterans Health Administration for Patients With Coronary Heart Disease. The American Journal of Cardiology, Volume 123, Issue 1, 1 January 2019, Pages 19-24
14. Hosseiniravandi M. Home-based telerehabilitation software systems for remote supervising: a systematic review. International Journal of Technology Assessment in Health Care 36, 113–125
15. Batalik L. Benefits and effectiveness of using a wrist heart heart rate monitor as a telerehabilitation device in cardiac patients. A randomized controlled trial. Medicine: March 2020 – Volume 99 – Issue 11
16. https://www.statista.com/forecasts/1145576/smartphone-users-in-switzerland
17. Kim JS. Need Assessment for Smartphone-Based Cardiac TelerehabilitationHealthc Inform Res. 2018 October;24(4):283-291.
18. Piotrowicz E. Hybrid comprehensive telerehabilitation in heart failure patients
(TELEREH-HF): A randomized, multicenter, prospective, openlabel, parallel group controlled trial—Study design and description of the intervention. American Heart Journal Volume 217, November 2019, Pages 148-158
19. Choxi R. Cardiac Rehabilitation and Implications During the COVID-19 Era,
American college of cardiology, Jan 04, 2021