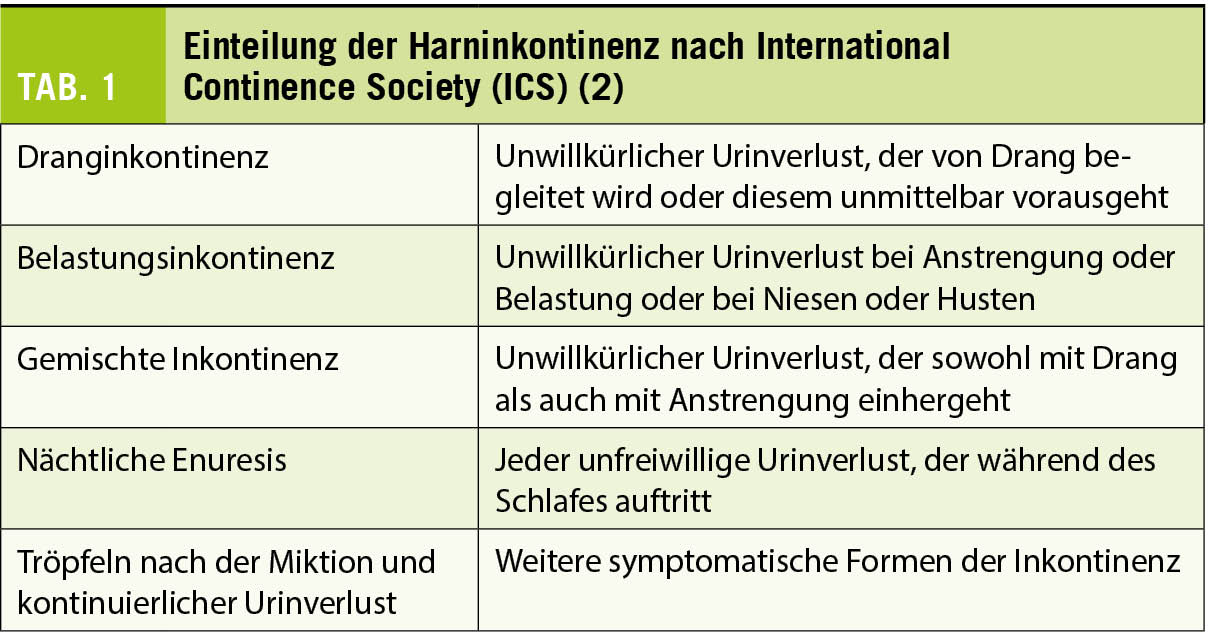
Auch wenn die Harninkontinenz häufig bei Frauen auftritt, betrifft Sie auch einen beträchtlichen Teil der Männer. Die geschätzte Prävalenz von Inkontinenz variiert von 11% bei den 60-64-jährigen bis 31% bei älteren Männern (1). Definiert wird sie gemäss der International Continence Society (ICS) als «unwillkürlicher objektivierbarer Urinverlust, welcher zu sozialen oder hygienischen Problemen führt» (2). Sie wird in drei Hauptformen unterteilt: Dranginkontinenz (urgency urinary incontinence), welche die häufigste Form bei Männern darstellt, Belastungsinkontinenz (stress urinary incontinence), welche in < 10% der Fälle auftritt, sowie Mischinkontinenz (mixed urinary incontinence, Tab. 1) (3).
 Bezüglich der Behandlungsmöglichkeiten stehen sowohl Lifestyle- Modifikationen, medikamentöse als auch chirurgische Methoden zur Verfügung. Der folgende Artikel soll einen kurzen Überblick über die Diagnostik sowie die Behandlungsmöglichkeiten schaffen.
Bezüglich der Behandlungsmöglichkeiten stehen sowohl Lifestyle- Modifikationen, medikamentöse als auch chirurgische Methoden zur Verfügung. Der folgende Artikel soll einen kurzen Überblick über die Diagnostik sowie die Behandlungsmöglichkeiten schaffen.
Diagnostik
Anamnese
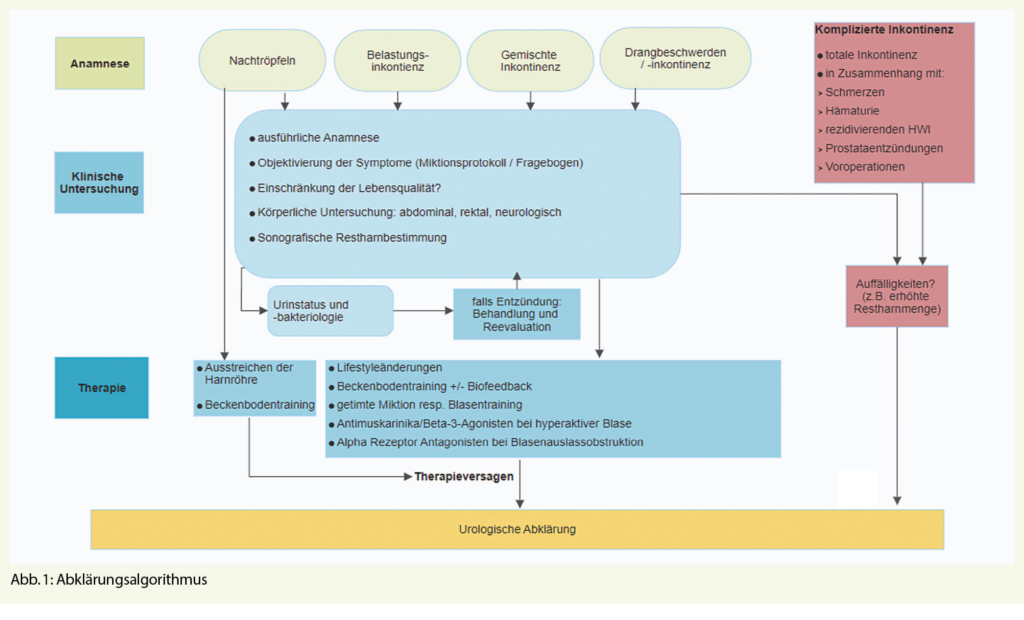
Gemäss ICS kann die Diagnostik in eine Basisabklärung, welche in der hausärztlichen Praxis erfolgen kann, und in eine erweiterte Diagnostik beim Spezialisten eingeteilt werden (4). Zu beachten ist, dass beim Mann die Inkontinenz häufig nicht als alleiniges Symptom auftritt, sondern in Zusammenhang mit anderen Symptomen (LUTS – Lower Urinary Tract Symptoms). Das wichtigste Instrument der Diagnosestellung einer Inkontinenz ist deshalb die ausführliche Anamnese, um mögliche Differentialdiagnosen wie Harnwegsinfekte, die Überlaufblase und eine gutartige Prostatavergrösserung zu erfassen. Hierzu können zur Hilfe auch Fragebögen eingesetzt werden, wie zum Beispiel der ICIQ (International Consultation on Incontinence Questionnaire, https://iciq.net.) (5).
Die wichtigsten Fragen der Anamnese betreffen die Häufigkeit, den Zeitpunkt, die Umstände und die Menge des Urinverlusts (6). Patienten welche zusätzlich über eine Alg- oder Makrohämaturie klagen, oder aber eine Anamnese von rezidivierenden Harnwegsinfekten haben, sollten einem Urologen respektive einer Urologin zu weiteren Abklärungen zugewiesen werden (7).
Zusätzlich sollte eine allgemeine Anamnese über bestehende Krankheiten, insbesondere neurologische Erkrankungen, Voroperationen sowie eine allfällige Medikamenteneinnahme durchgeführt werden.
Miktionsprotokoll
Zur besseren Objektivierung der Trink- und Miktionsgewohnheiten dient die Durchführung eines Miktionsprotokolls. Hierbei sollte an mindestens drei aufeinanderfolgenden Tagen eine genaue Dokumentation der Trinkmenge, Miktionshäufigkeit, der Miktionsmenge, des verspürten Harndrangs sowie allfälligen Inkontinenzereignissen geführt werden.
Körperliche Untersuchung
Neben der Anamnese gehört ebenfalls eine körperliche Untersuchung bei Erstkonsultation dazu. Es sollte hierbei sowohl eine Digital-Rektale Untersuchung (DRU) der Prostata zum Ausschluss eines suspekten Tastbefundes, aber auch zum Ausschluss einer Prostatitis durchgeführt werden. Neben der DRU gehört ebenfalls die abdominale Palpation zum Ausschluss von abdominellen Raumforderungen oder einer Überlaufblase dazu, sowie ein grober neurologischer Status und die Beurteilung des äusseren Genitales (7).
Labor
Zum Ausschluss eines Harnwegsinfektes sollte ein Urinstreifentest durchgeführt werden. Sollte sich hierbei der Hinweis auf eine Leukozyturie zeigen, empfiehlt sich die Anlage einer Urinbakteriologie sowie die resistenzgerechte antibiotische Behandlung. Während eines Harnwegsinfektes können sich die Symptome einer Harninkontinenz verschlechtern (8). Jedoch sollten ältere Menschen mit einer Urininkontinenz und einer asymptomatischen Bakteriurie nicht routinemässig antibiotisch behandelt werden (9).
Sonografie
Mittels sonografischer Untersuchung kann sowohl die postmiktionelle Restharnbestimmung, als auch eine ungefähre Abschätzung der Prostatagrösse erfolgen. Dadurch kann eine Überlaufblase ausgeschlossen werden.
Erweiterte Diagnostik
Zur erweiterten Diagnostik in der urologischen Sprechstunde gehören die Urinflussmessung, welche gewisse Hinweise auf eine infravesikale Obstruktion geben kann. Eine weiterführende urologische Abklärung stellt die Urodynamik dar. Durch die urodynamische Untersuchung kann zwischen einer Harnblasenspeicher- und Entleerungsstörung differenziert werden. Zudem kann die Funktion des Detrusors beurteilt und neurologische Ursachen festgestellt werden. Die Urethrozystoskopie (Blasenspiegelung) kann morphologische Veränderungen der Harnwege detektieren und dient insbesondere bei Hämaturie zum Ausschluss einer Malignität der Harnblase.
Therapie der Harninkontinenz
Konservativ
Zunächst sollte die Behandlung möglicher Begleiterkrankungen wie z.B. Metabolisches Syndrom, Herzinsuffizienz, neurologische Erkrankungen, obstruktives Schlafapnoesyndrom oder Obstipationen behandelt werden (7). Zeigt sich in der Untersuchung eine Blasenentzündung oder Prostatitis, sollte diese ebenso behandelt werden und im Anschluss eine Reevaluation der Inkontinenz stattfinden.
Bei einer vorherrschend störenden Nykturie sollte eine Flüssigkeitsrestriktion abends erfolgen, zusätzlich kann gegebenenfalls die Umstellung einer diuretischen Therapie eine Wirkung zeigen.
Weiter kann ein Beckenbodentraining unter Anleitung einer geschulten Physiotherapiefachkraft eine Besserung bringen. Eine schnellere Rehabilitation der Belastungsinkontinenz nach stattgehabter radikaler Prostatektomie durch Beckenbodentraining konnte nachgewiesen werden (10).
Medikamentöse Therapien
Zeigt sich kein signifikanter Restharn, können als medikamentöse Therapie der Dranginkontinenz Anticholinergika eingesetzt werden. Hierbei gibt es zwischen den auf dem Markt zugelassenen anticholinergen Medikamente keine grossen Unterschiede bezüglich der Wirksamkeit. Als häufigste Nebenwirkungen werden Mundtrockenheit, Obstipation, Fatigue, Verschwommensehen und kognitive Einschränkungen genannt (11). Insbesondere bezüglich letzterem ist bei älteren, kognitiv bereits eingeschränkten Patienten Vorsicht geboten.
Neben einer anticholinergen Therapie besteht die Möglichkeit einer Therapie mit einem Beta-3-Agonisten (Betmiga), welcher in einer Phase-III-Studie signifikant bessere Wirkung verglichen mit Placebo zeigte (12). Es besteht ausserdem die Möglichkeit der Kombination von Betmiga mit einem Anticholinergikum, wobei sich ein verbessertes Therapieansprechen zeigte (13).
Zeigt sich zusätzlich der Verdacht auf eine Prostatahyperplasie, können auch Alphablocker oder 5-Alpha-Reduktasehemmer als Therapie, gegebenenfalls in Kombination mit einem Anticholinergikum oder Beta 3 Mimetikum, eingesetzt werden (4).
Zeigt sich kein gutes Ansprechen auf die Therapie mittels Lifestylemodifikation, Beckenbodentraining und/oder medikamentöser Therapie, ist eine weiterführende urologische Abklärung empfohlen.
Interventionelle und operative Therapien
Sollte sich die medikamentöse Therapie ausgeschöpft oder sollten sich die unerwünschten Wirkungen zu dominant zeigen, gibt es für die Dranginkontinenz die Möglichkeit einer transurethralen Botoxinjektion (Onabotulinum Toxin A) in den Detrusor vesicae. Hierbei gilt zu beachten, dass es zu erhöhten Restharnmengen, sowie gegebenenfalls einer Notwendigkeit eines intermittierenden Selbstkatheterismus kommen kann (14). Die mediane Wirkzeit für Botox-Injektionen zeigte sich bei 7,5 Monaten (15).
Weitere Therapiemöglichkeiten ergeben sich durch elektrische Stimulation. Diese kann sowohl transkutan (TENS, transkutane elektrische Nervenstimulation), perkutan (PTNS, perkutane tibiale Nervenstimulation) oder über die sakrale Neuromodulation (SNM) erfolgen. Für die PTNS konnten hierbei Erfolgsraten zwischen 54 und 59% gezeigt werden (16). Eine Cochrane-Analyse konnte die Wirksamkeit von einer SNM-Implantation bei ansonsten therapierefraktären Patienten zeigen (17).
Bei einer Dranginkontinenz aufgrund einer Blasenauslassobstruktion gibt es neben der medikamentösen Therapie ebenfalls minimalinvasive (iTind, Prostataarterienembolisation etc.) oder operative (TUR-P, HoLEP, Aquaablation etc.) Verfahren.
Operativ gibt es insbesondere bei Belastungsinkontinenz nach radikaler Prostatektomie die Möglichkeit von urethralen Schlingen, welche jedoch mit einer hohen Rate an Komplikationen einhergehen (18). Eine weitere Therapieform besteht mit dem artifiziellen Sphinkter.
Sollten sich ausgesprochen schwere Verläufe einer Harninkontinenz zeigen, kann sowohl eine Blasenaugmentation als auch ein Ileum-Conduit (19) diskutiert werden.
Copyright Aerzteverlag medinfo
Klinik für Urologie
Kantonsspital St. Gallen,
Rorschacherstrasse 95
9007 St. Gallen
Anne.Neuenschwander@kssg.ch
Klinik für Urologie
Kantonsspital St. Gallen
Rorschacherstrasse 95
9007 St. Gallen
Klinik für Urologie
Kantonsspital St. Gallen
Rorschacherstr. 95
9007 St. Gallen
Die Autoren haben deklariert, keine Interessenskonflikte im Zusammenhang mit diesem Beitrag zu haben.
1. Shamliyan TA, Wyman JF, Ping R, Wilt TJ, Kane RL. Male urinary incontinence: prevalence, risk factors, and preventive interventions. Rev Urol. 2009;11(3):
145-65.
2. Abrams P, Cardozo L, Fall M, Griffiths D, Rosier P, Ulmsten U, et al. The standardisation of terminology of lower urinary tract function: report from the Standardisation Sub-committee of the International Continence Society. Neurourol Urodyn. 2002;21(2):167-78.
3. Abrams P, Andersson KE, Apostolidis A, Birder L, Bliss D, Brubaker L, et al. 6th International Consultation on Incontinence. Recommendations of the International Scientific Committee: EVALUATION AND TREATMENT OF URINARY INCONTINENCE, PELVIC ORGAN PROLAPSE AND FAECAL INCONTINENCE. Neurourol Urodyn. 2018;37(7):2271-2.
4. Abrams P, Andersson KE, Birder L, Brubaker L, Cardozo L, Chapple C, et al. Fourth International Consultation on Incontinence Recommendations of the
International Scientific Committee: Evaluation and treatment of urinary incontinence, pelvic organ prolapse, and fecal incontinence. Neurourol Urodyn. 2010;29(1):213-40.
5. Rosier PFWM, Schaefer W, Lose G, Goldman HB, Guralnick M, Eustice S, et al. International Continence Society Good Urodynamic Practices and Terms 2016: Urodynamics, uroflowmetry, cystometry, and pressure-flow study. Neurourol Urodyn. 2017;36(5):1243-60.
6. Milsom I, Abrams P, Cardozo L, Roberts RG, Thüroff J, Wein AJ. How widespread are the symptoms of an overactive bladder and how are they managed? A population-based prevalence study. BJU Int. 2001;87(9):760-6.
7. F.C. Burkhard (Chair) JLHRB, F. Cruz, G.E. Lemack, A.K. Nambiar, N. Thiruchelvam, A. Tubaro, Guidelines Associates: D. Ambühl DAB, F. Farag, R. Lombardo, M.P. Schneider. EAU Guidelines. Edn. presented at the EAU Annual Congress Amsterdam, 2020. ISBN 978-94-92671-07-3. EAU Guidelines Office, Arnhem, The Netherlands. http://uroweb.org/guidelines/compilations-of-all-guidelines/2020.
8. Arinzon Z, Shabat S, Peisakh A, Berner Y. Clinical presentation of urinary tract infection (UTI) differs with aging in women. Arch Gerontol Geriatr. 2012;55(1):
145-7.
9. Ouslander JG, Schapira M, Schnelle JF, Uman G, Fingold S, Tuico E, et al. Does eradicating bacteriuria affect the severity of chronic urinary incontinence in nursing home residents? Ann Intern Med. 1995;122(10):749-54.
10. Campbell SE, Glazener CM, Hunter KF, Cody JD, Moore KN. Conservative management for postprostatectomy urinary incontinence. Cochrane Database Syst Rev. 2012;1:Cd001843.
11. Shamliyan T, Wyman J, Kane RL. Nonsurgical Treatments for Urinary Incontinence in Adult Women: Diagnosis and Comparative Effectiveness. 2012.
12. Cui Y, Zong H, Yang C, Yan H, Zhang Y. The efficacy and safety of mirabegron in treating OAB: a systematic review and meta-analysis of phase III trials. Int Urol Nephrol. 2014;46(1):275-84.
13. Shin JH, Kim A, Choo MS. Additional low-dose antimuscarinics can improve overactive bladder symptoms in patients with suboptimal response to beta 3 agonist monotherapy. Investig Clin Urol. 2017;58(4):261-6.
14. Nitti VW, Dmochowski R, Herschorn S, Sand P, Thompson C, Nardo C, et al.
OnabotulinumtoxinA for the Treatment of Patients with Overactive Bladder and Urinary Incontinence: Results of a Phase 3, Randomized, Placebo Controlled Trial. J Urol. 2017;197(2S):S216-S23.
15. Visco AG, Brubaker L, Richter HE, Nygaard I, Paraiso MF, Menefee SA, et al. Anticholinergic therapy vs. onabotulinumtoxina for urgency urinary incontinence. N Engl J Med. 2012;367(19):1803-
16. Tutolo M, Ammirati E, Heesakkers J, Kessler TM, Peters KM, Rashid T, et al. Efficacy and Safety of Sacral and Percutaneous Tibial Neuromodulation in Non-neurogenic Lower Urinary Tract Dysfunction and Chronic Pelvic Pain: A Systematic Review of the Literature. Eur Urol. 2018;73(3):406-
17. Herbison GP, Arnold EP. Sacral neuromodulation with implanted devices for urinary storage and voiding dysfunction in adults. Cochrane Database Syst Rev. 2009(2):Cd004202.
18. Cornel EB, Elzevier HW, Putter H. Can advance transobturator sling suspension cure male urinary postoperative stress incontinence? J Urol. 2010;183(4):1459-63.
19. Gurung PMS, Attar KH, Abdul-Rahman A, Morris T, Hamid R, Shah PJR. Long-term outcomes of augmentation ileocystoplasty in patients with spinal cord injury: a minimum of 10 years of follow-up. BJU International. 2012;109(8):1236-42.