Zink ist nach Eisen das für den Menschen quantitativ bedeutsamste Spurenelement und hat strukturelle, regulatorische und katalytische Aufgaben bei einer Vielzahl von Enzymen. Klinisch ist es wichtig für Wachstum und Entwicklung, testikuläre Reifung, neurologische Funktionen, Wundheilung und Immunabwehr. In diesem Artikel werden aktuelle Aspekte zu Zink präsentiert.
Als Spurenelemente werden gewöhnlich Mineralstoffe definiert, die von Erwachsenen in Mengen von 1 bis 100 mg/Tag benötigt werden. Dazu gehören u.a. Kupfer, Mangan und Zink. Zink ist ein Übergangsmetall und liegt in organischen Verbindungen vorwiegend als zweiwertiges Kation vor. Historisch gesehen wurde ein schwerer Zinkmangel als Ursache für endemischen Hypogonadismus und Zwergwuchs im ländlichen Iran anerkannt und damit Zink als essentielles Spurenelement identifiziert. In den letzten Jahren hat die Beobachtung, dass ein subklinischer Zinkmangel die Inzidenz von Durchfall und Infektionen der oberen Atemwege sowie deren Morbidität und Mortalität signifikant erhöhen kann, grosses Interesse geweckt. Neben Mangel an Eisen, Jod und Vitamin A ist der Zinkmangel weltweit einer der wichtigsten Mikronährstoffmängel.
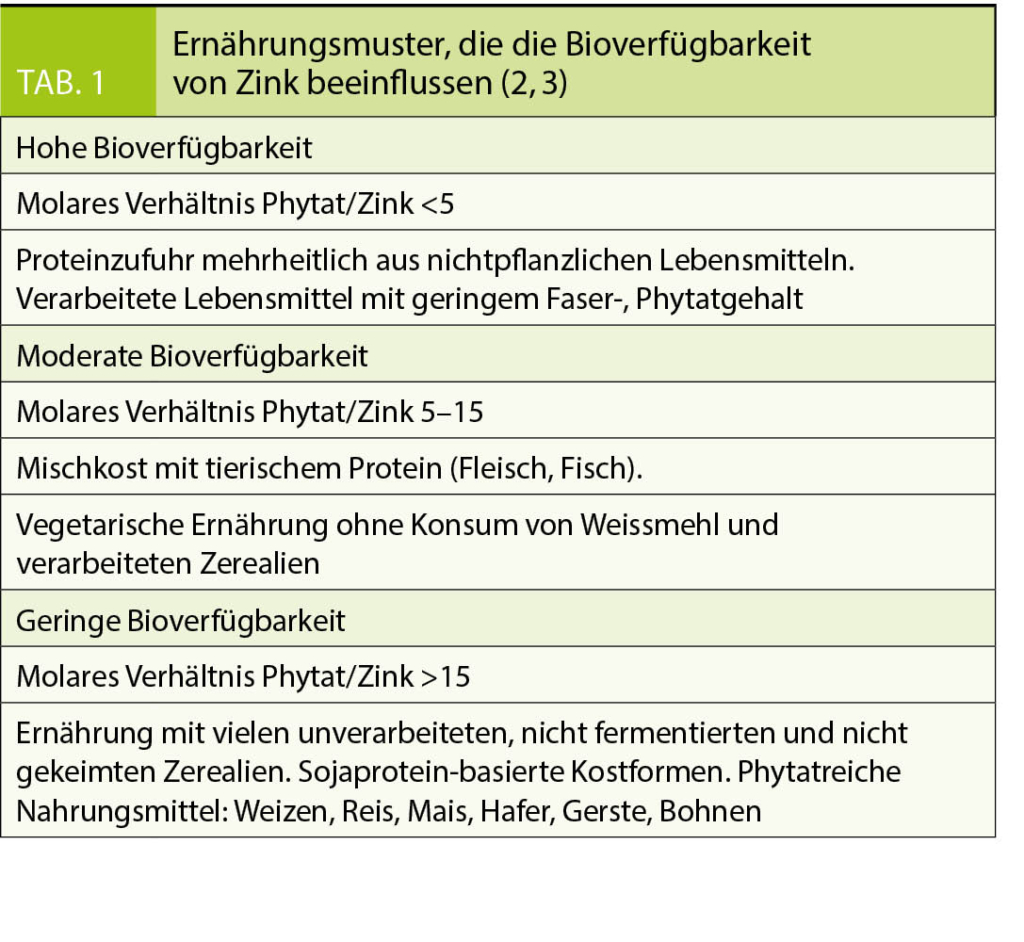
Nahrungsmittel tierischer Herkunft sind ausgezeichnete Zinkquellen, ebenso wie Nüsse und Linsen. Demgegenüber finden sich in Gemüse, Obst und Produkten aus Weissmehl nur geringe Mengen Zink. In der westlichen Ernährung werden Nahrungsmittel deshalb oft mit Zink angereichert, und diese Produkte stellen eine zunehmend wichtige Zinkquelle dar. Dabei spielt zur Bedarfsdeckung des Menschen nicht nur der absoluten Zinkgehalt der Nahrungsmittel eine Rolle, sondern in grossem Ausmass dessen Bioverfügbarkeit. Da vegetarische Kostformen hohe Mengen an Phytat, Nahrungsfasern und Kasein enthalten, ist bei diesen die Bioverfügbarkeit wegen der Bildung von unlöslichen Zinkkomplexen gering (1). Eine Zusammenstellung der Ernährungsmuster, die die Bioverfügbarkeit von Zink beeinflussen, findet sich in Tabelle 1.
Die empfohlene diätetische Referenzzufuhr (DRI) für Zink variiert je nach Alter und Geschlecht und steigt von 3 mg täglich in der frühen Kindheit bis zu 8 mg täglich bei erwachsenen Frauen und 11 mg täglich bei erwachsenen Männern (4). Während der Schwangerschaft und Stillzeit ist der Bedarf etwas höher. Von einer Zinkzufuhr von über 25 mg pro Tag wird abgeraten. Global gesehen haben ungefähr 45 Prozent der Erwachsenen eine unzureichende Zinkaufnahme (5). In Drittweltländern sind etwa 2 Milliarden Menschen von Zinkmangel betroffen, vor allem in den Ländern, in welchen Zerealien die Hauptnährstofflieferanten darstellen (6). Hingegen hat der Zinkverbrauch in der Schweiz mit 13,2 mg pro Tag wie auch der angenäherte Verzehr mit 12,5 mg pro Tag gegenüber der Abnahme gemäss dem 5. Schweizerischen Ernährungsbericht wieder leicht zugenommen und der angenäherte Verzehr liegt über der gewichteten empfohlenen Zufuhr, womit für die Schweiz insgesamt von einer ausreichenden Zinkversorgung ausgegangen werden darf (7).
Während der Verdauung wird das in der Nahrung enthaltene Zink freigesetzt und bildet Komplexe mit verschiedenen Liganden. Diese Zink-Ligand-Komplexe werden hauptsächlich im Zwölffingerdarm und im Jejunum sowohl aktiv als auch passiv absorbiert. Die Zinkabsorption kann bei einer Pankreasinsuffizienz beeinträchtigt sein, da Pankreasenzyme für die Freisetzung von Zink aus der Nahrung notwendig sind. Zink teilt einige gemeinsame absorbierende Komponenten mit Eisen und Kupfer, und die drei Mineralien können um die Absorption konkurrieren. Wie erwähnt verringert Phytinsäure die Zinkabsorption (1) und es konnte nachgewiesen werden, dass die Einnahme und Plasmakonzentration von Zink bei Menschen unter habitueller vegetarischer Ernährung signifikant tiefer ist als unter nicht-vegetarischer Ernährung (9) .
Der Gesamtkörperzinkgehalt beträgt bei Erwachsenen im Durchschnitt 1,5 bis 2,5 g (10), ähnlich dem von Eisen. Im Serum finden sich lediglich 0,1% des Gesamtkörperzinks, 2⁄3 an Albumin und 1⁄3 an alpha-2-Makroglobulin gebunden. 98% des Zinks sind intrazellulär lokalisiert. Ein grosser Teil davon befindet sich in Knochen- und Muskelpools mit langsamen Umsätzen, weiter finden sich hohe Konzentrationen in der Leber, in den männlichen Reproduktionsorganen sowie in Retina und Iris (2).
Der Hauptweg der Ausscheidung von Zink erfolgt über den Magen-Darm-Trakt. Bis zu 10 Prozent des zirkulierenden Zinks wird auch über den Urin ausgeschieden. Die Zinkhomöostase wird durch eine Kombination von Veränderungen der fraktionierten Absorption und der endogenen fäkalen Zinkausscheidung aufrechterhalten.
Biologische Rolle von Zink
Zink verdankt seine biologische Rolle der Fähigkeit, enge Bindungen mit bestimmten Aminosäuren, insbesondere Histidin und Cystein, zu bilden. Ungefähr 250 Proteine enthalten Zink. Dazu gehören Enzyme wie das Angiotensin-Converting-Enzym, alkalische Phosphatase, Carboanhydrase, DNA- und RNA-Polymerasen, Kupfer-Zink-Superoxiddismutase und Metallothionein sowie eine grosse Familie von Zinkproteinen, die an der Gentranskription beteiligt sind. Auf molekularer Ebene erfüllt Zink strukturelle, regulatorische und katalytische Aufgaben bei einer Vielzahl von Enzymen und ist für die Konfiguration nichtenzymatischer Proteine von Bedeutung. Zink hat damit strukturelle, regulatorische und katalytische Funktionen. Es spielt eine wichtige Rolle sowohl bei der Zellteilung als auch bei der Apoptose (programmierter Zelltod) und spielt somit eine Rolle bei Wachstum, Entwicklung, Gewebereparatur / Wundheilung und bei neurologischen Funktionen. Es ist auch am Lipid- und Glukosestoffwechsel sowie an der Immunität und der Reaktion auf Infektionen beteiligt (11).
Welche Vorerkrankungen und welche klinischen Symptome lassen an Zinkmangel denken?
Im Wesentlichen unterscheiden wir einen primären von einem sekundären Zinkmangel.
Die seltene primäre Acrodermatitis enteropathica (AE) ist eine autosomal rezessive Erkrankung, bei der die Zinkabsorption beeinträchtigt ist (12). Die AE ist durch Durchfall, Dermatitis, Alopezie, schlechtes Wachstum, Reizbarkeit und Lethargie und eine schlechte Immunfunktion gekennzeichnet, welche gewöhnlich nach dem Abstillen auftreten und unbehandelt zu Tod führen können. Die zeitlich unlimitierte hochdosierte orale Supplementation mit Zink (30 bis 45 mg pro Tag) führt zur Remission der Symptome.
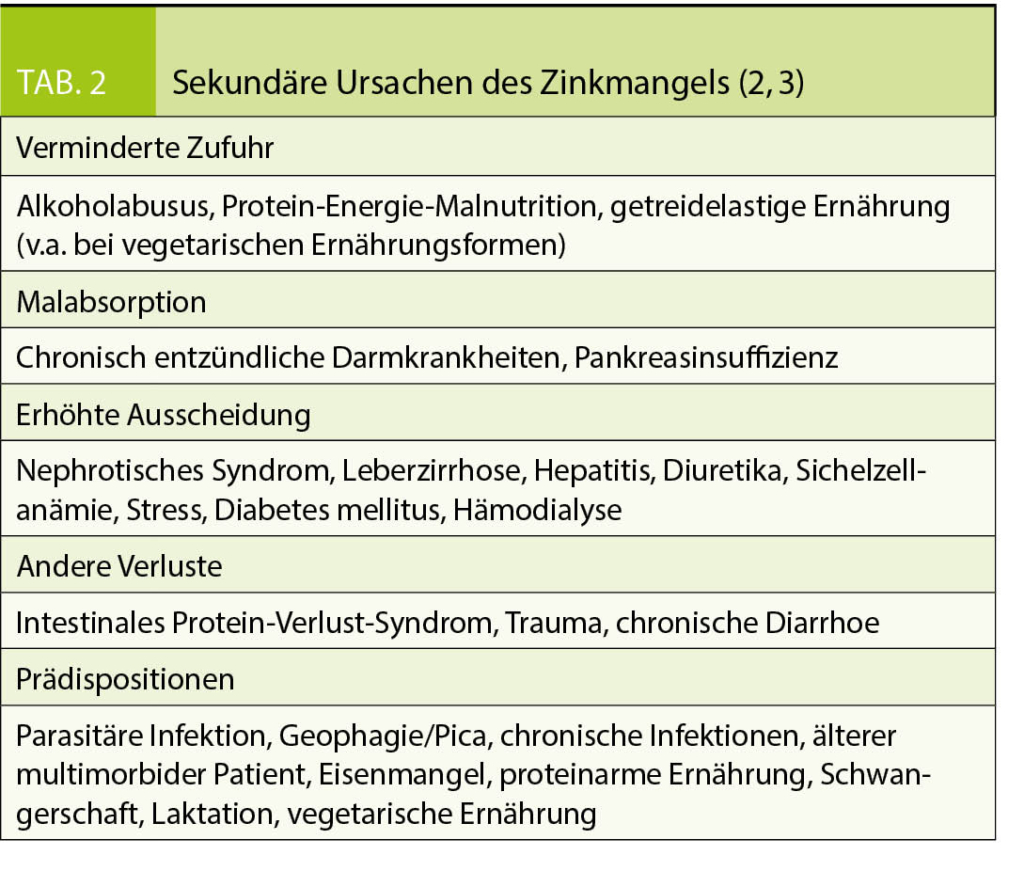
Sekundäre Ursachen für einen Zinkmangel sind bedingt durch verminderte Zufuhr, Malabsorption, erhöhte Ausscheidung und Verluste (Tab. 2).
Im klinischen Alltag können mit Zinkmangel assoziierte Symptome gehäuft bei chronischen Erkrankungen wie Malabsorptionssyndromen (wie z.B. chronisch entzündliche Darmerkrankungen) gefunden werden, nach Schwangerschaft und sehr langem Stillen. Eine verminderte Zinkabsorption und -speicherung sowie gelegentliche Fälle von symptomatischem Zinkmangel wurden auch bei Patienten nach Magenbypass infolge morbider Adipositas nachgewiesen (13). Patienten mit einer alkoholischen Zirrhose weisen häufig niedrige hepatische Zinkkonzentrationen auf.
Alle Formen von Mangelernährung können zu Zinkmangel führen. Im Rahmen einer Anorexia nervosa scheint eine wechselseitige negative Beeinflussung des Krankheitsverlaufs zu existieren, in dem die Fehlernährung zum Zinkmangel und dieser umgekehrt zu einer Überaktivierung des NMDA-Rezeptors führen kann. Dies führt zu hohen Glutamatspiegeln mit der Folge einer Störung der Synapsenbildung und der synaptischen Plastizität (14). Bei der Anorexie des alten Menschen mit schlechter Ernährungsqualität kann der ernährungsbedingte Zinkmangel durch Medikamente, die den Zinkverlust im Urin erhöhen, einschliesslich Thiazide, Schleifendiuretika und Angiotensin-Rezeptorblocker, zusätzlich akzentuiert werden (15).
In der orthomolekularen Medizin wird die sogenannte Kryptopyrrolurie als Ursache für einen kombinierten Zink- und Vitamin-B6-Mangel postuliert, die zu vielfältigen Symptomen von Nervensystem, Psyche, Augen, Verdauungsorgane und Bewegungsapparat führen sollen (16). Seit dem Nachweis, dass Kryptopyrrol im Urin gar nicht vorkommt, ist jedoch belegt, dass es keine Krankheit Kryptopyrrolurie gibt (17) und dementsprechend fehlen auch jegliche Studien dazu.
An klinischen Symptomen stehen dermatologische Veränderungen im Vordergrund, welche vor allem an den Extremitäten oder im Bereich von Körperöffnungen auftreten und häufig durch erythematöse, vesiculo-bullöse und pustulöse Läsionen gekennzeichnet sind. Weiter Haarausfall mit Veränderung der Haarfarbe und leichter Zupfbarkeit der Haare, Geruchs- und Geschmacksstörungen, die über Appetitverlust eine Mangelernährung verschlimmern können. Zinkmangel beeinträchtigt das Wachstum und kann zu verzögerter Geschlechtsreifung führen, zu Impotenz, Hypogonadismus, Oligospermie, Alopezie, Nachtblindheit. Zudem sind eine Immunschwäche mit Infektionsanfälligkeit und eine verzögerte Wundheilung von Bedeutung. Sowohl beim Typ 1- wie auch 2-Diabetes kann eine Hyperzinkurie vorliegen, die möglicherweise eine Rolle bei der mit Diabetes mellitus assoziierten Immundysfunktion spielt.
Beurteilung des Zinkstatus
Da die Plasmakonzentration von Zink nicht gut mit den Gewebespiegeln korreliert, können Personen mit Zinkmangel nicht zuverlässig identifiziert werden. Obwohl die Plasmakonzentration im Allgemeinen ein guter Index für den Zinkstatus bei gesunden Personen ist, ist sie bei entzündlichen Krankheitszuständen erniedrigt. Erythrozyten-Konzentrationen von Zink können ein nützlicheres Mass für den Zinkstatus während akuter oder chronischer Entzündungszustände liefern (18). Mehrere funktionelle Indizes können auch zur indirekten Beurteilung des Zinkstatus verwendet werden. Die Aktivität der alkalischen Phosphatase kann als unterstützender Marker für den Zinkstatus dienen (4). Da das meiste Zink an Albumin gebunden ist, kann die Plasmakonzentration bei Patienten mit Hypalbuminämie falsch tief sein (19).
In Anbetracht dieser Schwierigkeiten bewährt sich ein pragmatischer Ansatz zur Einschätzung eines Zinkmangels: typische Symptome eines Zinkmangels erkennen und anamnestisch erfassen, Messung der Serumzinkkonzentration zusammen mit dem CRP (als Mass für die Akutphasenreaktion, d.h. bei hohen CRP-Plasmakonzentrationen kann die Zinkplasmakonzentration falsch tief sein), «Bestätigung» durch einen tiefen Wert, Zinksupplementation mit Verschwinden der Symptome und Ansteigen der Serumzinkkonzentration. Angesichts des geringen Risikos einer Zinkersatztherapie kann eine solche je nach klinischem Kontext bei Patienten mit niedrigen Zinkspiegeln unabhängig vom Albuminstatus indiziert sein (19).
Potenzielle therapeutische Verwendung von Zink
Entzündungskrankheiten der Atemwege
Obwohl Zinkpräparate den Schweregrad und die Dauer der Symptome bei Erkältungen verringern können, ist deren Einsatz wegen unsicherer Vorteile und bekannter unerwünschter Wirkungen, insbesondere irreversibler Anosmie bei intranasaler Verabreichung, nicht empfohlen. In einem systematischen Review, der 17 Studien umfasste, reduzierte Zink zwar die Symptomdauer (mittlerer Unterschied -1,65 Tage, 95% CI -2,5 bis -0,8) bei Erwachsenen; es gab jedoch eine signifikante Heterogenität zwischen den Studien (20). Unerwünschte Wirkungen, einschliesslich schlechten Geschmacks und Übelkeit, waren in der Zink-Gruppe in allen Studien häufig.
Im Zusammenhang mit der COVID-19-Pandemie sind eine Reihe von Publikationen erschienen, die einen günstigen Effekt von Zink auf den Verlauf der Erkrankung hypothetisieren – einerseits infolge der bekannten Wirkung von Zink auf das Immunsystem; ein Bericht über 4 konsekutive Fälle beschreibt eine deutliche symptomatische Besserung innert 24 Stunden nach Beginn einer Therapie mit Zink in hoher Dosis (21). Und andererseits wegen möglicher Synergie bei der Behandlung von COVID-19 mit Chloroquin (22). Mangels eigentlicher Studien besteht aber keinerlei Evidenz für die postulierte günstige Wirkung von Zink.
Schlussendlich sei eine Meta-Analyse erwähnt, die bei schwer verlaufender Pneumonie eine signifikante Reduktion der Mortalität nachweisen konnte (23).
Altersbedingte Makuladegeneration
Zink scheint eine wichtige Rolle in der Pathogenese der altersbedingten Makuladegeneration (AMD) zu spielen. Dafür spricht, dass von AMD betroffene Retinabereiche hohe Zinkkonzentrationen aufweisen und im Alter der Zinkgehalt und die Aktivität einiger zinkabhängiger Enzyme in der Retina abnehmen (2). Die Frage, ob eine Zink Supplementation das Erkrankungsrisiko resp. die Krankheitsprogredienz einer AMD günstig beeinflussen könnte, wurde in verschiedenen Studien widersprüchlich beantwortet. In einer Cochrane-Analyse wurden fünf Placebo-kontrollierte Studien über den Einsatz von Zink in der Behandlung einer AMD zusammengestellt (24). Die Dauer der Supplementation und Nachsorge reichte von sechs Monaten bis zu sieben Jahren. Bei Personen, die Zinkpräparate einnehmen, war die Wahrscheinlichkeit eines Fortschreitens zu einer späten AMD (OR 0,83, 95% CI 0,70 bis 0,98; 3790 Patienten; 3 RCTs), zu einer neovaskulären AMD (OR 0,76, 95% CI 0,62 bis 0. 93; 2442 Patienten; 1 RCT) oder zu Visusverlust (OR 0,87, 95% CI 0,75 bis 1,00; 3791 Patienten; 2 RCTs) bei kleiner bis höchstens mässiger Evidenz um relativ 13 bis 24% reduziert, so dass der klinische Nutzen absolut im Vergleich zu den aktuellen Behandlungsmöglichkeiten kaum relevant sein dürfte.
Möglicher Einsatz in der Dermatologie
Zellwachstum, Zellvermehrung und Wundheilung sind direkt von Zink abhängig. Seit den frühen 1960er Jahren wurden immer wieder Versuche unternommen, die wundheilungsfördernde Wirkung von Zink nachzuweisen und es zeigte sich, dass eine systemische Zinksupplementation nur bei nachgewiesenem Zinkmangel erfolgreich ist (2). Die Datenlage ist insgesamt bescheiden. Eine Cochrane-Analyse fand in 6 kleineren Studien mit insgesamt 183 Patienten keinen Effekt einer oralen Zinksupplementation auf die Heilungsrate von arteriellen und venösen Beinulzera (25). Wird Zink aber lokal angewendet, kann mit einer hohen Zinkkonzentration im Wundgebiet gerechnet werden. Die topische Zinkapplikation führt zu einem «Autodebridement», ist antiinfektiös wirksam und unterstützt die Granulation und Epithelialisierung (2, 26). So wurde in einer Placebo-kontrollierten Studie nach einer Pilonidalsinusoperation die mittlere Heilungszeit von 62 um 8 auf 54 Tage reduziert, und nur 3 der lokal mit Zinkoxyd behandelten Patienten mussten mit Antibiotika behandelt werden gegenüber 12 unter Placebo (OR 0,16, % CI 0,03 bis 0,71, p = 0.007) (27). Weitere Studien bei topischer Applikation von Zink wären möglicherweise erfolgversprechender als die systemische Anwendung.
In einem Review-Artikel wurde kürzlich ein interessanter potenzieller Einsatz von Zink lokal vorgeschlagen: die Akne vulgaris. Sie ist eine chronische Erkrankung der Talgdrüsen, die sich als entzündliche oder nicht entzündliche Läsionen bei Personen jeden Alters zeigen kann. Die derzeitigen Standardbehandlungen können ein breites Spektrum an unerwünschten Wirkungen hervorrufen, darunter Trockenheit, Schälen, Erytheme und sogar fetale Defekte und embolische Ereignisse. Die Autoren kamen aufgrund der vorliegenden, leider insgesamt kleinen Studien zum Schluss, dass Zink gleich oder weniger wirksam war als orales Tetracyclin, gleich wirksam oder wirksamer als Erythromycin und Clindamycin und weniger wirksam als orales Minocyclin. Damit erwies sich topisches Zink als ebenbürtig mit Erythromycin und Clindamycin und könnte aufgrund seiner geringen Kosten, seiner Wirksamkeit und des Fehlens systemischer Nebenwirkungen eine vielversprechende Alternative zu anderen Aknebehandlungen darstellen (28).
Toxizität
Menschen sind tolerant gegenüber einer kurzfristigen hohen Zinkaufnahme von bis zu 100 mg/Tag (29). Mega-Dosis-Supplementierung oder hohe Zinkaufnahme aus kontaminierten Lebensmitteln oder Getränken wurde mit unspezifischen gastrointestinalen Symptomen wie Bauchschmerzen, Durchfall, Übelkeit und Erbrechen in Verbindung gebracht (10). Zink kann die Kupferabsorption stören, und eine hohe Zinkaufnahme (> 150 mg/Tag) kann zu Kupfermangel führen (8), was für die Behandlung der Wilson-Krankheit ausgenutzt werden kann. Als oberer Wert einer langfristig sicheren Gesamtzufuhr aus Nahrung und Supplementen gilt eine Aufnahme von 25 mg/Tag Zink.
Zusammenfassend
kann für Zink wie für Vitamine und andere Spurenelemente die Erkenntnis gewonnen werden, dass ein Mangel diverse Körperfunktionen und damit den Gesundheitszustand gefährdet und deshalb detektivisch gesucht, identifiziert und mit geeignetem Ersatz behoben werden soll. Hingegen besteht zu wenig Evidenz für einen therapeutischen Einsatz bei Personen mit normalem Zinkbestand.
Facharzt FMF Innere Medizin und Gastroenterologie
Neuhausstrasse 18
8044 Zürich
Schulthess_hk@swissonline.ch
Der Autor hat in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
1. Gibson RS, Raboy V, King JC. Implications of phytate in plant-based foods for iron and zinc bioavailability, setting dietary requirements, and formulating programs and policies. Nutr Rev 2018;76:793–804.
2. Imoberdorf R, Rühlin M, Ballmer PE. Zink ein lebensnotwendiges Spurenelement mit viel Potential. Swiss Med Forum 2010;10.
3. Suter PM. Checkliste Ernährung: 203 Tabellen. 3rd ed. Checklisten der aktuellen Medizin. Stuttgart: Thieme; 2008. 435 p.
4. Institute of Medicine. DRI: Dietary reference intakes for vitamin A, vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc : a report of the Panel on Micronutrients … and the Standing Committee on the Scientific Evaluation of Dietary Reference Intakes, Food and Nutrition Board, Institute of Medicine. Washington, D.C: National Academy Press; 2010. 773 p.
5. Briefel RR, Bialostosky K, Kennedy-Stephenson J, et al. Zinc intake of the U.S. population: findings from the third National Health and Nutrition Examination Survey, 1988-1994. J Nutr 2000;130:1367S-73S.
6. Prasad AS. Zinc deficiency. BMJ 2003;326:409–410.
7. Keller U, Beer M, editors. Sechster schweizerischer Ernährungsbericht. Bern, s.l.: Bundesamt für Gesundheit; 2012. 302 p.
8. Sturniolo GC, Mestriner C, Irato P, et al. Zinc therapy increases duodenal concentrations of metallothionein and iron in Wilson’s disease patients. Am J Gastroenterol 1999;94:334–338.
9. Foster M, Chu A, Petocz P, et al. Effect of vegetarian diets on zinc status: a systematic review and meta-analysis of studies in humans. J Sci Food Agric 2013;93:2362–2371.
10. Ross AC, editor. Modern nutrition in health and disease. 11th ed. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins; 2014. 1616 p.
11. Olechnowicz J, Tinkov A, Skalny A, et al. Zinc status is associated with inflammation, oxidative stress, lipid, and glucose metabolism. J Physiol Sci 2018;68:19–31.
12. Küry S, Dréno B, Bézieau S, et al. Identification of SLC39A4, a gene involved in acrodermatitis enteropathica. Nat Genet 2002;31:239–240.
13. Ruz M, Carrasco F, Rojas P, et al. Zinc absorption and zinc status are reduced after Roux-en-Y gastric bypass: a randomized study using 2 supplements. The American journal of clinical nutrition 2011;94:1004–1011.
14. Hermens DF, Simcock G, Dutton M, et al. Anorexia nervosa, zinc deficiency and the glutamate system: The ketamine option. Prog Neuropsychopharmacol Biol Psychiatry 2020;101:109921.
15. Macdonald JB, Connolly SM, DiCaudo DJ. Think zinc deficiency: acquired acrodermatitis enteropathica due to poor diet and common medications. Arch Dermatol 2012;148:961–963.
16. Stute P, Kohl J, Knes O. Das Chamäleon Kryptopyrrolurie. J. Gynäkol. Endokrinol. CH 2020;224:811.
17. Kinkeldei J. Kryptopyrrol, ein vergessener, aber wichtiger Laborparameter? / Kryptopyrrole: a forgotten but important diagnostic parameter? LaboratoriumsMedizin 2010;34:223–226.
18. Oakes EJC, Lyon TDB, Duncan A, et al. Acute inflammatory response does not affect erythrocyte concentrations of copper, zinc and selenium. Clin Nutr 2008;27:115–120.
19. Himoto T, Masaki T. Associations between Zinc Deficiency and Metabolic Abnormalities in Patients with Chronic Liver Disease. Nutrients 2018;10.
20. Science M, Johnstone J, Roth DE, et al. Zinc for the treatment of the common cold: a systematic review and meta-analysis of randomized controlled trials. CMAJ 2012;184:E551-61.
21. Finzi E. Treatment of SARS-CoV-2 with high dose oral zinc salts: A report on four patients. Int J Infect Dis 2020.
22. Shittu MO, Afolami OI. Improving the efficacy of Chloroquine and Hydroxychloroquine against SARS-CoV-2 may require Zinc additives – A better synergy for future COVID-19 clinical trials. Infez Med 2020;28:192–197.
23. Wang L, Song Y. Efficacy of zinc given as an adjunct to the treatment of severe pneumonia: A meta-analysis of randomized, double-blind and placebo-controlled trials. Clin Respir J 2018;12:857–864.
24. Evans JR, Lawrenson JG. Antioxidant vitamin and mineral supplements for slowing the progression of age-related macular degeneration. Cochrane Database Syst Rev 2017;7:CD000254.
25. Wilkinson EAJ. Oral zinc for arterial and venous leg ulcers. Cochrane Database Syst Rev 2014:CD001273.
26. Lansdown ABG, Mirastschijski U, Stubbs N, et al. Zinc in wound healing: theoretical, experimental, and clinical aspects. Wound Repair Regen 2007;15:2–16.
27. Agren MS, Ostenfeld U, Kallehave F, et al. A randomized, double-blind, placebo-controlled multicenter trial evaluating topical zinc oxide for acute open wounds following pilonidal disease excision. Wound Repair Regen 2006;14:526–535.
28. Cervantes J, Eber AE, Perper M, et al. The role of zinc in the treatment of acne: A review of the literature. Dermatol Ther 2018;31.
29. Wastney ME, Ahmed S, Henkin RI. Changes in regulation of human zinc metabolism with age. Am J Physiol 1992;263:R1162-8.