Die Häufigkeit von Schwangerschaften mit Herz-Kreislauf-Erkrankungen betreffen etwa 1-4% in der Schweiz und ist sowohl bei Frauen mit angeborenen Herzfehlern wie auch mit erworbenen Herzkrankheiten zunehmend (1). Die häufigsten kardialen peri- und postpartalen Manifestationen sind Arrhy-thmien und Herzinsuffizienz, seltener Myokardinfarkt oder Aortendissektion (2, 3).
Die Diagnose kardialer Erkrankungen während der Schwangerschaft kann eine Herausforderung sein, weil die Überlappung von kardiovaskulären Symptomen mit denen einer normalen Schwangerschaft sowohl Diagnosestellung wie auch den Beginn einer zeitgerechten und adäquaten Therapie verzögern kann (4). Dieser Artikel beinhaltet die Darlegung der physiologischen Veränderungen des Kreislaufs während der Schwangerschaft, bespricht die Risikostratifizierung von Frauen mit und ohne vorbestehende Herzkrankheiten und zeigt einen praktischen Algorithmus zur Diagnosefindung während der Schwangerschaft.
Physiologische Veränderungen des Kreislaufs in der Schwangerschaft
Hämodynamische Veränderungen
Antepartum. Wegen des Anstiegs von Östrogen und Progesteron und der Aktivierung des Renin-Angiotensin-Aldosteron Systems verursacht die Schwangerschaft einen kontinuierlichen Anstieg der Herzleistung und des Plasma-Volumens sowie eine Abnahme des mütterlichen systemischen Gefässwiderstandes (5). Der Blutdruck nimmt zunächst ab, steigt aber im dritten Trimester an (6).
Intra- und postpartum. Während und nach der Geburt kommt es zu dramatischen Veränderungen von Herzleistung, Herzfrequenz, Blutdruck und Plasmavolumen (7).
Obwohl Herzfrequenz und Blutdruck normalerweise innerhalb von 48 Stunden nach der Geburt sinken, kann der Blutdruck aufgrund von Flüssigkeitsverschiebungen zwischen den Tagen 3-6 postpartum steigen. Während dieses Zeitraums treten hypertensive Komplikationen und solche die mit einer Volumenbelastung zusammenhängen gehäuft auf (8). Der erhöhte hydrostatische Druck und der verringerte kolloidale osmotische Druck erhöhen zudem das Risiko eines Lungenödems bei Frauen mit Herzinsuffizienz oder Präeklampsie. Die mütterliche Hämodynamik kehrt normalerweise 3-6 Monate nach der Entbindung in den Zustand vor der Schwangerschaft zurück.
Strukturelle Veränderungen
Die Herzkammern passen sich während der Schwangerschaft an die Zunahme des Plasma-Volumens an. Das enddiastolische Volumen des linken Ventrikels steigt um etwa 10% (9).
Daten über die Auswurffraktion während der Schwangerschaft sind widersprüchlich (9, 10). Bei ungefähr 20% der Schwangeren besteht eine diastolische Dysfunktion, was während der Schwangerschaft zu Belastungsdyspnoe führen kann (11). Auch die strukturellen Veränderungen des gesunden mütterlichen Herzens kehren innerhalb 12 Monaten zum Ausgangswert zurück.
Hämatologische und metabolische Veränderungen
Hämatologische und metabolische Veränderung sowie ein Ungleichgewicht des Gerinnungssystems sind wichtige Faktoren für das kardiovaskuläre Risiko während der Schwangerschaft. Der überproportionale Anstieg des Plasma-Volumens im Vergleich zu den Erythrozyten führt zu einer physiologischen Anämie durch Hämodilution. Dies kann eine asymptomatische Herzinsuffizienz oder Myokardischämie demaskieren; und deshalb sollten die Hämatokrit-Werte jedes Trimenon kontrolliert werden.
Das erhöhte Thromboembolie-Risiko während der Schwangerschaft basiert auf einer Hyperkoagulabilität, einer venösen Stase, einer Kompression der unteren Hohlvene und Beckenvenen durch die sich vergrössernde Plazenta und auf einer verringerten Mobilität (12). Die Schwangerschaft hat auch einen Einfluss auf die Gerinnungsfaktoren, was sich insbesondere bei bestimmten Erkrankungen wie das Antiphospholipid-Syndrom negativ auswirken kann. Rauchen erhöht das Thromboserisiko in der Schwangerschaft zusätzlich.
Risikofaktoren für kardiovaskuläre Erkrankungen in der Schwangerschaft
Die Risikostratifizierung für kardiale Komplikationen in der Schwangerschaft unterscheidet sich bei Frauen mit und ohne vorbestehende Herzkrankheiten:
Bei Frauen ohne bekannte Herz-Kreislauf-Erkrankungen konnten vier Hauptrisikofaktoren evaluiert werden, welche die kardiovaskulär bedingte Sterblichkeit während der Schwangerschaft erhöhen:
1. Alter: Frauen über 40 Jahren haben eine 30-fach erhöhtes kardial bedingtes Sterblichkeitsrisiko im Vergleich zu Frauen unter 20 Jahren (13).
2. Rasse/Ethnizität: Schwarze Frauen haben ein 3-4-fach erhöhtes kardial bedingtes Sterblichkeitsrisiko im Vergleich zu weissen Frauen (14). Diese Daten wurden in den USA erhoben und sind teilweise durch strukturelle und soziale Probleme zu erklären.
3. Bluthochdruck: Hypertensive Erkrankungen betreffen bis zu 10% der Schwangerschaften und können zu mütterlicher Morbidität und Mortalität beitragen. Hypertensive Komplikationen während der Schwangerschaft tragen auch zu einem erhöhten kardiovaskulären Risiko nach der Schwangerschaft bei. So ist bei Frauen mit einer hypertensiven Komplikation während der Schwangerschaft die Inzidenz eines Myokardinfarktes 13-fach und die einer Herzinsuffizienz 8-fach höher im Langzeitverlauf als bei gesunden Frauen (15).
4. Adipositas: Die kardial bedingte Sterblichkeit erhöht sich bei adipösen Frauen, insbesondere in Assoziation mit einem obstruktiven Schlaf-Apnoe Syndrom.
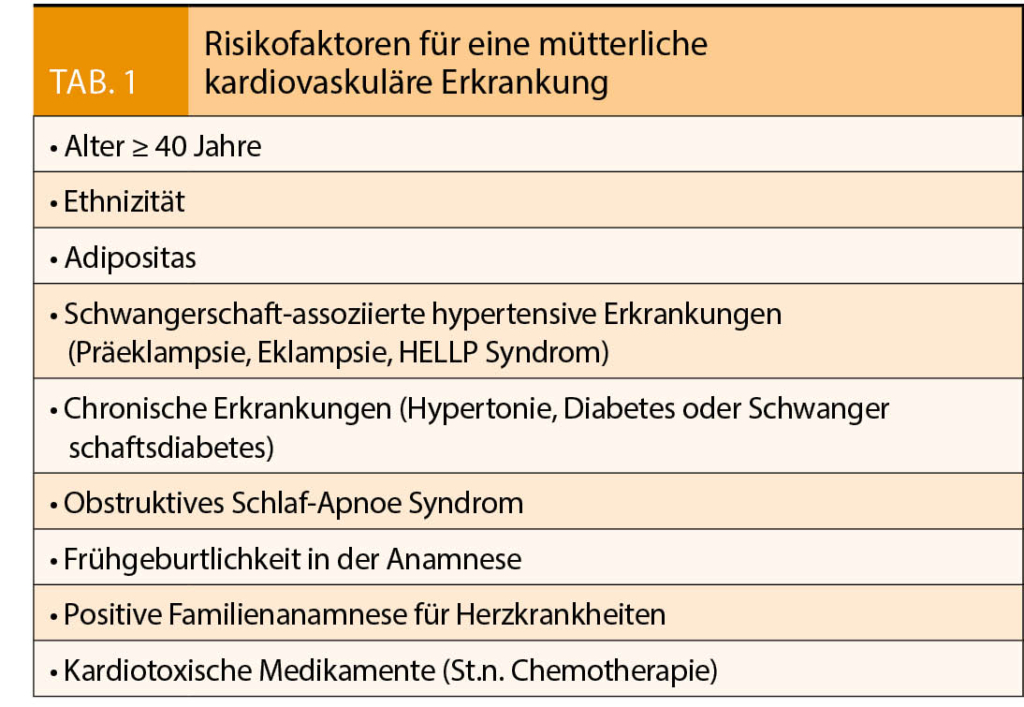
Bei Vorhandensein einer oder mehrerer dieser Risikofaktoren sollte während der Schwangerschaft ein Risikoscreening durchgeführt werden. Die Risikofaktoren für eine mütterliche kardiale Erkrankung sind in Tabelle 1 aufgelistet.
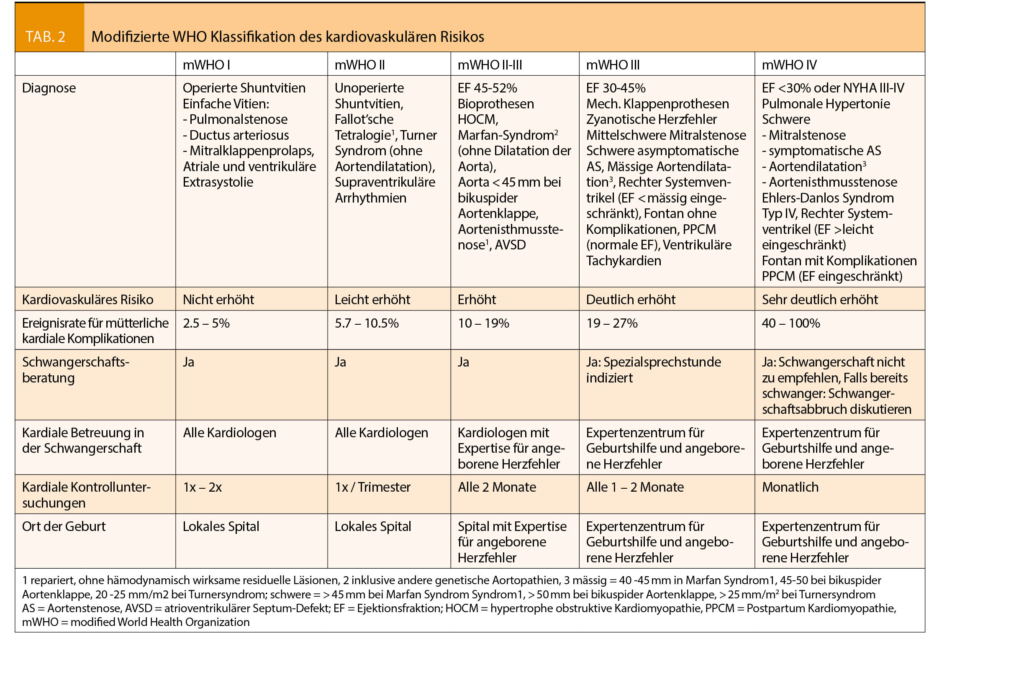
Frauen mit bekannten Herz-Kreislauf-Erkrankungen sollten idealerweise vor der Schwangerschaft, spätestens aber so früh wie möglich während der Schwangerschaft kardiologisch beurteilt werden. Dabei muss eine genaue Diagnose gestellt und die Auswirkungen der Schwangerschaft auf die zugrunde liegende Herz-Kreislauf-Erkrankung benennt sowie die potenziellen Risiken für die Frau und den Fötus abgeschätzt werden. Hilfreich ist dabei die Tabelle der modifizierten WHO Schwangerschafts-Risiko-Klassifizierung (Tab. 2). Schwangere mit einem WHO-Risiko II-III und höher bedürfen auf Grund des erhöhten Morbiditäts- und Mortalitätsrisikos einer interdisziplinären Konsultation sowie Betreuung und Geburt an einem Zentrumsspital.
Kardiale Symptome und deren Abklärungen in der Schwangerschaft
Symptome von Herzkrankheiten
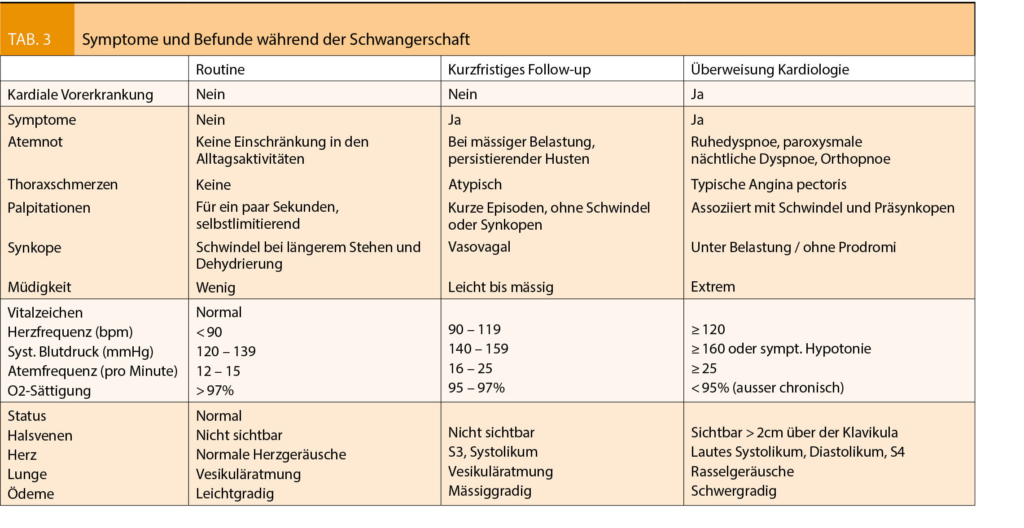
Symptome und klinische Befunde einer normalen Schwangerschaft können sich mit denen einer symptomatischen Herzerkrankung überschneiden. Um eine zugrunde liegende Herzerkrankung frühzeitig zu erkennen, müssen diese Zeichen von den Fachkräften erkennt werden. Ein frühzeitiges Erkennen und somit der frühzeitige Beginn einer adäquaten Therapie ist der wichtigste Schritt für eine verbesserte Prognose. Tabelle 3 listet die wichtigsten Symptome und Befunde auf und hilft zur weiteren Differenzierung (16).
Klinisches Assessment bei kardiovaskulären Symptomen in der Schwangerschaft
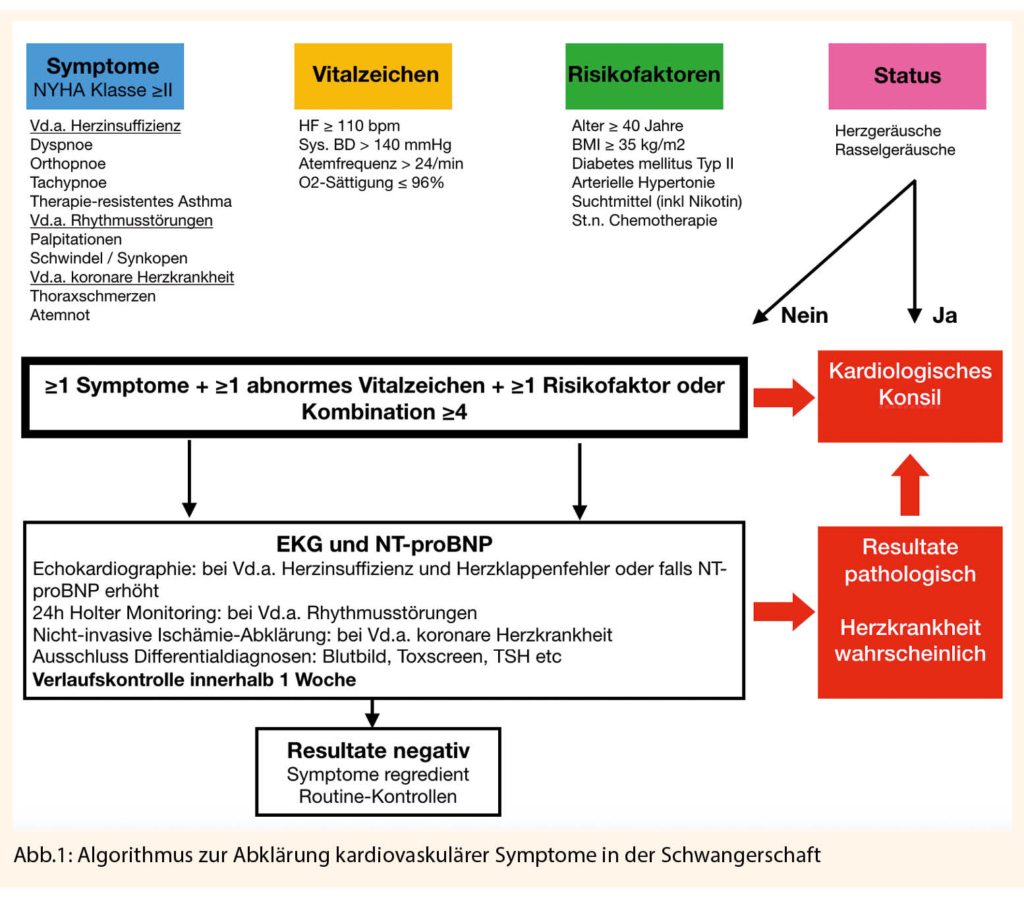
Alle Schwangeren mit vorbekannten Herzkrankheiten sowie Schwangere mit kardiovaskulären Symptomen (Kurzatmigkeit, Brustschmerzen oder Herzklopfen) brauchen ein kardiologisches Assessment. Abbildung 1 zeigt einen praktischen Algorithmus zur Abklärung von kardiovaskulären Symptomen in der Schwangerschaft (modifiziert von: California Department of Public Health, 2017).
Zusätzlich zu einer ausführlichen Anamnese (inklusive Familien- und Sozialanamnese) und einem kardiovaskulären Status stehen verschiedene diagnostische Hilfsmittel zur Verfügung:
NT-proBNP eignet sich in der Schwangerschaft sehr gut zur weiteren Diagnostik bei symptomatischen Patienten. Obwohl NT-proBNP in der Schwangerschaft ansteigt, übersteigt es bei herzgesunden Patienten die Normwerte nicht (17). Erhöhte NT-proBNP Werte bei Dyspnoe in der Schwangerschaft sind Hinweise für eine Herzinsuffizienz im Rahmen einer systolischen und/oder diastolischen Dysfunktion aber auch im Rahmen von hypertensiven Erkrankungen inklusive Präeklampsie (18, 19, 20). Deshalb sind bei Frauen mit vorbekannten Herzkrankheiten oder mit Risiko für kardiovaskuläre Krankheiten Messungen von NT-proBNP im ersten Trimenon als Baseline-Untersuchung sinnvoll.
Die Wertigkeit von hs-Troponin in der Schwangerschaft im Rahmen eines akuten Koronarsyndroms ist vergleichbar zu nicht schwangeren Frauen (21). Deshalb sollte hs-Troponin bei akuten Thoraxschmerzen immer bestimmt werden. Zu beachten ist jedoch, dass hs-Troponin in gewissen Situationen wie Präeklampsie, akuter Lungenembolie und bei Niereninsuffizienz erhöht sein kann. Die Bestimmung von D-Dimeren bei akuter Dyspnoe zum Ausschluss einer Lungenembolie ist in der Schwangerschaft wegen der tiefen Spezifizität nicht empfohlen. Ein EKG sollte bei allen Schwangeren mit Palpitationen, Herzrasen, Schwindel, Dyspnoe und Thoraxschmerzen durchgeführt werden. Bei pathologischem EKG muss eine kardiologische Standortbestimmung erfolgen (siehe Abb. 1). Bildgebende Diagnostik sollte individuell in Absprache nach kardiologischer Standortbestimmung erfolgen.
Copyright bei Aerzteverlag medinfo AG
Oberarzt Kardiologie
Leiter angeborene Herzfehler
Universitätsspital Basel
Petersgraben 4
4031 Basel
daniel.tobler@usb.ch
Der Autor hat keine Interessenkonflikte in Zusammenhang mit diesem Artikel.
1. Elkayam, U., et al., High-Risk Cardiac Disease in Pregnancy: Part I. J Am Coll Cardiol, 2016. 68(4): p. 396-410.
2. Curry, R., L. Swan, and P.J. Steer, Cardiac disease in pregnancy. Curr Opin Obstet Gynecol, 2009. 21(6): p. 508-13.
3. Fett, J.D., Peripartum cardiomyopathy: challenges in diagnosis and management. Expert Rev Cardiovasc Ther, 2016. 14(9): p. 1035-41.
4. Hameed, A.B., et al., Pregnancy-related cardiovascular deaths in California: beyond peripartum cardiomyopathy. Am J Obstet Gynecol, 2015. 213(3): p. 379 e1-10.
5. Sanghavi, M. and J.D. Rutherford, Cardiovascular physiology of pregnancy. Circulation, 2014. 130(12): p. 1003-8.
6. Shen, M., et al., Trajectory of blood pressure change during pregnancy and the role of pre-gravid blood pressure: a functional data analysis approach. Sci Rep, 2017. 7(1): p. 6227.
7. Kuhn, J.C., R.S. Falk, and E. Langesaeter, Haemodynamic changes during labour: continuous minimally invasive monitoring in 20 healthy parturients. Int J Obstet Anesth, 2017. 31: p. 74-83.
8. Sibai, B.M., Etiology and management of postpartum hypertension-preeclampsia. Am J Obstet Gynecol, 2012. 206(6): p. 470-5.
9. Savu, O., et al., Morphological and functional adaptation of the maternal heart during pregnancy. Circ Cardiovasc Imaging, 2012. 5(3): p. 289-97.
10. Melchiorre, K., et al., Maternal Cardiovascular Function in Normal Pregnancy: Evidence of Maladaptation to Chronic Volume Overload. Hypertension, 2016. 67(4): p. 754-62.
11. Goland, S., et al., Shortness of Breath During Pregnancy: Could a Cardiac Factor Be Involved? Clin Cardiol, 2015. 38(10): p. 598-603.
12. ACOG Practice Bulletin No. 196: Thromboembolism in Pregnancy: Correction. Obstet Gynecol, 2018. 132(4): p. 1068.
13. James, A.H., et al., Acute myocardial infarction in pregnancy: a United States population-based study. Circulation, 2006. 113(12): p. 1564-71.
14. Creanga, A.A., et al., Pregnancy-Related Mortality in the United States, 2011-2013. Obstet Gynecol, 2017. 130(2): p. 366-373.
15. Melchiorre, K., R. Sharma, and B. Thilaganathan, Cardiovascular implications in preeclampsia: an overview. Circulation, 2014. 130(8): p. 703-14.
16. Thorne, S., Pregnancy and native heart valve disease. Heart, 2016. 102(17): p. 1410-7.
17. Mayama, M., et al., Factors influencing brain natriuretic peptide levels in healthy pregnant women. Int J Cardiol, 2017. 228: p. 749-753.
18. McCullough, P.A., et al., B-type natriuretic peptide and clinical judgment in emergency diagnosis of heart failure: analysis from Breathing Not Properly (BNP) Multinational Study. Circulation, 2002. 106(4): p. 416-22.
19. Kampman, M.A., et al., N-terminal pro-B-type natriuretic peptide predicts cardiovascular complications in pregnant women with congenital heart disease. Eur Heart J, 2014. 35(11): p. 708-15.
20. Resnik, J.L., et al., Evaluation of B-type natriuretic peptide (BNP) levels in normal and preeclamptic women. Am J Obstet Gynecol, 2005. 193(2): p. 450-4.
21. Shade, G.H., Jr., et al., Troponin I in the diagnosis of acute myocardial infarction in pregnancy, labor, and post partum. Am J Obstet Gynecol, 2002. 187(6): p. 1719-20.