L’ érysipèle est caractérisé par un érythème clairement délimité, ne touchant que l’ épiderme et le derme, accompagné de fièvre, de lymphangite et de douleur. Divers facteurs de risque, notamment le lymphœdème, peuvent entraîner un érysipèle chronique récurrent. Le traitement conséquent des facteurs de risque peut minimiser le risque de récidive. Pour ce faire, il est nécessaire de reconnaître les diagnostics différentiels potentiels. Le traitement comprend une thérapie au stade aigu et éventuellement une prophylaxie à long terme.
Environ 10 % des patients atteints d’ érysipèle aigu ont une récidive dans les 6 mois et 30 % dans les 3 ans (1). Les personnes âgées sont les plus touchées. Les chiffres exacts sur la répartition par sexe ne sont pas disponibles. Une distribution saisonnière avec une incidence accrue en été peut être observée (2). En fonction des facteurs de risque présents, les régions du corps prédisposées sont les parties inférieures des jambes, les pieds, et les bras, mais n’ importe quelle partie de la peau peut être affectée. Les facteurs de risque sous-jacents ne concernent généralement pas le visage et la tête. Lors d’ une première infection, l’ érysipèle se manifeste souvent dans la région tibiale, alors qu’ en cas de récidives ce sont surtout les pieds qui sont affectés (2). Il n’ existe cependant actuellement pas de données complètes concernant ce phénomène.
Etiopathogénie
Facteurs de risque
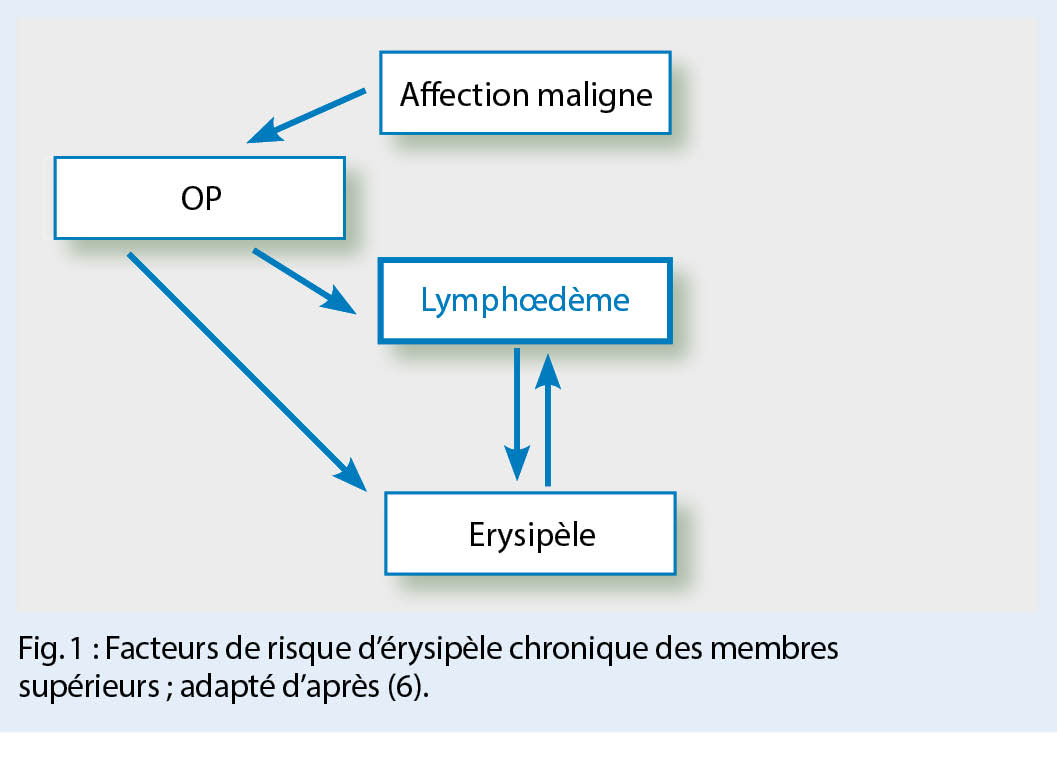
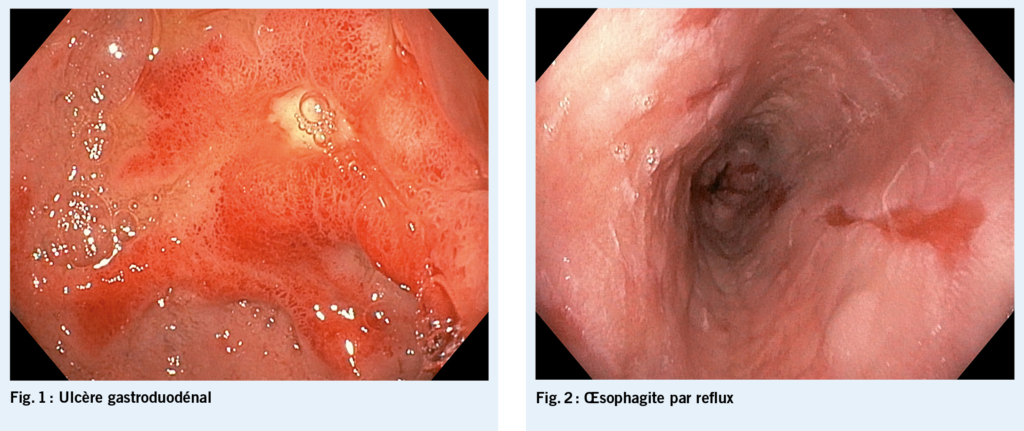
Une barrière cutanée perturbée, comme dans la dermatite de stase, une onychomycose et la dermatomyosite, peut constituer un point d’ entrée pour une récidive de l’ érysipèle. Les lésions facilitent l’ invasion bactérienne des tissus (3). Le facteur prédictif le plus important de récidive de l’ érysipèle est la présence d’ un lymphœdème chronique (1). Des érysipèles à répétition entraînent des lésions progressives et irréversibles des vaisseaux lymphatiques. L’ œdème riche en sérum qui en résulte constitue donc un risque supplémentaire de récidive. Les troubles du flux lymphatique peuvent aussi être causés par des lésions des vaisseaux lymphatiques dues à des infections, une radiothérapie et des interventions chirurgicales. Ces dernières comprennent, par exemple, la lymphadénectomie en cas de maladie tumorale et la saphénectomie en cas de pontage. En outre, la neuropathie chez les diabétiques, l’ insuffisance veineuse chronique et l’ obésité sont également des facteurs de risque. En particulier, le diabète sucré est considéré comme un facteur favorisant la fasciite nécrosante (4). Très rarement, des immunodéficiences primaires peuvent contribuer à la pathogenèse de l’ érysipèle récurrent. En fin de compte, le lymphœdème reste le facteur déterminant pour le développement d’ un érysipèle récurrent (fig. 1).
Facteurs de protection
Il est intéressant de noter que les patients atteints de BPCO sont moins susceptibles de présenter un érysipèle récurrent (6). Une explication possible pourrait être les antibiothérapies fréquentes pour le traitement des infections pulmonaires.
Agent pathogène
L’ agent pathogène le plus fréquent dans l’ érysipèle est le streptocoque bêta-hémolytique du groupe A (Streptococcus pyogenes). Les streptocoques du groupe C, G ou B font également partie du spectre pathogène. Ces derniers se produisent principalement chez les patients atteints de diabète sucré, lors d’ une chirurgie tumorale et après une radiation. Chez les patients immunosupprimés, les germes gram-négatifs tels que Pseudomonas aeruginosa et Escherichia coli jouent également un rôle. Le staphylocoque doré peut provoquer un tableau clinique similaire et est l’ agent pathogène le plus courant dans la cellulite, également fréquemment détecté dans le phlegmon (6).
Diagnostic
Présentation clinique et diagnostic
Le diagnostic est posé cliniquement. La triade typique de l’ érysipèle comprend l’ érythème, la fièvre et la lymphadénite. L’ érysipèle récurrent présente un tableau clinique moins prononcé avec une rougeur discrète et une hyperthermie, ainsi que des modifications mineures de la formule sanguine. Ceci est dû notamment à des modifications cutanées préexistantes comme dans l’ insuffisance veineuse chronique, le lymphœdème et les dermatoses telles que l’ intertrigo et la mycose des pieds (Tinea pedis). Les hémocultures sont systématiquement recommandées. L’ obtention de biopsies ou de matériel d’ aspiration des lésions ne fournit souvent pas de preuve culturelle de l’ agent pathogène. Les tests de résistance sont utiles en présence de staphylocoques dorés, en particulier en cas de suspiçion d’ un staphylocoque doré résistant à la méthicilline (4). Une biopsie ou un prélèvement par aspiration doit être effectué principalement chez les personnes immunodéprimées, en cas de lésions dues à des morsures d’ animaux ou en cas de staphylocoques dorés résistant à la méthicilline (5).
Complications
Un traitement inadéquat ou l’ absence de traitement de l’ érysipèle, ainsi que les facteurs de risque sous-jacents, peuvent entraîner une récidive de l’ érysipèle. Des complications surviennent chez environ 25 à 31 % (6) des patients. L’ incidence croissante des récidives entraîne des lésions irréversibles des vaisseaux lymphatiques, qui sont également considérées comme le facteur prédictif le plus important de la récidive. Les complications dermatologiques comprennent la sclérose, les modifications pigmentaires et la pachydermie. D’ autres conséquences peuvent être l’ éléphantiasis inflammatoire, l’ insuffisance veineuse, les abcès et la propagation des infections (septicémie, ostéomyélite, arthrite, tendinite septique).
Diagnostics différentiels
Pour poser un diagnostic correct, il est important de connaître les tableaux cliniques semblables. Les diagnostics erronés les plus courants sont la dermatite de stase aiguë et les piqûres d’ insectes sévères (7).
L’ érysipèle est une infection cutanée superficielle limitée à l’ épiderme et au derme. La cellulite, par contre, touche également les tissus sous-cutanés. Cliniquement, il est souvent impossible de distinguer l’ érysipèle de la cellulite, surtout dans les premiers stades. Par conséquent, on utilisera généralement des antibiotiques qui sont également efficaces contre le staphylocoque doré (4).
- Dermatite de stase aiguë : la zone érythémateuse est moins brillante et touche généralement les deux jambes. Elle s’ accompagne d’ un œdème qui peut être enfoncé plus profondément et d’ une dermatoliposclérose palpable. En présence d’ un lymphœdème, l’ œdème aigu récurrent de stase est une cause fréquente d’ erysipèle. Le diagnostic différentiel avec l’ érysipèle est difficile mais important pour éviter l’ administration inutile d’ antibiotiques.
- Réaction aux piqûres d’ insectes : après certaines piqûres de moustiques, un érythème brillant avec des extensions en forme de langue peut apparaître en quelques heures, plus rapidement que dans l’ érysipèle. La symptomatologie générale est légère.
- Fièvre méditerranéenne périodique : l’ érythème récurrent peut ressembler de près au tableau de l’ érysipèle. Les symptômes d’ accompagnement comprennent la fièvre, des symptômes arthritiques, péritonitiques et pleuraux.
- Erythème migrant : l’ érythème pâle indolore, nettement délimité, à propagation centrifuge, n’ a pas d’ extension et est moins aigu que l’ érysipèle.
- Dermatite de contact : après contact, un érythème prurigineux et nettement délimité apparaît en quelques heures. Il n’ y a pas de symptômes généraux.
- Herpès zoster : au stade initial, la douleur est importante. Au cours de la maladie, des vésicules apparaissent et la propagation est limitée à un dermatome, contrairement à l’ érysipèle.
- Erysipéloïde : les localisations sont souvent les mains et les doigts après contact avec la volaille, les porcs et les animaux marins. Au début, il y a une plaque rouge-livide plate et, au fur et à mesure de son évolution, un éclaircissement central avec un bord livide nettement délimité. Le diagnostic se fait par voie microbiologique ou histologique.
- Thrombophlébite : l’ induration douloureuse en forme de cordon peut être la cause de l’ érysipèle.
Erysipela carcinomatosum : le tableau clinique d’infiltration dure ne survient pas de manière aiguë. - Lymphangite aigüe : elle se caractérise par une rougeur linéaire le long d’ un trajet lymphatique, généralement sans symptômes généraux prononcés.
Traitement
Les patients ont besoin d’ une thérapie interdisciplinaire. L’ accent est mis sur le traitement des facteurs déclenchants afin de garantir une barrière cutanée et des tissus mous intacts. Cela permet une utilisation ciblée des antibiotiques et le maintien d’ un microbiome intact. Les mesures non pharmacologiques ont une importance capitale dans le traitement de l’ érysipèle récurrent.
Thérapie non-médicamenteuse
La mesure la plus importante est le traitement du site d’ entrée, comme la mycose des pieds, et les bons soins de la peau. Un traitement des troubles du drainage lymphatique est nécessaire. Le traitement par compression avec des bandages élastiques, le drainage lymphatique manuel ou par appareil sont importants. En raison du risque de propagation de l’ infection, le drainage lymphatique en cas d’ inflammation active ne doit être effectué que sous traitement antibiotique.
Traitement aigu
Au stade aigu, une antibiothérapie par amoxicilline/acide clavulanique 3 x 625 mg/jour est indiquée. La décision d’ opter pour un traitement oral ou intraveineux dépend de la gravité de l’ infection et des comorbidités existantes. En cas d’ allergie à la pénicilline, on utilisera la clindamycine 3 x 300 mg/jour par voie orale ou 3 x 600 mg/jour par voie intraveineuse (4).
Durée du traitement
La durée recommandée du traitement au stade aigu est de 5 à 7 jours.
Prophylaxie
L’ assainissement du site d’ entrée et le traitement des facteurs prédisposants sont les éléments les plus importants.
Récidive
Après l’ évaluation des risques, le patient reçoit des instructions exceptionnelles pour une mise en route rapide et indépendante des antibiotiques.
Evaluation des risques de l’ antibioprophylaxie
La prophylaxie antibiotique intermittente diminue le nombre de récidives mais ne doit être administrée qu’ après consultation d’ un spécialiste des maladies infectieuses. Compte tenu des données contradictoires, elle nécessite une évaluation minutieuse des risques et bénéfices. Des études montrent le bénéfice d’ une antibiothérapie à long terme surtout après la première récidive, d’ autres études décrivent un bénéfice après 3-4 récidives (5, 8).
Une prophylaxie à long terme peut être administrée avec la pénicilline V (phénoxyméthylpénicilline) 250 mg 2x/jour per os (5, 9, 10). En prophylaxie, l’ administration perorale est indiquée et mieux prouvée que le traitement parentéral (11). Lors de problèmes d’ observance thérapeutique, un traitement intramusculaire de 2 à 3 semaines par benzylpénicilline-benzathine (Tardocillin®) est recommandé. Si aucune récidive n’ est survenue après 6 mois, l’ intervalle peut être prolongé (11, 12). Il n’ existe pas de benzylpenicilline benzathine dépôt en Suisse, la substance doit donc être importée de l’ étranger, par exemple la Tardocilline®, qui est fabriquée en Allemagne. Aucune autorisation spéciale n’ est requise pour l’ utilisation en Suisse de préparations autorisées par l’ UE. La pénicilline G benzathine peut être commandée auprès des pharmacies hospitalières ou des pharmacies internationales. En cas d’ allergie à la pénicilline, la Clarithromycine 250 mg/j peut être utilisée par voie orale pendant 12 mois, il n’ y a cependant pas d’ évidence concernant la dose recommandée. Lérythromycine n’ est plus recommandée en raison de ses effets indésirables et de son taux d’ absorption défavorable (11). La prophylaxie des rechutes par la pénicilline sur une période de seulement 6 mois peut réduire le risque de rechute d’ environ 50 % (13).
Autres traitements médicamenteux
L’ association de corticostéroïdes et d’ antibiotiques dans le traitement de l’ érysipèle doit être envisagée, en particulier dans les cas graves et à haut risque de récidive (14). Un traitement concomitant à la cortisone peut entraîner une amélioration rapide de la douleur, de la fièvre et des résultats locaux. Il n’ existe cependant pas beaucoup de données ni de recommandations concernant l’ administration de corticostéroïdes dans l’ érysipèle chronique.
Récidive malgré une prophylaxie antibiotique
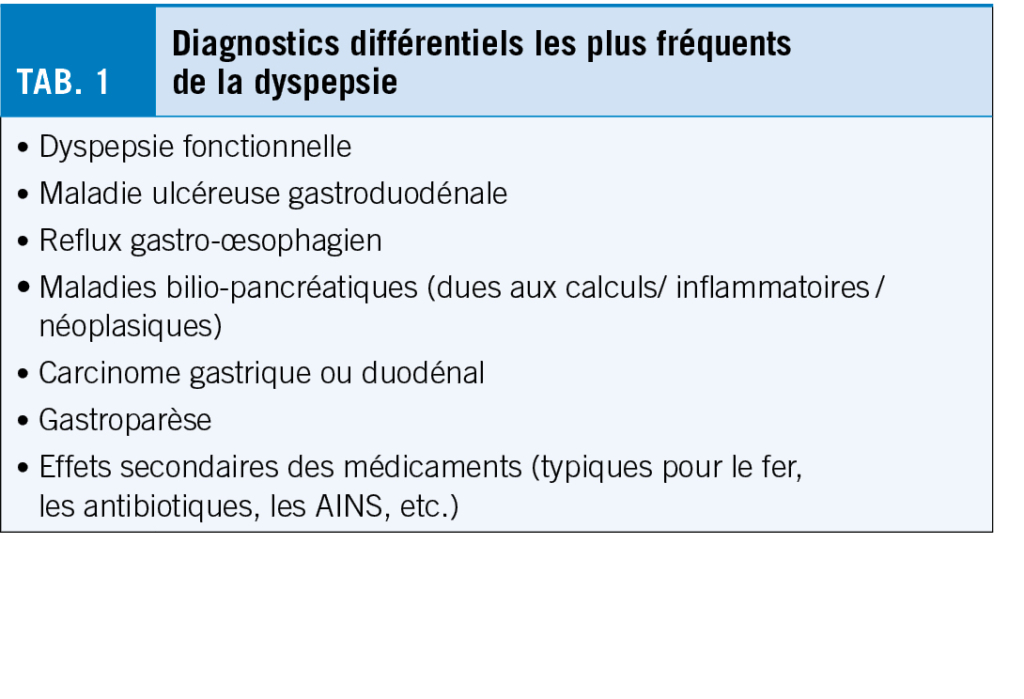
Une raison courante et quotidienne de la récidive est une compliance médicamenteuse insuffisante. Des effets secondaires indésirables ainsi que l’ ’utilisation incorrecte ou manquante de l’ antibioprophylaxie figurent parmi les raisons les plus fréquentes de la récidive de l’érysipèle (tab. 1).

Pour poser un diagnostic correct, la connaissance des diagnostics différentiels possibles est nécessaire. Une culture permettant de différencier les streptocoques des staphylocoques peut être utile pour le choix des antibiotiques (15).
Article traduit de «der informierte arzt » 05_2021
Copyright bei Aerzteverlag medinfo AG
Spital Männedorf
Asylstr. 10, 8708 Männdedorf
Spital Männedorf
Asylstr. 10, 8708 Männdedorf
d.schneider@spitalmaennedorf.ch
Les auteurs n’ ont aucun conflit d’ intérêts à déclarer en rapport avec cet article.
1. Jorup-Rönström C, Britton S. Recurrent erysipelas: predisposing factors and costs of prophylaxis. Infection. 1987 Mar-Apr;15(2):105-106.
2. Brishkoska-Boshkovski V, Dimitrovska I, Kondova-Topuzovska I. Clinical Presentation and Laboratory Characteristics in Acute and Recurrent Erysipelas. Open Access Maced J Med Sci. 2019;7(5):771-774.
3. Seybold U, Erysipel: Wann wird es kritisch? MMW Fortschritte der Medizin 2018 . 10 / 160
4. Bassetti S, Haut- und Weichteilinfektionen: Zellulitis, Erysipel und nekrotisierende Fasziitis, Schweiz Med Forum 2013;13(35):672–677
5. Thomas KS, Crook AM, Nunn AJ, et al. Penicillin to prevent recurrent leg cellulitis. N Engl J Med. 2013;368(18):1695-1703.
6. Inghammar M, Rasmussen M, Linder A. Recurrent erysipelas–risk factors and clinical presentation. BMC Infect Dis. 2014;14:270.
7. Sunderkötter, C. and Becker, K. (2015), Häufige bakterielle Infektionen der Haut-und Weichgewebe: Klinik, Diagnostik und Therapie. JDDG: Journal der Deutschen Dermatologischen Gesellschaft, 13: 501-5
8. Stevens DL, Bisno AL, Chambers HF, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the Infectious Diseases Society of America [published correction appears in Clin Infect Dis. 2015 May 1;60(9):1448.
9. Oh CC, Ko HC, Lee HY, Safdar N, Maki DG, Chlebicki MP. Antibiotic prophylaxis for preventing recurrent cellulitis: a systematic review and meta-analysis. J Infect. 2014;69(1):26-34.
10. Dalal A, Eskin-Schwartz M, Mimouni D, et al. Interventions for the prevention of recurrent erysipelas and cellulitis. Cochrane Database Syst Rev. 2017;6(6):CD009758. Published 2017 Jun 20.
11. S2k Leitlinie: Kalkulierte parenterale Initialtherapie bakterieller Erkrankungen bei Erwachsenen AWMF-Registernummer 082-006
12. Brishkoska-Boshkovski V, Kondova-Topuzovska I, Damevska K, Petrov A. Comorbidities as Risk Factors for Acute and Recurrent Erysipelas. Open Access Maced J Med Sci. 2019;7(6):937-942.
13. Thomas K, Crook A, et al. Prophylactic antibiotics for the prevention of cellulitis (erysipelas) of the leg: results of the UK Dermatology Clinical Trials Network’s PATCH II trial. Br J Dermatol. 2012;166(1):169-178
14. Solomon M, Barzilai A, Elphasy H, Trau H, Baum S. Corticosteroid Therapy in Combination with Antibiotics for Erysipelas. Isr Med Assoc J. 2018;20(3):137-140.
15. Koster JB, Kullberg BJ, van der Meer JW. Recurrent erysipelas despite antibiotic prophylaxis: an analysis from case studies. Neth J Med. 2007;65(3):89-94.