Die Schultergelenksarthrose kann in eine primäre Arthrose und eine sekundäre Arthrose eingeteilt werden. Während bei der primären Arthrose mit Ausnahme des eventuell höheren Alters und des damit einhergehenden Verschleisses keine eindeutige Ursache genannt werden kann, ist die sekundäre Arthrose auf einen klaren Grund zurückzuführen der eine frühzeitige Degeneration des Schultergelenkes auslöst. Stellt sich in der Anamnese und in der klinischen Untersuchung der Verdacht einer Schultergelenksarthrose, benötigt man zur weiteren Diagnostik eine Bildgebung in Form von Röntgenaufnahmen. Initial steht eine schmerzlindernde Kortisoninfiltration und anti-entzündliche medikamentöse Therapie im Vordergrund, welche durch physiotherapeutische Massnahmen begleitet werden sollte. Bei therapierefraktären Beschwerden und grossem Leidensdruck besteht die Indikation zur operativen Versorgung mittels einer Schulterendoprothese. Hierdurch kann sowohl im kurz- sowie langfristigen Verlauf eine deutliche Schmerzreduktion und Funktionsverbesserung erzielt werden und somit die Lebensqualität der Patienten verbessert werden. Zeigt sich eine fortgeschrittene Dezentrierung des Oberarmkopfes oder ein instabiles Drehzentrum ist die Versorgung mittels einer inversen Schulterendoprothese indiziert. Moderne Planungsverfahren erlauben die individuelle Anpassung der Schulterendoprothese an die individuelle Anatomie des Schulterblattes und Oberarmkopfes sowie die Körperhaltung der Patientinnen und Patienten.
Osteoarthritis of the shoulder joints can be divided into primary osteoarthritis and secondary osteoarthritis. While in the case of primary osteoarthritis, with the possible exception of older age and the associated wear and tear, no clear cause can be named, secondary osteoarthritis is due to a clear reason that triggers premature degeneration of the shoulder joint. If the history and clinical examination raise the suspicion of shoulder joint osteoarthritis, imaging in the form of X-rays is required for further diagnosis. Initially, the focus is on pain-relieving cortisone infiltration and anti-inflammatory drug therapy, which should be accompanied by physiotherapeutic measures. In cases where the symptoms are refractory to therapy and the patient is suffering greatly, there is an indication for surgical treatment with a shoulder arthroplasty. This can lead to a significant reduction in pain and an improvement in function in both the short and long term, thus improving the patient’s quality of life. If there is advanced decentering of the humeral head or an unstable center of rotation, treatment with a reverse shoulder arthroplasty is indicated. Modern planning procedures allow the shoulder arthroplasty to be individually adapted to the anatomy of the scapula and humeral head as well as the patient’s posture.
Key Words: Schulterschmerzen, Arthrose, Omarthrose, Schulterprothese, Inverse Prothese
Hintergrund
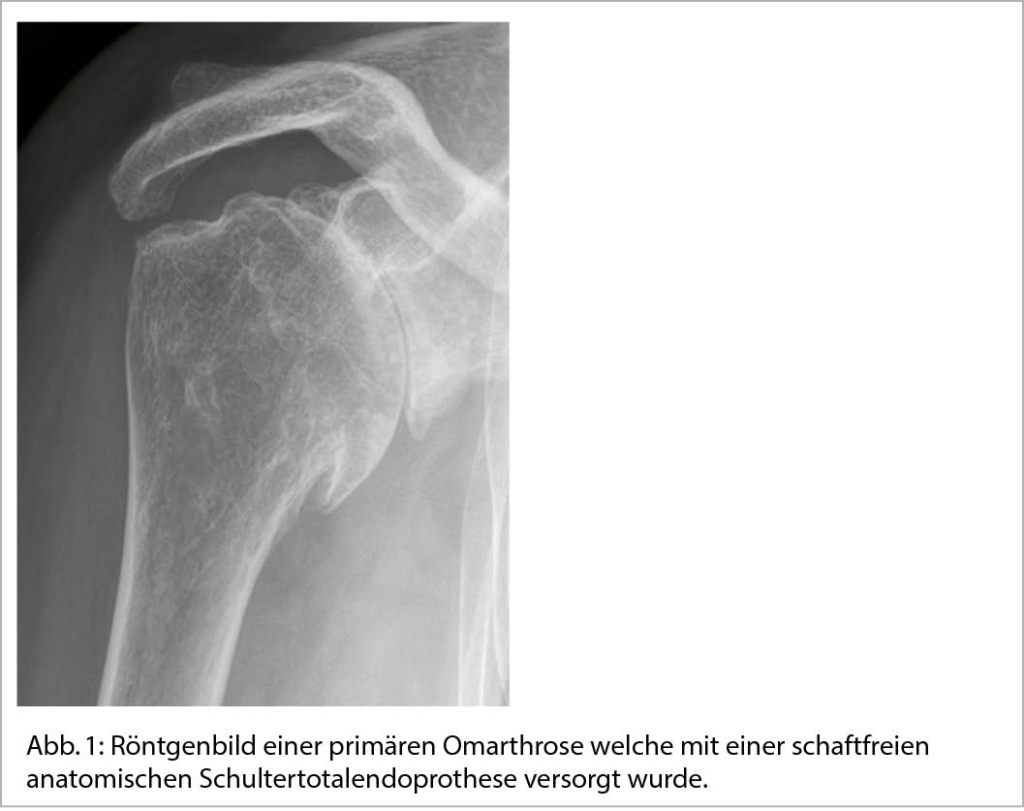
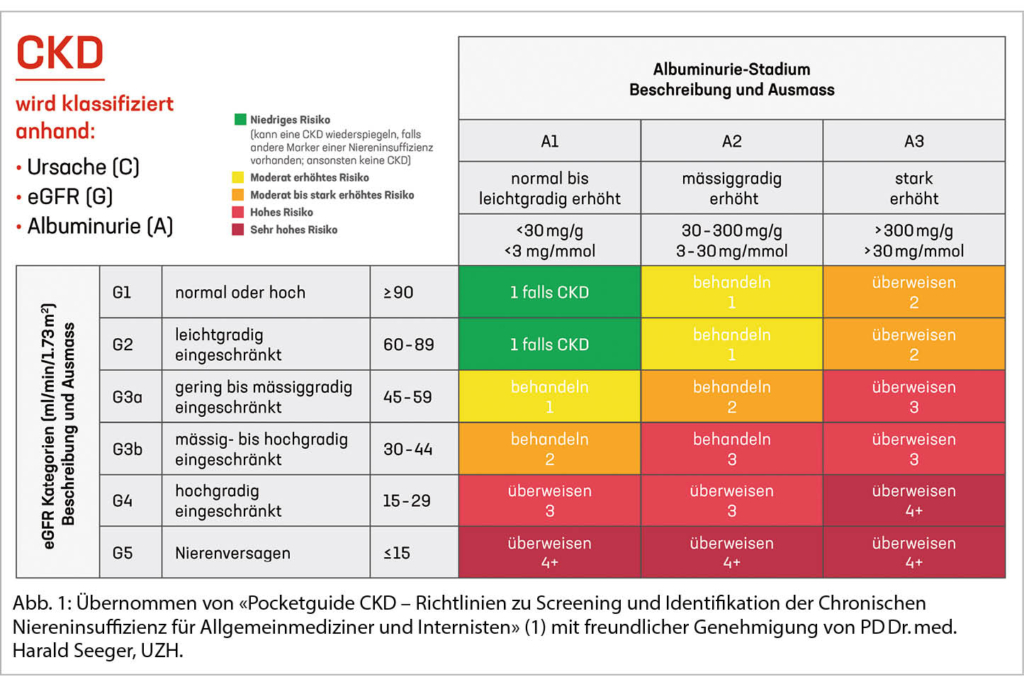
Schulterbeschwerden sind der dritthäufigste Vorstellungsgrund unter den muskuloskelettalen Beschwerden in der primären Gesundheitsversorgung. In 21% der durch den Hausarzt aufgrund von persistierenden Schulterschmerzen überwiesenen Patienten wird in der radiologischen Bildgebung eine Omarthrose diagnostiziert (1). In Zweidrittel der Fälle liegt den degenerativen Veränderungen des Knorpels und des angrenzenden Knochens sowie des periartikulären Weichteilgewebes kein spezifischer Auslöser zugrunde. Die Prävalenz dieser sogenannten primären Arthrose steigt mit zunehmendem Alter. Während 15% bereits in der 6. Lebensdekade betroffen sind, steigt der Anteil bei Patienten über 70 Jahren auf über 25% (2). Beeinflussbare Risikofaktoren für die primäre Arthrose stellen Übergewicht, Rauchen sowie systemische Erkrankungen wie arterielle Hypertonie dar (Abb. 1) (3).
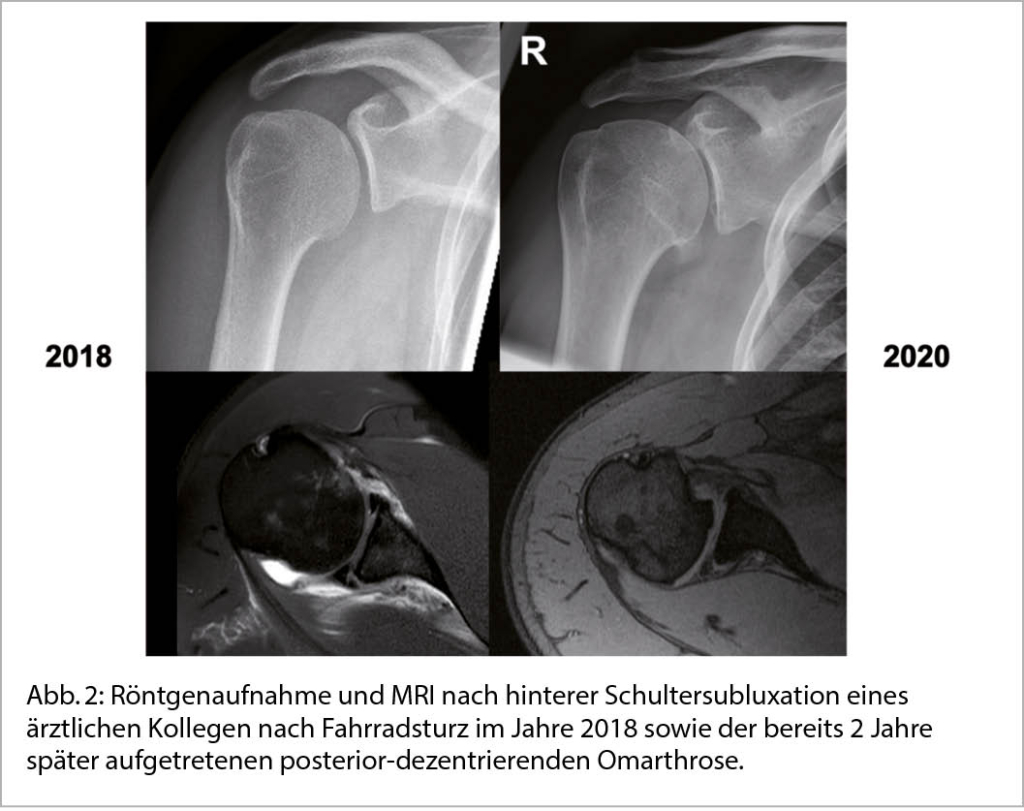
Die sekundäre GHA entstehen auf Basis einer klar definierten Ursache wie z.B. einer Gelenksinstabilität, Fehlstellung nach Trauma, oder einer medikamenteninduzierten Nekrose (Abb. 2).
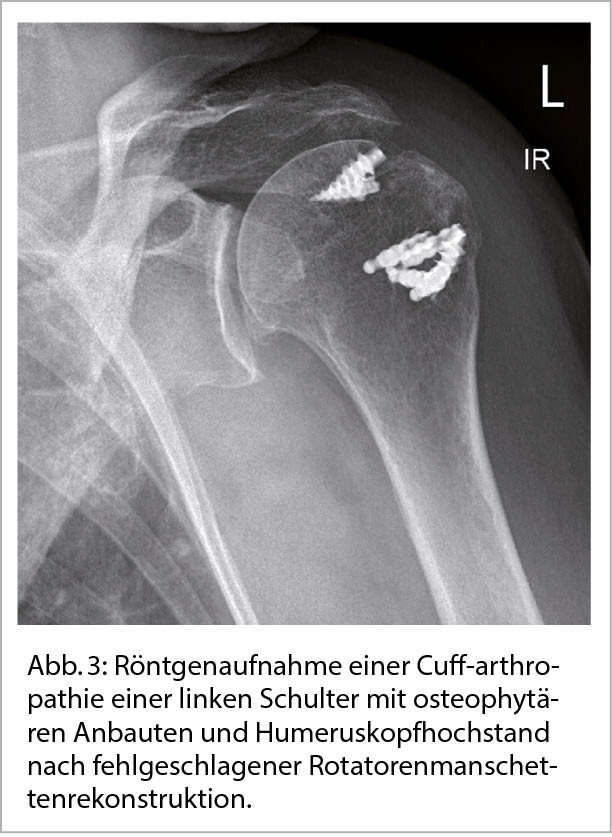
Eine sehr häufige Form der sekundären Schultergelenksarthrose ist die sogenannte Cuff-Arthropathie bei Patienten mit ausgeprägten Rotatorenmanschettenrupturen und konsekutivem Humeruskopfhochstand (Abb. 3) (4).
Tritt eine primäre Arthrose frühzeitig auf, so sollte nach einer versteckten Ursache geforscht werden. Kürzlich konnten wir z.B. in einer Studie zeigen, dass häufig vergleichsweise junge Männer betroffen sind, die Sportarten mit einer hohen Belastung der Schultergelenke ausüben wie z.B. Kraftsport und Kampfsport. Vermeintlich kann eine repetitive Überlastung und ein unausgeglichenes Training zu einer Dysbalance der schulterstabilisierenden Kräftepaare führen und in weiterer Folge eine posterior-exzentrische Arthrose begünstigen (3).
Diagnostik
Die Erstvorstellung erfolgt zumeist aufgrund eines zunehmenden Schulterschmerzes, der je nach Art der vorliegenden Arthrose als Belastungs-, Ruhe-, oder Nachtschmerz auftreten kann.
Während bei einer primären Omarthrose häufig die zunehmende Steife des Gelenkes einen Funktionsverlust bedingt, so kann bei einer Cuff-Arthropathie der Verlust der Rotatorenmanschette zu einer Pseudoparalyse der Schulter führen mit mangelnder aktiver (jedoch passiv erhaltener) Elevationsfähigkeit des Armes. Bei fortgeschrittenen Omarthrosen kann bei der klinischen Untersuchung häufig eine Krepitation in der Schulter bei passiver Bewegung wahrgenommen werden. Die primäre Diagnosesicherung erfolgt über eine konventionelle radiologische Bildgebung des Schultergelenks in 2 Ebenen (antero-posterior und axiale Aufnahme). Klassische radiologische Zeichen der Omarthrose umfassen osteophytäre Anbauten am Pfannenrand oder Oberarmkopf, Gelenkspaltverschmälerung, sowie subchondrale Zystenformationen und Sklerosierung. Die Beurteilung der Schweregrade nach radiologischen Gesichtspunkten korreliert häufig nicht mit der klinischen Symptomatik der Patienten weshalb eine sorgfältige klinische Untersuchung unumgänglich ist (5).
Nicht-operative Therapie
Nach Diagnosestellung ist eine gründliche Aufklärung über das vorliegende Krankheitsbild und das zu erwartende Voranschreiten der degenerativen Gelenksveränderungen notwendig. Die Entscheidung über die Therapie ist von den Schmerzen und der Funktions- bzw. Alltagseinschränkung abhängig unter Berücksichtigung des Aktivitätsniveaus und eventueller Begleiterkrankungen. Initial ist ein konservativer Therapieversuch empfohlen. Die symptomatische Schmerztherapie steht dabei im Vordergrund. Abhängig von den patientenspezifischen Risikofaktoren sind nicht-steroidale antiinflammatorische Medikamente über einen begrenzten Zeitraum Mittel der Wahl. Opioide sollten aufgrund des limitierten Effekts bei Gelenksschmerzen und ungünstigem Nebenwirkungsprofil, sowie erhöhtem Suchtpotential, nur in Ausnahmefällen verschrieben werden (5). Bei Schmerzexazerbation kann eine intraartikuläre Kortisoninfiltration unter Beachtung der Kontraindikationen eine deutliche, wenngleich häufig leider zeitlich begrenzte, Verbesserung der Schmerzsymptomatik und Schulterfunktion herbeiführen (6). Alternativ können intraartikuläre Infiltrationen mit Hyaluronsäure durchgeführt werden (7). Die klinische Wertigkeit von Hyaluronsäureinfiltrationen gegenüber Kortisoninfiltrationen muss noch in weiteren Vergleichsstudien näher untersucht werden (8). Weitere Forschungsschwerpunkte der intraartikulären Infiltrationstherapie sind derzeit Platelet-Rich Plasma- (PRP) und Zell-Therapien. Aktuell kann bei nicht ausreichender Datenlage jedoch noch keine generelle Therapieempfehlung gegeben werden (9). Wichtig ist eine Aufklärung über das Risiko einer iatrogenen Gelenksinfektion bei Gelenkinfiltrationen, wobei es sich um eine sehr seltene aber schwerwiegende Komplikation handelt. Um das Risiko eines periprothetischen Gelenksinfektes zu vermindern ist zudem von einer Gelenkinfiltration drei Monate vor einer geplanten Endoprothesenimplantation abzuraten (10).
Die Physiotherapie ist die zweite feste Säule der konservativen Therapie. Das Ziel ist die bestmögliche Erhaltung der Schulterbeweglichkeit und Kraft sowie die Schmerzreduktion. Im Fokus steht die Kräftigung der Humeruskopf-zentrierenden Rotatorenmanschette, sowie ausgleichende Entspannungsübungen zur Entlastung der periskapulären Muskelgruppen (11). Aktive Bewegung im Alltag und Sport mit wenig Belastung für die Schultern sind empfehlenswert, während Sportarten mit hoher schulterspezifischer Belastung gemieden werden sollten (3).
Operative Therapie:
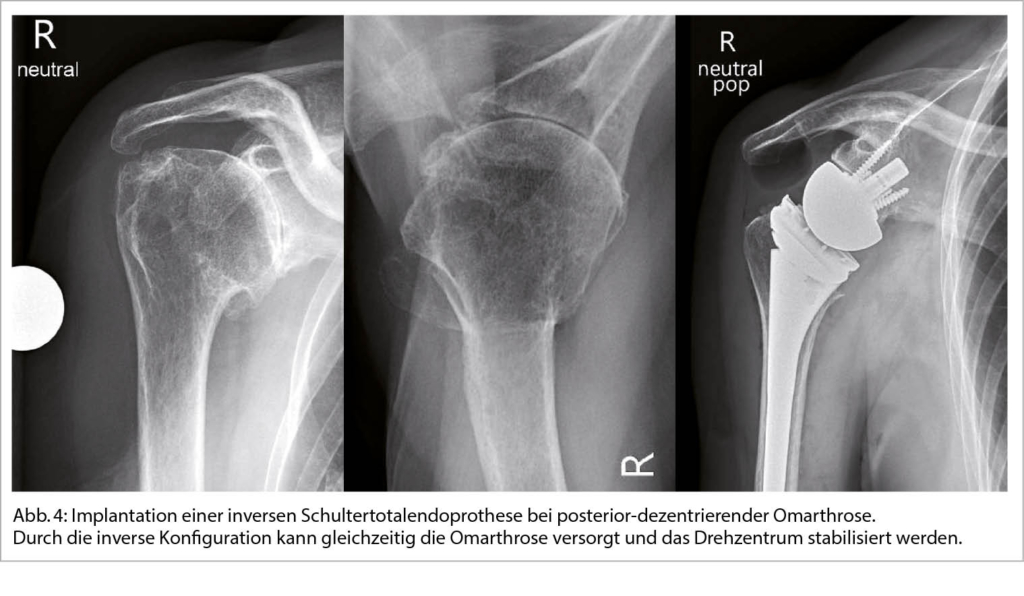
Ist die konservative Therapie ausgeschöpft kann durch die Implantation einer Schulterendoprothese eine zuverlässige Verbesserung der Beschwerden erreicht werden. Die Indikationen zur operativen Versorgung besteht bei therapieresistenten Schmerzen oder unzureichend kompensierbaren Einschränkungen des Bewegungsausmasses sowie zunehmendem Leidensdruck der Patienten. Eine endoprothetische Versorgung kann als anatomische (Total)endoprothese (aTSA) unter Erhalt der ursprünglichen Anatomie oder als inverse Totalendoprothese (rTSA) zur Stabilisierung des Drehzentrums erfolgen (Abb. 4) (12).
Wichtige Strukturen, die zur Zentrierung des Humeruskopfes beitragen sind knöchern die Schultergelenkspfanne sowie weichteilig die Muskeln und Sehnen der Rotatorenmanschette. Exzentrische Omarthrosen aufgrund einer schwerwiegenden Pfannendeformität und statischer Dezentrierung des Oberamkopfes oder aufgrund einer Rotatorenmanschetteninsuffizienz mit instabilem Gelenksdrehzentrum sprechen für die Implantation einer inversen Schulterendoprothese. Der Anteil der implantierten inversen Endoprothesen ist in den letzten Jahren aufgrund der vielfältigen Indikationserweiterungen und nicht zuletzt aufgrund der sehr guten und verlässlich erzielbaren Ergebnisse kontinuierlich gestiegen. Während die inverse Endoprothese durch das stabilere Drehzentrum überzeugt, ist bei der anatomischen Endoprothese das durchschnittlich zu erwartende postoperative Bewegungsausmass grösser. Bei Verlust der Stabilität des Drehzentrums im Verlauf nach Implantation einer anatomischen Schultertotalendoprothese aufgrund einer sekundären Rotatorenmanschetteninsuffizienz oder eines zunehmenden exzentrischen Pfannenabriebes ist der Wechsel auf eine inverse Prothese möglich (13).
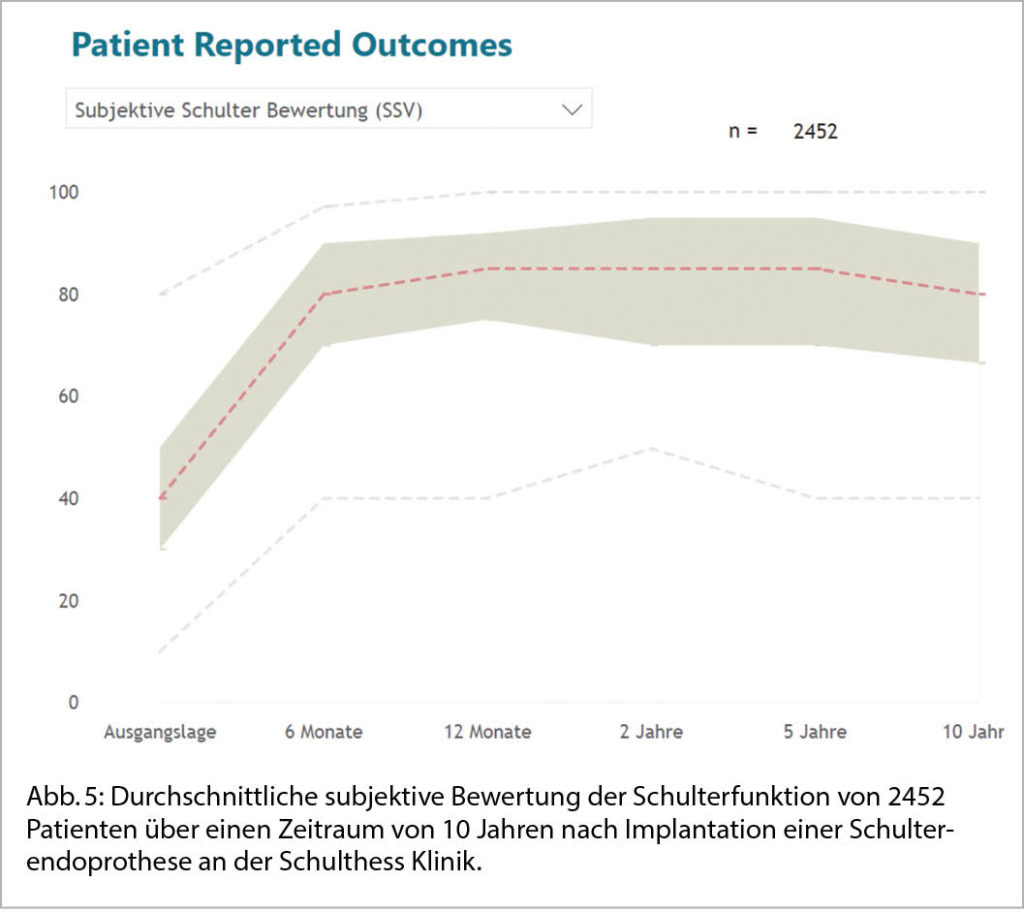
Generell, kann unabhängig von der Art der gewählten Schulterendoprothese bei Patientinnen und Patienten, die unter einer der verschiedenen Formen der Omarthrose leiden, eine zuverlässige Verbesserung der Schmerzen und des Bewegungsumfanges erreicht werden und über einen langen Zeitraum die Lebensqualität deutlich verbessert werden (Abb. 5).
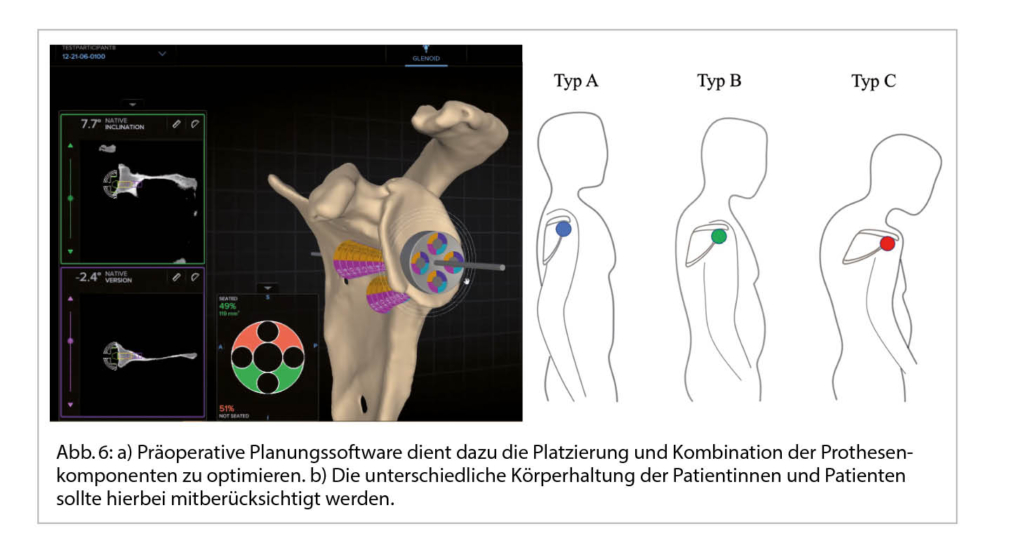
Präoperative Planungssoftware wird genutzt um die Platzierung und Kombination der Prothesenkomponenten zu simulieren und so intra- und postoperative Komplikationen aufgrund von Fehlimplantation und mechanischer Konflikte zu vermeiden.[14] In eigenen Arbeiten konnten wir zudem auf die Wichtigkeit der Miteinbeziehung der Patienten-individuellen Körperhaltung auf die präoperative Planung von Schulterendoprothesen zur Verbesserung des Bewegungsausmasses hinweisen (15). Eine angepasste Auswahl von Implantatkomponenten scheint in der Lage zu sein, die negativen Auswirkungen von häufig vorkommender kyphotischer Fehlhaltung auf das erzielbare Bewegungsausmass abzuschwächen (Abb. 6) (16).
Postoperativ erfolgt je nach Knochenqualität, Beschaffenheit der Sehnen und Art der Endoprothese typischerweise eine Ruhigstellung für 1-6 Wochen sowie eine schmerz- und funktionsadaptierte physiotherapeutische Beübung. Nach der Schulterendoprothesenimplantation werden die Patienten in regelmässigen Zeitabständen im behandelnden Zentrum nachuntersucht um mögliche Verschleisserscheinungen, Lockerung und andere auftretende Probleme frühzeitig zu erkennen. Bei Verdacht auf einen periprothetischen Infekt, Fraktur oder generellen Funktionsausfall sowie Schmerzzunahme sollte eine Überweisung an den Operateur erfolgen.
Copyright by Aerzteverlag medinfo AG
Schulter- und Ellenbogenchirurgie,
Schulthess Klinik, Zürich
Lengghalde 2
8008 Zürich
moroder.info@kws.ch
Prof. Moroder ist in der Entwicklung neuer Schulterendoprothesensysteme tätig (Arthrex Inc. und Medacta Corporate).
1. Tran G, Fascia D, Askew J et al. The prevalence of glenohumeral joint osteoarthritis in a primary care shoulder pain population referred for radiographs. Rheumatology 2021; 61: 1290-1292. doi:10.1093/rheumatology/keab867
2. Oh JH, Chung SW, Oh CH et al. The prevalence of shoulder osteoarthritis in the elderly Korean population: association with risk factors and function. Journal of Shoulder and Elbow Surgery 2011; 20: 756-763. doi:https://doi.org/10.1016/j.jse.2011.01.021
3. Plachel F, Akgün D, Imiolczyk JP et al. Patient-specific risk profile associated with early-onset primary osteoarthritis of the shoulder: is it really primary? Arch Orthop Trauma Surg 2021. doi:10.1007/s00402-021-04125-2. doi:10.1007/s00402-021-04125-2
4. Ibounig T, Simons T, Launonen A et al. Glenohumeral osteoarthritis: an overview of etiology and diagnostics. Scandinavian Journal of Surgery 2020; 110: 441-451. doi:10.1177/1457496920935018
5. Boselli KJ, Ahmad CS, Levine WN. Treatment of Glenohumeral Arthrosis. The American Journal of Sports Medicine 2010; 38: 2558-2572. doi:10.1177/0363546510369250
6. Metzger CM, Farooq H, Merrell GA et al. Efficacy of a single, image-guided corticosteroid injection for glenohumeral arthritis. Journal of Shoulder and Elbow Surgery 2021; 30: 1128-1134. doi:10.1016/j.jse.2020.08.008
7. Merolla G, Sperling JW, Paladini P et al. Efficacy of Hylan G-F 20 versus 6-methylprednisolone acetate in painful shoulder osteoarthritis: a retrospective controlled trial. MUSCULOSKELETAL SURGERY 2011; 95: 215-224. doi:10.1007/s12306-011-0138-3
8. Colen S, Geervliet P, Haverkamp D et al. Intra-articular infiltration therapy for patients with glenohumeral osteoarthritis: A systematic review of the literature. Int J Shoulder Surg 2014; 8: 114-121. doi:10.4103/0973-6042.145252
9. Rossi LA, Piuzzi NS, Shapiro SA. Glenohumeral Osteoarthritis: The Role for Orthobiologic Therapies: Platelet-Rich Plasma and Cell Therapies. JBJS Reviews 2020; 8: e0075. doi:10.2106/jbjs.Rvw.19.00075
10. Richardson SS, Schairer WW, Sculco TP et al. Comparison of Infection Risk with Corticosteroid or Hyaluronic Acid Injection Prior to Total Knee Arthroplasty. J Bone Joint Surg Am 2019; 101: 112-118. doi:10.2106/jbjs.18.00454
11. Bennell KL, Buchbinder R, Hinman RS. Physical therapies in the management of osteoarthritis: current state of the evidence. Current Opinion in Rheumatology 2015; 27
12. Berliner JL, Regalado-Magdos A, Ma CB et al. Biomechanics of reverse total shoulder arthroplasty. Journal of Shoulder and Elbow Surgery 2015; 24: 150-160. doi:https://doi.org/10.1016/j.jse.2014.08.003
13. Jo YH, Kim DH, Lee BG. When should reverse total shoulder arthroplasty be considered in glenohumeral joint arthritis? Clin Shoulder Elb 2021; 24: 272-278. doi:10.5397/cise.2021.00633
14. Verborgt O, Vanhees M, Heylen S et al. Computer Navigation and Patient-specific Instrumentation in Shoulder Arthroplasty. Sports Medicine and Arthroscopy Review 2014; 22: e42-e49. doi:10.1097/jsa.0000000000000045
15. Moroder P, Akgun D, Plachel F et al. The influence of posture and scapulothoracic orientation on the choice of humeral component retrotorsion in reverse total shoulder arthroplasty. J Shoulder Elbow Surg 2020; 29: 1992-2001. doi:10.1016/j.jse.2020.01.089
16. Moroder P, Urvoy M, Raiss P et al. Patient Posture Affects Simulated ROM in Reverse Total Shoulder Arthroplasty: A Modeling Study Using Preoperative Planning Software. Clin Orthop Relat Res 2022; 480: 619-631. doi:10.1097/corr.0000000000002003