Die fetale Hydronephrose (FH) kommt häufig vor, ist zwar mehrheitlich transient, jedoch für den Klinikalltag sehr relevant, da eine enge Korrelation zwischen der pränatalen Ausprägung der FH und postpartalen Komplikationen besteht. Eine Schwierigkeit des Screenings und der Diagnostik sowie des postpartalen Managements sind die je nach Land und Fachrichtung unterschiedlichen Klassifizierungen der Schweregrade.
Die fetale Hydronephrose ist ein häufig auftretendes Phänomen und deshalb sehr relevant für den klinischen Alltag. Sie kann in etwa 1 bis 4.5% aller Schwangerschaften beobachtet werden (1). Männliche Feten sind etwa doppelt so häufig betroffen wie weibliche Feten. Die Ursachen einer FH können vielfältig sein (2). In den meisten Fällen (50-70%) handelt es sich um einen transienten und physiologischen Zustand. Die Ursachen der vorübergehenden Dilatation des fetalen Nierenbeckens sind unbekannt.
Ziel der pränatalen Diagnose einer FH ist es, die Feten mit postpartal erhöhtem Risiko für Komplikationen im Sinne von Harnwegsinfektionen, Harnsteinen oder renaler Dysfunktion zu detektieren. Es gibt eine enge Korrelation zwischen der pränatalen Ausprägung der Hydronephrose und den postpartalen Komplikationen bzw. der postpartal notwendigen operativen Versorgung.
Eine Schwierigkeit des Screenings und der Diagnostik besteht in der sehr unterschiedlichen Klassifizierung der Schweregrade. Diese Einteilungen unterscheiden sich nicht nur von Land zu Land, sondern auch zwischen den einzelnen Fachrichtungen der Radiologie, der Geburtshilfe und der Pädiatrie (4, 5, 6).
Zwei internationale Klassifizierungsmethoden stellen das Grading der «Society for Fetal Urology » (SFU) und das Grading nach «Onen» dar.
Gemäss SFU werden 4 Grade anhand der Beurteilung des Nierenbeckens, der Nierenkelche und des Nierenparenchyms unterschieden.
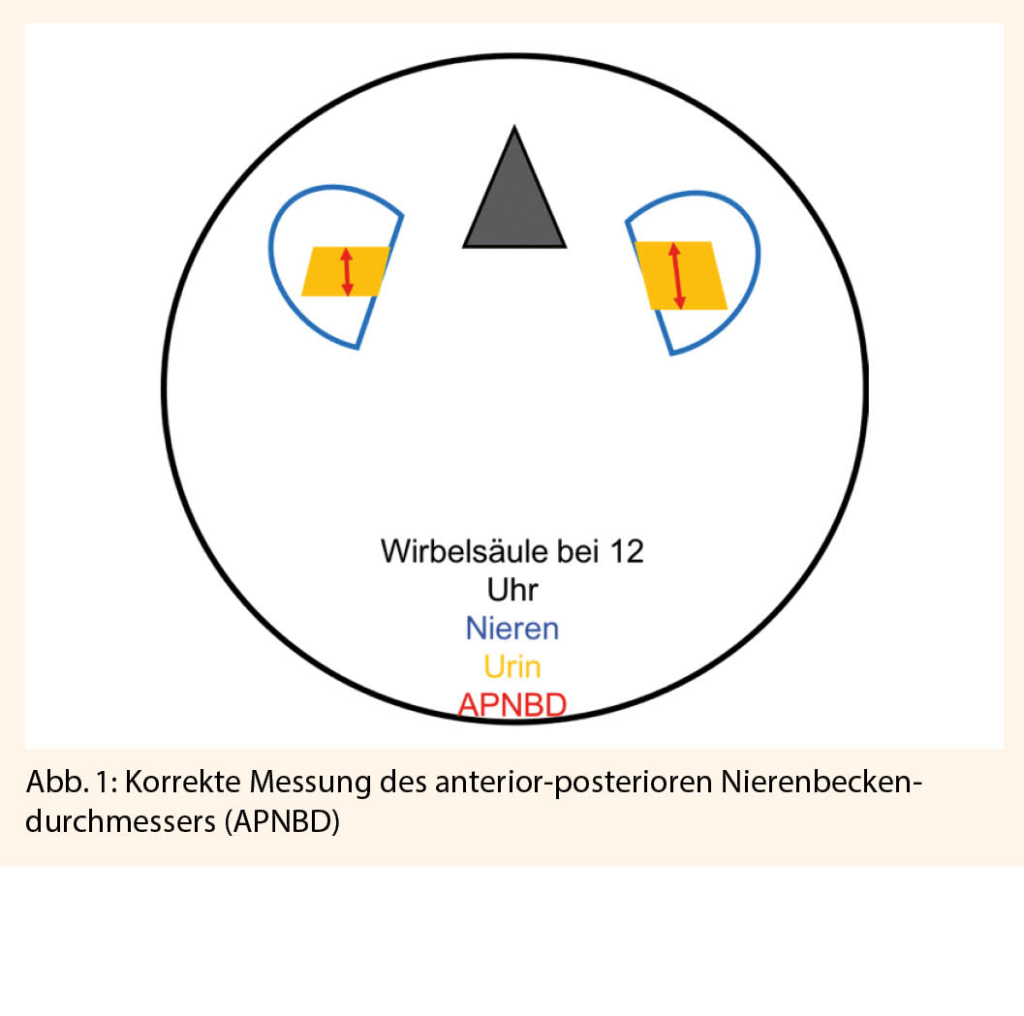
Pränatal wird primär meist der anterior-posteriore Nierenbeckendurchmesser (APNBD) angewendet, um die renale Flüssigkeitsansammlung quantitativ zu beschreiben. Die Messung sollte in einer transversalen Schnittebene mit der Wirbelsäule bei 6 oder 12 Uhr und von der jeweils inneren Grenze der Flüssigkeitsansammlung erfolgen.
Allerdings muss hierbei beachtet werden, dass der APNBD in Abhängigkeit zum Gestationsalter steht.
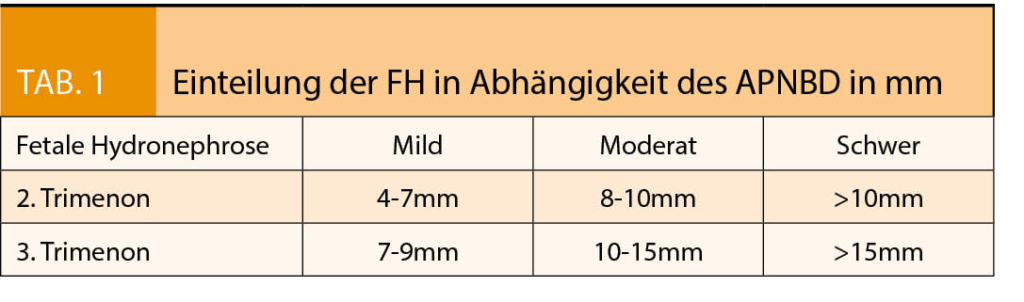
Deshalb kommt folgende Einteilung der FH im klinischen Alltag zum Einsatz (7, 8 , 9):
Ebenso muss beachtet werden, dass das Ausmass zusätzlich von der maternalen Hydrierung, der fetalen Nierenfunktion sowie der fetalen Harnblasenfüllung und deren Dynamik abhängig ist. Dementsprechend werden mehrere Messungen in einem möglichst grossen Zeitabstand während der Untersuchung empfohlen.
Entscheidend ist, dass ab einem APNBD von 4 mm im 2. Trimenon und 7 mm im 3. Trimenon Verlaufssonographien alle 4 Wochen durchgeführt werden sollten. In etwa 80% der im 2. Trimenon diagnostizierten Fälle mit milder Hydronephrose (4-7 mm) zeigen sich diese bereits vorgeburtlich wieder unauffällig, ohne jegliche renale Stauungszeichen (10).
Daraus abgeleitet scheint die FH im 3. Trimenon mit einem APNBD von über 7mm die höchste Vorhersagekraft bezüglich einer postnatal relevanten Hydronephrose zu haben.
Im Falle einer FH soll der Fetus hinsichtlich weiterer Fehlbildungen genau gescreent werden, um syndromale Erkrankungen mit der Indikation zur genetischen Abklärung nicht zu verpassen. Die milde fetale Hydronephrose stellt einen Softmarker für fetale Aneuploidien, insbesondere der Trisomie 21, dar (11, 12). Folglich weisen Feten mit einer Trisomie 21 in 17,6 % der Fälle eine milde Hydronephrose auf (13).
Weiter ist im Bereich des Urogenitaltraktes auf folgende Zusatzkriterien zu achten, die auch detailliert zu beschreiben sind (2).
Die Kriterien sind in den bereits oben erwähnten Klassifizierungen nach SFU (4) und Onen (5) enthalten.
- Dilatation der Nierenkelche
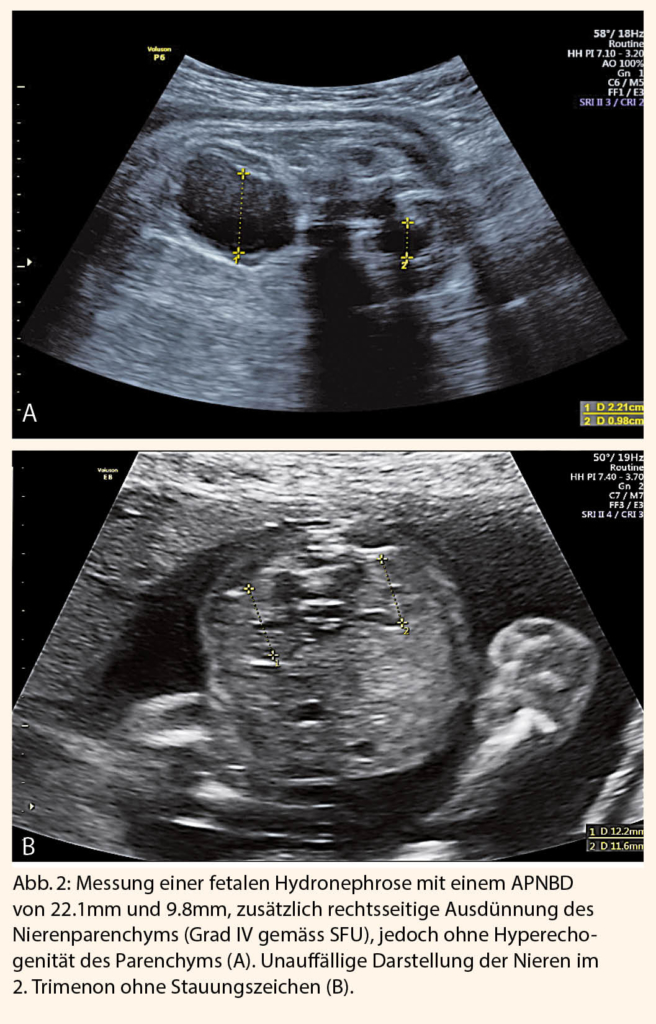
Eine zusätzliche Erweiterung der Nierenkelche spricht für eine fortgeschrittene Hydronephrose (Hydronephrose Grad II und III gemäss SFU). Hierbei ist wichtig, eine Verbindung zwischen Kelchen und Nierenbecken darzustellen, um die Erweiterung der Nierenkelche von Nierenzysten zu unterscheiden. - Ausdünnung und Echogenität des Nierenparenchyms
Eine Ausdünnung des Nierenparenchyms entspricht der maximalen Dilatation der Nierenkelche (Grad IV gemäss SFU).
Eine erhöhte Echogenität des Nierenparenchyms ist ebenso Zeichen einer obstruktiven Uropathie und ein ungünstiger prognostischer Faktor. - Nierenzysten
Hierbei handelt es sich um zystische Strukturen im Bereich des Nierenparenchyms ohne direkte Verbindung zum Nierenbecken. Eine Abgrenzung zur Hydronephrose mit Erweiterung der Nierenkelche ist von entscheidender Bedeutung, da ansonsten an den Formenkreis der multizystisch dysplastischen Nieren gedacht werden muss. - Ureterdilatation
In der Regel sind die Ureteren sonographisch nicht darstellbar, ausser es gibt eine diesbezügliche Auffälligkeit. Eine Dilatation spricht für eine Obstruktion im Bereich des ureterovesikalen Übergangs. - Auffälligkeiten der Harnblase
Hierbei soll die Harnblasenfüllung beachtet werden. Eine wenig gefüllte Harnblase kann gemeinsam mit einem Oligohydramnion ein Zeichen eingeschränkter Nierenfunktion sein.
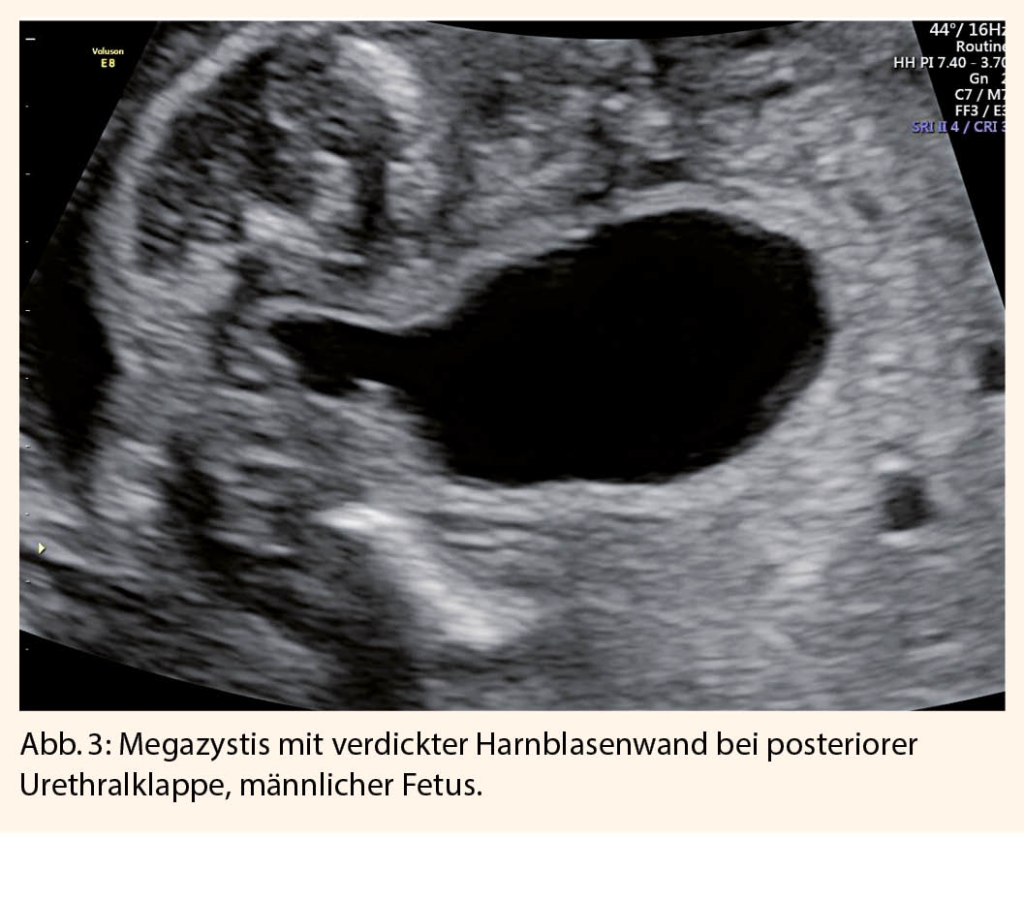
Von einer Megazystis spricht man im 1. Trimenon ab einem Longitudinaldurchmesser der Blase von 7 mm. Im 2. Trimenon entspricht eine fehlende Harnblasenentleerung über 45 Minuten einer Megazystis.
Ebenso soll die Wanddicke der Harnblase beurteilt werden, wobei eine Messung über 3 mm pathologisch ist. - Bestimmung des fetalen Geschlechts
Die Geschlechtsbestimmung ist wichtig, da gewisse Erkrankungen, wie die posteriore Urethralklappe ausschliesslich bei Knaben vorkommt und weibliche Feten mit einer Megazystis in aller Regel mit einem komplexen urogenitalen Fehlbildungssyndrom einhergehen (14). - Fruchtwassermenge
Ein besonders wichtiger Faktor bezüglich der Beurteilung renaler Auffälligkeiten stellt die Fruchtwassermenge dar, da ein Oligohydramnion auf eine eingeschränkte Nierenfunktion hinweisen kann und bei Auftreten im zweiten Trimenon zu eingeschränkter Lungenentwicklung im Sinne einer Lungenhypoplasie führen kann.
Geburtshilfliches Management
Bei einseitiger fetaler Hydronephrose und unauffälliger Fruchtwassermenge kann ein spontaner Wehenbeginn abgewartet werden.
Bei beidseitigen Befunden und/oder Oligohydramnion ist die dringende Vorstellung im Perinatalzentrum bezüglich des peri- und postpartalen Managements dringend notwendig.
Postpartales Management von Kindern mit pränatal diagnostizierter Hydronephrose
Am 2.-3. Lebenstag sollte eine sonographische Kontrolle der kindlichen Nieren erfolgen. Oft ist keine direkte chirurgische Versorgung nötig und eine weitere Verlaufskontrolle nach 4 Wochen indiziert. Bezüglich postpartalem Management von Kindern mit pränatal diagnostizierter Hydronephrose lässt die aktuelle Datenlage keine eindeutige Aussage bezüglich einer prophylaktischen Antibiose der Neugeborenen zu. Insbesondere bei ausgeprägtem oder beidseitigem Befund scheint diese allerdings sinnvoll, um die Zahl an febrilen Harnwegsinfektionen mit möglicherweise langfristigen Komplikationen mit irreversibler Schädigung und eingeschränkter Nierenfunktion zu senken (15, 16).
Hierfür wird eine Gabe von Amoxicillin 10 mg/kg Körpergewicht des Neugeborenen 2x täglich empfohlen (3).
Kantonsspital St.Gallen
Frauenklinik Geburtshilfe
Rorschacher Strasse 95
9007 St.Gallen
tina.fischer@kssg.ch
Kantonsspital St. Gallen
Frauenklinik
Rorschacherstrasse 95
9007 St. Gallen
1. Dudley JA, Haworth JM, McGraw ME, Frank JD, Tizzard EJ. Clinical relevance and implications of antenatal hydronephrosis. Arch Dis Child. (1997) 76:F31– 4.
2. Nguyen HT, Herndon CD, Cooper C, Gatti J, Kirsch A, Kokorowski P, et al. The
Society for Fetal Urology consensus statement on the evaluation and management of antenatal hydronephrosis. J Pediatr Urol 2010;6:212-31.
3. Neonatale Hydronephrose: Empfehlungen zur Betreuung in der Welschschweiz H. Chehade, P. Parvex, F. Cachat, J-B Meyrat, J. Birraux, et al. Paediatrica, Vol. 21 No. 2 2010
4. Fernbach SK, Maizels M, Conway JJ. Ultrasound grading of hydronephrosis:
introduction to the system used by the Society for Fetal Urology. Pediatr Radiol 1993;23:478-80.
5. Onen A. An alternative grading system to refine the criteria for severity of hydronephrosis and optimal treatment guidelines in neonates with primary UPJ-type hydro-nephrosis. J Pediatr Urol 2007;3:200-5.
6. Sanna Toiviainen-Salo, Laurent Garel, Andrée Grignon, Josee Dubois, et al. Fetal hydronephrosis: is there hope for consensus? Pediatr Radiol (2004) 34: 519.
7. Odibo AO, Marchiano D, Quinones JN, Riesch D, Egan JF,Macones GA. Mild pyelectasis: evaluating the relationship between gestational age and renal pelvic anterior-posterior diameter. Prenat Diagn 2003;23:824-7.
8. Chitty LS, Altman DG. Charts of fetal size: kidney and renal pelvis measurements. Prenat Diagn 2003;23:891-7.
9. https://fetalmedicine.org/education/fetal-abnormalities/urinary-tract/hydronephrosis
10. Hothi DK, Wade AS, Gibert R, et al. Mild fetal renal pelvis dilatation – much ado about nothing? Clin J Am Soc Nephrol. 2009;4:168-177.
11. Raniga, Sameer et al. “Ultrasonographic soft markers of aneuploidy in second trimester: are we lost?.” MedGenMed : Medscape general medicine vol. 8,1 9. 11 Jan. 2006
12. Orzechowski KM, Berghella V (2013) Isolated fetal pyelectasis and the risk of Down syndrome: A meta-analysis. Ultrasound Obstet Gynecol 42:615–621.
13. Nicolaides KH (2003) Screening for chromosomal defects. Ultrasound Obstet Gynecol 21:313–321.
14. Mc Hugo J, Whittle M (2001) Enlarged fetal bladders: Aetiology, management and outcome. PrenatDiagn 21:958–963.
15. Fetal megacystis: A systematic review. Taghavi, K. et al. Journal of Pediatric Urology, Volume 13, Issue 1, 7-15.
16. Silay, Mesrur Selcuk et al. Role of antibiotic prophylaxis in antenatal hydronephrosis: A systematic review from the European Association of Urology/European Society for Paediatric Urology Guidelines Panel. Journal of Pediatric Urology, Volume 13, Issue 3, 2017 June, 306 – 315
17. Canning DA. Urinary Tract Infections in Children with Prenatal Hydronephrosis: A Risk Assessment from the Society for Fetal Urology Hydronephrosis Registry.J Urol. 2018 May;199(5):1101.