Jeden Herbst wird das Thema Impfschutz durch die saisonale Grippeimpfung aktuell. Der jährlich im Frühling aktualisierte Schweizerische Impfplan des BAG ist Basis der Impfberatung. Die aktuellen Informationen zu den empfohlenen Impfungen und zur Impfstoffversorgung finden sich auch auf www.infovac.ch.
Jede Arztkonsultation bietet Gelegenheit zur Überprüfung des Impfschutzes und Durchführung allfälliger Nachholimpfungen. Bei fehlender oder unbekannter Grundimmunisierung soll der Impfschutz in jedem Alter evaluiert und ergänzt werden.
Einige Grundregeln sind dabei hilfreich:
- Die Anzahl nötiger Impfdosen ergibt sich aus dem Vergleich der «Soll-Impfdosen» (altersentsprechend gemäss Impfplan) mit den bisher erhaltenen Impfdosen.
- Es sind nie mehr Dosen indiziert als für die Grundimmunisierung von komplett Ungeimpften nötig wären (bei Totimpfstoffen wie z.B. dTpa-IPV, FSME, HPV, Hepatitis B sind dies in der Regel 3 Dosen).
- Die empfohlenen Zeitabstände sind Mindestabstände zur Ausbildung einer optimalen Impfantwort; längere Abstände sind immer möglich.
- Jede Dosis zählt! Eine begonnene, noch unvollständige Impfserie nicht wieder von vorne beginnen – auch wenn die letzten Dosen schon viele Jahre zurückliegen.
- Lebendimpfstoffe (MMR, Varizellen, Gelbfieber, Typhus, Herpes zoster (Zostavax®)) sind bei Schwangeren und immunsupprimierten Personen kontraindiziert.
- Mindestens 4 Wochen Abstand zwischen 2 verschiedenen viralen Lebendimpfstoffen einhalten (MMR und Varizellen auch am gleichen Tag möglich).
- Alle Totimpfstoffe können gleichzeitig oder in beliebigen zeitlichen Abständen zueinander verabreicht werden.
- Das Impfschema wird definiert durch das Alter, in dem die Impfserie begonnen wurde.
- Patienten mit oraler Antikoagulation oder Thrombozytenaggregationshemmern dürfen und sollen intramuskuläre Impfungen erhalten (Druckverband!).
- Serologien/Impfantikörperbestimmungen sind grundsätzlich nicht hilfreich zur Festlegung einer Impfindikation / eines Impfschemas und sollten deshalb nicht durchgeführt werden.
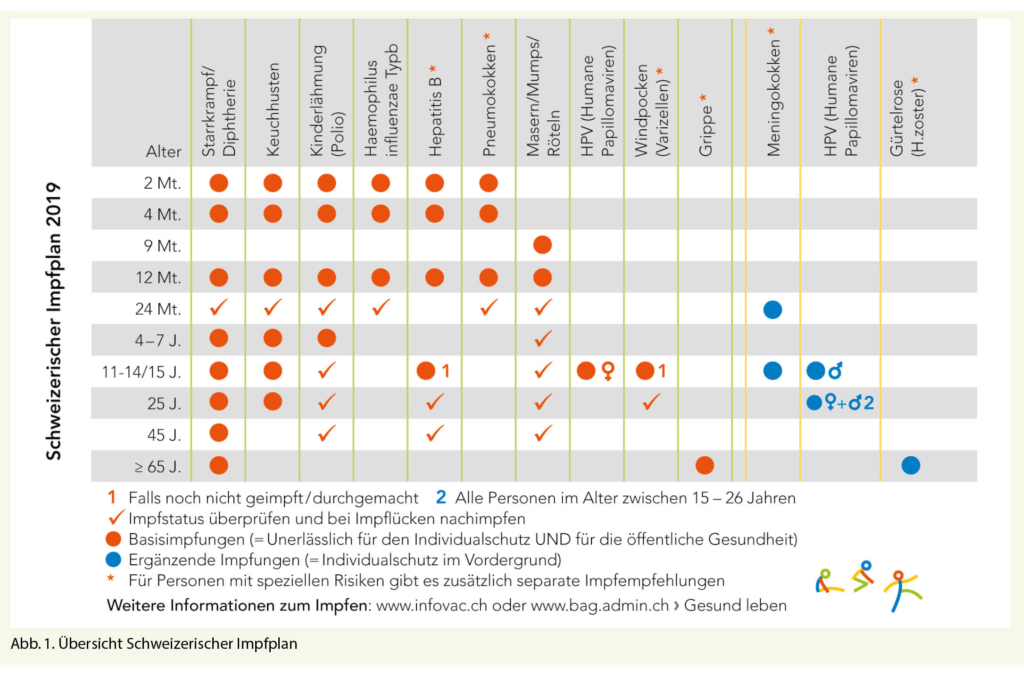
Die Kosten für fast alle im schweizerischen Impfplan empfohlenen Impfungen werden, abzüglich Franchise und Selbstbehalt, von der Krankenkasse übernommen (Ausnahmen: Pneumokokkenimpfung bei Personen > 5 Jahre, Impfung gegen Herpes zoster). Eine Übersicht der aktuellen Impfempfehlungen findet sich in der Synopsis des Schweizerischen Impfplans (siehe Abb. 1 und Tab. 2; Link aktiv in Online-Version).
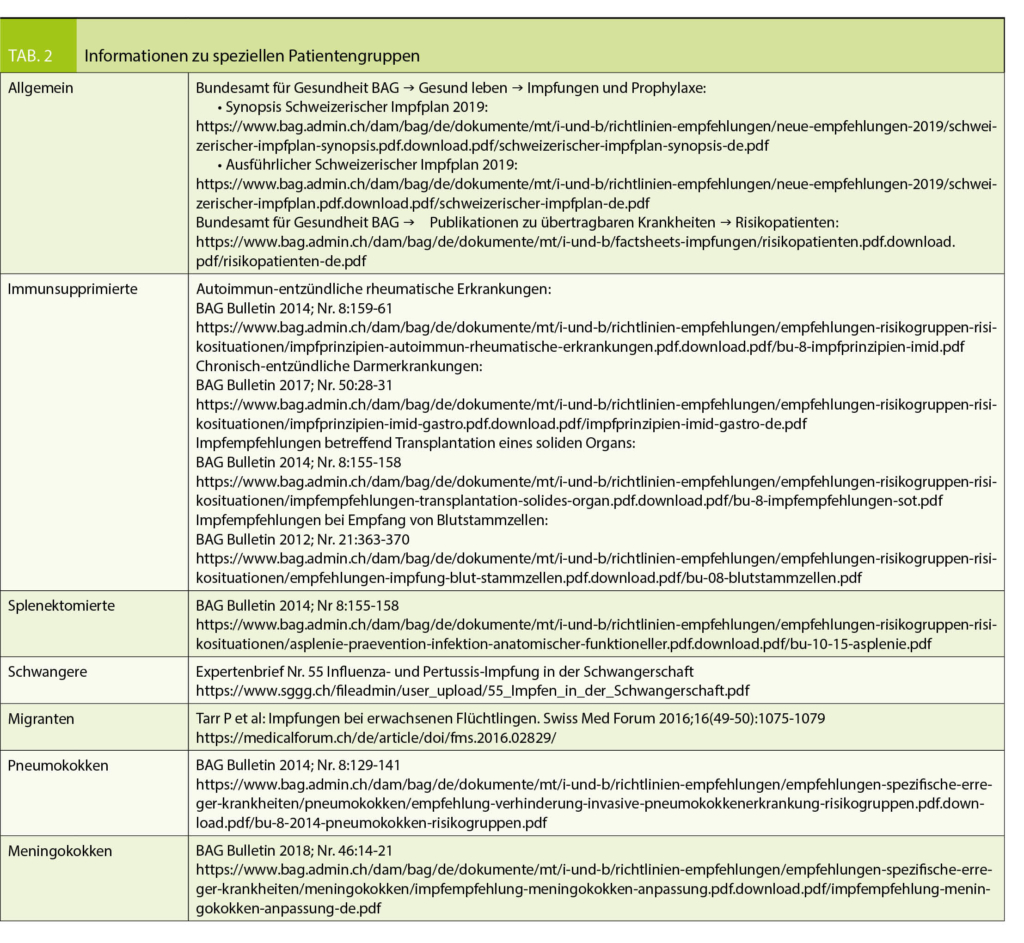
Zu zahlreichen speziellen Patientengruppen (z.B. Schwangere, Immunsupprimierte, Splenektomierte) existieren separate Empfehlungen, die für die Impfberatung hilfreich sind. Eine Übersicht findet sich in Tab. 2.
Saisonale Grippeimpfung
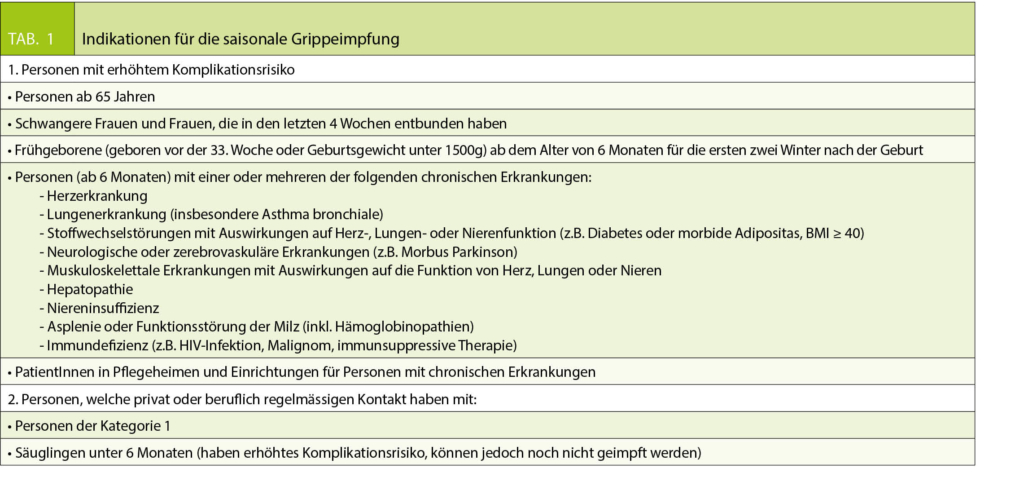
Schweregrad und Auswirkungen einer Influenza-Infektion werden oft unterschätzt. Patienten mit Influenza-Infektion haben u.a. auch ein deutlich erhöhtes Risiko für einen akuten Myokardinfarkt im folgenden Jahr (1). Influenza und influenzaähnliche Erkrankungen führen in der Schweiz jedes Jahr zu über 330 000 Arztkonsultationen und ca. 1500 Todesfällen (2). Die saisonale Grippeimpfung reduziert das Risiko einer Influenza-Infektion sowie die Gesamtmortalität und Hospitalisationsrate für Pneumonie und Influenza (3, 4) und ist bezüglich Schutzwirkung und möglichen Nebenwirkungen deutlich besser als ihr Ruf. Die häufig verwendeten, trivalenten inaktivierten Influenzaimpfstoffe zeigten in einer Metaanalyse eine Wirksamkeit von 59% bei gesunden Erwachsenen (5). Der Impfschutz hängt vom saisonalen Antigen-Match sowie von Alter und Immunstatus des Patienten ab. Durch die Verwendung von tetravalenten Impfstoffen, die einen zusätzlichen Influenza-B-Stamm enthalten, kann die Wahrscheinlichkeit eines Antigen-Mismatch reduziert werden. Der adjuvantierte Impfstoff (Fluad®), welcher für Erwachsene ≥ 65 Jahre zugelassen ist, löst bei diesen eine bessere Immunantwort aus, ist jedoch trivalent. Die Schutzwirkung einer Influenzaimpfung setzt nach 10-14 Tagen ein und hält etwa 3-4 Monate an. Da die Immunogenität der Influenzaimpfung bei Patienten in höherem Alter oder bei Grunderkrankungen vermindert sein kann, ist der Umgebungsschutz («Cocooning») enorm wichtig. Durch die Impfung naher Kontaktpersonen und dadurch Verminderung der Ansteckungsgefahr werden die besonders gefährdeten Personen indirekt geschützt. Dies gilt vor allem auch für Personen, die im Gesundheitswesen tätig sind und somit besonders oft Kontakt zu Risikopersonen haben. Die Grippeimpfung ist in der Schweiz für alle Personen mit erhöhtem Komplikationsrisiko sowie für Personen mit erhöhtem Übertragungsrisiko und deren Kontaktpersonen empfohlen (Tab. 1).
Pneumokokkenimpfung
Seit 2014 wird bei Risikopersonen mit entsprechender Indikation (siehe Abb. 1 und Tab. 2; Link aktiv in Online-Version) eine einmalige Impfung mit dem 13-valenten konjugierten Impfstoff
(Prevenar®) empfohlen. Diese führt bei älteren Erwachsenen zu einer Reduktion von invasiven Pneumokokkenerkrankungen um 75% und von Pneumokokkenpneumonien durch Impfserotypen um 45% (6).
Die Indikationen zur Pneumokokkenimpfung bei Risikopersonen entsprechen bis auf wenige Ausnahmen weitgehend denen der Influenzaimpfung (siehe Abb. 1 und Tab. 2; Link aktiv in Online-Version). Für Säuglinge ist die Pneumokokkenimpfung neu seit 2019 als Basisimpfung empfohlen. Leider ist der Impfstoff in der Schweiz nur für Kinder < 5 Jahren zugelassen, weshalb bei älteren Kindern und Erwachsenen keine Kostenübernahme durch die Grundversicherung der Krankenkasse erfolgt. Ein Antrag auf Kostenübernahme durch die Krankenkasse mit entsprechender Begründung zur Indikation kann hier oft helfen.
Impfung gegen Frühsommer-Meningoenzephalitis (FSME)
Seit 2019 gilt die ganze Schweiz ausser den Kantonen Genf und Tessin als FSME-Risikogebiet. Die Grundimmunisierung mit 3 Dosen sowie Boosterimpfungen alle 10 Jahre sind für alle Personen ab 6 Jahren empfohlen, welche in den Risikogebieten wohnen oder sich zeitweise dort aufhalten und die beruflich oder während der Freizeit ein Zecken-Expositionsrisiko aufweisen. Der ideale Zeitpunkt für den Impfbeginn ist die kalte Jahreszeit, um vor der vermehrten Zeckenaktivität im Frühling bereits mit 2 Dosen geschützt zu sein. Für die Langzeitimmunität braucht es eine dritte Dosis («Gedächtnisdosis») nach einem längeren Intervall von minimal 5 Monaten. In der Schweiz sind 2 FSME-Impfstoffe zugelassen, die austauschbar sind und äquivalent eingesetzt werden können (FSME-Immun® und Encepur®). Wenn möglich sollte eine Impfserie mit dem gleichen Impfstoff komplettiert werden, mit dem sie begonnen wurde, es kann jedoch bei Lieferengpässen auf den jeweils anderen Impfstoff ausgewichen werden. Dabei sollte grundsätzlich ein minimales Intervall von 2 Wochen zwischen den ersten beiden Dosen und ein minimales Intervall von 5 Monaten zwischen der 2. und 3. Dosis eingehalten werden. Bei Impfbeginn in der wärmeren Jahreszeit ist eine Verkürzung des Intervalls zwischen den ersten beiden Dosen auf 14 Tage empfehlenswert, um möglichst rasch einen Schutz aufzubauen. Eine FSME-Impfung direkt nach einem Zeckenstich ist möglich und sollte auch nicht verzögert werden, da ja offensichtlich ein Expositionsrisiko = Zeckenstich besteht. Der Schutz vor einer FSME-Infektion wird aktuell höher gewichtet als die Überlegungen zur allfällig erschwerten Diagnostik bei einer zeitnahen FSME-Infektion. In jedem Fall muss die geimpfte Person darüber informiert werden, dass eine FSME-Impfung nach Zeckenstich nur vor zukünftigen Infektionen schützt. Sie hat keine Wirksamkeit als postexpositionelle Prophylaxe und wirkt sich weder positiv noch negativ auf eine allfällige Infektion durch den aktuellen Zeckenstich aus.
Impfung gegen Herpes zoster
Die Impfung gegen Herpes zoster ist gemäss Schweizerischem Impfplan für alle Personen im Alter zwischen 65-79 Jahren sowie für in naher Zukunft immungeschwächte Patientinnen und Patienten im Alter von 50 bis 79 Jahren empfohlen (7). Aktuell ist in der Schweiz nur der virale Lebendimpfstoff gegen Herpes zoster (Zostavax®) verfügbar und zugelassen. Die Impfung erfolgt mit einer einzelnen, subkutan verabreichten Dosis und zeigt eine gute Wirksamkeit mit Verhinderung von ungefähr 51% der Herpes-zoster-Fälle und 67% der Fälle von postherpetischer Neuralgie bei gesunden 60-jährigen oder älteren Personen (8). Leider werden die Kosten für die Herpes zoster-Impfung nicht durch die Grundversicherung der Krankenkassen übernommen. In Europa und anderen Ländern ist ein rekombinanter Subunit-Impfstoff (Shingrix®) zugelassen und verfügbar, der auch bei immunsupprimierten Personen eingesetzt werden kann. Der Zeitpunkt einer Markteinführung dieses Impfstoffes in der Schweiz ist nicht bekannt. Im Einzelfall kann ein Import aus dem europäischen Ausland und die off label Anwendung des Subunit-Impfstoffs in Erwägung gezogen werden. Zu beachten ist dabei der Preis (keine Kostenübernahme durch die Krankenkasse) sowie die Notwendigkeit von 2 Impfdosen mit 2-6 Monaten Intervall.
Impfempfehlungen bei besonderen Patientengruppen
Bei besonderen Patientengruppen wie z.B. immunsupprimierten Personen, Reisenden oder Schwangeren ist das Ziel ebenfalls ein möglichst kompletter Impfschutz gemäss den Empfehlungen im Schweizerischen Impfplan. Erster Schritt ist dabei immer die Beurteilung des aktuellen Impfstatus, das Vorgehen zur Ergänzung und Komplettierung des Impfschutzes muss dann unter Berücksichtigung der individuellen Voraussetzungen festgelegt werden. Dabei helfen Ihnen die eingangs in diesem Artikel erwähnten Grundregeln, die entsprechenden Empfehlungsdokumente des BAG (Tab. 2) oder eine Mail-Anfrage an die Infovac-Experten (www.infovac.ch).
Migranten
Der Impfschutz von Migrantinnen und Migranten sollte bald möglichst nach Einreise überprüft und entsprechend ihrem Alter gemäss Schweizerischen Impfempfehlungen ergänzt werden (9). Im Zweifelsfall – bei fehlender Dokumentation und unsicherer Anamnese – kann die Person als ungeimpft betrachtet und entsprechend grundimmunisiert werden. Wichtig ist die Dokumentation der neu durchgeführten Impfungen mittels Impfausweis und die Sicherstellung und Überprüfung des Informationsflusses, z.B. bei Wechsel des Aufenthaltsortes.
Für die Praxis kann bei Jugendlichen > 12 J. und Erwachsenen folgendes Vorgehen gewählt werden (9):
- Erstkontakt: 1 Dosis dTpa-IPV (Boostrix Polio®) + 1 Dosis MMR + 1 Dosis Varizellen
- 1 Mo. nach Erstkontakt: jeweils 2. Dosis MMR und Varizellen, erste Dosis Hepatitis B
- 2 Mo. nach Erstkontakt: eine Dosis dT-IPV (Revaxis®) und zweite Dosis Hepatitis B
- 8 Mo. nach Erstkontakt: eine Dosis dT-IPV (Revaxis®) und dritte Dosis Hepatitis B
- HPV: 3 Dosen (0, 1-2, 6 Mo.) bei Alter 15 – 26 J.; vor 15. Geburtstag 2 Dosen (0, 6 Mo.)
- Meningokokken (Impfung mit MCV-ACWY, Menveo®): 1 Dosis bei Alter 11-15 J., nachholen bis zum 20. Geburtstag
Klinik für Infektiologie/Spitalhygiene
KSSG und Ostschweizer Kinderspital
St. Gallen
ana.steffen@kssg.ch
Klinik für Infektiologie/Spitalhygiene
KSSG und Ostschweizer Kinderspital
St. Gallen
Reisemedizin, Klinik für Infektiologie/Spitalhygiene
Kantonsspital St. Gallen
Rorschacher Strasse 95
9007 St. Gallen
Die Autoren haben in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
1. Kwong JC et al: Acute myocardial infarction after laboratory-confirmed influenza infection. N Engl J Med 2018;378:345-53
2. Bundesamt für Gesundheit (BAG) und Eidgenössische Kommission für Impffragen (EKIF): Bericht zur Grippesaison 2017/18. BAG Bulletin 2018; No32:9-21
3. Fireman B et al: Influenza vaccination and mortality: differentiating vaccine effects from bias. Am J Epidemiol 2009;170(5):650-6
4. Baxter R et al : Effect of influenza vaccination on hospitalizations in persons aged 50 years and older. Vaccine 2010;28(45):7267-72
5. Demicheli V et al: Vaccines for preventing influenza in healthy adults. Cochrane Database Syst Rev. 2018 Feb 1;2:CD001269
6. Bundesamt für Gesundheit (BAG) und Eidgenössische Kommission für Impffragen (EKIF): Pneumokokkenimpfung: Empfehlungen zur Verhinderung von invasiven Pneumokokkenerkrankungen bei Risikogruppen. BAG Bulletin 2014;No8:129-141
7. Bundesamt für Gesundheit (BAG) und Eidgenössische Kommission für Impffragen (EKIF): Empfehlungen zur Impfung gegen Herpes Zoster / « Gürtelrose». BAG Bulletin 2017;No47:12-15
8. Oxman MN et al: A vaccine to prevent herpes zoster and postherpetic neuralgia in older adults. N Engl J Med 2005;352(22):2271-84
9. Tarr P et al: Impfungen bei erwachsenen Flüchtlingen. Swiss Med Forum 2016;16(49-50):1075-1079