Outre le tabagisme, l’hypertension artérielle est le facteur de risque cardiovasculaire le plus important. La prévalence dépend fortement de l’âge. Même les patients très âgés (>80 ans) peuvent bénéficier d’une réduction modérée de la pression artérielle (valeur cible 150/80 mmHg). Cependant, des circonstances concomitantes telles que la fragilité, la multimorbidité et la polypharmacie rendent cette population très âgée particulièrement vulnérable, c’est pourquoi la thérapie doit être individualisée pour prévenir le surtraitement et les effets secondaires potentiels.
Avec l’ hypercholestérolémie, le diabète, l’ obésité et le tabagisme, l’ hypertension artérielle est l’ un des 5 facteurs de risque classiques responsables de la majorité des décès cardiovasculaires. Des études de cohortes prospectives ont également montré des preuves solides que le risque de développer une démence vasculaire est significativement plus élevé chez les patients souffrant d’ hypertension artérielle par rapport au groupe témoin normotendu (1). Les personnes hypertendues ont non seulement une espérance de vie moyenne réduite d’ environ 5 ans, mais elles souffrent également de morbidité cardiovasculaire pendant une durée moyenne de 2,1 ans de plus (2).
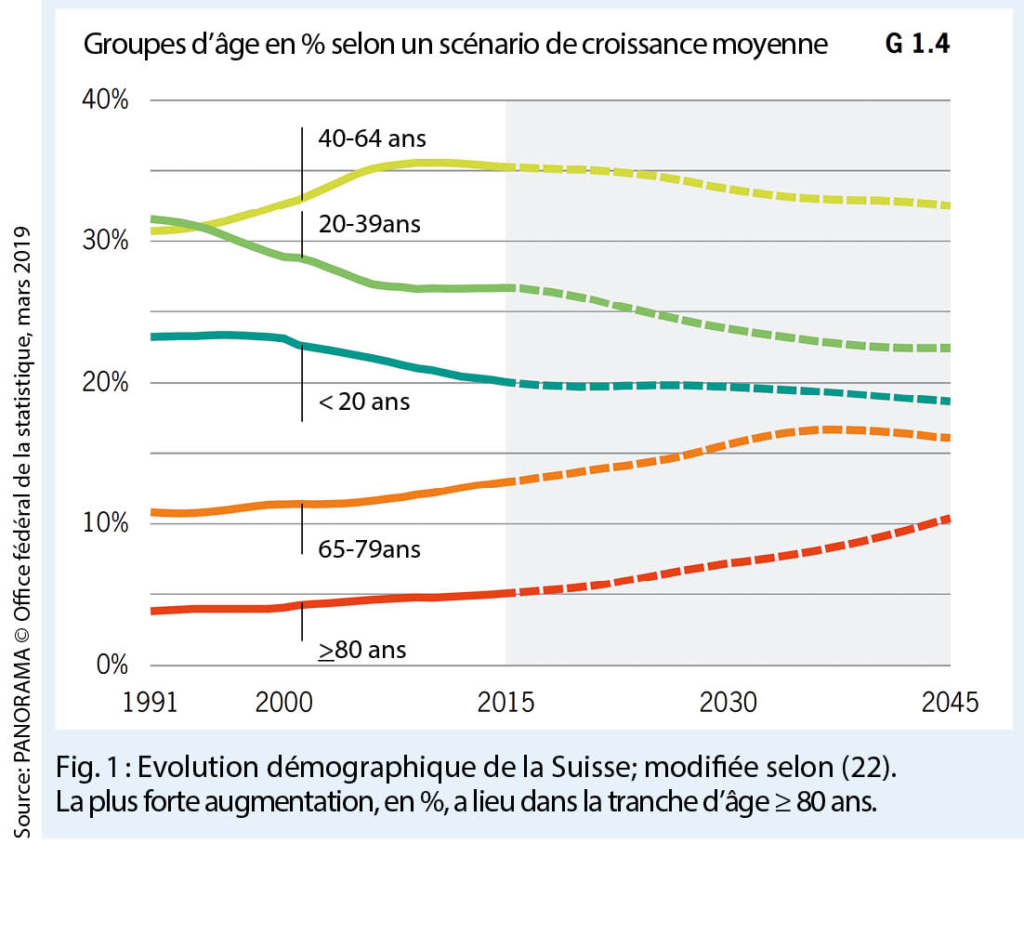
L’ hypertension artérielle (essentielle) est fortement dépendante de l’ âge, en plus des causes génétiques et environnementales. Dans les pays développés, plus de la moitié de la population de plus de 70 ans est touchée (3). Le processus de vieillissement démographique se poursuivra également en Suisse. Selon un scénario de croissance moyenne, la proportion de la population > 65 ans passera à environ 26 % d’ ici 2045, l’ augmentation relative la plus importante étant prévue dans le groupe des personnes âgées de 80 ans et plus (fig. 1). Une analyse de plus de 24 000 consultations dans les cabinets de médecins de famille en Suisse a montré que l’ hypertension artérielle était le motif le plus fréquent de consultation en cabinet, représentant 6,15% d’ un large éventail de 830 occasions de traitement différentes (4).
Il existe des preuves convaincantes de l’ efficacité de la réduction de la pression artérielle et de la réduction de la morbidité et de la mortalité cardiovasculaire précoce y étant associées (5). En raison de la prévalence élevée dans la population, le contrôle du tabagisme et de l’ hypertension artérielle offre le plus grand potentiel préventif pour réduire la mortalité cardiovasculaire (6). Les personnes de plus de 80 ans peuvent également bénéficier d’ une réduction de la pression artérielle : Dans l’ étude HYVET (7) (3845 patients, âge moyen 84 ans), une réduction de la pression artérielle d’ environ 175/90 mmHg à environ 145/80 mmHg a entraîné une diminution significative des apoplexies mortelles (avec un NNT d’ environ 25 sur 2 ans) et une réduction de la mortalité globale (7). Cependant, il est important d’ examiner de près cette population de patients, car la fragilité, la comorbidité et la polypharmacie sont des affections concomitantes courantes chez ces patients et, par conséquent, un traitement individualisé est approprié pour prévenir le surtraitement et les effets secondaires potentiels. Dans ce qui suit, nous abordons certains aspects du diagnostic et du traitement de l’ hypertension, en mettant l’ accent sur les patients âgés (> 65 ans) et très âgés (> 80 ans).
Définition de l’ hypertension : Quelles sont les limites et les méthodes de mesure de la pression artérielle ?
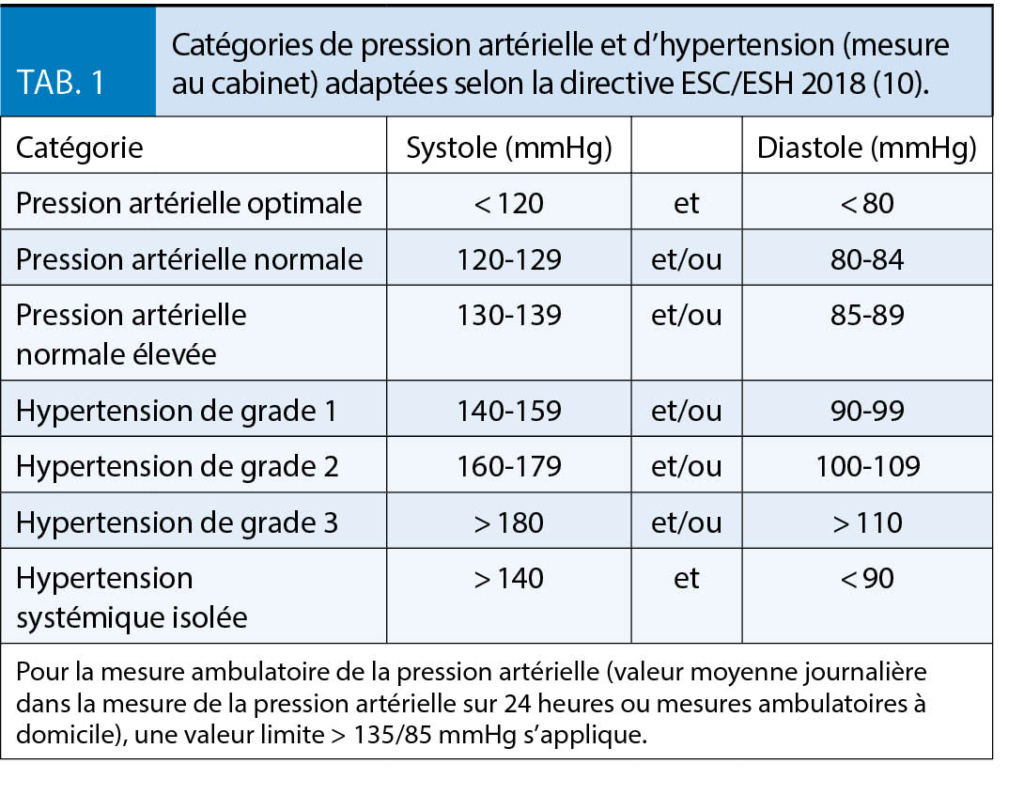
Depuis des années, l’ hypertension artérielle est définie en pratique comme une pression artérielle > 140/90 mmHg. Au cours des deux dernières années, les directives internationales ont été révisées. Aux Etats-Unis, la valeur seuil de l’ hypertension artérielle a été redéfinie à > 130/80 mmHg (8), ce qui a augmenté le nombre de patients hypertendus d’ environ 20 millions « en une nuit » aux seuls Etats-Unis. Le faible bénéfice et les effets secondaires potentiels d’ une thérapie plus intensive pour atteindre les nouvelles valeurs cibles ainsi que les conflits d’ intérêts potentiels entre les membres du Comité des lignes directrices ont été les raisons pour lesquelles l’ American College of Physicians (ACP) et l’ American Academy of Family Medicine (AAFP) n’ ont pas approuvé les nouvelles recommandations de limites (9). En Europe, les catégories de pression artérielle n’ ont pas été modifiées dans la directive ESC/ESH (10), qui a été révisée en 2018. La Société Suisse d’ Hypertension (www.swisshypertension.ch) approuve également ces recommandations. Pour l’ Europe et la Suisse, une valeur cible générale de < 140/90 mmHg, basée sur des mesures pratiques répétées (tab. 1), reste valable pour la population générale.
Dans la nouvelle directive ESC/ESH 2018, les mesures de la pression artérielle en ambulatoire (mesures à domicile, mesure de la pression artérielle sur 24 heures) sont de plus en plus recommandées comme alternatives aux mesures effectuées au cabinet. Cela présente l’ avantage, surtout concernant les patients âgés, de pouvoir détecter l’ hypertension de blouse blanche. Plus de 30 % des patients âgés sont concernés, c’ est-à-dire qu’ un patient âgé sur trois risque potentiellement d’ être surdiagnostiqué si l’ effet de blouse blanche n’ est pas pris en compte. Il en résulte un risque accru de surtraitement, potentiellement sans avantage, mais avec le risque d’ effets secondaires potentiels (11). Les valeurs obtenues de la mesure de la pression artérielle à domicile ont une signification pronostique pour les événements cardiovasculaires indépendamment des valeurs de mesure au cabinet (12), ce qui démontre le rôle important de la mesure de la pression artérielle à domicile dans le diagnostic et la surveillance du traitement. De plus, il est important d’ effectuer la mesure au cabinet chez les patients fragiles ou très âgés également en position debout, pour détecter une éventuelle hypotension (orthostatique). Cela peut avoir un effet délétère sur ces patients sous forme de chutes.
Qu’ en est-il de la précision de la mesure de la tension artérielle au poignet ? Ces dispositifs sont de plus en plus commercialisés et semblent plus pratiques à utiliser, en particulier pour les patients âgés. Une étude portant sur 605 patients de plus de 75 ans (âge moyen de 81,6 ans) a montré des valeurs comparables avec les mesures prises au bras dans le groupe d’ âge 75-80 ans. Dans le groupe > 80 ans, les valeurs systoliques mesurées au poignet étaient également comparables, sauf pour le sous-groupe de patients atteints de maladie artérielle périphérique occlusive (MAP). Dans ce sous-groupe, les valeurs au poignet étaient en moyenne inférieures de 5,5 mmHg par rapport aux mesures prises au bras (13). Des études supplémentaires sur la valeur de la mesure prise au poignet seraient ici souhaitables.
La fragilité : concept, signification et évaluation clinique
Les personnes fragiles sont vulnérables aux problèmes de santé, car ils ont beaucoup moins de ressources pour faire face à une maladie. Contrairement aux patients « robustes » ou en bonne santé du même âge, ils ont une espérance de vie considérablement réduite (14), ce qui rend le bénéfice d’ une intervention (dans notre cas, la réduction de la pression artérielle) de plus en plus improbable. En même temps la fragilité, du point de vue du médecin de famille, exige une attention accrue, ce qui protège ces patients vulnérables contre les diagnostics et les thérapies inutiles ou même nuisibles.
Comment mesurer la fragilité ? Dans la pratique, il existe des alternatives à l’ évaluation gériatrique détaillée. Par exemple, la vitesse de marche est un indicateur indépendant de la survie, indépendamment de l’ âge, du sexe, de l’ utilisation d’ une aide à la marche et de la maladie chronique (15). La vitesse de marche peut être facilement enregistrée sur une piste d’ essai de 4 m en pratique à l’ aide d’ un chronomètre. Sur une période d’ observation de 7 ans, il a été montré que chez les patients fragiles (définis comme ayant une vitesse de marche < 0,8 m/s), l’ hypertension artérielle (> 140/90 mmHg) n’ avait plus d’ influence sur la mortalité globale (16).
Il est également important de savoir que l’ évaluation clinique ou « intuition » du médecin de famille traitant est également une méthode validée pour la détection précoce des patients vulnérables présentant un risque accru de détérioration fonctionnelle (y compris le décès et l’ institutionnalisation) (17).
(Absence de) preuve de traitement de l’ hypertension dans la vieillesse et la fragilité
L’ étude HYVET (7) mentionnée ci-dessus est encore le seul essai prospectif randomisé et contrôlé qui a été mené explicitement chez des patients très âgés. Un résultat important a été que l’ effet positif d’ abaisser la tension artérielle d’ un niveau initial de 175/90 mmHg à une moyenne de 145/80 mmHg a été obtenu dans 25,8 % des cas avec la monothérapie (1,5 mg d’ indapamide). La directive 2018 de l’ ESC/EHS recommande aussi principalement la monothérapie pour les patients âgés de plus de 80 ans. Les comorbidités doivent également être prises en compte dans le choix du traitement. Par exemple, en présence d’ une coronaropathie, contrairement aux patients plus jeunes, un bêta-bloquant peut être le premier choix.
Dans l’ étude SPRINT, dont on a beaucoup parlé, moins d’ événements cardiovasculaires sont survenus dans le sous-groupe des patients de plus de 75 ans (âge moyen 79,9 ans) en raison de la réduction de la tension artérielle, mais au prix d’ effets secondaires nettement plus graves (chutes et déséquilibres électrolytiques nécessitant un traitement) dans le groupe d’ intervention (valeur cible 120 mmHg) par rapport au groupe témoin (valeur cible 140 mmHg) (18). C’ est important de le savoir : Les études SPRINT et HYVET ont exclu les patients de santé fragile, les patients des maisons de soins infirmiers et les patients atteints de démence et de statut à la suite d’ événements vasculaires cérébraux. Dans SPRINT, le diabète était également un critère d’ exclusion. En résumé, il existe des preuves que la maîtrise de la tension artérielle < 160 mmHg est efficace chez les patients très âgés et robustes (non frêles), mais l’ avantage d’ une baisse plus intense (< 140 mmHg) est faible et les effets secondaires graves sont fréquents.
Quelles sont les données disponibles pour les patients très âgés et fragiles présentant toutes les comorbidités mentionnées ci-dessus, qui constituent une partie importante de la routine quotidienne de la pratique ? Des études de cohorte bien contrôlées ont montré les résultats suivants : Une étude d’ observation en population auprès des individus âgés de plus de 85 ans de Leyde, aux Pays-Bas, a montré une augmentation significative de la mortalité globale chez les participants ayant des valeurs de pression artérielle traitées plus faibles (< 140 mmHg) par rapport à la population traitée ayant des valeurs de pression artérielle plus élevées (19). Une réduction de la pression artérielle < 140/90 mmHg a également été associée à une augmentation du taux de mortalité globale chez les plus de 80 ans dans une cohorte d’ âge représentative de l’ Allemagne (20). Dans une cohorte de patients israéliens de plus de 90 ans atteints d’ hypertension non traitée (> 140/90 mmHg), il n’ y avait aucune différence dans la mortalité à 5 ans, indépendamment des comorbidités, du traitement antihypertenseur et de l’ état fonctionnel (21).
Institut für Hausarztmedizin
Universität und UniversitätsSpital Zürich
Pestalozzistrasse 24
8091 Zürich
oliver.senn@usz.ch
Institut für Hausarztmedizin
Universität und UniversitätsSpital Zürich
Pestalozzistrasse 24
8091 Zürich
Les auteurs n’ ont déclaré aucun conflit d’ intérêts en rapport avec cet article.
1. Sharp SI, Aarsland D, Day S, Sonnesyn H, Alzheimer’s Society Vascular Dementia Systematic Review G, Ballard C. Hypertension is a potential risk factor for vascular dementia: systematic review. Int J Geriatr Psychiatry. 2011;26(7):661-9.
2. Franco OH, Peeters A, Bonneux L, de Laet C. Blood pressure in adulthood and life expectancy with cardiovascular disease in men and women: life course analysis. Hypertension. 2005;46(2):280-6.
3. Staessen JA, Wang J, Bianchi G, Birkenhager WH. Essential hypertension. Lancet. 2003;361(9369):1629-41.
4. Tandjung R, Hanhart A, Bartschi F, Keller R, Steinhauer A, Rosemann T, Senn O. Referral rates in Swiss primary care with a special emphasis on reasons for encounter. Swiss Med Wkly. 2015;145:w14244.
5. Ettehad D, Emdin CA, Kiran A, Anderson SG, Callender T, Emberson J, Chalmers J, Rodgers A, Rahimi K. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet. 2016;387(10022):957-67.
6. Patel SA, Winkel M, Ali MK, Narayan KM, Mehta NK. Cardiovascular mortality associated with 5 leading risk factors: national and state preventable fractions estimated from survey data. Ann Intern Med. 2015;163(4):245-53.
7. Beckett NS, Peters R, Fletcher AE, Staessen JA, Liu L, Dumitrascu D, Stoyanovsky V, Antikainen RL, Nikitin Y, Anderson C, Belhani A, Forette F, Rajkumar C, Thijs L, Banya W, Bulpitt CJ, Group HS. Treatment of hypertension in patients 80 years of age or older. N Engl J Med. 2008;358(18):1887-98.
8. Whelton PK, Carey RM, Aronow WS, Casey DE, Jr., Collins KJ, Dennison Himmelfarb C, DePalma SM, Gidding S, Jamerson KA, Jones DW, MacLaughlin EJ, Muntner P, Ovbiagele B, Smith SC, Jr., Spencer CC, Stafford RS, Taler SJ, Thomas RJ, Williams KA, Sr., Williamson JD, Wright JT, Jr. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2018;138(17):e484-e594.
9. Miyazaki K. Overdiagnosis or not? 2017 ACC/AHA high blood pressure clinical practice guideline: Consequences of intellectual conflict of interest. J Gen Fam Med. 2018;19(4):123-6.
10. Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, Clement DL, Coca A, de Simone G, Dominiczak A, Kahan T, Mahfoud F, Redon J, Ruilope L, Zanchetti A, Kerins M, Kjeldsen SE, Kreutz R, Laurent S, Lip GYH, McManus R, Narkiewicz K, Ruschitzka F, Schmieder RE, Shlyakhto E, Tsioufis C, Aboyans V, Desormais I, Group ESCSD. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J. 2018;39(33):3021-104.
11. Niiranen TJ, Jula AM, Kantola IM, Reunanen A. Prevalence and determinants of isolated clinic hypertension in the Finnish population: the Finn-HOME study. J Hypertens. 2006;24(3):463-70.
12. Ward AM, Takahashi O, Stevens R, Heneghan C. Home measurement of blood pressure and cardiovascular disease: systematic review and meta-analysis of prospective studies. J Hypertens. 2012;30(3):449-56.
13. Hoffmann U, Drey M, Thrun JM, Obermeier E, Weingart C, Hafner K, Sieber C. The role of wrist monitors to measure blood pressure in older adults. Aging Clin Exp Res. 2018.
14. Walter LC, Covinsky KE. Cancer screening in elderly patients: a framework for individualized decision making. JAMA. 2001;285(21):2750-6.
15. Studenski S, Perera S, Patel K, Rosano C, Faulkner K, Inzitari M, Brach J, Chandler J, Cawthon P, Connor EB, Nevitt M, Visser M, Kritchevsky S, Badinelli S, Harris T, Newman AB, Cauley J, Ferrucci L, Guralnik J. Gait speed and survival in older adults. JAMA. 2011;305(1):50-8.
16. Odden MC, Peralta CA, Haan MN, Covinsky KE. Rethinking the association of high blood pressure with mortality in elderly adults: the impact of frailty. Arch Intern Med. 2012;172(15):1162-8.
17. van Blijswijk SCE, Blom JW, de Craen AJM, den Elzen WPJ, Gussekloo J. Prediction of functional decline in community-dwelling older persons in general practice: a cohort study. BMC Geriatr. 2018;18(1):140.
18. Group SR, Wright JT, Jr., Williamson JD, Whelton PK, Snyder JK, Sink KM, Rocco MV, Reboussin DM, Rahman M, Oparil S, Lewis CE, Kimmel PL, Johnson KC, Goff DC, Jr., Fine LJ, Cutler JA, Cushman WC, Cheung AK, Ambrosius WT. A Randomized Trial of Intensive versus Standard Blood-Pressure Control. N Engl J Med. 2015;373(22):2103-16.
19. Streit S, Poortvliet RKE, Gussekloo J. Lower blood pressure during antihypertensive treatment is associated with higher all-cause mortality and accelerated cognitive decline in the oldest-old-data from the Leiden 85-plus Study. Age Ageing. 2018.
20. Douros A, Tolle M, Ebert N, Gaedeke J, Huscher D, Kreutz R, Kuhlmann MK, Martus P, Mielke N, Schneider A, Schuchardt M, van der Giet M, Schaeffner E. Control of blood pressure and risk of mortality in a cohort of older adults: the Berlin Initiative Study. Eur Heart J. 2019;40(25):2021-8.
21. Stessman J, Bursztyn M, Gershinsky Y, Hammerman-Rozenberg A, Jacobs JM. Hypertension and Its Treatment at Age 90 Years: Is There an Association with 5-Year Mortality? J Am Med Dir Assoc. 2017;18(3):277 e13- e19.
22. PANORAMA © BAG März 2019 https://www.bfs.admin.ch/bfs/de/home/statistiken/bevoelkerung.assetdetail.7846584.html