Die mechanische Rekanalisation grösserer Gefässverschlüsse beim ischämischen Schlaganfall, allein oder in Kombination mit einer intravenösen Lysetherapie, hat in den letzten Jahren zu einem deutlich verbesserten funktionellen Behandlungsergebnis geführt. Entscheidend dazu beigetragen hat die Verbesserung der Rettungskette («Time is brain»; Zeit vom Symptombeginn bis zum Eintreffen in einem Akutspital mit der Möglichkeit zur Behandlung von Hirnschlägen), die Auswahl geeigneter Patienten und die rasante Weiterentwicklung der zur Verfügung stehenden Materialien wie Stentretriever und Aspirationskatheter. Im Weiteren sollen die Möglichkeiten der endovaskulären Therapie dargestellt werden.
Efforts have been made for many years to recanalize closed larger intracranial vessels endovascularly. Initial experiments with a helical thrombus extraction system (Merci-Device) did not provide satisfactory recanalization rates. Only since the emergence of large-lumen, flexible aspiration catheter and the use of intracranial stents as thrombus extraction system (stent retriever) are potent methods available. In 2015, several independent studies demonstrated the effectiveness of thrombectomy. In a meta-analysis of 5 large prospective randomized studies (MR CLEAN, ESCAPE, REVASCAT, SWIFT PRIME, EXTEND IA), 46% of patients achieved a functionally independent status (mRS 0-2) 90 days after intra-arterial recanalization,
Stent Retriever
In 2009 it was reported for the first time that occlusion of the cerebral artery was successfully recanalized with a solitaire stentretriver (2). This self-expanding stent is fixed to a wire, inserted through a microcatheter, and unfolds upon withdrawal of the microcatheter over the thrombus. As a result, the thrombus is fixed between the stent and the vessel wall, the stent meshes push into the thrombus and so unfolded stent and thrombus can be removed together from the vessel. Numerous different retrievers have been developed. The mesh design, the stent length, the diameter and also the radial force were varied. With strict patient selection, recanalization rates (TICI 2b-3) up to 88% are achieved. The rate of symptomatic intracranial haemorrhage shows no significant difference to the sole intravenous lysis therapy and is between 0 and 3% (3). A principal problem is that, to place the retriever, the vascular closure must first be passed through a microcatheter. Thrombus material can be dislocated peripherally. This problem is of minor importance in daily practice. However, if the thrombus is not firmly fixed to the stent upon retraction, it may detach proximally from the stent retriever in the vascular segment and cause embolism in a new vascular territory. Therefore today this technique is usually combined with a flow reversal. For this purpose, a large-lumen access catheter is placed in the proximal internal carotid artery, which is provided at the distal end with a circular balloon. Prior to thrombectomy, the proximal ACI passager is occluded by balloon insufflation and suction placed in the catheter lumen so that the ACI reverses flow and free emboli are withdrawn. In a retrospectively analyzed cohort, the risk of unwanted emboli could be reduced from 32% to 7% (4).
ADAPT-Aspiration
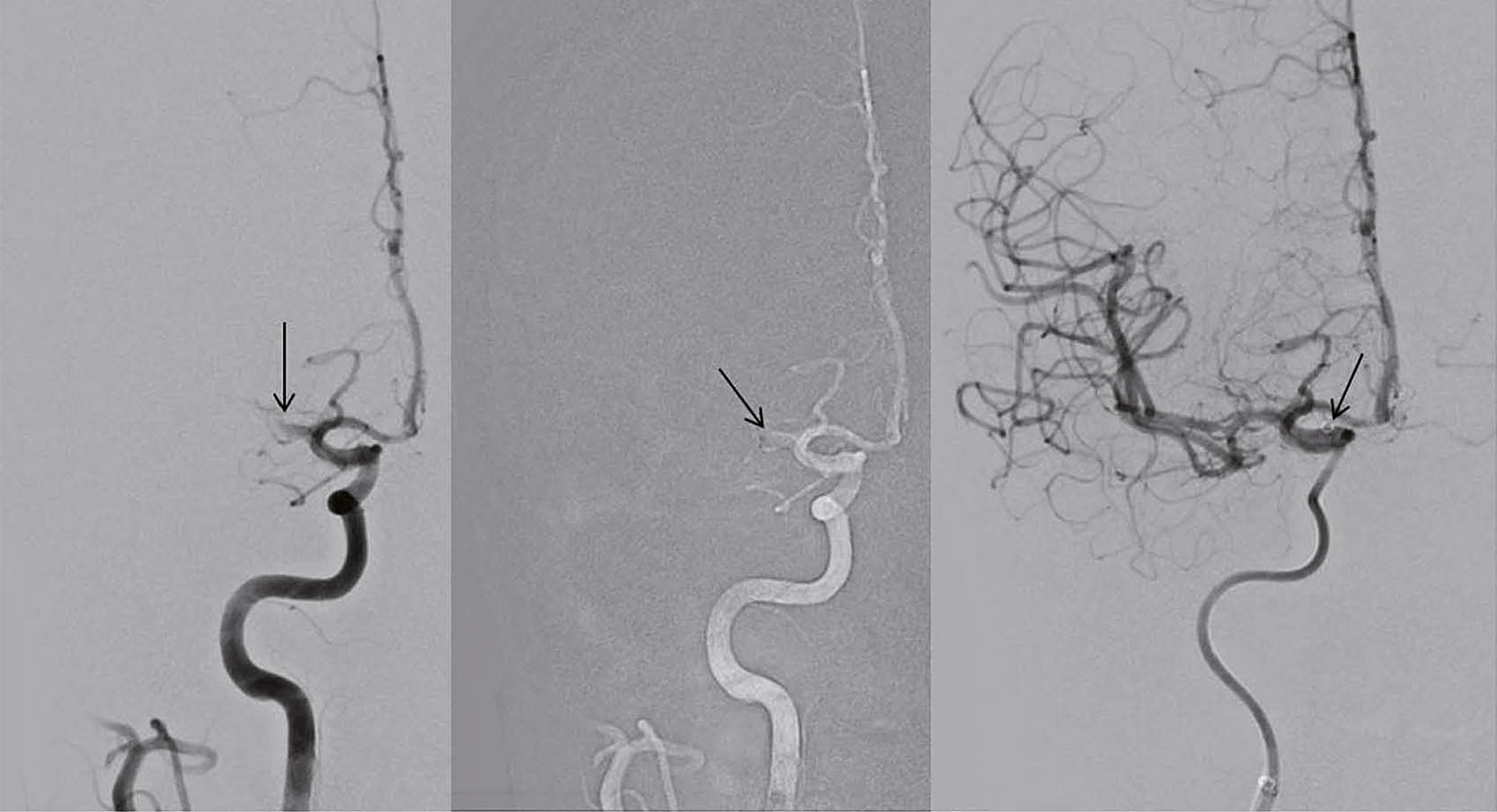
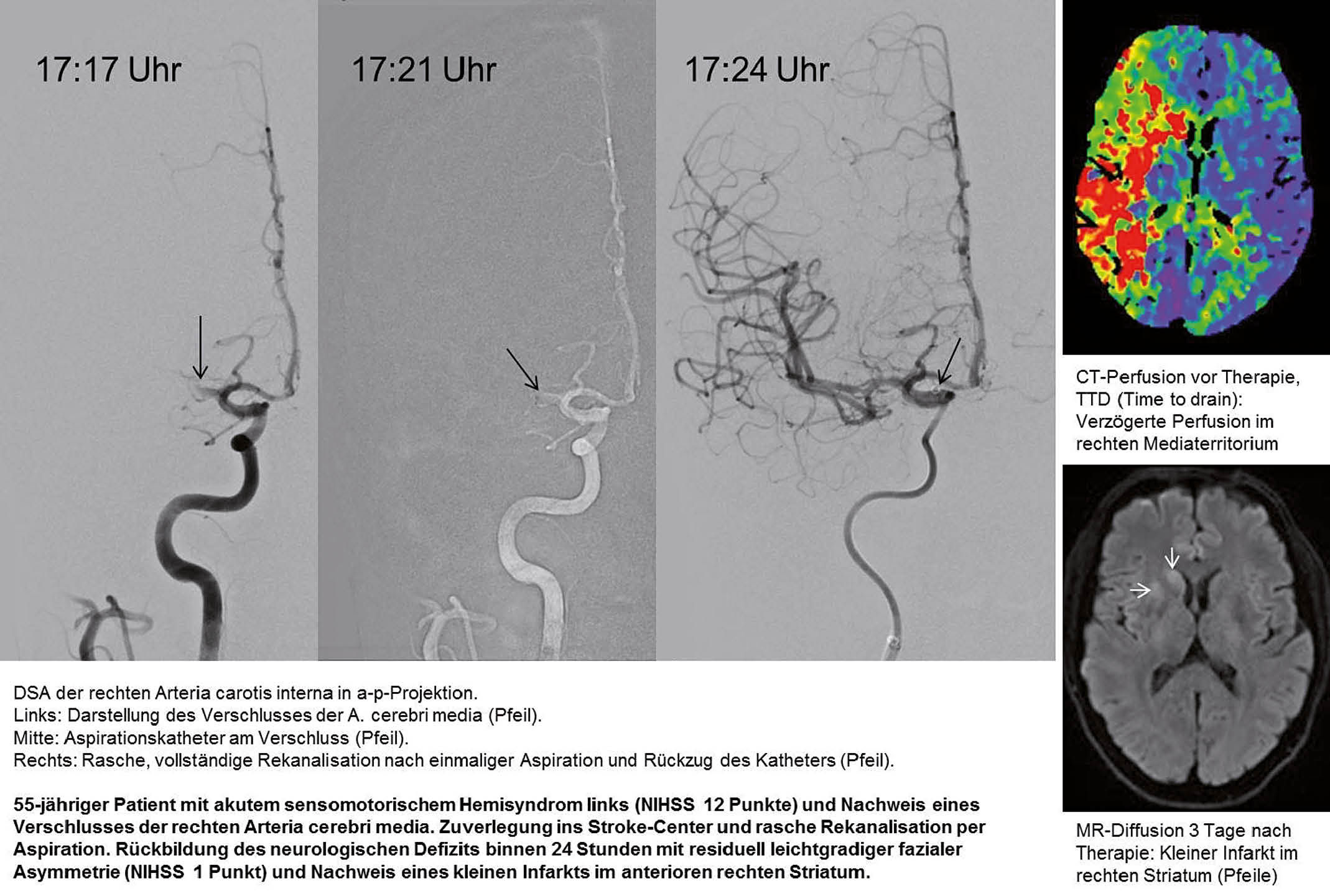
Parallel konnte 2010 gezeigt werden, dass mittels Aspiration zerebrale Gefässe rekanalisiert werden können (5). Bei der ADAPT-Technik (a direct aspiration first pass technique) wird der Aspirationskatheter proximal des Thrombus platziert und kontinuierlich Sog über eine Pumpe angelegt. Sistiert der Rückfluss im System, zeigt dies das Ansaugen des Thrombus an. Der Sog wird für ca. 90 Sekunden belassen, der Thrombus dabei in den Katheter gesaugt oder an dessen Spitze fixiert und idealerweise beim Rückzug des Katheters vollständig entfernt. Bei langen oder wandadhärenten Thromben kann es zum Abreissen des Thrombus kommen, sodass ein Teil verbleibt und der Vorgang wiederholt werden muss. Rasch hat sich gezeigt, dass neben der Flexibilität des distalen Katheterendes das Lumen des Katheters wesentlich zum Aspirationserfolg beiträgt. So konnte bei zunehmender Flexibilität der Katheter der Innendurchmesser von 50“ auf 70“ (Angabe in Tausendstel Inch, 70“ = 1,78 mm) gesteigert werden. Eine kürzlich veröffentliche prospektiv randomisierte Studie zeigt Rekanalisationsraten (TICI 2b-3) mit dem Aspirationssystem allein von 71% und in Kombination mit anderen Methoden bis 93% (6). Die Aspirationstechnik führte sehr rasch zum Erfolg, die mittlere Zeit zwischen Gefässpunktion und Rekanalisation betrug 31 Minuten und die Rate unerwünschter Embolien in neue Gefässterritorien lag bei 1,5%.
SOLUMBRA
Führt eine Methode allein nicht zum Erfolg, so können Methoden kombiniert werden. Dabei wird der Aspirationskatheter (PenUMBRA-System) proximal des Thrombus platziert und koaxial über einen Mikrokatheter ein Stent-Retriever (SOL-itaire) über dem Thrombus platziert. Unter kontinuierlicher Aspiration kann nun der Stent-Retriever samt Thrombus in den Aspirationskatheter gezogen werden. Die Kombination aller Methoden ermöglicht heute Rekanalisationsraten von über 90%.
Verschluss proximaler Gefässe
Ist die Ursache einer intrakraniellen Embolie eine arteriosklerotisch bedingte hochgradige zervikale Stenose oder ein Verschluss der A. carotis interna, so kann dies in der gleichen Sitzung behandelt werden. Unterschiedliche Strategien wurden publiziert, wobei prospektiv randomisierte Daten fehlen. Eine retrospektive Metaanalyse von 33 Studien zeigt keinen signifikanten Unterschied, ob zuerst der distale oder der proximale Verschluss behandelt wurde, oder ob eine Ballonangioplastie mit oder ohne Stent-Implantation durchgeführt wurde (7).
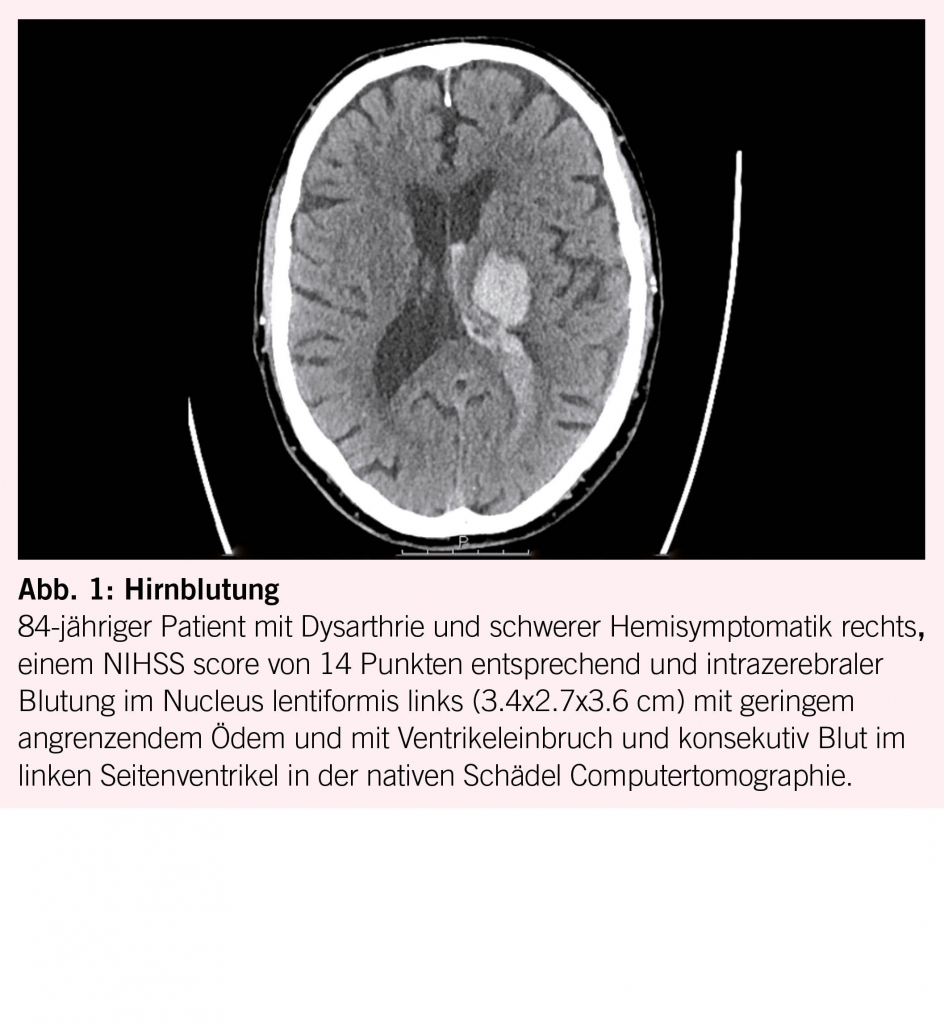
In St. Gallen führen wir bei hochgradigen Stenosen oder Verschlüssen in der Regel eine proximale Stent-PTA durch. Dies hat den Vorteil, dass die Emboliequelle ausgeschaltet ist, ein guter Blutfluss vorliegt und eine unbehinderte Passage bis zum Thrombus möglich ist, insbesondere wenn das Thrombusextraktionsmanöver wiederholt werden muss. Um frühe Stentverschlüsse zu vermeiden, ist eine Thrombozytenaggregationshemmung nötig, was das Risiko einer zerebralen Blutung erhöhen kann. Ein pragmatischer Ansatz ist die intravenöse Gabe von 500 mg Acetylsalicylsäure während der Intervention und der Start einer doppelten Thrombozytenhemmung 12–24 Stunden nach Intervention, nachdem eine intrakranielle Hämorrhagie mittels nativer Computertomographie ausgeschlossen wurde.
Astverschlüsse
Ob Patienten mit kleineren Gefässverschlüssen (Truncus superior oder inferior der Arteria cerebri media, Arteria cerebri anterior oder posterior) und schwerwiegender Symptomatik wie Hemiparese, Aphasie, Hemianopsie oder Neglect von einer endovaskulären Intervention profitieren, ist nicht eindeutig geklärt. Kleinere Stentretriever und Aspirationskatheter werden entwickelt, um peripher gelegene Verschlüsse zu erreichen. Retrospektiv analysierte Daten zeigen die technische Machbarkeit der endovaskulären Therapie mit guten Rekanalisationsraten bis 83% bei einem zerebralen Blutungsrisiko von 7%. Ein funktionell gutes Ergebnis (mRS 0-2) erreichten jedoch nur 30% der Patienten (8).
Verschluss proximaler Gefässe
Ist die Ursache einer intrakraniellen Embolie eine arteriosklerotisch bedingte hochgradige zervikale Stenose oder ein Verschluss der A. carotis interna, so kann dies in der gleichen Sitzung behandelt werden. Unterschiedliche Strategien wurden publiziert, wobei prospektiv randomisierte Daten fehlen. Eine retrospektive Metaanalyse von 33 Studien zeigt keinen signifikanten Unterschied, ob zuerst der distale oder der proximale Verschluss behandelt wurde, oder ob eine Ballonangioplastie mit oder ohne Stent-Implantation durchgeführt wurde (7).
In St. Gallen führen wir bei hochgradigen Stenosen oder Verschlüssen in der Regel eine proximale Stent-PTA durch. Dies hat den Vorteil, dass die Emboliequelle ausgeschaltet ist, ein guter Blutfluss vorliegt und eine unbehinderte Passage bis zum Thrombus möglich ist, insbesondere wenn das Thrombusextraktionsmanöver wiederholt werden muss. Um frühe Stentverschlüsse zu vermeiden, ist eine Thrombozytenaggregationshemmung nötig, was das Risiko einer zerebralen Blutung erhöhen kann. Ein pragmatischer Ansatz ist die intravenöse Gabe von 500 mg Acetylsalicylsäure während der Intervention und der Start einer doppelten Thrombozytenhemmung 12–24 Stunden nach Intervention, nachdem eine intrakranielle Hämorrhagie mittels nativer Computertomographie ausgeschlossen wurde.
Astverschlüsse
Ob Patienten mit kleineren Gefässverschlüssen (Truncus superior oder inferior der Arteria cerebri media, Arteria cerebri anterior oder posterior) und schwerwiegender Symptomatik wie Hemiparese, Aphasie, Hemianopsie oder Neglect von einer endovaskulären Intervention profitieren, ist nicht eindeutig geklärt. Kleinere Stentretriever und Aspirationskatheter werden entwickelt, um peripher gelegene Verschlüsse zu erreichen. Retrospektiv analysierte Daten zeigen die technische Machbarkeit der endovaskulären Therapie mit guten Rekanalisationsraten bis 83% bei einem zerebralen Blutungsrisiko von 7%. Ein funktionell gutes Ergebnis (mRS 0-2) erreichten jedoch nur 30% der Patienten (8).
Erweiterung des therapeutischen Fensters auf 24 Stunden
Neuere Studien haben untersucht, ob Patienten auch später als sechs Stunden nach Symptombeginn von einer Rekanalisation profitieren können. Eine prospektive, randomisierte, multizentrische Studie (DAWN-Trial) konnte zeigen, dass bis 24 Stunden nach Symptombeginn, Patienten mit einem Verschluss der intrakraniellen Arteria carotis interna oder proximalen Arteria cerebri media bei anhaltendem Mismatch mit hohem Schweregrad des neurologischen Defizits und kleinem demarkiertem Infarkt mittels Rekanalisierung in 49% der Fälle einen funktionell unabhängigen Status (mRS 0-2) nach 90 Tagen erreichten, während dies bei der Kontrollgruppe mit konservativer Therapie nur in 13% der Fall war (9). Das Risiko für eine symptomatische Hirnblutung und die Mortalität waren dabei in beiden Gruppen gleich. Ähnliche Ergebnisse konnten in der DEFUSE 3 Studie in einem Zeitfenster bis 16 Stunden nach Symptombeginn gezeigt werden (10).
Patienenselektion
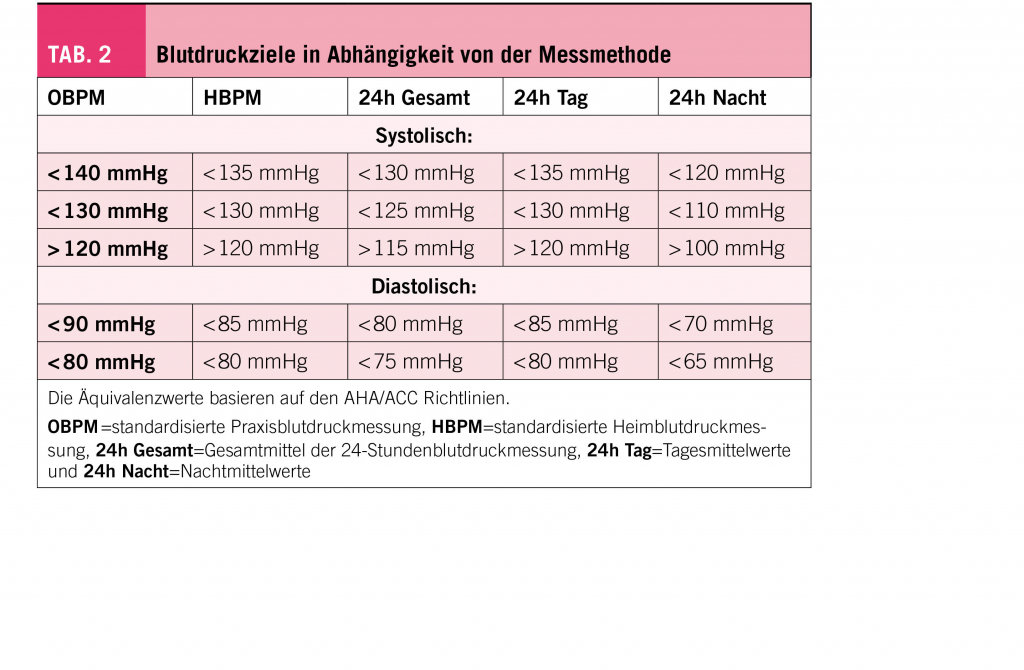
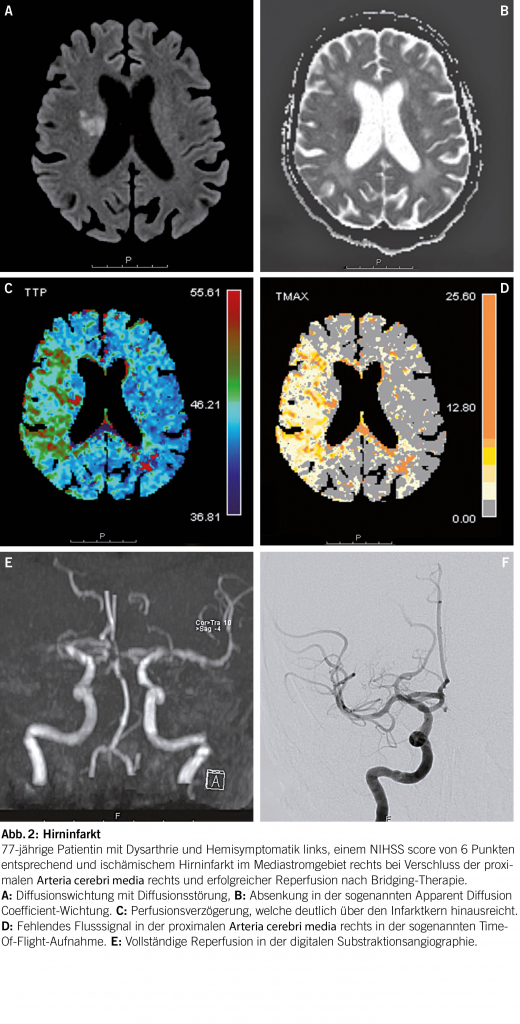
Wichtig für den Erfolg einer Intervention ist die Auswahl geeigneter Patienten. Von einer endovaskulären Therapie profitieren Patienten mit einem Verschluss grosser zerebraler Gefässe, wie der distalen Arteria carotis interna, der Arteria cerebri media (Hauptast oder kaliberkräftige Äste) oder der Arteria basilaris. Dabei sollte ein Mismatch zwischen demarkiertem Infarkt und verzögert perfundiertem Hirngewebe vorliegen, welches die Penumbra – das oligäme, rettbare Hirngewebe – angibt. Der Gefässverschluss kann per CT- oder MR-Angiographie der Kopf- und Halsgefässe dargestellt werden. Eine zusätzliche Perfusionsmessung (CT oder MRT) zur Abschätzung des Mismatchs ist im Zeitfenster von über 6 Stunden oder bei unklarem Symptombeginn («Wake-up-Stroke») zur Bestimmung der Penumbra zwingend nötig und bei Astverschlüssen zur Indikationsstellung oft hilfreich.
Diagnostische und interventionelle Neuroradiologie
Klinik für Radiologie und Nuklearmedizin
Kantonsspital St. Gallen
Rorschacherstrasse 95
9007 St. Gallen
claudia.hader@kssg.ch
Diagnostische und interventionelle Neuroradiologie
Klinik für Radiologie und Nuklearmedizin
Kantonsspital St. Gallen
Rorschacherstrasse 95
9007 St. Gallen
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Beitrag deklariert
1. Goyal M et al. Endovascular thrombectomy after large-vessel ischemic stroke: a meta-analysis of individual patient data from five randomizsed trials. Lancet. 2016;387:1723-31.
2. Castano C et al. Use of the New SolitaireTM AB Device for Mechanical Thrombectomy when Merci Clot Retriever Has Failed to Remove the Clot. Intervent Neuroradiol 2009;15:209-214.
3. Saver JL et al. Stent-Retriever Thrombectomy after Intravenous t-PA vs. t-PA Alone in Stroke. NEJM. 2015;372:2285-95.
4. Lee DH et al. Effective use of ballon guide catheters in reducing incidence of mechanical thrombectomy related distal embolization. Acta Neurochir. 2017;159(9):1671-1677.
5. Tarr R et al. The POST trial: initial post-market experience of the Penumbra system: revascularisation of large vessel occlusion in acute ischemic stroke in the United States and Europe. J NeuroIntervent Surg. 2010; 2:341-4.
6. Schramm P et al. ADAPT Technique with ACE68 and ACE64 reperfusion catheters in ischemic stroke treatment: results from the PROMISE study. J NeuroIntervent Surg 2018;0:1-6.
7. Wilson MP et al. Management of tandem occlusions in acute ischemic stroke- intracranial versus extracranial first and extracranial stenting versus angioplasty alone: a systematic review and meta-analysis. J Neurointerv Surg. 2018;10(8):721-728.
8. Grossberg JA et al. Beyond Large Vessel Occlusion Strokes, Distal Occlusion Thrombectomy. Stroke. 2018;49:1662-1668.
9. Nogueira RG et al. Thrombectomy 6 to 24 Hours after Stroke with a Mismatch between Deficit and Infarct. New Engl J Med. 2018; 378: 11-21.
10. Albers GW et al. Thrombectomy for Stroke at 6 to 16 Hours with Selection by Perfusion Imaging. New Engl J Med. 2018; 378: 708-18.w